LiFePO4/石墨电芯在失控过程中的产气情况
2022-11-09张海林杨海超
汪 涛,张海林,杨海超
(上海电气国轩新能源科技有限公司,上海 200041)
磷酸铁锂(LiFePO4)晶体为稳定的橄榄石结构,具有安全性高、对环境友好、成本低和循环性能好等特点,已广泛应用于动力、基站、储能电站等领域用的锂离子电池。液态电解质锂离子电池在热滥用、电滥用和机械滥用条件下,内部会发生剧烈的化学反应,进而产热,热量大量累积,形成不可逆的失控,存在起火爆炸的风险[1]。针对锂离子电池失控的预警和储能电站的消防设计,是目前亟需解决的问题。
锂离子电池失控时产生的气体具有较好的灵敏性、特征性,且易于检测,可为电池管理系统提供良好的检测和诊断功能。胡丽娜等[2]研究了软包装钴酸锂正极锂离子电池在过充、过放和长期浮充时发生气胀的原因,发现不同滥用条件下的产气明显不同。王铭民等[3]发现,LiFePO4正极锂离子电池从过充到热失控是一个渐变的过程,初期的产气以H2、CO 和CO2为主,后期会产生HCl、HF。这些研究结果,已部分应用在储能电站的早期预警和消防控制领域。
锂离子电池在循环过程中一直在发生氧化还原反应,不同健康状态下,电芯产气成分和含量均会有差异,给电池系统使用周期内的安全预警和消防设计带来困难。本文作者以LiFePO4正极锂离子电池为研究对象,通过过充电、45 ℃高温存储、130 ℃/150 ℃热箱和短路等滥用条件测试,重点对比循环前后的产气,试图寻找可实现探测电池失控预警的参数,为电池系统使用周期的安全预警和消防设计提供参考。
1 实验
1.1 样品的选择
实验选用20 只本公司生产的0595131-6 Ah 软包装锂离子电芯。正极活性物质为LiFePO4(合肥产,99.5%);负极为人造石墨(上海产,99.5%);隔膜为12 μm 聚乙烯(PE)+4 μm Al2O3陶瓷涂层(河北产);电解液为1 mol/L LiPF6/EC+PC+EMC(体积比35 ∶5 ∶60,添加2.5% VC,南通产)。电芯化成的步骤为:0.02C恒流充电240 min,随后0.180C恒流充电100 min。
以每组2 只平行样,将选取的电芯编组为1~10 号,气体测试结果为2 只平行样的均值;1~5 号电芯用CT2001A 电池测试系统(武汉产)在45 ℃下循环200 次。循环步骤为:以1.00C恒流充电至3.650 V,转恒压充电至0.05C;静置30 min 后,以1.00C恒流放电至2.000 V,静置30 min。相应的电芯用途如表1 所示。
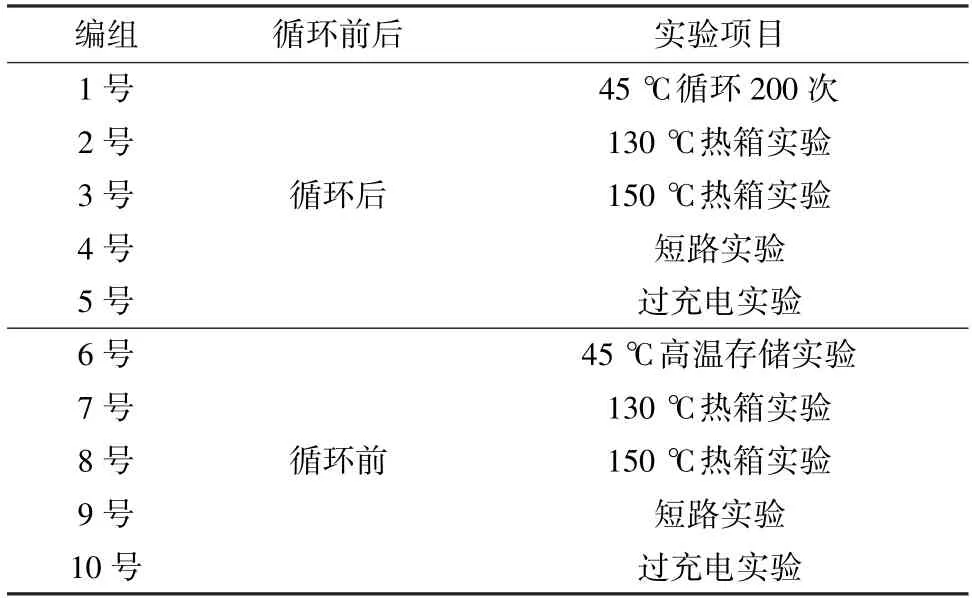
表1 样品测试情况Table 1 Test condition of samples
1.2 电池失控测试
失控测试的电芯,均在25 ℃下充满电,方法为以1.00C恒流充电至3.650 V,转恒压充电至0.05C。
45 ℃高温存储实验:剪开电芯铝塑膜,将卷芯部分裸露后,放置在密封性好且有氩气保护的45 ℃温箱中,分别搁置4 h、50 h、100 h 和190 h,收集温箱内气体,进行分析。
过充电实验:将电芯以1.00C恒流充电至5.475 V,完成过充电测试,收集电芯内部气体,进行分析。
热箱实验:将电芯放置在130 ℃/150 ℃的温箱中,搁置30 min 后,完成热箱实验,收集电芯内部气体,进行分析。
短路实验:将电芯正负极通过外部小于3 mΩ 的内阻短接10 min,完成短路测试,收集电芯内部气体,进行分析。
1.3 气体成分分析
用微样进样器抽取目标气体,完成气体收集。采用GC-2030 气相色谱仪(日本产)分析气体成分,注入量为0.5 ml,进样口温度设为260 ℃,分离柱温度为230 ℃,柱箱温度设为40 ℃,保温2 min 后,以10 ℃/min 的速率升温至230 ℃,保温2 min 后,自然降温,载气为高纯氦气,检测器为介质阻挡放电等离子体检测器(BID),温度为240 ℃。计算45 ℃高温存储气体体积分数时,需扣除空气中CO2的含量。
2 结果与讨论
2.1 循环前后气体分析
图1 为1 号电芯45 ℃循环趋势图。

图1 1 号电芯45 ℃循环趋势图Fig.1 Cycle trend chart of No.1 cell at 45 ℃
从图1 可知,在45 ℃环境中循环200 次后,电芯的容量保持率在90%以上。
循环前后电芯产气情况如图2 所示,作为参照,循环前气体来自化成后的电芯。

图2 循环前后电芯产气情况Fig.2 Gas generation of the cell before and after cycle
文献[4]记载,电芯中H2的来源主要有4 种:①电解液和电芯极片的水分分解;②电解液溶剂还原分解反应产生的自由基;③电解液溶剂在正极氧化分解产生的R-H+在负极的还原(电位高于4.00 V);④LiC6与正负极黏结剂的过氧化反应。循环前电芯只完成了化成的首次充电,因此H2的来源仅包括前两种,发生的反应如式(1)-(4)所示:
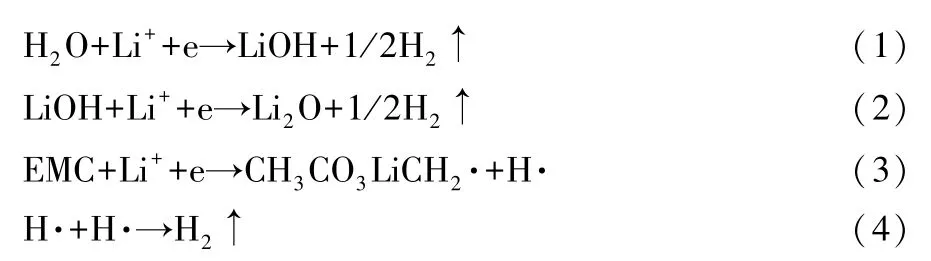
循环后电芯H2的来源与循环前基本一致。极片和电解液中的水分会在化成时全部分解,循环时无水分分解,因此循环后电芯的H2体积分数降低了1.3%,与实际情况吻合。
电芯化成后的气体,仅来源于充电时固体电解质相界面(SEI)膜形成阶段电解液溶剂在负极表面与LiC6的还原,其中CO 与CO2在EC、PC 和EMC 溶剂还原中均有生成;同时,溶剂分解特征气体中,EC 还原生成C2H4,PC 还原生成C3H6,EMC 还原生成CH4和C2H6,VC 也会分解产生少量C2H4;形成的SEI 膜厚度为纳米级别,由致密的稳态无机物层(LiF、LiCO3)和疏松多孔的亚稳态有机物层(ROCO2Li、ROLi,R 为烃烷基)组成,发生的反应如式(5)-(13)所示:

电芯经历多次充放电,会持续发生电解液溶剂在负极表面的还原及在正极表面的氧化,新出现的C2H2来自EMC 在LiFePO4呈弱氧化性条件下的氧化反应;CO2、CO、CH4和C2H6的含量略有增加,与循环中SEI 膜存在部分亚稳态有机物层的分解和EMC 参与的SEI 膜修复有关,符合实际情况;VC 在SEI 膜成膜阶段基本分解完成,因此在循环过程中,C2H4含量略有降低。气体成分在循环前后变化不大,表明电芯在正常使用过程中,不会产生明显的气体差异。
2.2 电芯45 ℃高温存储实验气体分析
45 ℃下,电芯经不同时间存储后的产气情况见图3。
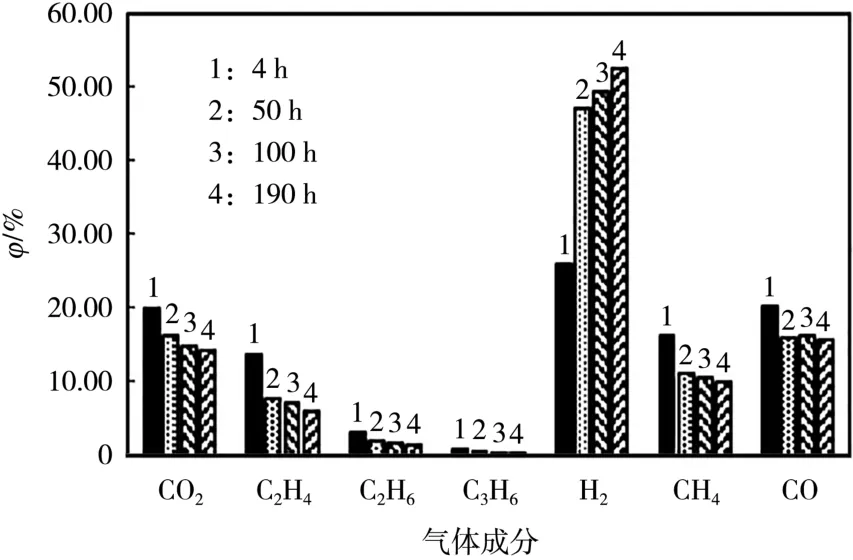
图3 存储实验电芯产气情况Fig.3 Gas generation of the cell during storage experiment
从图3 可知,45 ℃电芯满电存储未产生新气体,由于温度和电压不高,可以忽略正极氧化,气体均来自负极LiC6与电解液溶剂的还原。静置4 h,含量由高到低依次为H2、CO、CO2、CH4、C2H4、C2H6和C3H6,含碳气体来自EC 与EMC 为溶剂的电解液分解,H2则来自电解液溶剂化反应分解的自由基。CO2含量升高是由亚稳态的SEI 膜有机物层分解造成,CH4含量升高则与EMC 参与的SEI 膜修复有关。随着静置时间的延长,H2含量明显增加,但含碳气体均减少,是由于45 ℃下SEI 膜不再分解,且静置后电压逐渐下降,减缓了电解液溶剂与LiC6的还原,此时发生的是电解液溶剂的自由基转化反应,静置50 h,H2含量比静置4 h 增长近一倍。静置时间进一步延长,电压达到稳态,所有反应均达到平衡,无新反应发生,故静置190 h 与100 h 产气的含量基本一致。电芯45 ℃高温存储时,可通过H2含量是否升高作为预警。
2.3 电芯过充电实验气体分析
循环前后电芯经过充电实验后的产气情况见图4。

图4 过充电实验电芯产气情况Fig.4 Gas generation of the cell during overcharge experiment
根据H2来源分析,过充电时电压达到5.00 V 以上,故除电解液溶剂化反应的自由基之外,电解液溶剂在正极氧化分解产生的R-H+在负极的还原,是H2的主要来源;同时,负极石墨锂化程度提高,不能忽略锂金属与正极黏结剂聚偏氟乙烯(PVDF)和负极黏结剂丁苯橡胶(SBR)/聚甲基纤维素钠(CMC)的产氢反应;其中,锂金属与PVDF 的反应为:
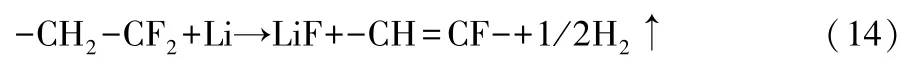
过充电时,锂金属枝晶会与电解液发生一系列的化学反应,加速内部产热和产气。当温度达到60 ℃时,会加速电解液分解放热,造成电芯温度迅速上升;当温度达到100 ℃时,会消耗大量的锂;随着温度升高到120 ℃,SEI 膜中的亚稳态有机物层物质全部分解为无机物,生成CO2;待温度上升到130 ℃以上,电芯隔膜开始发生热缩和熔化,此时产生的电芯内部局部微短路,会发生电解液溶剂的分解,生成C3H8[5],如式(15)-(20)所示。

过充电时,电芯会产生一定的CO2;循环后,CO2含量有所降低,与循环过程中电芯SEI 膜逐步重组修复时,部分有机物转化为无机物有关;CH4、C2H6和C3H8含量的提高,均来自电解液溶剂EMC 的分解。电芯循环中的过充预警依据,可参考是否会产生含量更高的CH4、C2H6和C3H8等气体。
2.4 热箱实验电芯气体分析
图5 为电芯在130 ℃/150 ℃热箱中搁置30 min 的产气情况。
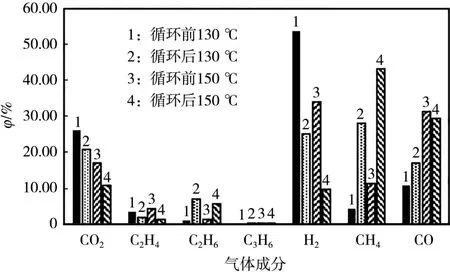
图5 130 ℃和150 ℃热箱实验电芯产气情况Fig.5 Gas generation of the cell during hot box experiments at 130 ℃ and 150 ℃
从图5 可知,在130 ℃和150 ℃下,电芯分别处于微短路和轻度短路状态,会产生大量CO2。在130 ℃下搁置循环后,电芯的H2、CO2含量较循环前下降。CO2含量下降与循环时SEI 膜修复消耗有机物层有关;H2含量下降是由于高活性下溶剂化反应产生的自由基减少。在130 ℃下搁置循环后,电芯的C2H6、CH4和CO 含量明显升高,是因为电芯处在微短路状态,且温度较高,溶剂化反应活性强。CO 含量增加与EMC参与SEI 膜的修复有关;CH4与C2H6含量增加来自EMC 还原。在150 ℃下,搁置电芯处于轻度短路状态,产气特征与130 ℃一致,循环后电芯的CO2、H2和C2H4含量明显降低,C2H6、CH4含量明显增加;由于在150 ℃时电芯基本上不再发生SEI 膜修复,循环前后CO 含量差异不大。循环后电芯的130 ℃/150 ℃热箱测试,CH4含量迅速增加可作为预警条件。
2.5 短路实验电芯气体分析
循环前后电芯短路测试后产气情况见图6。

图6 短路实验电芯产气情况Fig.6 Gas generation of the cell during short circuit experiment
从图6 可知,短路后电芯产气成分与过充电实验一致。循环后电芯气体的CO2、H2和CO 含量相对循环前有所降低,影响因素分别为循环过程中SEI 膜有机物层的重组分解消耗、高活性下溶剂化反应自由基减少及EMC 不再参与SEI膜修复;C2H4、C2H6、C3H6和CH4含量有所增加,表明高活性下电解液溶剂EC、PC 与EMC 会加剧分解。循环后电芯短路时,可通过C2H6、C3H6和CH4含量是否升高作为预警。
3 结论
对LiFePO4/石墨电芯在失控过程中的产气成分进行分析,发现电解液溶剂的正极氧化和负极还原是产气的主因。电芯正常充放电,产气主要为H2、CO 和C2H4,循环后除产生少量氧化性气体C2H2外,其他气体成分和含量与循环前差别不大。电芯经过充电、45 ℃高温存储、130 ℃/150 ℃热箱和短路等测试后,CO2含量均显著增加,且有机烃类气体和无机CO 等气体含量也发生变化。在45 ℃下,随着存储时间的延长,H2含量逐渐增加,而含碳气体含量逐渐降低;与循环前相比,循环后电芯在过充电时产生更多的CH4、C2H6和C3H8;在130 ℃热箱实验中,H2含量降低,C2H6、CH4和CO含量升高,150 ℃热箱实验的产气趋势与130 ℃热箱实验基本一致,但CO 含量变化较小;短路实验中,C2H6、C3H6和CH4含量均升高。以上结果,可作为电芯失控条件下安全预警的检测依据。
