贝伐珠单抗联合放疗治疗肺癌脑转移的临床疗效及对患者免疫功能、肿瘤标志物的影响
2022-11-08杨海林白英伟魏少贤席颖
杨海林,白英伟,魏少贤,席颖
濮阳市油田总医院1放疗科,2普通外科,河南 濮阳 457000
肺癌是常见恶性肿瘤之一,具有较高的发病率和病死率[1-2]。随着治疗方法的不断改进,肺癌患者的生存期也逐渐延长,但远处转移的风险也明显增加,特别是脑转移,可达23%~65%[3]。多数脑转移会引起瘤周水肿,使颅内压升高,并可能在短时间内引发脑疝,导致患者呼吸和心搏骤停,加速患者死亡,因此,若不采取积极有效的治疗措施,多数脑转移患者的生存时间约为3个月,少数患者可达12个月[4-5]。目前,临床常采用全脑放疗治疗肺癌脑转移,可有效改善单发转移瘤患者的生存期,但预后效果仍较差[6]。贝伐珠单抗是一种重组人源化单克隆抗体,能够抑制肿瘤组织血管内皮细胞的有丝分裂,干扰肿瘤组织新生血管生成,破坏机体现存血管,使肿瘤细胞缺血缺氧,从而发挥抗肿瘤效果[7]。目前,贝伐珠单抗联合放疗或化疗的效果尚未在肺癌脑转移患者中证实,因此,本研究旨在探讨贝伐珠单抗联合放疗对肺癌脑转移患者的肿瘤标志物、免疫功能等的影响,以期为此类患者提供更好的治疗,现报道如下。
1 资料与方法
1.1 一般资料
选取2015年1月至2018年12月濮阳市油田总医院收治的肺癌脑转移患者。纳入标准:①经CT等影像学检查和病理检查证实为肺癌脑转移;②年龄≥18岁;③生存时间≥3个月;④未合并其他恶性肿瘤;⑤临床资料完整。排除标准:①合并心、肝、肾等严重疾病;②有颅内出血倾向;③既往接受过类似治疗。依据纳入和排除标准,本研究共纳入80例肺癌脑转移患者,依据治疗方案的不同分为观察组(n=44)和对照组(n=36),对照组患者给予单纯放疗,观察组患者给予贝伐珠单抗联合放疗。对照组中,男20例,女16例;≤60岁25例,>60岁11例;病理类型:腺癌28例,鳞状细胞癌8例;脑内病灶数目:≤3个11例,>3个25例。观察组中,男27例,女17例;≤60岁26例,>60岁18例;病理类型:腺癌32例,鳞状细胞癌12例;脑内病灶数目:≤3个14例,>3个30例。两组患者性别、年龄、病理类型和脑内病灶数目比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准通过,所有患者均知情同意并签署知情同意书。
1.2 治疗方法
对照组患者给予单纯放疗,根据患者临床症状给予甘露醇1~3次/天或地塞米松1次/天。采用elekta versa-HDTM电子直线加速器,6MV-X线进行等中心全脑放疗,照射剂量每次3 Gy,每周5次,共放疗4周。观察组患者在对照组的基础上,在放疗中或放疗结束后给予贝伐珠单抗5 mg/kg,每2周1次,治疗2次。
1.3 观察指标和评价标准
①依据实体瘤疗效评价标准[8]评估两组患者的临床疗效:完全缓解(complete response,CR),所有目标病灶消失,至少持续4周;部分缓解(partial response,PR),基线病灶长径总和缩小≥30%,至少持续4周;疾病稳定(stable disease,SD),基线病灶长径总和缩小<30%或增大<20%;疾病进展(progressive disease,PD),基线病灶长径总和增大≥20%或出现新病灶。客观缓解率=(PR+CR)例数/总例数×100%,疾病控制率=(PR+CR+SD)例数/总例数×100%。②治疗前和治疗后1周,抽取两组患者静脉血5 ml,3000 r/min离心10 min,分离血清,采用流式细胞仪检测两组患者免疫功能指标,包括 CD3+、CD4+、CD8+,计算 CD4+/CD8+。③治疗前和治疗后1周,比较两组患者肿瘤标志物水平,包括癌胚抗原(carcinoembryonic antigen,CEA)、甲胎蛋白(α-fetal protein,AFP)及神经元特异性烯醇化酶(neuron specific enolase,NSE)。正常参考值范围:CEA 为 0~5.0 ng/ml,AFP 为 0~20.0 ng/ml,NSE为0~16.3 ng/ml。④比较治疗期间两组患者的不良反应发生情况,包括胃肠道反应、静脉血栓栓塞、高血压、蛋白尿、颅内出血。⑤采用电话、门诊复查等方式对两组患者进行为期2年的随访,随访时间截至2020年12月,比较两组患者的总生存期(overall survival,OS)。
1.4 统计学方法
采用SPSS 22.0软件对所有数据进行统计分析,计量资料以均数±标准差(±s)表示,组间比较采用两独立样本t检验,组内比较采用配对t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验;采用Kaplan-Meier法绘制生存曲线,组间比较采用Log-rank检验;以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效的比较
观察组患者的客观缓解率为81.82%(36/44),高于对照组患者的58.33%(21/36),差异有统计学意义(χ2=5.331,P=0.021);观察组患者的疾病控制率为95.45%(42/44),明显高于对照组患者的75.00%(27/36),差异有统计学意义(χ2=6.985,P=0.008)。年龄≤60岁与>60岁观察组患者的客观缓解率分别为80.77%(21/26)和83.33%(15/18),与对照组患者的60.00%(15/25)和 54.55%(6/11)比较,差异均无统计学意义(χ2=2.648、1.575,P>0.05)。(表1、表2)
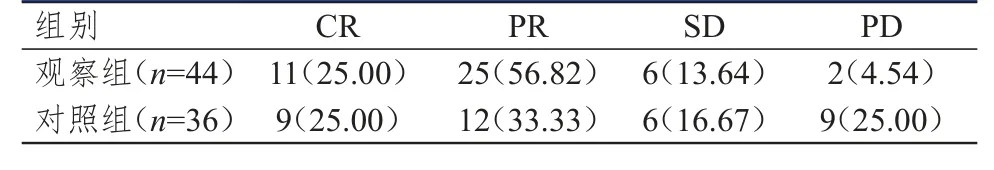
表1 两组患者的临床疗效[n(%)]
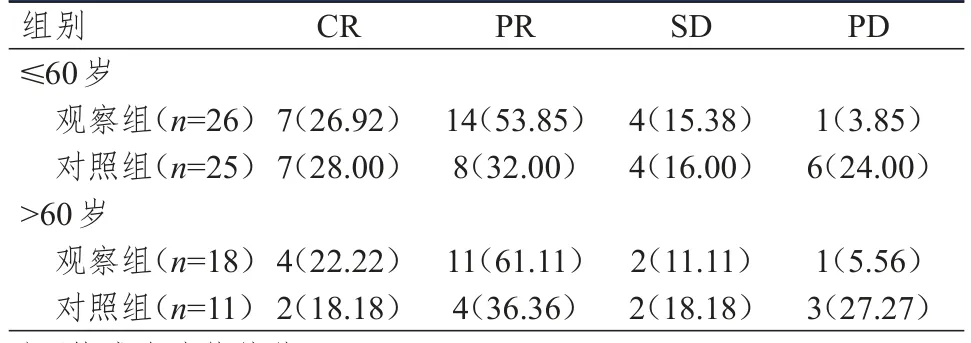
表2 不同年龄两组患者的临床疗效[n(%)]*
2.2 免疫功能指标的比较
治疗前,两组患者 CD3+、CD4+、CD8+水平和CD4+/CD8+比较,差异均无统计学意义(P>0.05)。治疗后,两组患者CD3+、CD4+水平和 CD4+/CD8+均低于本组治疗前,CD8+水平均高于本组治疗前,且观察组患者CD3+、CD4+水平和CD4+/CD8+均高于对照组,CD8+水平低于对照组,差异均有统计学意义(P<0.05)。(表3)
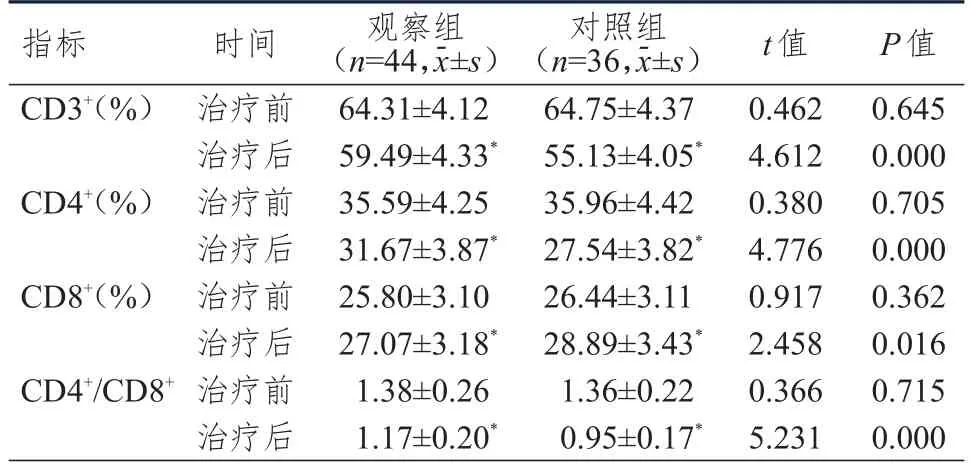
表3 治疗前后两组患者免疫功能指标的比较
2.3 肿瘤标志物水平的比较
治疗前,两组患者CEA、AFP、NSE水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者CEA、AFP、NSE水平均明显低于本组治疗前,且观察组患者CEA、AFP、NSE水平均明显低于对照组,差异均有统计学意义(P<0.01)。(表4)
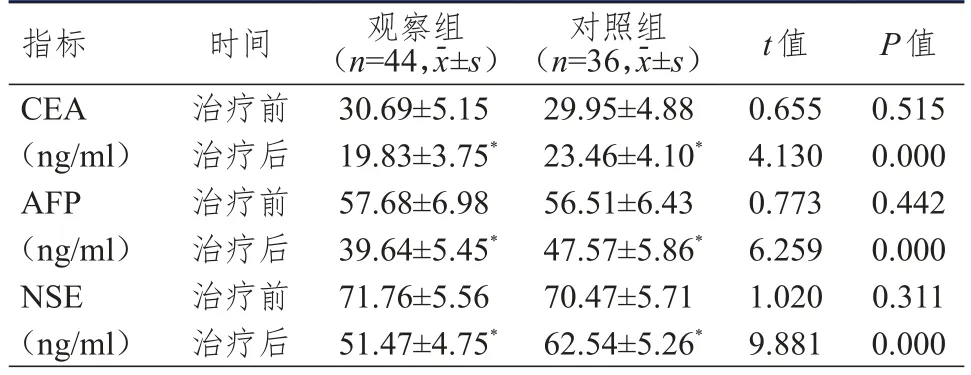
表4 治疗前后两组患者肿瘤标志物水平的比较
2.4 不良反应发生情况的比较
观察组患者的不良反应总发生率为29.55%(13/44),与对照组患者的19.44%(7/36)比较,差异无统计学意义(χ2=1.077,P=0.299)。(表5)
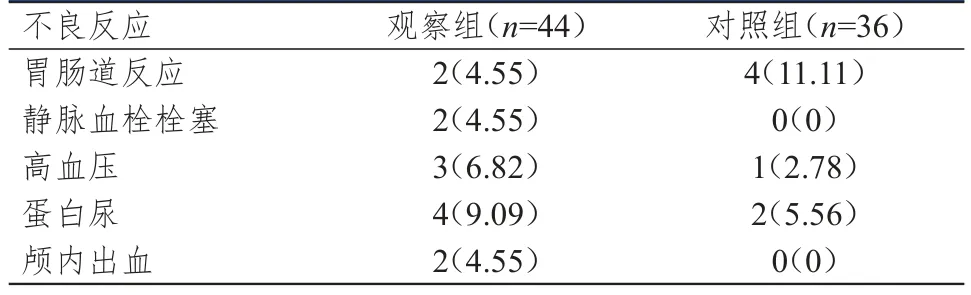
表5 两组患者的不良反应发生情况[n(%)]
2.5 生存情况的比较
随访2年,观察组患者的中位OS为16.0个月,2年总生存率为27.27%;对照组患者的中位OS为11.0个月,2年总生存率为16.67%;观察组患者的2年总生存率高于对照组,差异有统计学意义(χ2=9.357,P<0.05)。(图1)

图1 观察组(n=44)和对照组(n=36)肺癌患者的OS曲线
3 讨论
肺癌脑转移的标准治疗方法是放疗,能明显改善患者的神经系统症状,提高生活质量,延长生存时间[9]。脑转移瘤会破坏血脑屏障,而放疗会增加毛细血管内皮细胞膜的通透性,加剧血脑屏障的损伤,此外,多数患者还会出现脑水肿和瘤周水肿加重的情况,严重影响患者的预后[10]。相关研究指出,贝伐珠单抗能够降低血管通透性,减少水肿形成[11]。本研究探讨贝伐珠单抗联合放疗治疗肺癌脑转移的临床疗效及安全性,以期能够为此类患者提供更好的治疗。
本研究结果显示,观察组患者的客观缓解率和疾病控制率分别为81.82%和95.45%,均高于对照组患者的58.33%和75.00%,表明贝伐珠单抗联合放疗比单一放疗的治疗效果更佳,疾病控制更加稳定。这可能是因为贝伐珠单抗是一种人源化血管内皮生长因子的单克隆抗体,能够结合游离的血管内皮生长因子,阻断其通路,从而能够抑制肿瘤新生血管生成,改变肿瘤微环境,抑制肿瘤细胞增殖和迁移,疗效确切[12]。同时,本研究结果显示,年龄≤60岁与>60岁观察组患者的客观缓解率分别为80.77%和83.33%,与对照组患者的60.00%和54.55%比较,差异均无统计学意义(P>0.05),提示不同年龄段不会影响两种治疗方案的疗效。
肿瘤的发生、进展和转移均与患者的免疫功能密切相关,因此,免疫功能也是评估肿瘤治疗疗效的重要指标[13]。肺癌脑转移患者的免疫功能受到明显抑制,免疫功能低下,使机体抗肿瘤能力也明显下降[14]。本研究结果显示,治疗后,两组患者CD3+、CD4+水平和CD4+/CD8+均低于本组治疗前,CD8+水平均高于本组治疗前,且观察组患者CD3+、CD4+水平和 CD4+/CD8+均高于对照组,CD8+水平低于对照组,提示两种治疗方法均可使患者的免疫功能受到一定损伤,而贝伐珠单抗在一定程度保护了患者的免疫功能,与周芳等[15]的研究结果一致。
肿瘤标志物是肿瘤细胞或组织自身释放的某种物质进入人体血液和淋巴液中,常见的肺癌脑转移的肿瘤标志物有CEA、AFP及NSE[16]。健康人体中CEA基因在上皮细胞腺腔面的刷状缘上表达,发生癌变后,CEA基因的表达明显上调[17]。AFP是一种与肿瘤相关的糖蛋白,癌变后血清AFP水平会急剧升高[18]。NSE是一种γγ型烯醇化酶,主要存在于神经元、神经内分泌细胞等,对肺癌的诊断具有较高的特异度和灵敏度[19]。本研究结果显示,治疗后,两组患者CEA、AFP、NSE水平均明显低于本组治疗前,且观察组患者CEA、AFP、NSE水平均明显低于对照组,差异均有统计学意义(P<0.01)。这两种治疗方案均可降低患者的血清肿瘤标志物水平,而贝伐珠单抗联合放疗对降低肿瘤标志物水平的效果更显著,这与贝伐珠单抗的抗肿瘤作用有关,与王霞等[20]的研究结果一致。
肺癌脑转移放疗联合或不联合贝伐珠单抗治疗期间的不良反应主要包括胃肠道反应、静脉血栓栓塞、高血压、蛋白尿、颅内出血,本研究结果显示,观察组患者的不良反应总发生率为29.55%,略高于对照组患者的19.44%,但差异无统计学意义(P>0.05),说明贝伐珠单抗在一定程度上安全性较好。此外,本研究结果显示,观察组中位生存时间为16.0个月,2年生存率为27.27%;对照组中位生存时间为11.0个月,2年生存率为16.67%,提示贝伐珠单抗联合放疗能显著延长患者的生存期。
综上所述,与单一放疗相比,贝伐珠单抗联合放疗可有效改善肺癌脑转移患者的临床疗效,缓解细胞免疫功能损伤,降低血清肿瘤标志物水平,不良反应轻微,延长生存期。但本研究为单中心回顾性分析,样本量也较小,且贝伐珠单抗和放疗是否有协同作用尚未明确,下一步可开展前瞻性、多中心的大样本量研究,以得到更为确切的结论。
