老年患者非体外循环冠状动脉搭桥联合肺肿瘤切除的围手术期疗效分析
2022-11-06刘欢陆小虎刘翔王晓伟
刘欢 陆小虎 刘翔 王晓伟
由于经济发展和生活习惯的改变,肺部肿瘤合并冠状动脉粥样硬化性心脏病(冠心病)的老年患者逐渐增加,如吸烟既是肺部肿瘤的危险因素,也可促进冠心病的发生和进展[1]。当同时患有冠心病和肺部肿瘤时,如何进行手术治疗仍有争议。若分阶段施行手术,先行肺肿瘤切除可能因为冠心病无法耐受手术,增加风险。而先行冠心病手术治疗,因术后需抗血小板治疗可能导致肺部手术出血风险增加,或因延迟手术导致肺部肿瘤扩散[2]。限于病例数较少,目前有关老年患者同期行冠心病和肺部肿瘤治疗的疗效及安全性的临床研究仍较缺乏。本文对2018 至2020 年于我科就诊并同期行非体外循环冠状动脉搭桥(OPCAB)联合肺肿瘤切除治疗的21 例患者行回顾性分析,并与同期行单纯OPCAB 治疗的患者对比,评估联合手术的安全性及有效性,为临床诊疗决策提供参考。
1 对象与方法
1.1 研究对象
采用回顾性研究,选取2018 年1 月至2020 年12 月于南京医科大学第一附属医院心脏大血管外科同期行OPCAB 联合肺肿瘤切除治疗的老年患者21 例作为联合手术组,其中男性14 例,女性7例,平均年龄(69.6±5.3)岁。选择年龄、性别匹配,且同期行单纯OPCAB 治疗的患者65 例作为对照组,其中男性44 例,女性21 例,平均年龄(70.4±6.2)岁。所有患者术前均行冠状动脉造影明确冠心病诊断,胸部CT 明确肺部占位情况,必要时行PET-CT 排除肿瘤转移。纳入标准:(1)年龄≥60 周岁;(2)冠状动脉造影诊断为单支或多支冠状动脉严重狭窄病变(狭窄程度≥70%);(3)胸部CT 检查明确肺部占位有手术指征。排除标准:(1)合并严重脏器功能不全,不能耐受手术;(2)急性心肌梗死,近3 个月内脑梗死;(3)肺部肿瘤已转移,无手术指征。
1.2 手术方法
联合手术组依据冠状动脉狭窄及肺部肿瘤位置选择合适的手术体位,采用双腔气管插管;对照组采用单腔气管插管。开胸后以1 mg/kg 行肝素化,联合手术组取左侧乳内动脉及大隐静脉备桥血管,对照组常规采用左侧乳内动脉和大隐静脉,多根动脉化搭桥同时选择左桡动脉备桥血管。
对照组行常规OPCAB,手术完成后即止血关胸。联合手术组在完成OPCAB 后先关闭心包保护桥血管,鱼精蛋白充分中和肝素,观察患者血流动力学状况,再决定是否继续进行肺部手术。单纯正中或左后外侧切口继续打开胸膜腔行肺部肿瘤切除,正中+侧卧切口则在完全关闭胸部切口后变换体位,再行肺部肿瘤切除,其中楔形切除要求切缘距离肿块>2 cm。术中肿瘤切除标本送快速病理检测,根据结果决定是否需扩大切除范围及淋巴结清扫。
1.3 统计学分析
采用SPSS 19.0 统计软件进行数据分析处理,计量资料以均数±标准差表示,比较采用t检验,计数资料以例数(百分比)表示,比较采用卡方检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 基本临床资料
21 例联合手术组患者术前胸部CT 诊断为磨玻璃结节10 例,软组织或实性结节11 例,肿块直径0.8~5.0 cm,PET-CT 排除肿瘤转移,术前肺肿瘤TNM 分期为ⅠA1 例、ⅠB9 例、ⅠC7 例、ⅡA3 例、ⅡB1 例。
2 组患者术前年龄、性别、体质量指数(BMI)、纽约心脏病协会(NYHA)心功能分级、高血压史、糖尿病史、经皮冠状动脉介入术(PCI)史、吸烟史、饮酒史、左室射血分数(LVEF)、左主干病变比例差异均无统计学意义(P>0.05),但对照组3 支病变比例显著高于联合手术组(70.8% 对 28.6%,P=0.001),见表1。
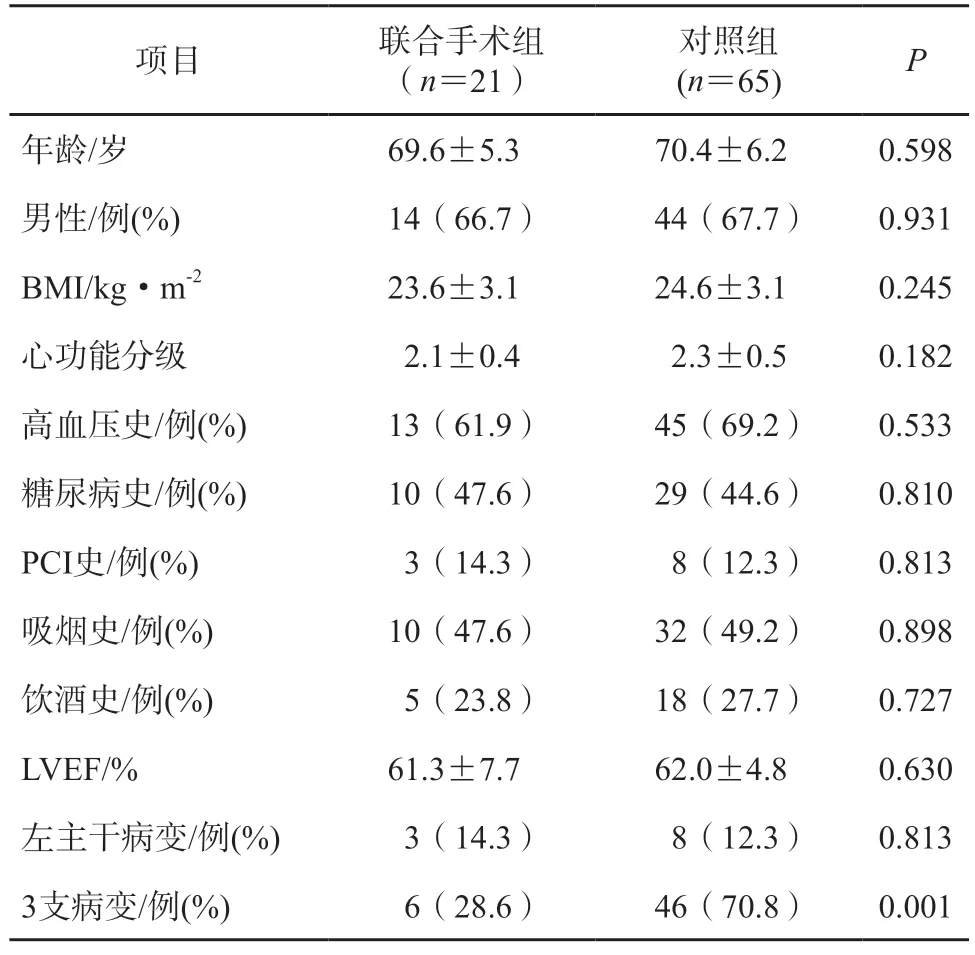
表1 2组一般情况对比
2.2 手术相关临床指标比较
联合手术组21 例患者均顺利同期完成OPCAB 及肺肿瘤切除手术,体位选择单纯正中位11 例,正中+侧卧位6 例,单纯左后外侧位4 例;肺楔形切除8 例、肺叶切除12 例、楔形联合肺叶切除1 例。术后病理诊断浸润性腺癌15 例、鳞状细胞癌3 例、良性病变3 例。
联合手术组的手术时间较对照组明显延长,联合手术组搭桥数目少于对照组,且全静脉搭桥比例明显增高。全动脉搭桥比例、术后24 h 引流量、呼吸机时间、术后住院时间差异均无统计学意义,见表2。
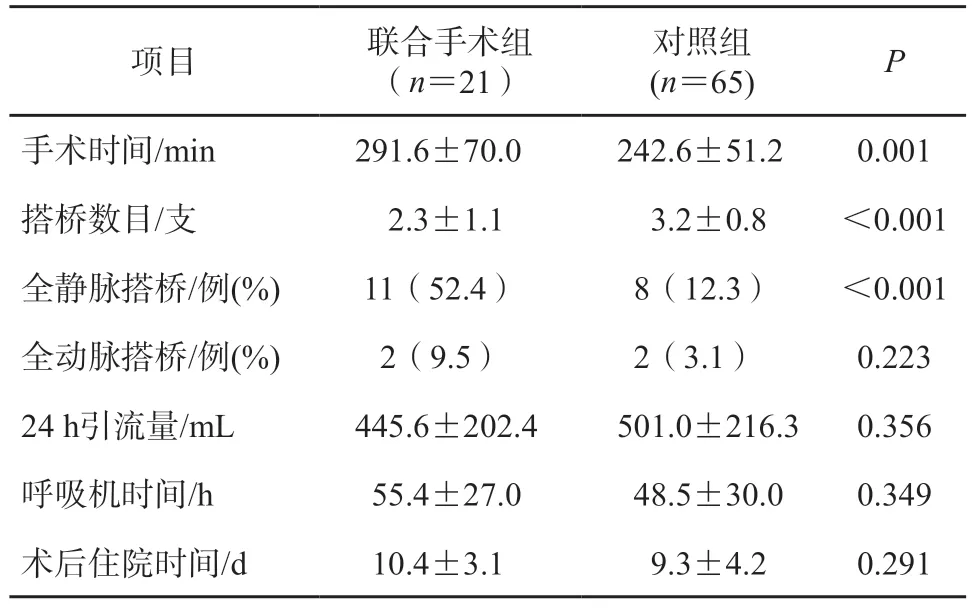
表2 两组手术相关临床指标对比
2.3 术后并发症
联合手术组与对照组在术后肺部感染、二次气管插管、透析、主动脉球囊反搏(IABP)植入、体外膜肺氧合(ECMO)治疗等方面的差异均无统计学意义(P均>0.05)。联合手术组1 例患者术后出现心脏骤停,经抢救后康复出院,无死亡病例。对照组1 例患者术后因多器官功能衰竭,经抢救无效死亡,1 例患者术后行ECMO 支持,后家属放弃治疗而死亡,见表3。
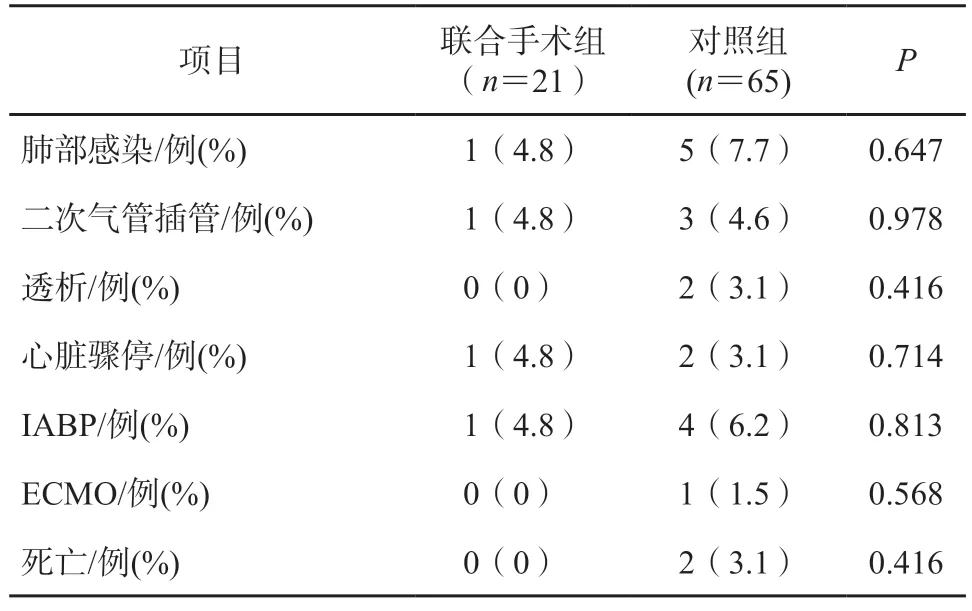
表3 两组手术并发症对比
3 讨论
冠心病合并肺部肿瘤的手术治疗目前仍有争议,若手术分阶段进行,无论是采用介入或是外科手术治疗冠心病后,患者均需进行一段时间的抗血小板治疗,再行肺部肿瘤切除,可能延误病情,使肿瘤恶化。若选择同期行手术治疗,并发症发生风险可能更高。本研究结果显示,联合手术组与对照组的围手术期疗效相当。联合手术组3 支病变数、搭桥数目相对较少,且全静脉搭桥比例高,患者的冠心病病变程度较对照组轻。在选择手术方式时,为减少手术时间、降低手术难度和风险,超过半数的患者采用了全静脉搭桥。虽然联合手术组手术时间较长,但患者术后恢复时间与并发症发生风险与对照组均无明显差异。已有相关研究表明,同期行心脏手术联合肺肿瘤切除术是安全、有效的手术方式[3],对于50 岁以上患者同期施行OPCAB 联合肺肿瘤切术也安全有效[4]。本研究对象均为60 岁以上老年患者,进一步证实了上述研究结果。
本研究所有OPCAB 操作均在非体外循环下完成。若采用传统体外循环下冠状动脉搭桥术(CCAB),可能导致肿瘤细胞通过体外循环转移扩散,如果必需采用CCAB,建议先行肺肿瘤切除,再行搭桥手术[5]。体外循环手术需要使用更大剂量的肝素抗凝,且管道对血小板功能有破坏,在同期行肺肿瘤手术时,肺部出血的风险也相应增加[6]。虽然采用CCAB 时,静止的心脏和无血的操作视野可使再血管化操作更为准确[7],但OPCAB 可能减少出血、肾功能不全、脑血管事件等并发症的发生率[8]。有研究表明,施行心脏手术及肺切除联合手术时,避免体外循环操作可以减少失血及术后气管插管时间[9]。因此,对于冠心病合并肺部肿瘤,我们建议选择OPCAB。
本研究肺部肿瘤的诊断主要依靠胸部CT 和全身PET-CT 检查,21 例患者术后病理有3 例为良性病变,这3 例良性病变术前病灶的胸部CT 描述均为实性结节伴(或不伴)毛刺,余病变CT 均准确诊断,确诊率85.7%。术前应根据患者肿块位置、大小及冠状动脉病变决定手术体位。单纯正中体位手术创伤小,可避免术中体位变化,但正中切口暴露相对困难,不便进行系统性淋巴结清扫及肺叶切除,尤其左下肺叶肿瘤较为困难。采用打开右侧胸膜及通过心包将心脏往右侧牵拉可协助操作,也有研究建议对于Ⅰ期和Ⅱ期非小细胞肺癌可采用选择性淋巴结清扫即可[10]。若左冠状动脉系统病变合并左肺肿瘤可采用左后外侧切口,对于难以行单一切口完成的同期手术,可术中变换体位进行。术中应根据快速病理结果,决定是否需要行肿瘤根治术。如果心脏手术后患者血流动力学不稳定,应避免强行同期肺肿瘤切除。我们在收集研究对象资料时,有2 例因未能成功行同期手术治疗而转为分期手术,未纳入本研究。
也有研究选择先行肺部肿瘤切除,再同期行冠心病手术治疗。一些患者由于肺部肿瘤大小、位置、胸膜粘连、使用双侧乳内动脉等因素,若先行OPCAB,可能在后续行肺手术时会损伤桥血管。然而,冠心病合并肺部肿瘤的患者,在未先行冠心病治疗前,侧卧位可能影响血流动力学稳定,并且创伤大的胸部手术可能诱发心肌缺血甚至心肌梗死,造成灾难性后果。
冠心病合并肺部肿瘤同期手术相对于单纯OPCAB 或肺肿瘤手术的风险增加,对患者的术前筛选和评估很重要,尤其对于60 岁以上的老年患者,应尽可能缩短手术时间,如采取全静脉搭桥方式。本研究未纳入明显心功能不全患者。对于病情较重,冠状动脉造影显示靶血管不佳者,采取全静脉搭桥,可降低手术操作难度,减少手术时间,避免围手术期并发症的发生。联合手术组全静脉搭桥有11 例,比例远高于行单纯OPCAB 的对照组。
本回顾性研究仍有不足之处,如患者例数较少,联合手术组冠心病严重程度相对较轻,缺乏长期随访。今后仍需纳入更多病例,进行更长时间的随访观察研究。
临床工作中冠心病合并肺部肿瘤的老年患者常面临无处求医,无法抉择的窘境。由于病情复杂,常需要心脏内科、心脏外科以及胸外科等多科室诊疗。同期施行OPCAB 联合肺肿瘤切除术对于此类患者可谓一举两得,但手术创伤大,对技术要求高。为降低手术风险及并发症发生率,应在术前对患者全面评估,依据实际情况制定个体化手术方案。
