MPN法在注射用利福平中间体需氧菌总数检测中的研究
2022-11-04王连国易大为周少彤马辉
王连国 易大为 周少彤 马辉


【关键词】利福平;中间体;需氧菌总数;MPN
利福平(Rifampicin)是利福霉素B的一种衍生物,具有抗菌力强,抗菌谱广的特性。其低浓度抑菌,高浓度杀菌,对结核杆菌、多数革兰氏阳性菌有强大快速的抗菌作用,同时对麻风杆菌、某些革兰氏阴性菌有抑制作用[1]。通常利福平被制成胶囊或片剂等口服剂型,与其他抗结核药合用协同杀菌,而注射用利福平作为利福平口服制剂的替代剂型,在病人不耐受口服治疗时使用[2]。
目前国内尚无用于利福平无菌制剂直接分装的原料药。注射用利福平的一般工藝是在利福平非无菌原料药中加入适当助溶剂,经浓配、稀释、除菌过滤、冷冻干燥而成。有文献指出,非无菌物料除菌过滤前的生物负载应尽量最小化,以防止对过滤介质的挑战,降低最终产品的品质,有必要设定预过滤中间体的微生物限度[3]。通常建议最终过滤除菌前,料液的微生物负荷不超过10 cfu/100 mL[4]。可见,未经过滤除菌的料液的生物负载,即注射用利福平中间体的微生物污染水平是注射用利福平无菌工艺过程的关键指标,关乎注射剂成品的无菌水平。因此,建立注射用利福平中间体微生物限度的检查方法具有一定的现实意义,具体研究如下。
1 试验材料
1.1 供试样品
注射用利福平中间体,批号:20201204、20201210,沈阳某药厂生产。
1.2 仪器
HFSAFE-1500 生物安全柜(上海力申科学仪器有限公司);KB240 培养箱(Binder corporation Germany);SX-700 高压灭菌器(TOMY. KOGYO. Japan);SHB-ⅢA循环水式多用真空泵(郑州长城科工贸有限公司);GN-6 Metricel Grid 滤膜及滤器(Pall corporation USA);MaxQ 4000 恒温摇床(赛默飞世尔科技有限公司);HTY-2000A集菌仪(杭州泰林生物技术设备有限公司);EVS3 全封闭式滤器(杭州泰林生物技术设备有限公司)。
1.3 菌种
枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501]、金黄色葡萄球菌(StapHylococcus aureus)[CMCC(B)26003]、铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B)10104]、大肠埃希菌(Escherichia coli)[CMCC(B)44102]、白色念珠菌(Candida albicans)[CMCC(F)98001]、黑曲霉(Aspergillus niger)[CMCC(F)98003]均由中国食品药品检定研究院提供。上述试验菌经复苏、传代,用0.9%无菌氯化钠溶液稀释制成含菌数约为10~102 cfu/ml的溶液,临用新制。
1.4 试剂
丙三醇(国药集团化学试剂有限公司,批号20160203);氯化钠(国药集团化学试剂有限公司,批号2019318)。
1.5 培养基
胰酪大豆胨液体培养基(TSB,北京三药科技开发公司,批号20200918);胰酪大豆胨琼脂培养基(TSA,北京三药科技开发公司,批号20201015);沙氏葡萄糖琼脂培养基(SDA,北京三药科技开发公司,批号20201015);SCDLP 液体培养基(北京三药科技开发公司,批号20200921)。上述培养基均为即用型成品培养基,使用前进行培养基适用性检查,均符合规定。
2 试验方法
2.1 薄膜过滤法测定需氧菌总数的验证试验
由于利福平抗细菌力很强,验证试验中每张滤膜的载药量均设置为10 mL的注射用利福平中间体,污染微生物的限度拟设定≤1 cfu/10mL。取10 mL的注射用利福平中间体,用0.9%无菌氯化钠溶液稀释至200 mL,作为供试品溶液,临用新制。
取供试品溶液200 mL 经薄膜过滤,用保温至44 ℃的含5%丙三醇的SCDLP液体培养基1000 mL冲洗滤膜滤器,每次冲洗量为100 mL,在最后一次冲洗液中加入小于100 cfu 金黄色葡萄球菌,过滤,转移滤膜,菌面朝上贴于胰酪大豆胨琼脂培养基平板上。
按上述处理方法,分别在最后一次冲洗液中加入小于100 cfu 的铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌和黑曲霉,过滤,转移滤膜,菌面朝上贴于胰酪大豆胨琼脂培养基平板上。同法测定供试品对照组及菌液对照组菌数、阴性对照。上述平板于30~35 ℃倒置培养3~5 天,观察,计数。
2.2 MPN法结合薄膜过滤法测定需氧菌总数的验证试验
本试验主要考察拟定方法去除抗菌活性成分的效果。取注射用利福平中间体30 mL,用0.9%无菌氯化钠溶液稀释至400 mL,作为供试品溶液①;取中间体3 mL,用0.9%无菌氯化钠溶液稀释至40 mL,作为供试品溶液②;取中间体0.3 mL,用0.9%无菌氯化钠溶液稀释至10 mL,作为供试品溶液③,备用。
取三联集菌器,用0.9%无菌氯化钠溶液润湿滤器及滤膜。取供试品溶液①400 mL,全部通过三联集菌器过滤。用2700 mL的含5%丙三醇的无菌SCDLP液体培养基冲洗滤器,每次每膜冲洗100 mL,在最后一次冲洗液中分别于每个滤筒中加入小于100 cfu 的金黄色葡萄球菌,过滤,每个滤筒中各加入100 mL 的胰酪大豆胨液体培养基。在30~35 ℃培养3天,观察结果。
又取MPN法供试品溶液①,按上述方法操作,分别于每个滤筒中加入小于100 cfu 的大肠埃希菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉,过滤,每个滤筒中各加入100 mL的胰酪大豆胨液体培养基。在30~35 ℃培养3 天,观察结果。
2.3 MPN法结合薄膜过滤法测定需氧菌总数的适用性试验
取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、大肠埃希菌、白色念珠菌菌液(10~102 cfu/mL)作为第一稀释级的试验菌液;继续10 倍稀释和100 倍稀释,作为第二稀释级和第三稀释级的试验菌液。
取MPN法供试品溶液①400 mL全部通过三联集菌器过滤,用2700 mL的44 ℃含5%丙三醇的无菌SCDLP 液体培养基冲洗滤器,每次每膜冲洗100 mL,各管中加100 mL胰酪大豆胨液体培养基,各管中接种第一稀释级的金黄色葡萄球菌菌液;取MPN法供试品溶液②40 mL全部通过三联集菌器过滤,用2700 mL的44 ℃含5%丙三醇的无菌SCDLP 液体培养基冲洗滤器,每次每膜冲洗100 mL,各管中加100 mL胰酪大豆胨液体培养基,各管中接种第二稀释级的金黄色葡萄球菌菌液;取MPN法供试品溶液③10 mL全部通过三联集菌器过滤,用2700 mL的44 ℃含5%丙三醇的无菌SCDLP 液体培养基冲洗滤器,每次每膜冲洗100 mL,各管中加100 mL胰酪大豆胨液体培养基,各管中接种第三稀释级的金黄色葡萄球菌菌液。
上述9 管于30~35 ℃培养3 天,观察,计数。根据微生物生长的管数,从《中国药典》2020 版“1105 非无菌产品微生物限度检查:微生物计数法”表3 试验组中查金黄色葡萄球菌的最可能数[5]。另取三套三联集菌器,各管中加100 mL胰酪大豆胨液体培养基,每一稀释级金黄色葡萄球菌菌液取3 份1 mL分别接种至100 mL胰酪大豆胨液体培养基中,于30~35 ℃培养3 天,观察,计数。根据微生物生长的管数从表3 中查菌液对照组中金黄色葡萄球菌的最可能数及对照组菌数的95%置信限。其他试验菌(大肠埃希菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌)的计数方法同金黄色葡萄球菌。
2.4 含中和剂冲洗液无毒性的证实试验
取三联集菌器,用1000 mL的含5%丙三醇的无菌SCDLP液体培养基冲洗滤器,每次每膜冲洗100 mL,在最后一次冲洗液中分别加入小于100 cfu 的试验菌,各管中加100 mL胰酪大豆胨液体培养基,在30~35 ℃培养3天,观察结果。
3 结果
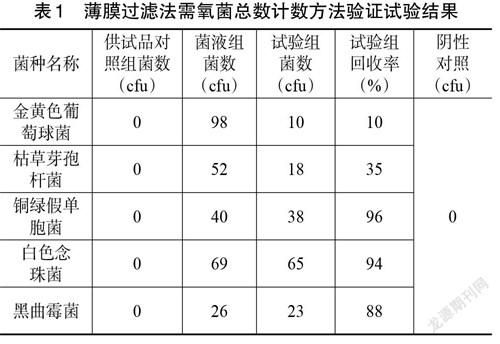
3.1 薄膜过滤法的验证试验结果
试验结果见表1。金黄色葡萄球菌和枯草芽孢杆菌试验组菌回收率均低于0.5,铜绿假单胞菌、白色念珠菌和黑曲霉试验组菌回收率在0.5~2 范围内,按照《中国药典》2020 版“1105 非无菌产品微生物限度检查:微生物计数法”供试品中微生物回收的判定原则,上述方法不适于需氧菌总数测定。
3.2 MPN法结合薄膜过滤法的验证试验结果
试验结果见表2。用2700 mL的44 ℃含5%丙三醇的无菌SCDLP液体培养基冲洗滤器9 次,各试验菌在72 h 内生长良好,可以按此方法去除抗菌活性。
3.3 MPN法结合薄膜过滤法计数方法适用性试验结果
试验结果见表3。采用MPN法结合薄膜过滤法,各试验菌的菌数均在各菌液对照组菌数的95%置信限内,可作为此品种的需氧菌总数的计数方法。
3.4 含中和剂冲洗液无毒性证实试验结果
试验结果见表4,各试验菌在规定时间内均生长良好,含5%丙三醇的无菌SCDLP液体培养基对各试验菌无毒性。
4 结果
4.1 经验证,注射用利福平中间体需氧菌总数可采用MPN法结合薄膜过滤法测定
在规定培养条件下,若供试品各浓度的试验管均无菌生长,即生长管数为0、0、0,则每100 mL中间体中污染的需氧菌总数报告值<3 cfu,该计数方法的检出限低于本品预设微生物污染最大允许值10 cfu/100 mL,可用于本品需氧菌总数测定。
4.2 注射用利福平(中间体)-微生物限度检查法正文表述
分别取本品30 mL(相当于3 份10 mL)、3 mL(相当于3 份1 mL)和0.3 mL(相当于3 份0.1 mL),分别溶于0.9%无菌氯化钠溶液400 mL、40 mL 和10 mL 中,作为供试品溶液①、②和③。
取全封闭滤器3 组,分别用0.9%无菌氯化鈉溶液润湿滤器及滤膜。取供试品溶液①,经薄膜过滤法处理,用44 ℃含5%丙三醇的无菌SCDLP液体培养基2700 mL分次冲洗,每次每膜冲洗100 mL,冲洗9 次,各管中加胰酪大豆胨液体培养基100 mL;同法处理供试品溶液②和③。按《中国药典》2020 版中规定的MPN法进行培养,记录每一稀释级微生物生长的管数,从表3 中查每100 mL 供试品中需氧菌总数的最可能数。每100 mL供试品中需氧菌总数不得过10 cfu。
5 讨论
虽然MPN 法(Most-Probable-Number Method)用于微生物计数时精确度较差,但对微生物污染量很小的供试品,MPN法可能是最适合的方法[6],比较适合本品种的限度要求。利福平对多种病原微生物均有较强抗菌活性,本品设定的微生物污染允许限又相对苛刻,这种情况下MPN法更适宜注射用利福平中间体需氧菌总数测定。
SCDLP 液体培养基中含有一定量的中和剂和表面活性剂,每1000 mL培养基中含蛋白胨20 g,氯化钠5 g,磷酸氢二钾2.5 g,葡萄糖2.5 g,卵磷脂1 g,吐温-80 7 g。冲洗液使用44 ℃含5%丙三醇的无菌SCDLP液体培养基,丙三醇有一定的助溶作用,温热的冲洗液可提高冲洗效果。
《中国药典》指出MPN法不适于霉菌计数,考虑利福平的抗菌谱中不包括霉菌,故本品仍存在霉菌污染的风险,宜参考有关研究[7],增加霉菌数检测。
