应用重庆卒中评分预测腔隙性卒中患者短期不良预后风险
2022-11-03金迪李芹吴月霞朱慧单勇刘海超王起张绿明王培福杨静
金迪,李芹,吴月霞,朱慧,单勇,刘海超,王起,张绿明,王培福,杨静
腔隙性卒中(lacunar stroke,LS)是急性缺血性脑卒中的一种常见类型,在不同人群中的发病率约15%~25%[1]。LS主要见于基底节区、放射冠和脑干,病灶直径2~20 nm,多由大脑半球或脑干深部的小穿支动脉闭塞所致。通常认为LS 的预后较为良好,但约有20%~230%的LS 患者会在起病48~72 h 内出现肢体运动功能障碍、吞咽困难或意识水平进行性加重[2]。该现象被称为早期神经功能缺损进展(early neurological deterioration,END),目前尚无有效的对因治疗方法,属于较为难治的脑血管疾病。相对于无神经功能恶化的患者,END通常具有更高的致残率[3]、更长的住院时间,严重影响患者的生存质量。因此,早期识别高风险LS人群对于预防END至关重要。
重庆卒中量表(Chongqing stroke scale,CQSS)是2021年由我国学者发表的量表,可用于预测脑卒中后出现不良预后及END 的风险[4]。该量表主要通过言语、上肢运动、下肢运动和意识水平4个项目对患者进行打分,满分11分。纳入起病24 h以内的院前急性脑梗死患者215例,首次评分>6分时更容易出现不良预后,同时有9.30%的患者出现了END,且END组在90 d的死亡率是非END 组的3 倍,提示该量表对于脑卒中的不良预后预测有较好的指导意义。由于脑卒中各个病因分型可能导致不同程度的神经功能缺损,在预后方面也存在一定差别。因此,本文拟通过CQSS 量表对LS患者进行评估,探讨该量表对出院时患者不良预后及END发作风险的预测效能。
1 资料与方法
1.1 一般资料
通过注册登记连续收集2020年6月1日至2021年5 月31 日期间在航天中心医院神经内科住院的急性LS患者。入选者需满足TOAST分型中对于小动脉闭塞型脑梗死的诊断标准[5],同时通过1.5T 或3.0T 头颅核磁检查确认存在新发梗死灶,且该梗死灶为本次卒中发作的责任病灶。排除标准为:既往脑梗死病史导致合并严重功能障碍[即改良Rankin 量表(modified Rankin Scale,mRS)≥3 分],合并载体动脉中重度狭窄,其他明确病因引起的脑梗死(如心源性栓塞、凝血功能异常、感染或免疫性血管炎等),合并其它可能导致病情加重的疾病(如重症肺炎、感染性休克、严重心功能不全等)。本研究已通过航天中心医院医学伦理委员会审查。入组者均自愿参加并签署知情同意书。
1.2 方法
1.2.1 CQSS评分 CQSS评分主要包含语言、上肢运动、下肢运动、意识水平共4个评分项目。量表具体赋值标准为:①语言:0 分=正常;1 分=轻到中度损害,表现为语言流利性和清晰度受损,尚能与他人交流;2分=与他人交流困难;3分=缄默、只能说出单个字词或无意义的音节。②上肢运动:0 分=正常;1 分=轻到中度力弱,能持物或抬臂;2分=不能持物或抬臂,但有肢体活动;3分=无自主活动。③下肢运动:0分=正常;1分=轻到中度力弱,能自主站立;2分=不能独自站立,但有肢体活动;3分=无自主活动。④意识水平:0分=清醒;1分=意识水平下降但对言语或刺痛有反应;2分=昏迷且对任何刺激无反应。
1.2.2 结局事件 由神经内科专科医生在患者出院时对其病情进行评估。①主要结局事件:出院时存在中重度残疾,即mRS≥3 分。②次要结局事件:出现END,具体包括:(a)起病7 d 内出现神经功能缺损加重,且症状持续≥24 h;(b)美国国立卫生院脑卒中量表(National Institutes of Health Stroke Scale,NIHSS)评分总分较入院时增加≥2分,或意识障碍、运动障碍评分增加≥1分,或出现新的神经系统缺损症状[6]。
1.3 统计学处理
采用EPIDATA 3.0软件进行数据收集、录入及数据库建立,采用SPSS26.0和R 4.2软件进行统计分析。符合正态分布以及方差齐性的计量资料以(±s)表示,组间比较采用独立样本均数t检验;不符合正态分布的数据以中位数和四分位间距[M(Q25,Q75)]表示,组间比较采用秩和检验;计数资料以率或构成比表示,组间比较采用χ2检验,Fisher精准检验或Cochran-Mantel-Haensze卡方检验;通过Pearson相关分析判断CQSS 和NIHSS评分的关联性;P<0.05为差异有统计学意义。
运用受试者工作特性曲线(receiver operator characteristic curve,ROC)判断CQSS 对90 d 不良预后和END 发生的预测效能分析,通过计算曲线下面积(area under the curve,AUC)判断CQSS 对上述指标的预测价值。通常认为,AUC<0.5 提示没有诊断价值,AUC 在0.5~0.7 提示具备较低的准确性,AUC >0.7具备一定的准确性,AUC值越趋近于1,诊断工具的准确性越高。使用约登指数计算截断(Cut-off)值。
2 结果
2.1 基线资料及评分
本研究共纳入满足入组要求的LS患者294例,其中男204 例(69.4%),女90 例(30.6%)。根据出院时的mRS评分分为预后不良组(mRS≥3分)58例和预后良好组(mRS<3 分)236 例;出院时无死亡病例。2 组的年龄、既往卒中病史、入院前mRS 评分差异无统计学意义(P>0.05);女性LS 患者出现预后不良的风险高于男性患者(P<0.05);预后不良组的首次CQSS 评分总分均高于预后良好组(P<0.05),但2 组CQSS 的各项目评分分值差异无统计学意义(P>0.05);预后不良组的首次NIHSS评分高于预后良好组(P<0.05);相关分析表明,首次CQSS 评分和NIHSS 评分之间存在显著的相关性(Pearson系数=0.914,P<0.001)。60 例患者在观察时间内出现END,2 组END 的发生率差异无统计学意义(P>0.05);但预后不良组CQSS评分增加的平均分数明显高于预后良好组(P<0.05);见表1、表2。
表1 预后不良组和预后良好组的临床资料[(±s)或例(%)或M(Q25,Q75)]

表1 预后不良组和预后良好组的临床资料[(±s)或例(%)或M(Q25,Q75)]
组别预后良好组预后不良组t/W/χ2值P值例数236 58年龄/岁65.51±12.09 66.75±12.77-0.66 0.50男性171(83.8)33(56.9)5.32 0.02既往卒中史60(25.4)11(20.0)0.73 0.39院前mRS评分/分0(0,0)0(0,0)6920 0.83首次NIHSS评分/分2(1,3)2(1,4)4817 0.002发生END 28(46.7)32(53.3)0.36 0.54
表2 预后不良组和预后良好组的CQSS评分[例(%)或M(Q25,Q75)或(±s)]
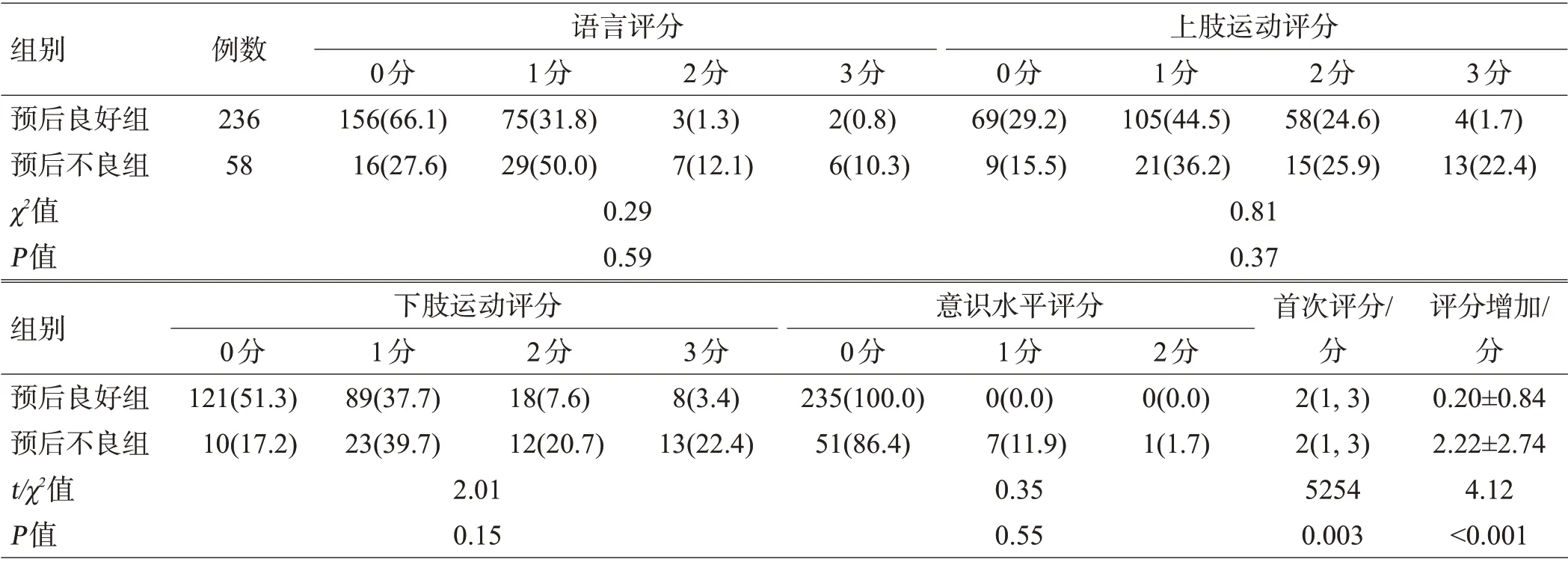
表2 预后不良组和预后良好组的CQSS评分[例(%)或M(Q25,Q75)或(±s)]
组别预后良好组预后不良组χ2值P值例数236 58语言评分0分156(66.1)16(27.6)0.29 0.59 1分75(31.8)29(50.0)2分3(1.3)7(12.1)3分2(0.8)6(10.3)上肢运动评分0分69(29.2)9(15.5)0.81 0.37 1分105(44.5)21(36.2)2分58(24.6)15(25.9)3分4(1.7)13(22.4)组别预后良好组预后不良组t/χ2值P值下肢运动评分0分121(51.3)10(17.2)2.01 0.15 1分89(37.7)23(39.7)2分18(7.6)12(20.7)3分8(3.4)13(22.4)意识水平评分0分235(100.0)51(86.4)0.35 0.55 1分0(0.0)7(11.9)2分0(0.0)1(1.7)首次评分/分2(1,3)2(1,3)5254 0.003评分增加/分0.20±0.84 2.22±2.74 4.12<0.001
2.2 CQSS对不良预后结局预测价值的ROC分析
CQSS对LS患者在出院时存在不良预后的风险具有较好的预测意义(AUC=0.760,95%CI0.692-0.829,P<0.001)。通过计算判断出Cut-off值为5分(灵敏度39.7%,特异度94.1%,约登指数0.338),提示CQSS 评分为5 分时对患者出现不良预后结局的预测效能最高,见图1。以该截断值作为分组依据,将患者分为CQSS<5分组(257例)和CQSS评分≥5分组(37例),CQSS 评分≥5 分组的不良预后发生率显著高于CQSS<5分(P<0.01),2组的END事件的发生率差异无统计学意义(P>0.05),表3。
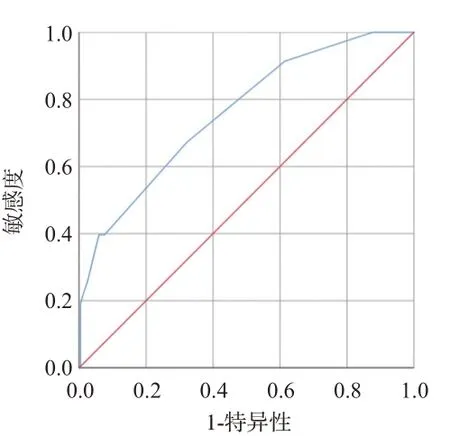
图1 CQSS预测出院时不良预后的ROC曲线

表3 不同CQSS评分的LS患者出院不良预后和END事件发生率比较/[例(%)]
2.3 CQSS对END发生预测价值的ROC分析
CQSS对出现END事件的预测准确度较低(AUC=0.613,95%CI0.538-0.689,P=0.007)。该指标的Cut-off值为2 分(灵敏度80.0%,特异度35.9%,约登指数0.159),即CQSS评分为2分时对END事件的预测效能最好,见图2。此外,对症状加重后进行再次CQSS 评分,取2 次得分的差值进行ROC 分析,可观察到其Cut-off值为1分(灵敏度55.2%,特异度91.1%,约登指数0.463),即CQSS 分数的增加对END 事件具有较好的预测效能(AUC=0.742,95%CI0.658-0.825,P<0.001)。

图2 CQSS预测END事件的ROC曲线
3 讨论
LS的不良结局严重影响患者的生活质量。CQSS评分是一项主要用于评价院前急性脑梗死患者神经功能缺损程度的量表。相对于传统的NIHSS、斯堪的纳维亚卒中量表,CQSS 的评分在保持与NIHSS 评分一致性较高的基础上,对评分项目进行一定程度的简化,仅选取言语功能、运动功能和意识水平作为最有代表性的症状。因此,该评分能够帮助医护人员快速评估患者的病情,对缺乏临床经验的使用者较友好,适合应用于院前及门急诊的快速筛查。在本研究中,首次CQSS评分和NIHSS评分之间存在显著的相关性(P<0.001),提示CQSS评分对患者临床症状的评估能力与NIHSS 评分相近,在临床工作中可以考虑将CQSS 作为卒中患者首诊时的评估工具之一。
CQSS研究认为,当患者起病时评分<6分可能会获得更好的预后(灵敏度50.0%,特异性91.9%)。在本项研究结果显示,CQSS为5分时其识别不良预后的预测效能最佳。以该得分为依据分组对比后发现,首次CQSS 评分≥5 分组的不良预后发生率显著高于CQSS<5 分组(P<0.01),这一结论与CQSS 研究基本相符。在本研究中,截断值略低于CQSS研究,这可能与本研究中纳入的病例多为临床症状较轻的LS 有关。我们的研究中剔除了合并有载体动脉中重度狭窄或闭塞的患者,而这类人群多伴有更严重的神经功能缺损以及更容易出现进展性卒中[7]。
在本研究中,20.6%的LS 患者在起病后出现了END事件,高于CQSS研究(9.3%),但与现有研究较为接近[8-10]。发病率的不同可能与对END 定义存在异质性有关。本研究选取的观察时间为起病后1 周内,故END发生率较CQSS研究更高。由于现有研究数量和样本量的限制,END的危险因素和确切机制尚不完全明确,现有研究推测主要的发病机制包括[2,11]:①责任血管的血栓不断进展、闭塞,或者是由于不稳定斑块脱落导致远端皮质分支闭塞,导致原有梗死体积的扩大或出现新的梗死;②合并糖尿病或伴有剧烈的血压波动;③炎症细胞和促炎性细胞因子释放增加;④梗死核心低灌注区域与皮质脊髓束重叠。由于END与LS患者的不良预后密切相关,因此早期筛选出END高风险患者并进行及时医疗干预十分重要。在本研究中,CQSS 预测END 的AUC 为0.613,提示其对于后者的预测价值一般,较难以通过首次CQSS评分,即单纯依靠临床症状来预测出现END的风险。因此,可能需要结合END 的发病机制、化验指标、影像学证据等多种指标来进行判断,尚需更多研究来进行更进一步的研究和探讨。
本研究存在一定的局限性。首先,本研究选择入组的病例均为LS患者,故多数患者的临床症状相对较轻,CQSS评分偏低,可能存在一定的选择偏倚。其次,部分患者在入院前已经出现症状加重,患者对于症状的评分具有主观性,故在回顾其起病时的症状评分时可能存在回忆偏倚。第三,本研究为单中心临床研究,因此在进行ROC 分析时可能存在样本量相对较少的不足,从而影响对AUC的计算和截断值的选择。后续可通过增加样本量、详细询问病史等方法提高研究的准确度。
综上所述,CQSS评分可以通过临床症状对脑卒中患者进行预后评估,评分越高,出现不良预后的风险越大,这有助于医护人员进行早期临床决策。该量表与NIHSS评分具备显著的相关性,且评分项目更加简化,能够较准确地识别在出院时可能出现不良预后的LS患者。CQSS 对于END 事件的预测效果一般,提示除考虑临床症状外,还需要结合发病机制、化验指标、影像学证据等多种指标进行综合判断,尚需要进一步研究探讨以提高对END事件的预测效能。
