酱香型酒醅中一株曲霉的鉴定及生物学特性分析
2022-11-01王新叶王永欢陈晓青罗贞标李红霞李芳香
王新叶, 王永欢, 陈晓青, 罗贞标, 李红霞, 李芳香, 赵 亮
茅台学院 酿酒工程系,贵州 仁怀 564500
酒醅是白酒发酵的主要载体基质,其微环境具有高浓度乙醇、高浓度有机酸、低pH等特点[1]。霉菌是白酒酿造过程中主要的真菌,包括曲霉(Aspergillus)、根霉(Rhizopus)、红曲霉(Monascus)等,这些优势真菌产生的糖化酶、液化酶、纤维素酶、蛋白酶、酯化酶、果胶酶、单宁酶等对分解酿酒原料中的淀粉、蛋白质等大分子物质具有积极的推动作用,使得整个反应体系中糖类及氨基酸含量升高,可为其他微生物的代谢提供物质基础,也为后续的酒体风味形成奠定基础[2,3]。同时,霉菌还可以在一定程度上利用酿酒原料中不易被分解的纤维素,在提高原料使用率上起到一定作用[4]。
曲霉是丝状真菌的一个属,包含350多个种[5]。曲霉属微生物的繁殖主要通过形成无性孢子(分生孢子)而产生称为分生孢子头的多细胞结构,而分生孢子头的形态(无性孢子的大小、颜色和排列)是曲霉属内鉴定和分类的关键参数[6,7]。曲霉属的微生物能够产生大量的代谢产物以及大量的酶,例如米曲霉可以用来生产天门冬氨酸蛋白酶[8],曲霉属的菌种已广泛应用于生物技术领域[9-11]。工业上重要的曲霉菌主要属于两大类曲霉菌——黑曲霉类和黄曲霉类。黑曲霉类包括26个种,例如鲁氏曲霉(A.luchuensis)、黑曲霉(A.niger)和管曲霉菌(A.tubingensis)[12-14]。黄曲霉菌(A.flavus)和寄生曲霉菌(A.parasiticus)能够产生黄曲霉毒素,引起侵袭性曲霉菌病或过敏性支气管肺曲霉菌病,严重影响公共卫生[15]。非黄曲霉毒素产生菌——米曲霉(A.oryzae)、大豆曲霉(A.sojae)及玉米曲霉(A.tamarii)主要用于食品发酵和酶的生产[16,17]。
在本研究中,从酱香型酒醅中分离筛选得到了一株霉菌,通过形态学和分子生物学对菌株进行了鉴定,对菌株的纤维素酶等七种胞外酶产生能力及环境耐受性进行了测定,并用GC-MS测定了菌株的代谢产物,为菌种的潜在应用提供了参考。
1 材料与方法
1.1 材料
酱香型酒醅(贵州省仁怀市红土地酿酒作坊)。
1.2 培养基
(1) 马铃薯葡萄糖琼脂(Potato Dextrose Agar,PDA)培养基:马铃薯200 g,蔗糖20 g,蒸馏水1 000 mL,pH 5.5~6.0。
(2) 糊精培养基:糊精20 g,硝酸钠3 g,氯化钾0.5 g,磷酸氢二钾1 g,七水合硫酸亚铁0.01 g,七水合硫酸镁5 g,蒸馏水1 000 mL,pH 6.5。
(3) 改良葡萄糖酵母浸粉蛋白胨(Glucose Yeast Extract Peptone,GYP)培养基:可溶性淀粉2 g,葡萄糖1 g,酵母膏0.1 g,蛋白胨0.5 g,琼脂20 g,蒸馏水1 000 mL,pH 5.5~6.0。
(4) 改良酵母提取物和胰蛋白胨(Yeast Extract and Tryptone,YP)培养基:羧甲基纤维素钠5 g,酵母膏0.1 g,蛋白胨0.5 g,琼脂20 g,水1 000 mL,pH 5.5~6.0。
(5) 改良酪素培养基:磷酸二氢钾0.003 6 g,硫酸亚铁0.000 02 g,磷酸氢二钠0.010 7 g,胰蛋白胨0.000 05 g,硫酸镁0.005 g,干酪素0.04 g,CaCl20.000 2 g,氯化钠0.001 6 g,氯化锌0.001 4 g,琼脂20 g,蒸馏水1 000 mL,pH 6.5。
(6) 改良PDA培养基:马铃薯200 g,蔗糖20 g,三丁酸甘油酯4 g,琼脂20 g,蒸馏水1 000 mL,pH 6.5。
(7) 果胶酶产生培养基:酵母膏1 g,果胶5 g,琼脂20 g,蒸馏水1 000 mL,pH 5.5~6.0。
(8) 改良马丁氏培养基:葡萄糖10 g,蛋白胨5 g,磷酸二氢钾1 g,七水合硫酸镁0.5 g,琼脂20 g,蒸馏水1 000 mL,pH 6.5。
(9) 环境耐受性检测培养基,基础培养基为YPD培养基,根据需要加入乙醇或乳酸。
(10) 镇达等培养基[18]:乳酸5 g,酵母膏2 g,硫酸铵2 g,磷酸氢二钠14.3 g,磷酸二氢钾3 g,水合硫酸锰0.28 mg,七水合硫酸亚铁0.3 mg,七水合硫酸镁0.06 mg,氯化钙1 mg,硫酸铜0.05 mg,硫酸锌0.05 mg,硼酸0.05 mg,1 000 mL蒸馏水。
1.3 菌株的分离纯化
称取10 g酱香型酒醅加入到90 mL无菌水中,震荡30 min。静置5 min,吸取上清液1 mL加入到9 mL无菌水中,作为10-1。将菌悬液进行逐级稀释至10-2、10-3、10-4、10-5,选取10-3、10-4、10-5三个浓度的稀释液,分别吸取100 μL涂布在PDA培养基上,每个梯度做三个重复。将平板倒置于28 ℃培养箱中,培养3 d~5 d。挑取霉菌的单个菌丝接种于新的PDA培养基上,进行纯化2~3次。
1.4 菌株的形态学鉴定
挑取霉菌的单个菌丝点接于PDA培养基上,培养3 d后,观察菌落形态。在载玻片上加一滴无菌水,挑取霉菌的菌丝在无菌水中涂布均匀,滴加一滴亚甲基蓝染色液,盖上盖玻片后,在光学显微镜下观察菌丝形态。
1.5 菌株的分子生物学鉴定
用真菌基因组DNA提取试剂盒(索莱宝,货号:D2300)提取霉菌的基因组DNA,以引物NS1(GTAGTCATATGCTTGTCTC)和NS8(TCCGCAGGTTCACCTACGGA)扩增霉菌的18S rDNA,PCR产物送上海生物工程有限公司进行测序,测序结果提交到NCBI的GenBank数据库中进行BLAST比对。下载同源性较高的已知菌株的18S rDNA序列,利用MEGA 7.0.26软件构建系统发育树。
1.6 霉菌的酶活特性分析
(1) 糖化酶:将霉菌点接于糊精培养基培养3 d~5 d后,在培养基上加入0.02 mol/L碘液,若菌落周围能够形成无色透明圈,则菌株具有糖化酶产生能力。
(2) 液化酶(α-淀粉酶):将霉菌点接于改良GYP培养基,培养3 d~5 d后,在菌落周围滴加卢戈氏碘液,若菌落边缘出现黄色透明圈,则菌株具有液化酶产生能力。
(3) 纤维素酶:将霉菌点接于改良YP培养基,培养3 d~5 d后,在菌落周围滴加0.2%刚果红溶液,放置10 min后,用1 mol/L氯化钠溶液冲洗,若菌落边缘出现黄色透明圈,则菌株具有纤维素酶产生能力。
(4) 蛋白酶:将霉菌点接于改良酪素培养基,培养3 d~5 d后,若菌落周围出现透明圈,则菌株具有蛋白酶产生能力。
(5) 酯化酶:将霉菌点接于改良PDA培养基,培养3 d~5 d后,若菌落周围出现透明圈,则菌株具有酯化酶产生能力。
(6) 果胶酶:将霉菌点接于果胶酶产生培养基,培养3 d~5 d后,在平板上滴加1%十六烷基三甲基溴化铵水溶液,若菌落周围出现透明圈,则菌株具有果胶酶产生能力。
(7) 单宁酶:吸取0.1 g/mL的单宁酸溶液1 mL,添加到改良马丁氏培养基上,涂布均匀,形成白色不透明的单宁薄层,接种霉菌,培养3 d~5 d后,若菌落周围出现透明圈,则菌株具有单宁酶产生能力。
1.7 霉菌的环境耐受性分析
(1) 温度耐受性:挑取霉菌的菌丝,用划线法接种到YPD培养基上,将平板置于4 ℃、28 ℃、37 ℃、45 ℃的恒温培养箱中,培养3 d后,观察菌株生长情况。
(2) 乙醇耐受性:配制YPD固体培养基,添加无水乙醇至体积浓度为2%、4%、6%。挑取霉菌的菌丝用划线法接种到乙醇梯度培养基上,将平板置于28 ℃的恒温培养箱,培养3 d后,观察菌株的生长情况。
(3) 乳酸耐受性:配制YPD固体培养基,添加乳酸至质量浓度为10 g/L、30 g/L和50 g/L。挑取霉菌的菌丝用划线法接种到乳酸梯度培养基上,将平板置于28 ℃的恒温培养箱中,培养3 d后,观察菌株的生长情况。
1.8 霉菌代谢产物解析
以乳酸为唯一碳源的Lu-Ye培养基为发酵培养基,150 r/min,28 ℃恒温培养3 d后,8 000 r/min离心10 min,收集上清液。将上清液用0.2 μm微孔滤膜过滤后,用气-质联用色谱检测发酵产物。色谱质谱检测条件为色谱柱:安捷伦DB-5,30 m×0.32 mm,0.25 μm;载气:氦气;流速:1.8 mL/min,分流比=5∶1;升温程序:40 ℃,保持4 min;10 ℃/min升至100 ℃,保持0 min;25 ℃/min升至200 ℃,保持0 min;前进样口温度:150 ℃;离子源温度:230 ℃;四极杆温度:150 ℃;进样量:1 μL;Mass Range:20m/z~150m/z;离子源:EI;扫描方式:SIM/SCA。
1.9 数据分析
采用Excel统计分析实验过程获得的数据。
2 结果与讨论
2.1 霉菌的筛选和鉴定
(1) 形态学鉴定
以PDA为筛选培养基,从酱香型酒醅中筛选得到1株霉菌JP7。该菌株在PDA平板上生长良好,生长3 d后,能够形成较大的菌落,菌落表面微皱、干燥,不透明,边缘不整齐,菌落内部为黄绿色,边缘为灰白色,菌落于培养基连接紧密,不易挑起。
在显微镜下观察到霉菌JP7的菌丝分支较少,分生孢子头呈菊花状,分生孢子头上着生球形或近球形的孢子,如图1所示。

图1 霉菌JP7的显微形态观察
(2) 霉菌的分子生物学鉴定
如图2所示,基于18S rDNA序列的系统发育分析,JP7与AspergillusversicolorNRRL 238聚称1簇,两株菌的同源性最高,且两株菌的18S rDNA序列相似性为99.69%,因此将JP7归属于Aspergillusversicolor,将JP7命名为AspergillusversicolorJP7。
2.2 霉菌的酶活特性分析
如表1所示,A.versicolorJP7在糊精培养基(糖化酶产生)、改良GYP(液化酶产生)、改良酪素(蛋白酶)、改良PDA培养基(酯化酶产生)、果胶酶产生培养基和马丁氏培养基等6种培养基上均能生长,但是不能形成特征透明圈。结果表明A.versicolorJP7不具备糖化酶、液化酶、蛋白酶、酯化酶、果胶酶和单宁酶产生能力。A.versicolorJP7能够在改良YP培养基上生长,并形成透明圈,表明A.versicolorJP7具有纤维素酶产生能力。如图3所示,A.versicolorJP7在改良YP培养基上形成的菌落直径为0.5 cm,黄色透明圈直径为2.5 cm,透明圈与菌落直径比为5。
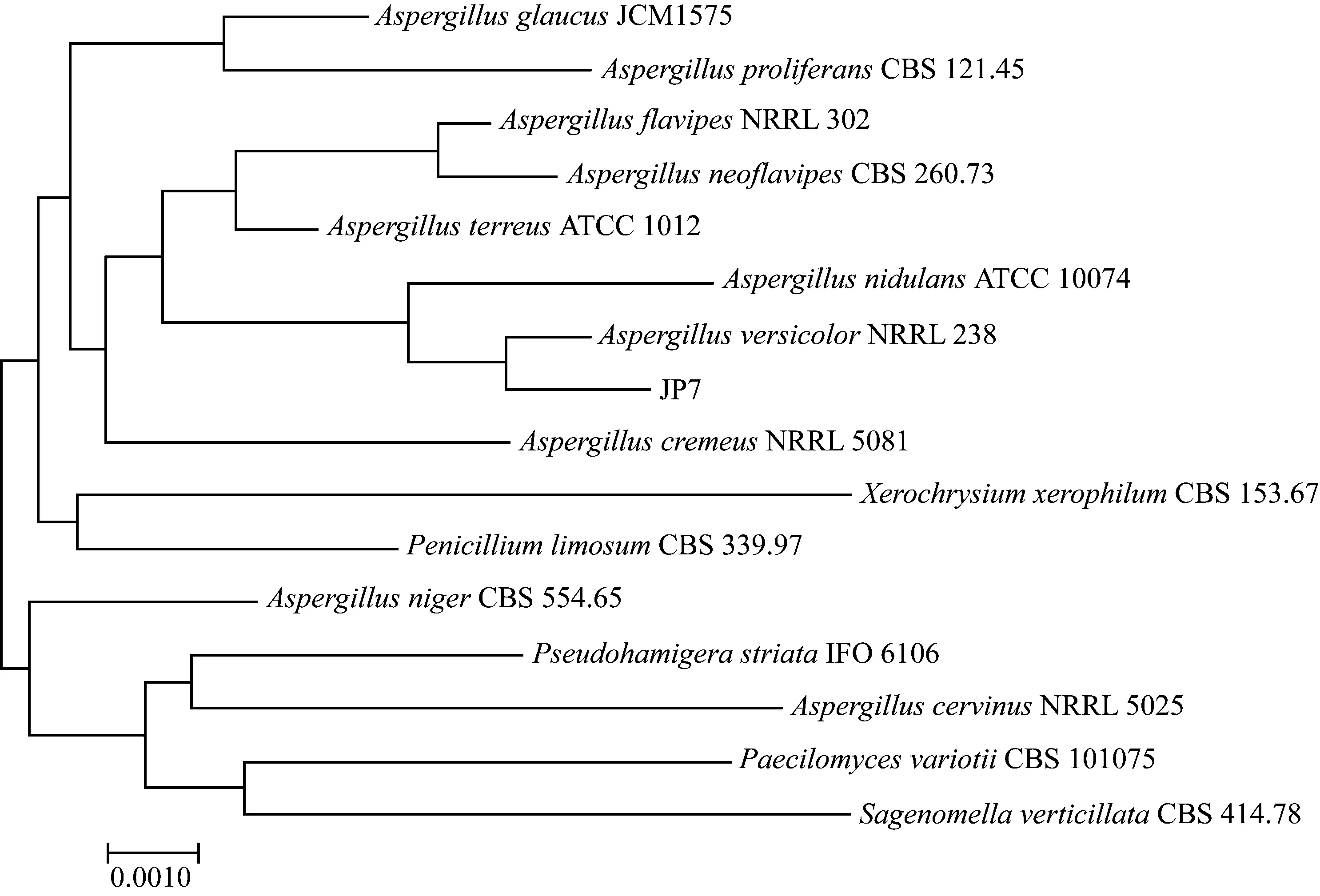
图2 系统发育树

表1 A. versicolor JP7的产酶能力检测

图3 A. versicolor JP7在改良YP培养基上形成的透明圈
2.3 霉菌的环境耐受性分析
(1) 温度耐受性
如表2所示,在设置的4个温度梯度中,A.versicolorJP7只能在28 ℃培养箱中生长,高温和低温都不能生长。

表2 A. Versicolor JP7温度耐受性测定
(2) 乙醇耐受性
如表3和图4所示,随着乙醇体积浓度的升高,A.versicolorJP7的生长逐渐减弱,酒精浓度达到6%时,A.versicolorJP7的生长受到明显抑制。

表3 A. Versicolor JP7酒精耐受性测定
(3) 乳酸耐受性
如表4和图5所示,乳酸对A.versicolorJP7的生长有明显的影响,随乳酸浓度升高,菌体生长逐渐减弱。当乳酸浓度达到50 g/L时,A.versicolorJP7的生长受到明显抑制。

从左到右,分别代表不同的乙醇浓度梯度:0%、2%、4%、6%图4 菌株JP7在乙醇梯度培养基上的生长情况

表4 A. Versicolor JP7乳酸耐受性测定
2.4 霉菌的代谢产物解析
如表5所示,以乳酸为唯一碳源进行液体发酵,用乙酸乙酯萃取后,A.versicolorJP7主要产生7种代谢产物,其中1,2-丙二醇和己烷的产量最高。

表5 A. versicolor JP7发酵产物解析
3 结论
本研究以乳酸为唯一碳源从酱香型酒醅中筛选得到一株霉菌JP7,该霉菌菌落上呈现1种以上颜色,中部为黄色,边缘为灰白色,在显微镜下能观察到曲霉特征的菊花状分生孢子头。基于菌株18S rDNA的系统发育分析,该菌属于杂色曲霉A.versicolor,因此,将JP7命名为A.versicolorJP7。A.versicolorJP7具有较强的纤维素酶产生能力,在改良YP培养基上形成的透明圈与菌落直径比为5。从温度、乳酸和酒精三个方面考察菌株对环境的耐受性,菌株的最适生长温度为28 ℃,低温和高温均不能生长;菌株对酒精的最高耐受浓度为6%;菌株对乳酸的耐受能力较强,可达到50 g/L。通过GC-MS检测,在以乳酸为唯一碳源的发酵培养基中,A.versicolorJP7利用乳酸主要产生了7种代谢产物,其中1,2-丙二醇和己烷的产量较高。
已见文献报道的乳酸利用菌主要是细菌,包括丙酸杆菌属、芽孢杆菌属、梭菌属、脱硫肠状菌属、泥杆菌属、葡萄球菌属、土孢杆菌属等[19-21],其中,芽孢杆菌属的菌株最多[22]。乳酸是酒醅中含量最高的有机酸,在泸型酒中,发酵结束时其质量浓度范围在15 g/L ~20 g/L酒醅左右,而在酱香型酒中,中后期轮次酒醅中乳酸含量可达到20 g/kg~40 g/kg酒醅[18-19],据此可以推测酱香型酒醅可能含有更丰富的乳酸利用菌种质资源,有待进一步开发利用。高浓度的乙醇耐受能力是乳酸降解菌应用于白酒生产的前提,乙醇浓度超过6%,乳酸利用菌的生长受到明显抑制,而菌株对乳酸的降解率也大幅度下降[1]。在本研究中,乙醇浓度达到6%,A.versicolorJP7的生长受到明显的抑制,因此,A.versicolorJP7能否作为乳酸降解菌应用到白酒生产中,需在高浓度乙醇环境中对菌株的乳酸降解能力进行进一步的测定。
杂色曲霉(A.versicolor)是曲霉属的一种常见种,属于杂色曲霉群。杂色曲霉产生的杂色曲霉素(Sterigmatocystin,STG)是黄曲霉毒素B1、G1等的前体物质,结构与黄曲霉毒素极为相似,都含有双呋喃环结构[23]。毒理学试验表明:杂色曲霉素具有肝毒性和免疫抑制效应,可诱发肝癌等癌症疾病[24-25]。近年来,杂色曲霉的次级代谢产物越来越受到关注。A.versicolorZZ761能够产生1种新的吲哚二萜和15种已知化合物,这种新的吲哚二萜针对大肠杆菌的最小抑菌浓度是20.6 μmol/L,对白色念珠菌的最小抑菌浓度为22.8 μmol/L[26]。而 LI TX等人[27]从A.versicolorZZ761中分离得到两种新的化合物——曲酮A和曲酮B,这两种物质是曲酸的衍生物,在体内外均具有消炎作用。A.versicolorJP7利用乳酸主要产生1,2-丙二醇和己烷。1,2-丙二醇和己烷是重要的工业原料,丙二醇本身可以作为溶剂、抗冻剂和保护剂,还可以参与多种化学合成反应,能够作为单体参与聚酯、聚醚和聚氨酯和合成,是具有广阔应用前景的化工原料之一[28]。己烷在有机合成中有重要的应用,主要用作溶剂、化学试剂、涂料稀释剂及聚合反应的介质等[29]。丙二醇和己烷主要通过化学法进行合成,化学合成法存在一些问题:对设备有高压和高温的要求、反应过程中需使用昂贵的催化剂、释放有毒的中间体、依赖不可再生材料、低产量和复杂性等[30]。本研究为进一步探究微生物法生产丙二醇和己烷提供理论依据。
