脉搏指数连续心排血量监测改善急性心肌梗死合并心原性休克患者临床预后研究
2022-10-25游洁芸耿立沈运丽黄晶王兴旭王亮张奇郭蔚
游洁芸 耿立 沈运丽 黄晶 王兴旭 王亮 张奇 郭蔚
急性心肌梗死合并心原性休克(acute myocardial infarction with cardiogenic shock,AMICS)患者的救治面临严峻挑战。经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)显著改善了急性心肌梗死患者预后,但心原性休克仍是急性心肌梗死患者死亡的主要原因[1-2]。全球注册研究显示AMICS总体发生率为4%~12%,30 d死亡率高达40%~45%[2-4]。除了对此类患者进行快速而有效的再灌注治疗,实时准确的血流动力学监测也是制订有效治疗策略的基石;更好地掌握急性期患者的血流动力学状态有助于优化治疗,进而改善预后[5]。
脉搏指数连续心排血量监测(pulse index continuous cardiac output,PiCCO)是一种基于经肺热稀释法和动脉脉搏轮廓分析法的血流动力学监测新方法,具有方便、安全、连续、实时、微创、可重复等优点,能全面准确地反映血流动力学动态变化,有助于优化危重患者的管理[6-10]。目前PiCCO已被证实能有效指导感染性休克、急性呼吸窘迫综合征等危重患者的液体管理[9,11],但国内外对于PiCCO在心血管急危重症中的应用报道甚少,其在AMICS患者治疗决策的潜在价值仍有待进一步研究。本研究旨在评估AMICS患者完成急诊PCI后应用PiCCO监测对改善临床预后的作用,为临床治疗提供依据。
1 对象与方法
1.1 研究对象
前瞻性收集2016年6月至2021年6月上海市东方医院心内科收治的135例AMICS患者资料,根据入排标准筛选,并进行1∶1倾向性评分匹配,最终PiCCO组和对照组(未接受PiCCO监测)各50例患者纳入分析(图1)。纳入标准:(1)年龄≥18岁,男性或者非妊娠期女性;(2)符合AMICS诊断;(3)接受急诊PCI。排除标准:(1)周围性血管疾病;(2)严重的心脏瓣膜病;(3)应用体外膜肺氧合治疗;(4)孕妇或哺乳期妇女;(5)未接受急诊PCI;(6)合并心脏机械性并发症。本研究方案经上海市东方医院伦理委员会批准,所有患者签署书面知情同意书。

图1 研究流程
1.2 临床诊断标准
急性心肌梗死的定义依据欧洲心脏病学会(European Society of Cardiology,ESC)/美国心脏病学会基金会(American College of Cardidogy Foundation,ACCF)/美国心脏协会(American Heart Association,AHA)/世界心脏病联盟(World Heart Federation,WHF)指南:(1)存在心肌缺血症状;(2)心肌肌钙蛋白大于正常参考值上限的第99百分位;(3)与急性心肌梗死相适应的心电图ST段抬高或压低的动态变化。经超声心动图和冠状动脉造影确认心肌梗死的部位[12]。心原性休克的诊断标准如下[2-3,13]:(1)存在心功能不全的客观证据;(2)收缩压<90 mmHg(1 mmHg=0.133 kPa)持续超过30 min,或应用血管活性药物和(或)循环辅助装置支持下收缩压维持>90 mmHg;(3)心脏指数(cardiac index,CI)<2.2 L/(min·m2);(4)组织灌注不足的临床体征(皮肤发绀或花斑、精神状态改变、少尿或周围血管收缩等)。
1.3 干预措施
所有患者均依据指南接受急诊PCI以及抗血小板等冠心病药物治疗[5,13]。对照组根据主诊医师可获得的检查结果、监测信息及临床经验决定患者住院期间药物治疗方案。PiCCO组患者在接受急诊PCI返回心脏监护室后即刻进行PiCCO。按照规范操作流程进行操作,依据血流动力/容量管理决策流程树及时调整药物治疗策略(图2)。PiCCO操作流程主要包括:除中心静脉导管外,股动脉置入PiCCO导管,并连接至PiCCO plus模块系统(Pulsion Medical Systems,Munich,Germany)。至少每8 h手动校准1次,以确保测量精度。中心静脉导管注射0℃~4℃生理盐水15~20 ml 3次,获取反映心脏收缩力、前负荷、后负荷和肺水肿的血流动力学参数,主要包括:CI、左心室收缩力指数(left ventricular contractility index,dPmax)、全心射血分数(global ejection fraction,GEF)、全心舒张末期容积指数(global end-diastolic volume index,GEDVI)、全身血管阻力指数(systemic vascular resistance index,SV R I)、血管外肺水指数(extravascular lung water inde,EVLWI)等。使用主动脉内球囊反搏(intra-aortic balloon pumping,IABP)治疗的患者,在IABP待机1 min后测量血流动力学参数。在患者病情稳定24~48 h,或最多维持10 d后,结束PiCCO监测。

图2 血流动力/容量管理决策流程树
1.4 研究终点
主要终点为 30 d内全因死亡。次要终点:(1)首次住院天数;(2)30 d内再入院;(3)30 d内心原性死亡。其他观察指标包括住院期间机械通气、静脉抗心力衰竭药物治疗时间(包括强心药物、利尿剂、血管收缩药物、血管扩张药物);心力衰竭相关临床指标变化趋势,包括高敏肌钙蛋白T(high-sensitive troponin T,hs-TnT)、N末端B型脑钠肽前体(amino-terminal probrain natriuretic peptide,NT-proBNP)、左心室射血分数(lef t ventricular ejection f raction,LVEF)、血清肌酐(serum creatinine,Scr)、谷丙转氨酶(glutamic pyruvic transaminase,GPT);以及出血、血肿、栓塞、感染等操作相关并发症的发生率。强心药物包括多巴酚丁胺、左西孟旦、米力农。利尿剂包括呋塞米、托拉塞米。血管收缩药物包括多巴胺>5 μg/(kg·min)、去甲肾上腺素、肾上腺素。血管扩张药物包括硝酸甘油、硝普钠、人重组脑钠肽。
1.5 统计学分析
所有数据采用SPSS 25.0进行统计分析。采用Logisitic回归模型对两组患者按照1∶1进行倾向性评分匹配,匹配参数包括基线年龄、性别、身体质量指数,卡钳值为0.02。连续变量以均数±标准差或中位数(四分位数间距)表示,采用独立样本t检验或单因素方差分析进行比较;分类变量以频率和百分比表示,采用卡方检验或Fisher精确概率法检验进行比较;非正态分布数据采用Wilcoxon秩和检验。通过单因素分析比较两组临床特征、心力衰竭相关临床指标和血流动力学参数,并通过Student-Newman-Keuls进行多组均数间两两比较,用Kaplan-Meier曲线法观察临床终点事件,Log rank检验比较生存曲线,计算风险比(hazard ratio,HR)和95%可信区间(confidence interval,CI)。双侧检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组临床特征比较
住院期间PiCCO组应用强心药物和血管收缩药物比例明显高于对照组(P=0.001,P=0.004),其余资料两组比较差异均无统计学意义(均P>0.05,表1)。

表1 倾向性评分匹配后两组基线临床特征及治疗情况
2.2 研究终点
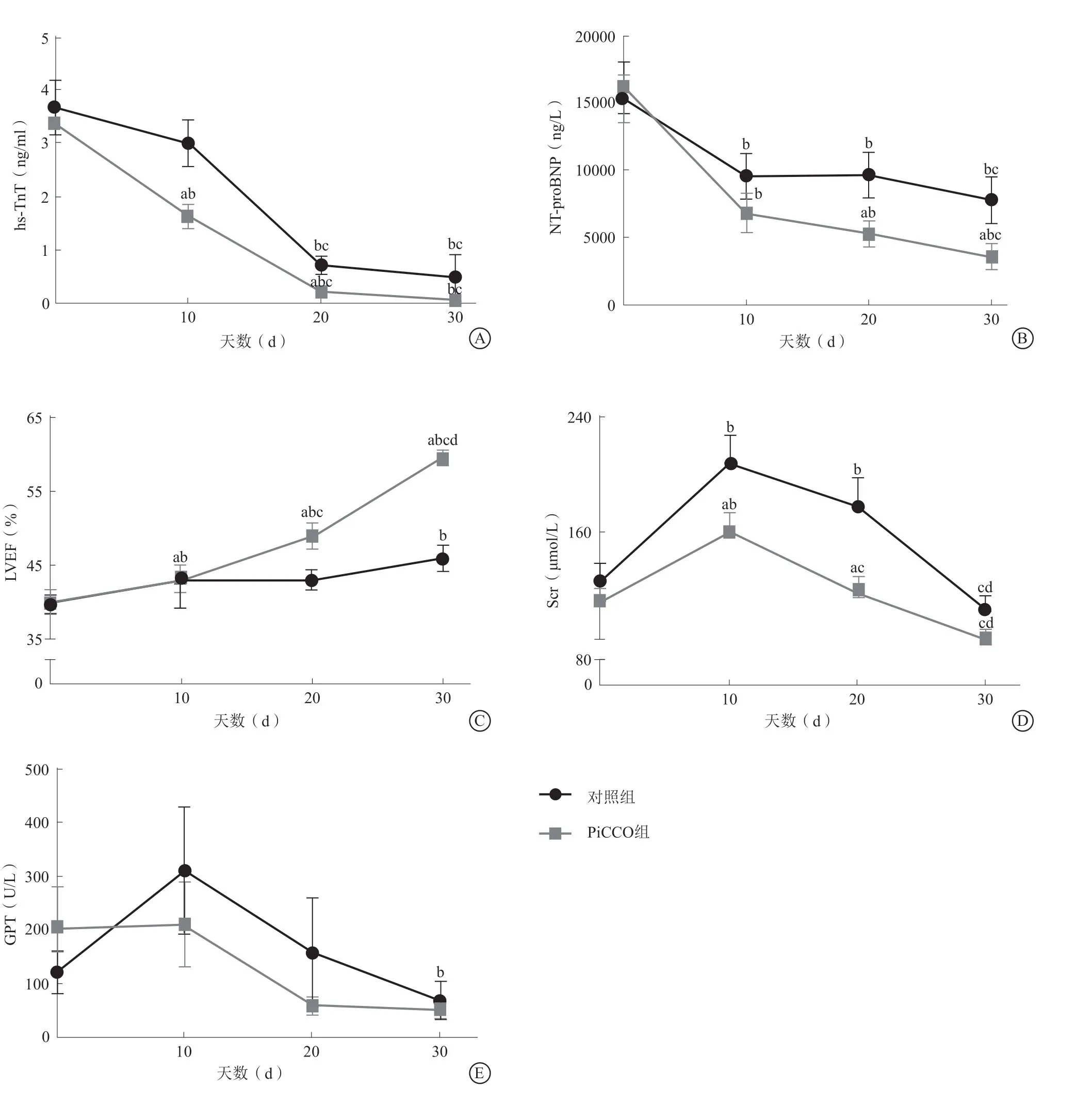
经倾向性评分匹 配后比较两组终点事件发现,PiCCO组较对照组30 d内全因死亡率(16%比34%,P=0.024)、心原性死亡率(14%比30%,P=0.042)明显下降(图3),再入院率显著降低(2%比14%,P=0.027),首次住院时间更短[(17.60±1.06)d比(24.32±2.19)d,P<0.001]。两组出血、血肿、栓塞、感染等操作相关并发症的发生率差异均无统计学意义(均P>0.05)。PiCCO组hs-TnT、NTproBNP、LVEF、Scr水平较对照组更迅速且显著得到改善(均P<0.05,图4)。

图3 两组30 d 全因死亡率及心原性死亡率比较 A.全因死亡率;B.心原性死亡率
2.3 PiCCO组血流动力学参数的变化
单组观察表明,PiCCO组患者在心脏收缩力(GEF)、后负荷(SVRI)、肺水肿(EVLWI)和CI等血流动力学指标参数上改善趋势明显(表2)。
表2 PiCCO 组血流动力学参数的变化(±s)

表2 PiCCO 组血流动力学参数的变化(±s)
注:a,与第0 天比较,P <0.05;b,与第1 天比较,P <0.05;PiCCO,脉搏指数连续心排血量监测;CI,心脏指数;dPmax,左心室收缩力指数;GEF,全心射血分数;GEDVI,全心舒张末期容积指数;SVRI,全身血管阻力指数;EVLWI,血管外肺水指数。
血流动力学参数 参考值 第0 天 第1 天 第2 天 第3 天 F 值 P 值CI[L/(min · m2)] 3.0~3.5 1.94±0.43 2.29±0.51a 2.49±0.65ab 2.59±0.58ab 15.953 <0.001 dPmax(mmHg/s) 900~1 200 807.90±39.26 820.24±36.52 822.60±35.74 852.47±43.47 0.231 0.875 GEF(%) 25~35 12.94±3.89 15.17±4.51a 15.85±5.07a 16.52±5.87a 6.265 <0.001 GEDVI(ml/m2) 680~800 804.83±24.79 795.87±23.34 793.29±22.90 792.27±20.82 0.061 0.980 SVRI(dyn·s·cm-5 · m2) 1 700~2 400 3 092.77±135.81 2 575.41±100.20a 2 338.77±93.57a 2 268.96±82.67ab 12.365 <0.001 EVLWI(ml/kg) 3~7 11.87±5.03 10.09±4.01a 10.04±3.97a 9.36±3.10a 3.936 0.009
3 讨论
本研究结果表明,PiCCO监测可显著改善AMICS患者在接受急诊PCI后30 d的临床预后,降低全因死亡和心原性死亡率。单组观察发现,PiCCO组患者各项血流动力学客观指标改善明显。基于PiCCO监测结果,及时、动态地调整干预药物,使受损心脏在短期内取得做功氧耗、前负荷以及后负荷之间新的平衡,平稳度过休克急性期,可能是改善患者预后的关键因素之一。
近三十年,心血管疾病治疗手段和方式发展迅速,极大改善了患者的预后,但AMICS死亡率仍居高不下,并未发生明显改变。既往研究表明,紧急血运重建、去甲肾上腺素及左西孟旦的应用有助于改善患者预后,而其他包括血小板糖蛋白Ⅱb/Ⅲa受体拮抗剂、一氧化氮合成酶抑制剂、低温治疗、IABP以及循环机械辅助装置的应用等措施,均未被证明可改善患者预后[14]。既往针对这部分患者临床救治方法的探索中,往往聚焦于治疗器械的研发和应用。血流动力学监测已被指南推荐为休克患者救治的必要措施,但其在AMICS患者中的应用仍存在较大不足。患者症状、体征以及实验室检查结果的改变,往往滞后于血流动力学参数的动态变化。及时、有效的血流动力学监测,可为快速诊断、动态调整治疗药物和改善预后提供帮助[15]。
Swan-Ganz右心导管是被公认为血流动力学监测的金标准,但这一经典方法的创伤性较大、并发症较多,提供的数据为非连续性,不能供于实时监测,在临床实际工作中的使用率并不高[16-17]。PiCCO监测能实时准确地获取反映心脏收缩力、前负荷、后负荷、肺水肿情况等血流动力学参数,有助于根据监测结果动态调整治疗策略,以期迅速建立并维持稳定的循环状态[6-10]。对于AMICS患者的管理,PiCCO较右心导管具有显著优势:(1)PiCCO中心静脉置管往往是心原性休克患者抢救和治疗所必须的,只需额外在动脉端置入一根4 F导管,相对于右心导管创伤小、并发症少;(2)PiCCO提供连续的血流动力学参数,帮助临床医师动态监测整个循环系统的实时变化,并及时调整治疗策略;(3)PiCCO独有的参数EVLWI对心原性休克患者的液体管理非常有效,与患者的临床预后密切相关。
既往研究发现,与中心静脉压或右心导管相比,PiCCO监测指导治疗能显著缩短脓毒症或呼吸窘迫综合征患者的重症监护室住院时间,改善血流动力学和供氧指数,减少机械通气时间[9]。但国内外目前很少有研究探讨PiCCO对AMICS患者临床预后的影响。本研究发现,PiCCO组较对照组更充分地应用强心药物和血管收缩药物,这提示了在PiCCO监测结果指导下,可更为及时、合理地调整药物方案,促进心脏功能和前后负荷达到新的平衡,能更为个体化地稳定患者循环状态。
本单中心研究入选样本量相对小,研究结论仍有待更大样本或多中心随机对照临床研究证实。本研究中未将PiCCO监测与其他血流动力学监测方法,如右心导管等作比较,因而无法判定各种血流动力学监测方法的优劣。总体上讲,对于AMICS患者,无论采用何种手段,只要获得必要的血流动力学参数,即可对其治疗进行及时、动态调整,从而有助于改善临床预后。另外,本研究仅入选了接受急诊PCI的AMICS患者,对于PiCCO在未接受急诊PCI的AMICS患者及其他非心肌梗死导致的心原性休克患者中的作用仍有待于更多研究观察。研究仅观察了30 d的短期临床随访结果,PiCCO血流动力学监测带来的短期生存获益是否能转化为长期效应,仍有待于进一步临床随访。
总之,本研究结果提示,对于急诊P C I 的AMICS患者,后期住院期间进行PiCCO监测,有助于及时调整干预药物,促进心脏功能的恢复,从而改善患者预后。研究结果有望改善AMICS高死亡率这一临床困境。
利益冲突所有作者均声明不存在利益冲突
