基于一测多评法的当归药材质量控制研究
2022-10-21李小阳翟小林裴纹萱宋学斌王晶娟
李小阳,翟小林,王 丹,范 晶,裴纹萱,董 玲,孙 裕,宋学斌,王晶娟*
基于一测多评法的当归药材质量控制研究
李小阳1, 4,翟小林1,王 丹1,范 晶1,裴纹萱2,董 玲2,孙 裕3,宋学斌3,王晶娟1*
1. 北京中医药大学中药学院,北京 102488 2. 北京中医药大学生命科学学院,北京 100029 3. 兰州佛慈制药股份有限公司,甘肃 兰州 730046 4. 中国中医科学院中医药信息研究所,北京 100700
建立一测多评法(quantitative analysis of multi-components by a single marker,QAMS)同时测定当归中阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞的含量。采用Waters X-Select CSH色谱柱(250 mm×4.6 mm,5 μm),以0.085%磷酸-水溶液(A)-乙腈(B)为流动相,梯度洗脱,体积流量1.0 mL/min,柱温40 ℃,检测波长265 nm。在线性范围内各成分线性良好(2>0.999)。以藁本内酯为内标,阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯和丁烯基苯酞的相对校正因子分别为1.073 4、0.564 8、0.468 1、0.926 2、1.083 5;同时采用外标法测定这6个成分的含量,将2种方法进行分析比较,结果没有明显差异。建立了当归药材中阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞6个成分的QAMS法,该法可用于当归的质量控制。
当归;一测多评法;阿魏酸;洋川芎内酯I;洋川芎内酯H;阿魏酸松柏酯;藁本内酯;丁烯基苯酞
当归,又名文无,是伞形科植物当归(Oliv.) Diels.的干燥根。味甘、辛,性温,归肝、心、脾经,有补血活血、调经止痛、润肠通便的功效[1]。目前,对于当归化学成分及药理作用的研究已经较为全面。当归中的化学成分主要包括苯酞类、香豆素类、黄酮类、有机酸类及其他成分[2-3]。它的药理作用广泛,既能作用于心血管系统和血液系统,还有抗炎、抗氧化和增强免疫的功效[4-9]。
阿魏酸是当归中的主要活性成分,以游离型或结合型存在于药材中。阿魏酸与松柏醇结合形成的阿魏酸松柏酯是最主要的结合形式之一[10]。阿魏酸松柏酯有很高的生物活性,它不仅是当归挥发油中抗氧化活性的来源[11],还是谷胱甘肽S-转移酶的强抑制剂,对潜在肿瘤多药耐药有逆转作用[12]。但它不稳定,极易在光和高温的条件下分解为阿魏酸[10]。目前,《中国药典》2020年版中对当归的要求为阿魏酸含量不得少于0.05%。有文献建议,由于结合型阿魏酸与游离型阿魏酸之间的转化关系,应当将总阿魏酸含量作为当归的质量评价指标[13]。除此以外,药典中并未对当归中的另一主要活性成分藁本内酯的含量加以控制。基于本课题组对当归的前期研究[14-15],以及当归中苯酞类成分之间的相互转化作用[16-17],本课题组建立了一测多评法(quantitative analysis of multi-components by a single marker,QAMS)同时测定[18-19]当归中阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞的含量测定方法,为中药当归质控标准的制定提供一种方法和手段。
1 材料
BSA124S型、CPA225D型电子分析天平,德国Sartorius公司;SB5200T型超声仪,宁波新芝生物公司;2998PDA型Waters液相色谱仪(检测器),美国Waters公司。色谱纯甲醇、乙腈、甲酸和磷酸为Fisher公司生产。
实验所收集的当归样品均经北京中医药大学中药学院鉴定系王晶娟副教授鉴定为伞形科植物当归(Oliv.) Diels.的干燥根。样品信息见表1。阿魏酸(批号H25M6L1)对照品购于源叶生物,洋川芎内酯I(批号180428)、洋川芎内酯H(批号180121)、丁烯基苯酞(批号171004)、藁本内酯(批号170804)对照品购于北京四面体生物科技发展有限公司,质量分数大于98%。对照品阿魏酸松柏酯(171216)购于北京四面体生物科技发展有限公司,质量分数大于95%。
表1 当归样品信息
Table 1 Information of Angelicae Sinensis Radix
批号采集时间产地批号采集时间产地 12015岷县西寨镇刘家堡村172016岷县喇嘛村 22015岷县蒲麻乡化力沟村182016漳县尖子村 32015岷县西寨镇192016漳县金钟镇 42015渭源县祁家庙乡瓦楼村202016漳县寨子川村 52015渭源县祁家庙乡212016漳县曾家河村 62015渭源县祁家庙乡烟雾沟村222016漳县四族乡年家门村 72015漳县金钟镇大石门村232017湖北恩施红土乡石窑村 82015漳县大草滩新联村242017岷县清水镇清水村 92015漳县尖子村252017岷县十里镇甘寨村 102015漳县寨子川村262017岷县梅川镇马家沟村 112015漳县四族乡年家门村272017渭源县莲峰镇簸箕湾村 122015漳县喇嘛村282017云南沾益县播乐乡 132016岷县西寨镇刘家堡村292017漳县殪虎桥镇东桥村 142016岷县西寨镇302017漳县金钟镇尖子村 152016岷县禾驮乡甘滩村312017甘肃(燕京饮片厂) 162016岷县蒲麻乡化力沟村
2 方法与结果
2.1 色谱条件
色谱柱为Waters X-Select CSH(250 mm×4.6 mm,5 μm)。进样量10 μL,检测波长265 nm,体积流量1.0 mL/min,柱温40 ℃,流动相为0.085%磷酸水(A)-乙腈(B),梯度洗脱:0~20 min,15%~26%B;20~23 min,26%~46%B;23~45 min,46%B;45~50 min,46%~90%B;50~55 min,90%B。
2.2 对照品溶液的制备
精密称取阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞对照品适量,分别置棕色量瓶中,加甲醇稀释定容置刻度线,得到的溶液质量浓度依次为3.2、4.1、0.7、13.9、80.4和8.4 μg/mL。由于本实验使用的对照品多数性质不稳定,制备后应立即使用,临时保存可置于−20 ℃冷冻,但再次使用前需重新标定含量。
2.3 供试品溶液的制备
取当归粉末(过三号筛)约0.2 g,精密称定,置具塞锥形瓶中,分别加入95∶5甲醇甲酸20 mL,称定质量,超声提取30 min,放冷,再称定质量,用95∶5甲醇甲酸补足减失的质量,摇匀,静置,取上清液用0.45 μm微孔滤膜滤过,取续滤液作为供试品溶液。
2.4 色谱条件的优化
为保证被定量化合物良好的分离度和适当的保留时间,本实验对流动相梯度程序、柱温和检测波长进行了考察。本实验用PDA检测器的高效液相色谱仪对样品进行全波长扫描,在265 nm处各主要吸收峰强度较大,且各峰与在260 nm和270 nm处的吸收度差别较小,故选择了265 nm为扫描波长,图1为255、265、275、285和300 nm下的色谱图;为提高藁本内酯和相邻色谱峰丁烯基苯酞的分离度,本实验尝试了多个流动相梯度,最后确定为上述的梯度程序。应用以上所建立的色谱条件进行分析,所得到的对照品和样品的色谱图见图2,图中,6个被测化合物都实现了良好的分离。色谱图中的6个待测化合物的鉴别是通过对比保留时间以及加入对照品的方法完成的。
2.5 方法学考察
2.5.1 线性关系考察、检测限和定量限测定 精密吸取对照品贮备液分别稀释至6个不同浓度,按“2.1”项下色谱条件分别测定阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞的峰面积,以质量浓度为横坐标(),峰面积为纵坐标(),计算标准曲线,结果见表2。当信噪比(/)为3时的被测物浓度为检测限,/为10时的被测浓度为定量限,据此测得6个成分的检测限和定量限见表2。

1-阿魏酸 2-洋川芎内酯I 3-洋川芎内酯H 4-阿魏酸松柏酯 5-藁本内酯 6-丁烯基苯酞
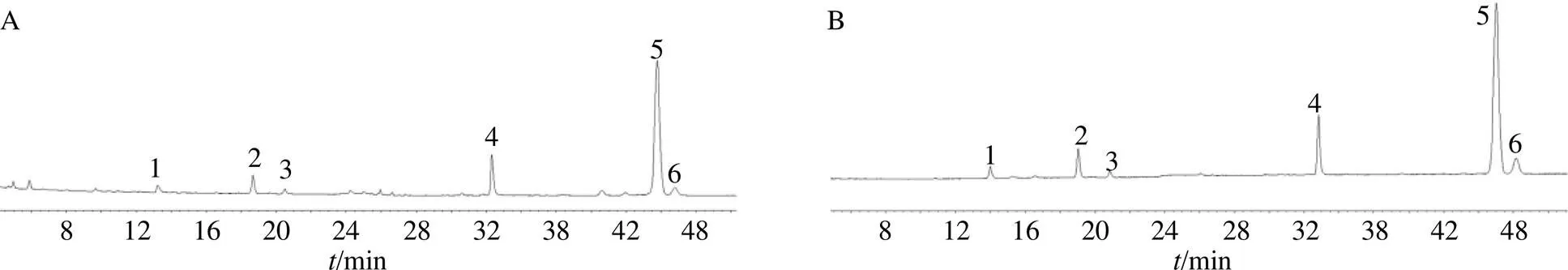
1-阿魏酸 2-洋川芎内酯I 3-洋川芎内酯H 4-阿魏酸松柏酯 5-藁本内酯 6-丁烯基苯酞
表2 6种化合物的标准曲线、检测限及定量限
Table 2 Liner correlation, limit of detection and limit of quantitation of six components
化合物回归方程线性范围/(μg·mL−1)R2检测限/ng定量限/ng 阿魏酸Y=13 106 X-3 508.41.58~12.630.999 426.7289.06 洋川芎内酯IY=23 996 X-4 150.42.03~16.250.999 613.9146.37 洋川芎内酯HY=29 926 X-1 8320.37~2.930.999 511.7339.09 阿魏酸松柏酯Y=14 943 X-14 8936.95~55.580.999 423.2177.36 藁本内酯Y=13 975 X-58 66440.21~321.700.999 524.3080.99 丁烯基苯酞Y=12 544 X-8 568.94.21~33.710.999 627.8792.90
2.5.2 精密度试验 精密吸取同一供试品溶液10 μL,按“2.1”项下方法连续进样6次,记录峰面积,阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞保留时间的RSD分别为1.14%、0.99%、0.97%、0.52%、0.80%和0.82%,峰面积的RSD分别为1.98%、1.77%、2.00%、1.03%、0.68%和0.79%,表明仪器精密度良好。
2.5.3 稳定性试验 取同一供试品溶液,室温下放置,分别在0、2、4、8、12、24 h进样,测定峰面积,阿魏酸、洋川芎内酯I、藁本内酯和丁烯基苯酞峰面积的RSD分别为0.95%、0.40%、0.44%、0.32%、0.29%和1.11%,表明供试品溶液在24 h内测定结果稳定。
2.5.4 重复性试验 重复称取同一供试品6份,约0.2 g,精密称定,按“2.1”项下方法制备样品,测定,阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞RSD均小于2%。表明该方法的重复性良好。
2.5.5 加样回收率试验 重复称取当归药材粉末6份,每份约0.1 g,精密称定,分别精密加入含阿魏酸(0.104 μg)、洋川芎内酯I(0.122 μg)、洋川芎内酯H(0.024 μg)、阿魏酸松柏酯(0.431 μg)、藁本内酯(2.413 μg)和丁烯基苯酞(0.211 μg)的对照品溶液,照“2.1”项下方法制备,测定并计算加样回收率,阿魏酸、洋川芎内酯I、藁本内酯和丁烯基苯酞的平均加样回收率分别为98.45%、97.04%、97.57%、100.24%、102.25%和101.34%,RSD分别为2.37%、2.89%、2.47%、1.46%、1.93%和2.02%。
2.6 相对校正因子(fs/i)的计算
精密吸取混合对照品溶液10 μL,按“2.1”项下色谱条件测定,进样4次,记录各化合物的色谱峰面积,根据s/i计算公式[18],以藁本内酯为内标,计算阿魏酸对藁本内酯的校正因子1,洋川芎内酯I对藁本内酯的校正因子2,洋川芎内酯H对藁本内酯的校正因子3,阿魏酸松柏酯对藁本内酯的校正因子4和丁烯基苯酞对藁本内酯的校正因子5的平均值,分别为1.078 7、0.565 3、0.466 9、0.950 1、1.156 9。
s/i=s/f=(s/s)/(A/C)
s为藁本内酯内标物的峰面积,s为藁本内酯内标物的浓度,A为被测指标组分的峰面积,C为被测指标组分的浓度
2.7 f的重复性考察
2.7.1 不同仪器及色谱柱对RCF的影响 取“2.2”项下的混合对照品溶液,分别精密吸取10 μL,分别采用Waters X-Select CSH-1、Waters X-Select CSH-2、Waters X-Select CSH-3色谱柱,在WATERS2998 PDA和岛津SPD-20A高效液相色谱仪上进样检测,求算以藁本内酯作为参照成分时,5种成分的s/i,结果说明s/i在使用不同仪器时的耐用性良好,结果见表3。
表3 不同仪器和色谱柱测得相对校正因子
Table 3 RCFs determined by different instruments and columns.
仪器色谱柱相对校正因子 f阿魏酸/藁本内酯f洋川芎内酯I/藁本内酯f洋川芎内酯H/藁本内酯f阿魏酸松柏酯/藁本内酯f丁烯基苯酞/藁本内酯 Waters2998 PDAWaters X-Select CSH-11.121 4 0.568 4 0.465 9 0.946 0 1.159 6 Waters X-Select CSH-21.107 6 0.562 3 0.493 4 0.944 1 1.132 0 Waters X-Select CSH-31.092 7 0.555 2 0.467 7 0.942 3 1.132 3 岛津SPD-20AWaters X-Select CSH-11.052 8 0.571 4 0.461 6 0.908 1 1.024 3 Waters X-Select CSH-21.024 1 0.567 2 0.459 6 0.911 7 1.026 0 Waters X-Select CSH-31.041 7 0.564 2 0.460 6 0.904 9 1.026 8 平均值1.073 4 0.564 8 0.468 1 0.926 2 1.083 5 RSD/%3.661.012.732.145.92
2.7.2 测定不同体积流量对值的影响 用同一台液相色谱仪,分别在0.95、1.00、1.05 mL/min的体积流量下测定阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞的峰面积,计算的平均值分别为1.125 0、0.578 1、0.474 5、0.960 3、1.153 9,RSD分别为0.82%、1.63%、7.75%、2.50%和1.27%。结果表明在同一台高效液相色谱仪上,体积流量变化的影响不大。
2.7.3 测定不同柱温对值的影响 用同一台液相色谱仪,分别在柱温为35、40、45 ℃的条件下测定阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞的峰面积,计算的平均值分别为1.120 3、0.569 4、0.473 3、0.947 5、1.139 9,RSD分别为2.88%、1.60%、1.46%、0.70%和1.76%。结果表明在同一台高效液相色谱仪上,柱温的变化对值的影响不大。
2.8 样品的含量测定
采用常规对照品外标法和QAMS法分别测定了31批当归中阿魏酸、洋川芎内酯I、洋川芎内酯H、阿魏酸松柏酯、藁本内酯和丁烯基苯酞的含量,见表4。结果显示2种方法所测得的含量无明显差异。
表4 当归样品中6种化合物的含量 (n=3)
Table 4 Contents of investigated compounds in Angelicae Sinensis Radix (n=3)
编号阿魏酸/(mg·g−1)洋川芎内酯I/(mg·g−1)洋川芎内酯H/(mg·g−1)阿魏酸松柏酯/(mg·g−1) QAMS外标法QAMS外标法QAMS外标法QAMS外标法 10.285 0.285 0.781 0.781 0.149 0.149 3.034 3.032 20.442 0.441 0.746 0.746 0.138 0.138 1.670 1.669 30.365 0.365 0.406 0.406 0.084 0.084 1.476 1.475 40.352 0.352 0.476 0.476 0.090 0.090 1.672 1.671 50.283 0.283 0.633 0.633 0.113 0.113 2.649 2.648 60.438 0.438 0.519 0.520 0.089 0.088 3.001 3.000 70.454 0.454 0.479 0.479 0.089 0.089 0.769 0.769 80.502 0.501 0.826 0.826 0.156 0.156 4.837 4.835 90.535 0.535 0.494 0.495 0.093 0.093 0.747 0.747 100.350 0.350 0.422 0.422 0.087 0.087 0.816 0.816 110.508 0.508 1.105 1.105 0.212 0.212 6.469 6.466 120.455 0.455 0.417 0.417 0.075 0.075 0.756 0.756 130.360 0.360 1.048 1.048 0.197 0.197 3.062 3.060 140.360 0.360 0.398 0.398 0.071 0.070 0.601 0.601 150.356 0.355 0.771 0.772 0.148 0.148 4.669 4.667 160.390 0.390 1.151 1.151 0.232 0.232 3.173 3.171 170.473 0.473 0.541 0.541 0.105 0.105 1.275 1.274 180.425 0.425 0.806 0.806 0.138 0.138 1.251 1.250 190.375 0.375 0.908 0.908 0.162 0.162 1.834 1.833 200.368 0.368 0.404 0.404 0.074 0.074 0.577 0.576 210.461 0.460 1.058 1.058 0.200 0.200 4.146 4.145 220.359 0.359 1.096 1.096 0.207 0.207 5.670 5.668 230.507 0.506 0.710 0.711 0.114 0.114 1.309 1.308 240.361 0.361 0.450 0.451 0.087 0.087 4.144 4.142 250.334 0.334 0.223 0.223 0.045 0.045 2.851 2.849 260.368 0.368 0.874 0.874 0.139 0.139 2.178 2.177 270.291 0.291 0.163 0.163 0.025 0.024 3.999 3.997 280.186 0.185 0.319 0.319 0.062 0.062 8.973 8.969 290.509 0.509 0.350 0.350 0.072 0.072 3.589 3.587 300.448 0.448 1.174 1.174 0.228 0.228 5.186 5.183 310.501 0.500 1.240 1.240 0.216 0.216 2.855 2.854
续表4

编号Z-藁本内酯/(mg·g−1)Z-丁烯基苯酞/(mg·g−1)总阿魏酸/(mg·g−1)总苯酞/(mg·g−1) 外标法QAMS外标法QAMS外标法QAMS外标法 113.519 0.867 0.866 3.319 3.318 15.315 15.314 210.441 0.990 0.989 2.112 2.111 12.315 12.314 3 9.457 0.587 0.587 1.841 1.840 10.534 10.534 4 7.936 0.698 0.697 2.024 2.023 9.200 9.199 511.698 0.796 0.795 2.932 2.931 13.241 13.240 613.603 0.836 0.835 3.439 3.438 15.047 15.047 7 6.203 0.839 0.838 1.223 1.223 7.610 7.609 819.244 1.046 1.045 5.339 5.336 21.272 21.270 9 6.281 0.789 0.788 1.282 1.282 7.657 7.656 10 6.409 0.749 0.748 1.166 1.165 7.667 7.666 1129.650 1.455 1.453 6.977 6.974 32.422 32.420 12 6.516 0.781 0.780 1.211 1.210 7.790 7.789 1315.283 1.202 1.201 3.422 3.420 17.731 17.730 14 5.025 0.959 0.957 0.962 0.961 6.452 6.451 1519.051 1.034 1.033 5.025 5.022 21.004 21.003 1614.351 1.148 1.146 3.563 3.561 16.882 16.880 17 8.128 0.775 0.774 1.748 1.747 9.549 9.548 18 9.167 1.251 1.249 1.676 1.675 11.363 11.361 1910.702 1.045 1.044 2.209 2.208 12.817 12.816 20 5.799 0.817 0.816 0.944 0.944 7.094 7.093 2119.680 1.185 1.184 4.607 4.605 22.123 22.122 2224.250 1.190 1.189 6.030 6.027 26.743 26.742 2311.983 1.101 1.100 1.815 1.814 13.908 13.907 2418.081 0.796 0.795 4.505 4.503 19.415 19.415 2516.036 0.573 0.573 3.185 3.183 16.878 16.877 2612.463 1.317 1.316 2.546 2.545 14.794 14.792 2715.584 0.452 0.451 4.290 4.288 16.224 16.223 2831.470 0.698 0.697 9.159 9.155 32.549 32.549 2918.864 0.821 0.820 4.098 4.096 20.107 20.106 3021.847 1.354 1.352 5.634 5.631 24.603 24.602 3115.800 1.286 1.285 3.356 3.354 18.543 18.542
3 讨论
由于当归中主要包括有机酸类、苯酞类以及香豆素类成分,为了能较全面地评价药材质量,本实验除了对色谱条件进行优化,还对当归样品提取条件进行优化,主要包括提取方式、提取溶剂和提取时间3个方面。本实验首先考察了回流提取和超声提取的差异,发现由于阿魏酸松柏酯是阿魏酸的结合形式存在于药材中,且易受热分解为阿魏酸,因此其对提取方式的选择最敏感。由于超声提取效率较高,及其操作的便捷性,本实验选择超声提取作为当归的提取方法。在超声提取时间的选择上,本实验共筛选了超声15、30、45、60 min 4个梯度。结果表明超声15 min对总阿魏酸的提取效果最好,超声30 min对苯酞类成分的提取效果最好,综合考虑选择超声提取时间为30 min。
在提取溶剂方面,本实验考察了不同体积分数的甲醇溶液:70%甲醇、80%甲醇、90%甲醇、纯甲醇和95%甲醇-5%甲酸溶液[13]。70%、80%甲醇对阿魏酸提取率最高,而阿魏酸松柏酯在95%甲醇- 5%甲酸溶液中最稳定,提取率最高。从总阿魏酸、藁本内酯及丁烯基苯酞含量来看,最终选择了95%甲醇-5%甲酸溶液作为当归的提取溶剂。最终确定的提取方法为95%甲醇-5%甲酸溶液超声提取30 min。
本实验建立的高效液相色谱法实现了同时对当归中6个成分的含量测定,为提高当归质量控制标准提供了科学、简便的方法。在药典规定成分的基础上,从阿魏酸改为总阿魏酸,并增加了苯酞类成分作为指标,可以更加全面地控制当归药材质量,为当归质量标准提升提供参考。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典[S]. 一部. 2020: 28.
[2] 陈江弢, 杨崇仁. 当归属植物的研究进展 [J]. 天然产物研究与开发, 2004, 16(4): 359-365.
[3] Chen X P, Li W, Xiao X F,. Phytochemical and pharmacological studies on[J]., 2013, 11(6): 577-587.
[4] Chang C W, Chen Y M, Hsu Y J,. Protective effects of the roots ofon strenuous exercise-induced sportsin rats [J]., 2016, 193: 169-178.
[5] Zhuang C, Xu N W, Gao G M,. Polysaccharide fromprotects chondrocytes from H2O2-induced apoptosis through its antioxidant effects[J]., 2016, 87: 322-328.
[6] Lee J, Choi Y Y, Kim M H,. Topical application ofimproves pruritus and skin inflammation in mice with atopic dermatitis-like symptoms [J]., 2016, 19(1): 98-105.
[7] 闫安, 谢云亮. 当归多糖对脑缺血再灌注损伤大鼠脑组织氧化应激水平及炎症因子表达的影响 [J]. 中国实验方剂学杂志, 2018, 24(2): 123-127.
[8] Hua Y L, Yao W L, Ji P,. Integrated metabonomic-proteomic studies on blood enrichment effects ofon a blood deficiency mice model [J]., 2017, 55(1): 853-863.
[9] 王晓萍, 周明旺, 康开彪, 等. 岷当归有效成分对高同型半胱氨酸血症致兔动脉粥样硬化的影响 [J]. 中国中医药信息杂志, 2018, 25(2): 51-54.
[10] Li S L, Yan R, Tam Y K,. Post-harvest alteration of the main chemical ingredients inChuanxiong Hort. () [J].(), 2007, 55(1): 140-144.
[11] Li S Y, Yu Y, Li S P. Identification of antioxidants in essential oil ofusing HPLC coupled with DAD-MS and ABTS-based assay [J]., 2007, 55(9): 3358-3362.
[12] Chen C, Wu C H, Lu X H,. Coniferyl ferulate, a strong inhibitor of glutathione S-transferase isolated from, reverses multidrug resistance and downregulates P-glycoprotein [J]., 2013, 2013: 639083.
[13] Lu G H, Chan K, Leung K,. Assay of free ferulic acid and total ferulic acid for quality assessment of[J]., 2005, 1068(2): 209-219.
[14] 郭怡祯, 王晶娟, 刘洋, 等. 当归多成分“质代关联”研究 [J]. 中草药, 2016, 47(15): 2701-2706.
[15] 鲁利娜, 王晶娟, 王新利, 等. 当归质量控制成分遴选研究 [J]. 西部中医药, 2017, 30(10): 22-26.
[16] 左爱华, 程孟春, 卓荣杰, 等. Z-藁本内酯降解产物的UPCL-QTOF-MS和NMR结构鉴定 [J]. 药学学报, 2013, 48(6): 911-916.
[17] Yan R, Ko N L, Li S L,. Pharmacokinetics and metabolism of ligustilide, a major bioactive component inin the rat [J]., 2008, 36(2): 400-408.
[18] 王智民, 钱忠直, 张启伟, 等. 一测多评法建立的技术指南 [J]. 中国中药杂志, 2011, 36(6): 657-658.
[19] Hou J J, Wu W Y, Da J,. Ruggedness and robustness of conversion factors in method of simultaneous determination of multi-components with single reference standard [J]., 2011, 1218(33): 5618-5627.
Quality control ofbased on quantitative analysis of multi-components by a single marker
LI Xiao-yang1,4, ZHAI Xiao-lin1, WANG Dan1, FAN Jing1, PEI Wen-xuan2, DONG Ling2, SUN Yu3, SONG Xue-bin3, WANG Jing-juan1
1. School of Chinese Materia Medica, Beijing University of Chinese Medicine, Beijing 102488, China 2. School of Life Sciences, Beijing University of Chinese Medicine, Beijing 100029, China 3. Lanzhou Foci Pharmaceutical Co., Ltd., Lanzhou 730046, China 4. Insttute of Information on Traditional Chineses Medicine, Chinese Academy of Chinese Medical Sciences, Beijing 100700, China
To establish a HPLC method for the determination of ferulic acid, senkyunolide I, senkyunolide H, coniferyl ferulate, ligustilide and butylidenephthalide in Danggui () using quantitative analysis of multi-components by a single marker (QAMS).The analysis was performed on a Waters X-Select CSH column (250 mm×4.6 mm, 5 μm), with 0.085% phosphoric acid (A) and acetonitrile (B) as mobile phase at the flow rate of 1 mL/min for gradient elution, as well as the wavelength was 265 nm and the column temperature was 40 ℃.All calibration curves showed good linearity (2>0.999) within the concentration range. Ligustilide was used as the internal reference standard, and five relative correction factors (RCF) of ferulic acid, senkyunolide I, senkyunolide H, coniferyl ferulate and butylidenephthalide to ligustilide were calculated, which were 1.073 4, 0.564 8, 0.468 1, 0.926 2 and 1.083 5, respectively. Their content inwas determined by both external standard method and QAMS method. There were no significant differences between two methods.The method of QAMS for six components determination inwas established, which can be used for the quality control of
(Oliv.) Diels.; QAMS; ferulic acid; senkyunolide I; senkyunolide H; coniferyl ferulate; ligustilide; butylidenephthalide
R286.2
A
0253 - 2670(2022)20- 6354 - 07
10.7501/j.issn.0253-2670.2022.20.006
2022-03-03
国家中药标准化项目“大黄等6种中药饮片标准化建设”(ZYBZH-Y-GS-10-B)
李小阳,硕士,研究方向为民族药学。Tel: 15810864572 E-mail: lxy@bucm.edu.cn
王晶娟,教授,研究方向为中药鉴定与质量评价方法。Tel: 13691355913 E-mail: wangjj@bucm.edu.cn
[责任编辑 时圣明]
