不同吸入氧浓度对胸腔镜手术术后肺部并发症的影响
2022-10-21章利川王新强
章利川 谢 晨 王新强
湖州市第一人民医院麻醉科,浙江湖州 313000
胸腔镜手术由于创伤小、恢复快成为胸科手术常规方式。单肺通气(one lung ventilation,OLV)可有效实施肺隔离,便于术野暴露和操作,目前已在电视辅助胸腔镜手术(video–assisted thoracic surgery,VATS)中广泛使用。OLV 时萎陷的患侧肺由于淋巴循环中断、促炎因子释放增加及缺血再灌注损伤可能导致肺损伤;而高氧流量及过度灌注也可能使健侧肺遭受非特异性损伤。目前临床上术中吸入氧浓度(fraction of inspired oxygen,FiO)在肺通气保护策略(lung protective ventilation strategy,LPVS)中并未明确。本研究将探讨VATS 术中不同FiO对术后低氧血症和肺不张的影响,为临床提供可能的参考意义。
1 资料与方法
1.1 一般资料
选取2021 年1 至7 月于湖州市第一人民医院因肺结节拟行全身麻醉下胸腔镜肺部分切除术患者98例,术前根据随机数字表法将患者依次纳入低FiO组(=48)和高FiO组(=50)。两组患者的一般资料比较,差异均无统计学意义(>0.05),具有可比性,见表1。纳入标准:①ASA Ⅰ~Ⅱ级;②年龄18~65 岁;③均接受胸腔镜肺部分切除术。排除标准:①术前上呼吸道感染、胸部CT 提示异常;②肺炎、肺大疱、慢性支气管炎、肺气肿、支气管扩张、肺不张、气胸、胸腔积液、肺水肿;③多部位联合手术;④术前血气PaO/FiO<300mmHg(1mmHg=0.133kPa);⑤入室SpO低于95%;⑥2 周内臂丛神经阻滞或全身麻醉病史;⑦术中胸腔镜中转开胸;⑧术中及术后SpO持续低于90%,且术后带管送往ICU。本研究获湖州市第一人民医院医学伦理委员会审批(审批号:021KYLL047),患者入组前均签署知情同意书。
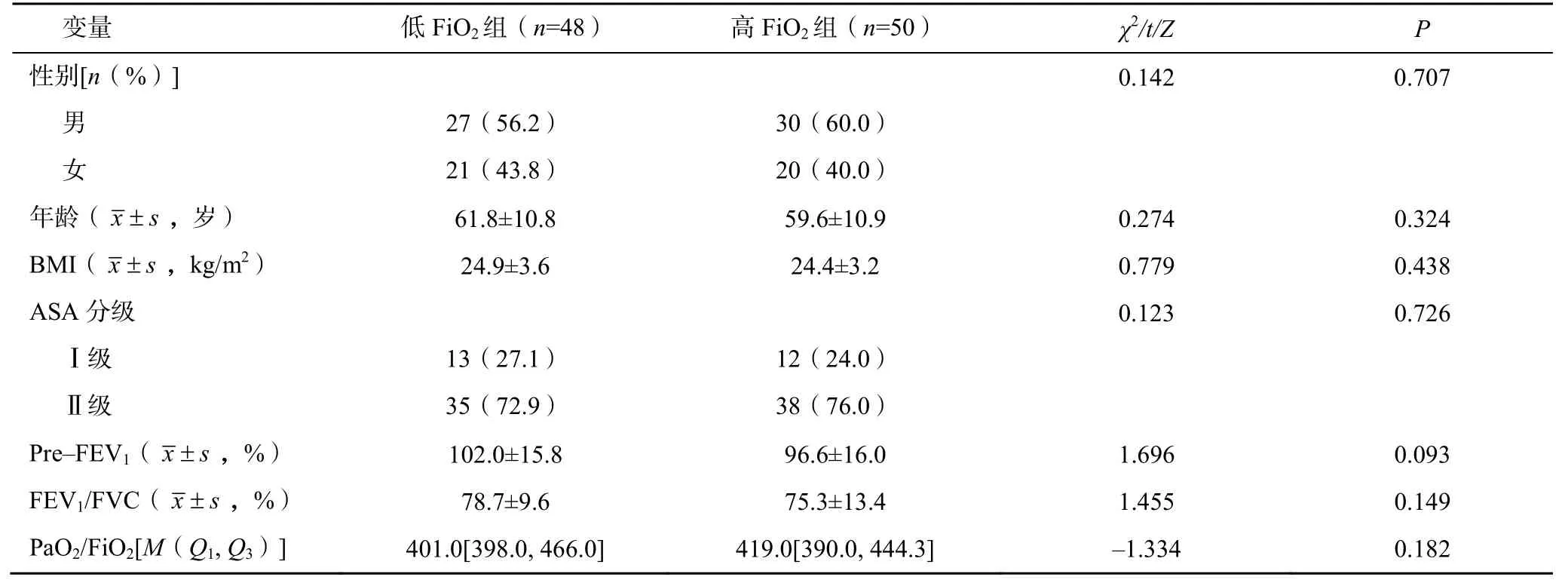
表1 两组患者的一般资料比较
1.2 麻醉方法
患者入手术室后常规心电监护,局麻下建立颈内静脉通路补液,桡动脉置管测量有创动脉压并测血气分析。麻醉诱导前,由2 名有丰富肺超声经验的麻醉医师对患者进行术侧膈肌移动度超声测量,随后面罩吸纯氧6L/min 约3min,采用咪达唑仑0.02~0.05mg/kg、舒芬太尼0.6~0.8μg/kg、依托咪酯0.25~0.35mg/kg 及顺式阿曲库铵0.2~0.3mg/kg 诱导,随后置入双腔气管导管(根据术前气管测量选择适宜型号,一般女性35#,男性37#),并在纤维支气管镜引导下定位。麻醉维持采用吸入七氟烷联合静脉泵注丙泊酚–瑞芬太尼,肌松剂追加使用顺式阿曲库铵3~5mg/次,维持麻醉深度脑电双频指数(bispectral index,BIS)于40~60。术中机械通气采取OLV–容量控制模式,潮气量(tidal volume,Vt)4~6ml/kg,呼吸频率12~15 次/min,吸呼比为1∶2,呼气末正压通气(positive end expiratory pressure,PEEP)为5cmHO,以满足气道压力(airway pressure,Paw)≤25cmHO 且呼气末二氧化碳(exhalal carbon dioxide,PCO)为35~45cmHO。FiO设置低FiO组为50%~60%,高FiO组为61%~80%,氧流量为0.8~1L/min。手术于侧卧位进行,由同一组胸外科医师操作。关胸前进行肋间神经阻滞(0.5%罗哌卡因,100mg),外科医师通过腔镜屏幕可视下由经管麻醉医师进行肺复张,压力为20~25cmHO,持续时间为10~20s,至肺完全膨胀。肺复张完毕后通气模式则改为双肺通气,Vt 为6~8ml/kg,其余参数设置不变,连接胸腔闭式引流。术毕给予托烷司琼5mg 预防术后恶心呕吐,并将患者送至麻醉恢复室(postanesthesiacare unit,PACU)进一步复苏。术后镇痛采用经静脉患者自控镇痛(patient controlled intravenous analgesia,PCIA)(舒芬太尼100μg+托烷司琼5mg+生理盐水稀释至100ml,2ml/h)。拔管前予以新斯的明0.02mg/kg,心率明显下降则予阿托品0.005~0.01mg/kg。拔管后鼻导管吸氧3L/min,30min 后再次进行动脉血气分析。且上述2 名麻醉医师对患者依次进行床旁超声检查判断有无肺不张,由手术操作导致气胸及胸腔积液亦做相应记录,同时测量手术侧膈肌移动度判断呼吸恢复情况。患者安返病房后,于术后24h 及48h 再次进行肺超声及膈肌超声检查。
1.3 观察指标
主要观察指标:①手术方式、手术时间、单肺通气时间等;②术后氧合指数(PaO/FiO);③术后低氧血症(PaO/FiO<300mmHg)及术后肺不张发生率。次要观察指标:①术中平均SpO值和最低SpO值;②术后膈肌移动度。
1.4 统计学方法

2 结果
2.1 两组患者术中及术后指标比较
术中两组患者平均SpO与最低SpO比较,差异无统计学意义(=0.392)。术后低FiO组患者的PaO/FiO低于高 FiO组,差异有统计学意义(<0.01);两组患者的低氧血症发生率比较,差异无统计学意义(=0.654),见表2。
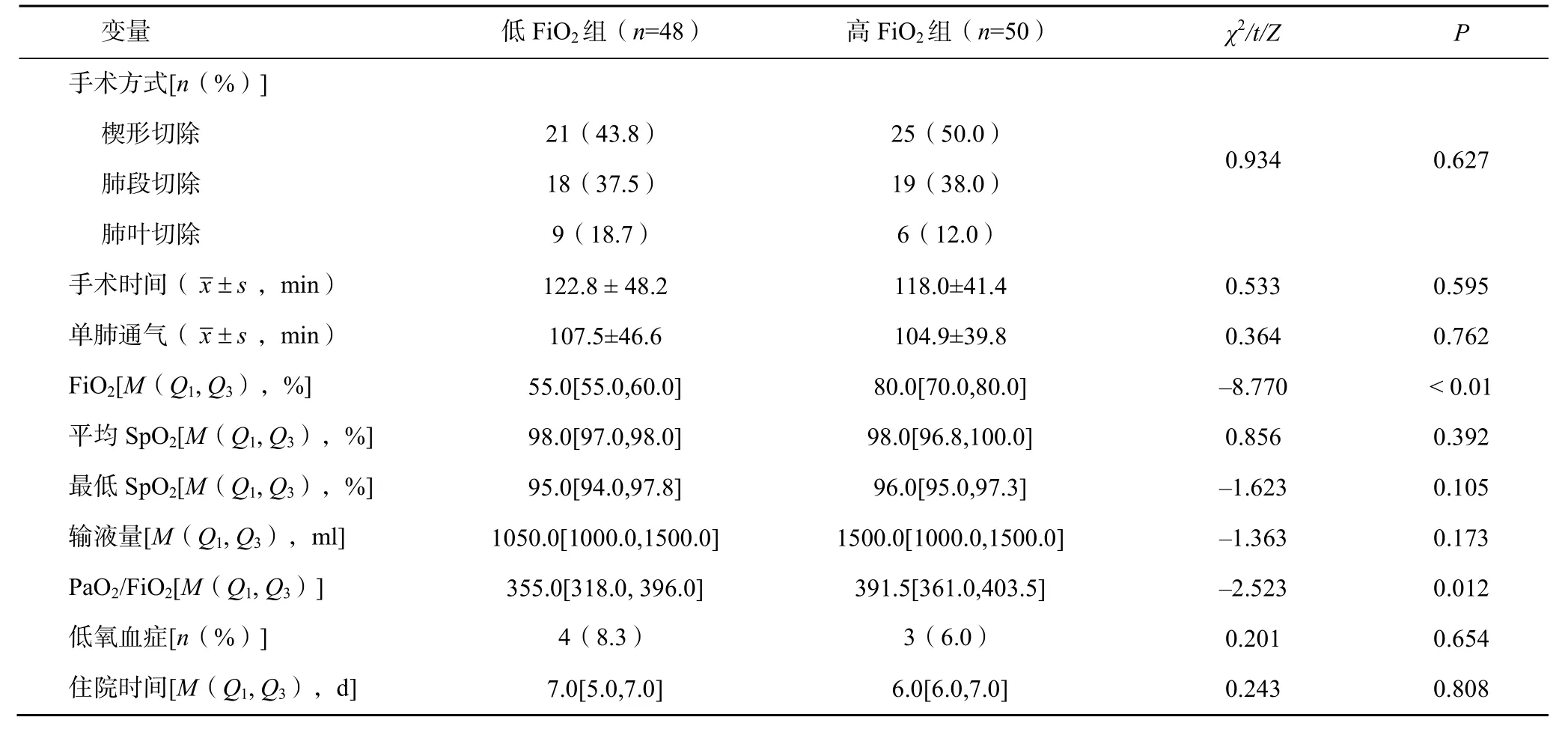
表2 两组患者术中及术后指标比较
2.2 两组患者术后气胸与胸腔积液发生情况比较
患者拔管后30min、术后24h 及48h 肺超声检查均未见明显肺不张。手术操作导致少量气胸与胸腔积液随时间呈下降趋势,组间比较差异无统计学意义(>0.05),见表3,4。
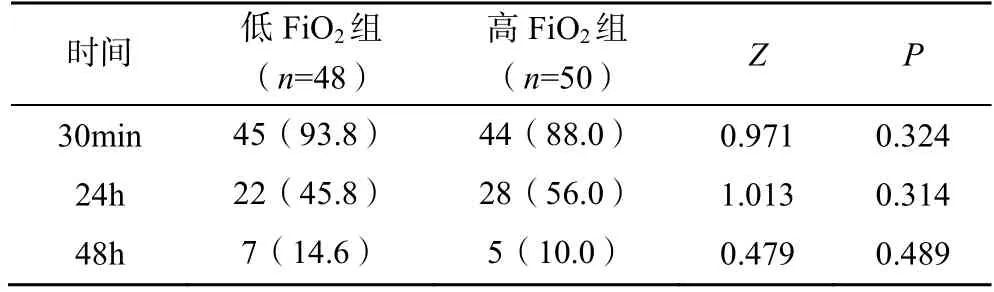
表3 两组患者术后不同时间气胸发生率比较[n(%)]
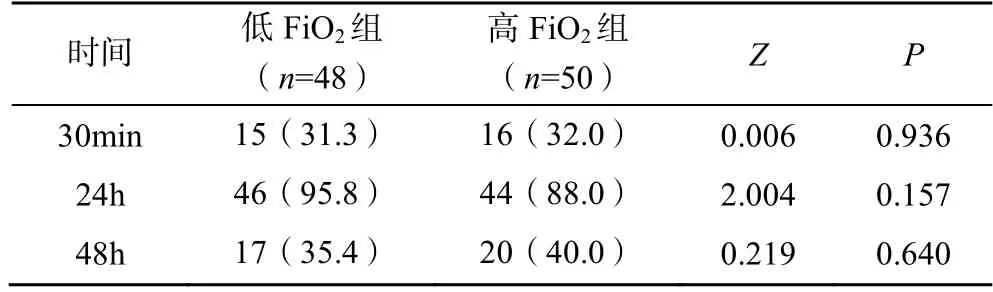
表4 两组患者术后不同时间胸腔积液发生率比较[n(%)]
2.3 两组患者围手术期膈肌移动度比较
与术前相比,低FiO组与高FiO组术后30min膈肌移动度明显下降(<0.01),术后24h 及48h恢复至术前水平,组间比较差异均无统计学意义(>0.05),见表5。

表5 两组患者围术期膈肌移动度变化比较()
3 讨论
OLV 使得复杂的肺、纵隔、食管等胸科手术顺利进行,但可能造成肺内分流增加和低氧血症,缺氧可能导致房颤、心肌抑制、肺动脉高压及术后认知功能障碍发生率增加。故VATS 围手术期低氧血症仍是麻醉医师迫切关注的首要问题。氧浓度过高可能导致吸收性肺不张、冠状动脉和周围血管过度收缩。Raikhelkar 等证实,采用中等度FiO具有肺保护作用,本研究采用低FiO50%~60%和高FiO61%~80%进行比较,结果显示,低FiO和高FiO均可完成OLV 手术,证实VATS 术中采用FiO50%~60%,术后低氧血症或肺部并发症发生率并未增加,同时验证较低FiO具有肺保护作用。
高潮气量(Vt>10ml/L)和高气道压(Paw>28cmHO)导致通气侧肺过度灌注和膨胀引起肺泡弥漫性损伤,故急性肺损伤(acute lung injury,ALI)在健侧肺更常见,但在临床上尚未被重视。肺保护通气(lung protective ventilation,LPV)可保持足够的气体交换,保护肺部免受炎症侵袭。低Vt(4~6ml/kg)联合适度PEEP,同时保障Paw< 25cmHO 已被证明可减少急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)患者肺容积损伤、肺不张和气压伤。PEEP 可在一定程度上避免肺泡塌陷和肺内分流造成死腔量增加,缺乏PEEP 又可导致肺不张发生。肺复张方法(recruitment maneuver,RM)联合PEEP 则进一步促使肺泡膨胀,改善V/Q 失调、增加肺顺应性。本研究中,两组患者皆采用低Vt、添加PEEP 和RM 来避免肺膨胀不全和过度膨胀,故两组尤其高FiO组术后随访并未出现明显肺不张。
虽然低Vt、PEEP 联合RM 作为LPV 主要内容已达成共识,但当前有关胸腔镜手术LPV 并未对FiO有明确规定,国内外探讨术中不同FiO对术后肺部并发症影响的报道较少,故临床中对FiO设置多数依据麻醉医师的经验和偏好。由于OLV 时病理生理变化复杂,术中FiO对肺内分流、再灌注损伤及炎症因子释放等产生不同程度影响,故本研究以术后肺不张及低氧血症为主要观察指标,亦是临床上患者术后常用观察项目,为临床上精准麻醉的实施提供基础。虽然高FiO组氧合指数显著高于低FiO组,但氧合指数受FiO影响,术后是否需要干预主要取决于低氧血症发生。本研究结果证实,FiO50%~60%即可有效维持术中氧合,且未导致术后低氧血症发生率增加,可能原因如下:其一,本研究纳入人群为健康成年患者,排除术前肺部存在异常者,患者术前肺功能正常,对FiO50%~60%可有效耐受。故针对老年患者及术前肺部影像学检查患者,相关研究需进一步探讨,亦是本研究的主要不足之处;其次,胸腔镜手术日益进步,创伤小、手术时间短也是患者预后较好的因素之一,且手术结束后拔管前肺复张可有效避免术后肺不张;由于在早期研究中本团队已证实床旁肺超声与胸部CT 相比具有极高准确性,为避免患者术后来回转运及辐射损伤,故采用肺超声作为术后随访的主要检查工具;最后,早期下床活动及翻身拍背咳痰的有效病房宣教及患者配合等诸多因素,使得术后48h 内随访两组患者均未发生肺不张,呼吸功能亦逐渐恢复至正常水平。
综上所述,胸腔镜手术基于低Vt、PEEP 联合RM 的LPVS,与高FiO相比,较低FiO可有效维持术中氧合且未导致术后低氧血症发生率增加。同时术后48h 内未发生肺不张,呼吸功能恢复至术前水平,但远期并发症有待进一步研究。
