薏苡仁新标准中玉米赤霉烯酮测定法的方法确认及验证过程
2022-10-20谢燕
谢燕
福建省龙岩市食品药品检验检测中心,福建龙岩 364000
薏苡仁收载于《中华人民共和国药典》(简称《中国药典》)2020年版一部,来源于禾本科植物薏米Coix lacryma-jobi L.var.ma-yuen(Roman.)Stapf的干燥成熟种仁。新版《中国药典》与旧版比较,薏苡仁项下只新增了玉米赤霉烯酮的限量检查,其他无变化,《中国药典》同时也新增了玉米赤霉烯酮测定法的两个方法:液相色谱法和液相色谱-串联质谱法。药品检验机构在首次使用薏苡仁新标准时,必须进行方法确认,并对分析方法中关键的指标进行有选择性的验证。验证的指标有:专属性、准确度、精密度、检测限、定量限、线性、范围和耐用性。实验室应验证哪些指标,并没有一个统一明确的规定,这就导致实验室需要自主判断方法的复杂程度,确定哪些方法学参数对检验结果影响最大。本文以“玉米赤霉烯酮测定法”的第二法为实例,对方法确认的内容进行阐述。
1 材料与方法
1.1 材料
1.1.1 样品
薏苡仁,采购于普通药店,样品信息具体见表1。所有批次样品粉碎过2号筛备用。

表1 样品信息
1.1.2 标准品
玉米赤霉烯酮对照溶液(中国食品药品检定研究院,批号:610022-202101)。
1.1.3 主要试剂
甲醇、乙腈为色谱纯,水为一级水,氯化钠为分析纯;ZearaStar型免疫亲和柱(Romer labs),Whatman玻璃微纤维滤纸(cytiva)。
1.1.4 主要仪器

1.2 方法
1.2.1 色谱-质谱条件

1.2.1.2 质谱条件 采用电喷雾离子源(electrospray ion source,ESI),负离子扫描,多反应监测(multiple reaction monitoring,MRM)模式,离子源温度:500℃,电喷雾电压:-4500 V,气帘气:35.0 psi,离子源气1:50 psi,离子源气2:50 psi,碰撞气:氩气。组分的质谱分析参数见表2。

表2 玉米赤霉烯酮的保留时间及质谱分析参数
1.2.2 溶液的制备
1.2.2.1 对照品贮备溶液 精密量取玉米赤霉烯酮对照溶液1 ml置于100 ml量瓶中,加甲醇定容至刻度,摇匀,即得。经含量折算后,浓度为101 ng/ml。
1.2.2.2 供试品溶液 取薏苡仁粉末20 g,加氯化钠4 g,精密加入90%乙腈100ml,匀浆处理2min(13000r/min),离心10 min(4000 r/min),精密量取上清液10 ml,置50 ml量瓶中,用水稀释至刻度,摇匀,离心10 min,用玻璃纤维滤纸滤过,精密量取续滤液20 ml通过免疫亲和柱,用水10 ml重力自然洗脱,弃去洗脱液,使空气进入柱子,将水挤出柱子,再用1.5 ml甲醇浸泡柱子约3 min后收集洗脱液,置2 ml量瓶中,并用甲醇稀释至刻度,摇匀,用微孔滤膜(0.22 μm)滤过,取续滤液即得。
1.2.2.3 空白溶液 除不加供试品外,同供试品溶液操作制备。
1.2.2.4 对照品加标溶液 精密量取玉米赤霉烯酮对照溶液适量加90%乙腈制成0.1 μg/ml的溶液。
2 方法确认的验证内容与结果
2.1 专属性(空白试验)
采用空白溶液来判断在目标物区域是否存在干扰。当空白溶液的干扰峰峰面积不高于标准曲线浓度最低点峰面积的一半时,可认为专属性良好。结果显示空白溶液在对照品相同保留时间处无干扰峰(图1)。
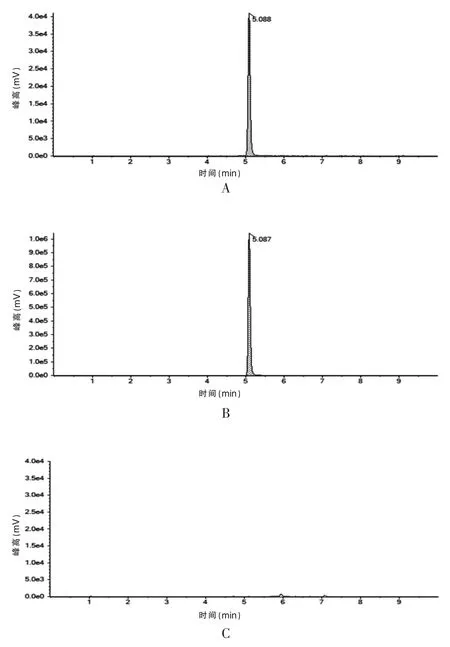
图1 薏苡仁(174.9/317.3)色谱图
2.2 准确度(加样回收试验)
精密称取薏苡仁(批号:2009004)粉末20 g,精密加入对照品加标溶液20 ml,按照“1.2.2.2”项下方法制备加标样品溶液,平行制备6份,依法进行测定,计算回收率,具体见表3,结果提示方法的回收率良好。

表3 加标回收试验结果(n=6)
2.3 精密度
2.3.1 方法精密度(重复性)
取同一批样品(批号:2009004)按照“2.2”项下方法制备加标样品溶液,平行制备6份,依法进行测定,计算RSD为3.09%,结果表明方法的精密度良好。
2.3.2 仪器精密度
精密量取同一对照品溶液连续进样测定7次,测定峰面积的RSD,结果为1.02%,表明仪器精密度良好。
2.4 检测限
检测限可分为两个部分,仪器检出限和方法检出限,验证的是方法检出限,本文采用信噪比法进行分析,精密量取“2.2”项下的加标样品溶液适量,不断稀释至被测物质注入超高效液相色谱-质谱仪后的信噪比≥3∶1。结果显示玉米赤霉烯酮峰的信噪比为7,相应的加标样品溶液浓度为0.0404 ng/ml,当供试品溶液中药材含量为0.4 g/ml时,本实验检出限为0.1 μg/kg,标准规定检出限为1 μg/kg,表明方法灵敏度良好。
2.5 定量限
采用信噪比≥10:1测定定量限时,本实验定量限为0.3 μg/kg。根据《中国药典》的要求,定量限结果应符合准确度和精密度要求,因此要用与0.3 μg/kg这个数据含量相近的样品进行验证。在进行方法确认时笔者认为无须采用此定量限,在能满足小于标准规定的定量限4 μg/kg时同时也满足获得的信噪比大于等于10∶1即可。因此本实验以校准曲线最低点的浓度(1.515 ng/ml)作为定量限(3.8 μg/kg)。
验证过程:精密称取薏苡仁(批号:2009004)粉末20 g,精密加入对照品加标溶液0.5 ml,按照“1.2.2.2”项下方法制备加标样品溶液,平行制备3份,依法测定峰面积,重复测定3次,计算回收率,结果显示信噪比平均值为508,精密度和准确度结果见表4。
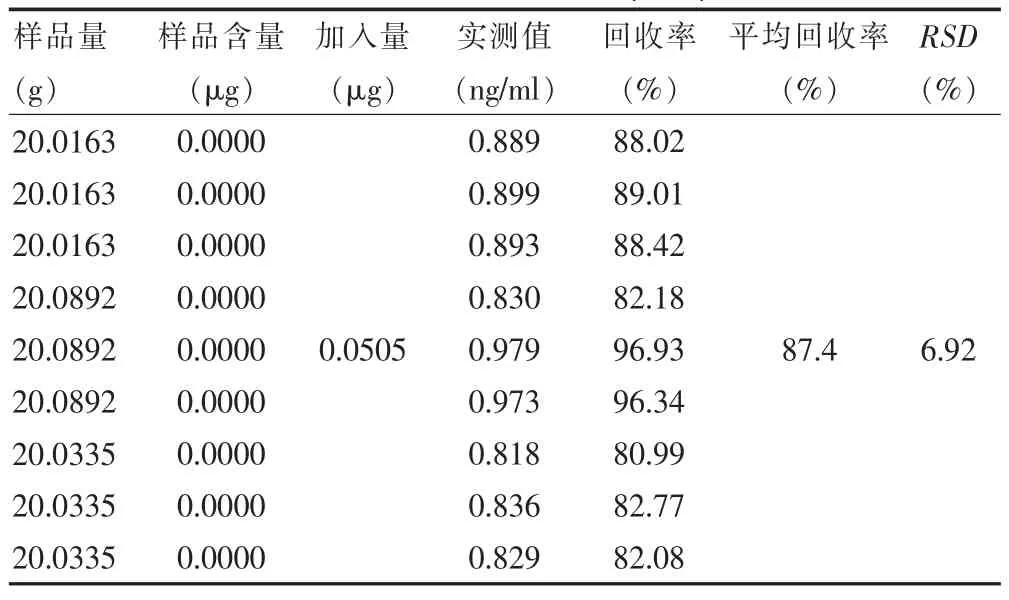
表4 定量限验证结果(n=9)
2.6 线性关系考察
精密量取对照品贮备溶液,用甲醇稀释制成浓度为1.515、5.050、10.100、20.200、50.500、75.750 ng/ml的系列对照品溶液。精密吸取上述系列对照品溶液各5 μl,注入超高效液相色谱-质谱仪,测定峰面积,重复测定2次,以峰面积为纵坐标,进样浓度为横坐标,绘制标准曲线。结果显示在1.515~75.750 ng/ml范围内呈良好的线性关系,具体见图2。
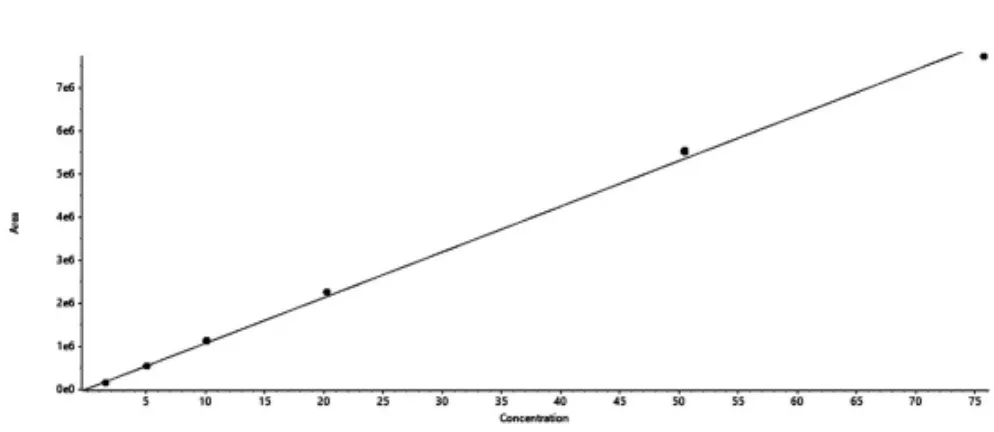
图2 薏苡仁(174.9/317.3)线性关系
2.7 样品测定
取3个批次样品依法操作,计算供试品的含量(表5)。

表5 样品中玉米赤霉烯酮的含量测定结果和检测结果
3 讨论
3.1 实验过程遇到的问题
在供试品溶液的制备过程中,发现离心并不能使溶液澄清,上清液仍浑浊,通过免疫亲和柱时,流速十分缓慢,因此增加了玻璃纤维滤纸过滤这一步骤;其次,每一步洗脱都要等到柱内液体近干时再进行下一步,否则目标物还未被吸附就随着洗脱液一起被洗脱出去;最后增加甲醇浸泡这一步骤也是为了充分将目标物洗脱出来,提高回收率。
3.2 离子对的选择
《中国药典》没有指定定量离子对,笔者选用了响应值高(174.9/317.3)的作为定量离子对,这是为了提高检出限,便于定量。
3.3 报告限的使用
在“中药中有害物质痕量残留检测分析质量控制指导原则”(中国食品药品检定研究院2015年试行版本)中提到了“报告限”,指的是被作为数值报告的最低浓度,一般等于或略高于最低校准浓度,可以是“2.5”节的定量限,也可以是1/10最大残留限量(maximum residue limit,MRL),只要能满足风险分析的技术要求,实验室可以自行拟定。例如薏苡仁标准规定每1000 g含玉米赤霉烯酮不得过500 μg,本文便以1/10 MRL作为报告限(即50 μg/kg),见表5;将报告限的数值固定后,就不必每一次都测定检出限,可以节约很多的人力和物力。
4 结论
方法确认过程并不是方法验证的重复过程,而是实验室在实际检验条件下进行的适应性考察,需要充分考虑分析方法的复杂程度以及被测样品的特点;对于玉米赤霉烯酮测定法这种前处理过程复杂且浓度范围较大的痕量分析方法,建议对检测限、定量限、专属性、准确度、精密度等5个指标进行验证;对于含量测定这种常量分析方法,建议对准确度、精密度、专属性进行验证;而对于鉴别方法来说,建议对专属性进行验证。
