锂离子电池二硫化钼基负极材料研究进展
2022-10-18杨慎慎
王 伟,刘 伟,吴 杨,杨慎慎
(1.河南科技大学材料科学与工程学院,河南洛阳471023;2.金属材料磨损控制与成型技术国家地方联合工程研究中心)
近年来,锂离子电池(LIBs)以其容量大、体积小、循环寿命长以及清洁无污染等特点广泛应用于电动汽车、便携式设备和可穿戴电子产品[1-4]。石墨由于导电性好、放电平稳、价格便宜,成为目前应用最广泛的商用LIBs负极材料[5]。但石墨存在两个明显缺陷[5-6],一是电化学性能相对较差,库伦效率和倍率性能较低,理论容量仅为372 mA·h/g;二是石墨与电解液相容性差,电解液中的溶剂分子在充放电过程中也会随锂共嵌入石墨层间,使石墨的晶体结构发生膨胀,从而直接影响其循环性能和嵌锂容量。因此石墨负极已逐渐不能满足LIBs 未来大容量、大功率充放电的需求。
金属硫化物因其特殊的类石墨烯层状结构以及高比容量(如MoS2理论容量达670 mA·h/g)的特点,成为极具发展潜力的LIBs用负极材料[7-8]。MoS2具有典型的类石墨烯结构,层内Mo—Mo间距为0.315 nm,以共价键结合,减缓了充放电过程中的体积膨胀效应;层间以弱范德华力结合,为锂离子的扩散提供了便利的通道,便于锂的脱嵌反应。单独使用MoS2作为负极材料也存在一些不足,MoS2材料本身表面能较大,易堆叠团聚,降低了材料与电解液的接触面积,使锂离子难以嵌入材料内部进行反应,导致材料的容量迅速降低;充放电时锂离子的嵌入脱出会导致较大的形变。另外,MoS2导电性较差,离子迁移率低,导致整个体系内阻较高。因此,MoS2材料作为锂离子电池负极材料在实际应用中还具有很大的限制。
近年来大量的研究工作表明MoS2粉体材料的纳米化和复合化是解决上述MoS2负极材料问题最为有效的两种途径。MoS2尺度达到纳米级后能够显著增加反应的活性位点,提高离子输运效率、提升结构稳定性。目前文献中所制备出的MoS2纳米形貌包括一维(1D)的纳米线[9]、纳米管[10],二维(2D)的纳米片[11-12]以及三维(3D)的纳米花[13-14]、纳米球[15]等。除了有效调控MoS2的纳米形貌,复合化也是提高MoS2电极材料综合性能的常用方法。可通过将MoS2与其他单质或化合物等复合的手段减少纳米片层的堆叠和聚集,同时提高整体结构的导电性,改善MoS2负极材料电化学性能和循环过程中的体积膨胀问题,提高其循环稳定性。
在实际研究工作中,MoS2材料复合的过程中往往需要同时控制其纳米形貌,因此,本文按照不同材料体系分类总结了MoS2分别与碳材料、锡、过渡金属氮化物、金属氧化物以及硫化物复合方面的研究进展,并对未来MoS2基复合材料的发展方向进行了展望,为MoS2基材料能实际应用于新能源和纳米复合材料等领域提供借鉴。
1 二硫化钼基负极材料研究进展
1.1 二硫化钼/碳基复合材料
目前,可与MoS2协同复合的碳材料分为无定形碳和特定形貌的纳米碳材料。
1.1.1 二硫化钼/无定形碳
无定形碳(如糖碳)孔隙率大、原料丰富、价格低廉。CHANG 等[16]以钼酸钠、硫脲和葡萄糖为原料,首次通过水热反应合成类石墨烯结构的MoS2单层纳米片与无定形碳结构的复合物。该MoS2@C复合物的电化学性能较单一MoS2有了显著提升,葡萄糖添加量为1 g 时,最高可逆容量为962 mA·h/g,并可在循环充放电100次后仍保持在912 mA·h/g。艾经伟等[17]以苹果酸为碳源,采用连续的水热法-热分解碳包覆-水热法,将无定形碳包覆在MoS2纳米带上,得到了3 层分级结构的C@MoS2@C 复合材料。该材料在200 mA/g的恒流充放电条件下循环100次后放电比容量达到1 025.5 mA·h/g,甚至在1 A/g 的大电流密度下的放电比容量仍高达820 mA·h/g,证明这种碳包覆结构的构建充分发挥了碳材料的导电性,大幅提高了MoS2的稳定性。XU 等[18]采用一步水热法在改性竹炭(MBC)上生长出均匀分散的MoS2纳米花,初始容量高达1 867 mA·h/g,在200 mA/g的电流密度下循环200次后的可逆容量为672 mA·h/g,甚至在1 600 mA/g的高电流密度下循环200次后仍然可达581 mA·h/g。实验证明MBC 的多孔结构和大的比表面积可以缓解MoS2的体积膨胀,提高电导率,从而达到提升MoS2电化学性能的效果。虽然无定形碳能够在一定程度上提升MoS2的结构稳定性,但仍然面临包覆层数及厚度不可控、造粉困难等问题,从而导致制备结果可重复性较差。
1.1.2 二硫化钼/特定形貌的碳
特定形貌的纳米碳材料如碳纳米管(CNTs)、石墨烯等由于比表面积大、导电性好、柔韧性高,也是MoS2/C复合材料的关注焦点[19]。CNTs长径比大、离子扩散路径短、电子传递效率高,可以有效地与MoS2产生协同效应。LEI 等[20]采用化学气相沉积(CVD)法将碳纳米管均匀地沉积在碳纤维布(CFC)上,形成CNT-CFC基体。之后分别以Na2MoO4和L-半胱氨酸为钼源和硫源,在CNT-CFC上生长出渔网状MoS2金属相异质结构(3D@1T-MoS2的合成机理如图1所示)。图2为3D@1T-MoS2样品在Ar气氛下700 ℃煅烧前后的电镜照片。由图2可以看出,纳米管结构的3D@1T-MoS2直径约为300 nm,部分纳米管结构的有机物在煅烧后发生碳化,结构收缩。煅烧前小尺寸的MoS2(约为20 nm)在纳米管结构上垂直生长,但经煅烧后转变为直径约为300 nm的独立1T 相,并被石墨碳覆盖。3D@1T-MoS2和3D@1TMoS2-700电极具有良好的倍率性能和库伦效率,其最高比容量分别为1 454 mA·h/g 和1 955 mA·h/g(如图3 所示)。MoS2-CNT 具有良好的电化学性能且高温退火后锂储存能力显著提高。
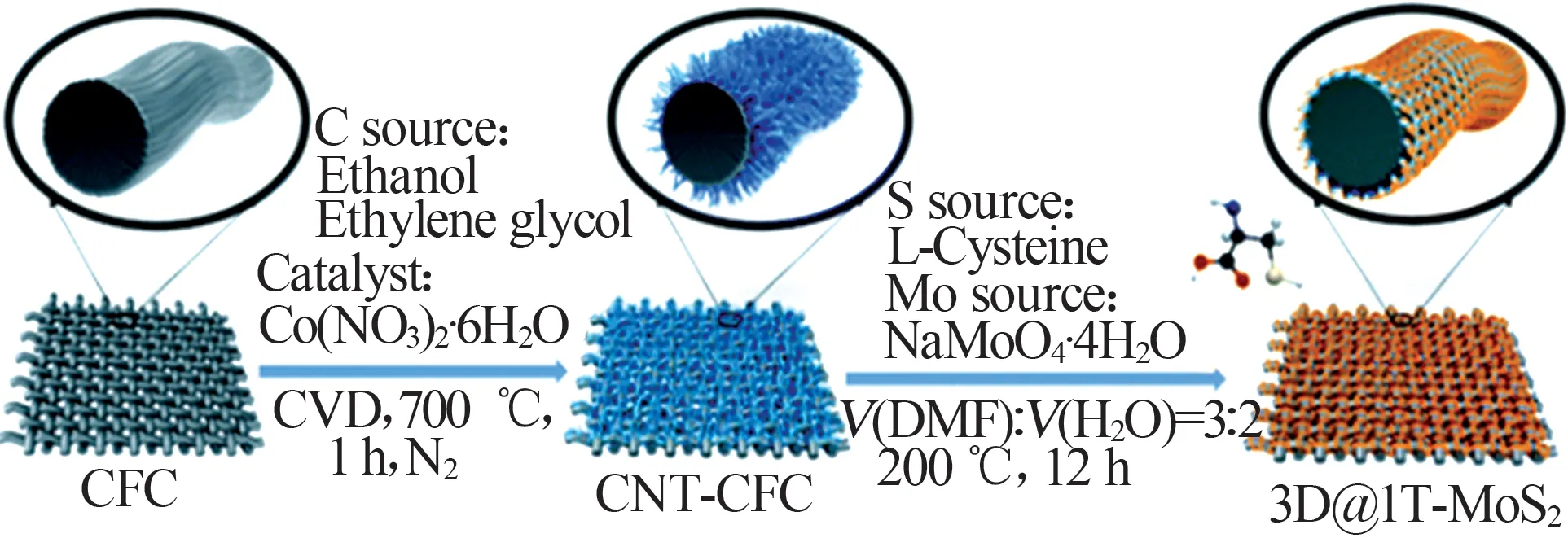
图1 3D@1T-MoS2的合成机理示意图[20]Fig.1 Schematic illustration of synthesis mechanism of 3D@1T-MoS2[20]

图2 700 ℃退火前/后3D@1T-MoS2的SEM和TEM图[20]Fig.2 SEM and TEM images of 3D@1T-MoS2 before/after annealing at 700 ℃[20]
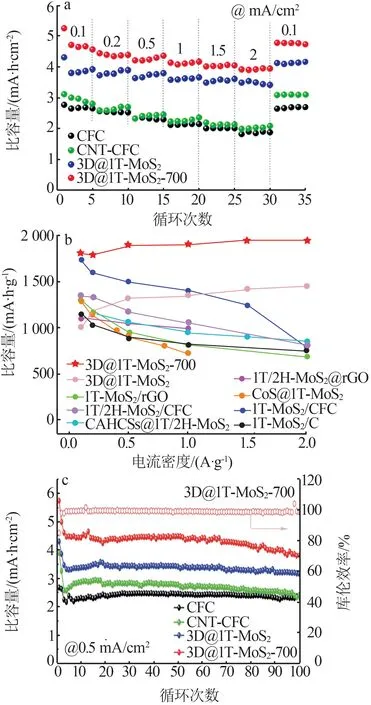
图3 3D@1T-MoS2样品电化学性能[20]Fig.3 Electrochemical properties of 3D@1T-MoS2 samples[20]
石墨烯由于其优良的导电性、热稳定性和化学稳定性、较大的比表面积和柔韧性,也可作为生长纳米MoS2的有效衬底。水热法和溶剂热法是制备MoS2/石墨烯复合材料最常用的方法。XUE 等[21]以聚苯乙烯为硬模板,采用水热法成功合成了二硫化钼/还原氧化石墨烯(rGO)空心复合材料。空心的二硫化钼微球粒径约为180 nm,分散在石墨烯表面,在500 mA/g 电流密度下循环100 次后的比容量达752.4 mA·h/g。由于纳米二硫化钼具有较高的表面能,发生了自聚集现象,与其他碳材料相比并未凸显石墨烯自身的优势。因此,保持二硫化钼与石墨烯较大的接触面积是充分发挥二硫化钼/石墨烯复合材料优势的关键。研究发现根据二维石墨烯材料构建三维结构是解决这一问题的有效途径。LONG等[22]采用水热法合成了一种独特的MoS2/石墨烯复合材料(MoS2/GrF),由于“空间限制”效应,二硫化钼微球(平均直径为750 nm)贯穿石墨烯纳米片,不仅有效抑制了MoS2沿着(002)面的团簇现象,而且使(002)晶面间距由0.62 nm 扩大到0.72 nm,为扩大MoS2基材料的嵌锂容量提供了理论依据。同时,在石墨烯层之间生长的二硫化钼可以形成良好的接触,减少了接触电阻。MoS2/GrF 电极具有良好的可逆容量,在100 mA/g 的电流密度下循环200 次后比容量可达1 510 mA·h/g。WANG 等[23]以P123 为模板,采用水热法在泡沫石墨烯(GF)表面自组装生成蜂窝状二硫化钼(HC-MoS2@GF)(合成设计原理如图4所示)。图5为HC-MoS2合成样品的FESEM图,从图5a~c 可以看出合成的纳米片的横向尺寸约为100 nm,相邻的纳米片随机连接,自组装成三维蜂窝结构。这种内部的交联结构可以有效地防止重复充放电过程后的片层聚集和机械失效。多孔结构保证了MoS2纳米片与电解液的高接触面积,也便于锂离子和电子的快速输送,从而具有优异的电化学性能。与此形成强烈对比的是,在没有GF 的情况下,完全相同的合成工艺产生了直径约为1.5 μm 的MoS2空心球(HC-MoS2),空心球是由相互连接的纳米薄片构成的,厚度约为200 nm(见图5d),比HCMoS2@GF 复合结构的壁厚几十倍。MoS2片层约为3~5 层,沿(002)晶面的层间距为0.64 nm,沿(100)晶面的层间距为0.27 nm,与2H-MoS2晶型基本吻合。HC-MoS2@GF 展现了极佳的循环稳定性,在200 mA/g 电流密度下循环40 次后的比容量可达1 100 mA·h/g,容量保持率为99%。在5 A/g 的高电流密度下,比容量可达800 mA·h/g。
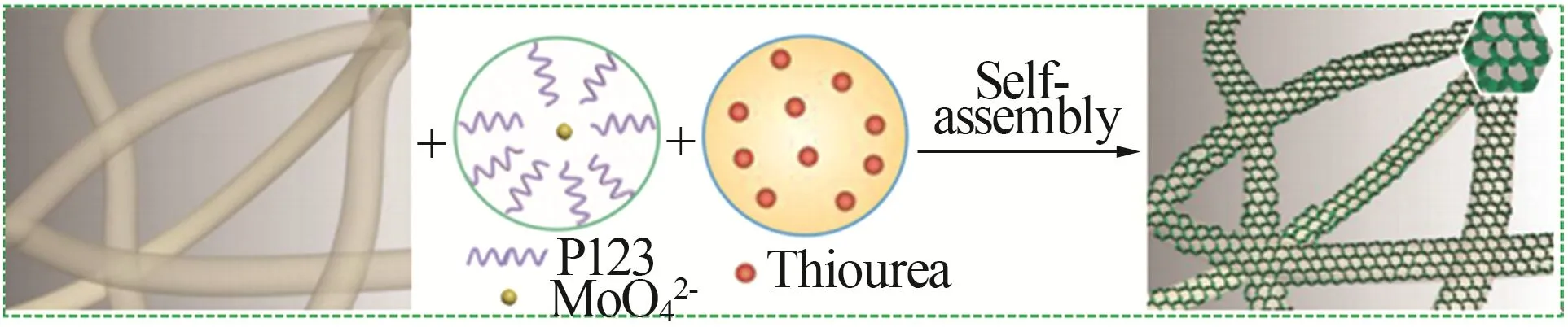
图4 蜂窝状纳米结构MoS2@GF合成原理图[23]Fig.4 Schematics of the fabrication of the honeycomblike nanoarchitectures MoS2@GF[23]

图5 HC-MoS2在有/无GF基质条件下合成样品的FESEM图[23]Fig.5 FESEM images of HC-MoS2 synthesized sampleswith/without GF substrate[23]
MoS2/特定形貌的碳基复合材料能够改善电化学性能主要有以下原因。第一,花状的MoS2微球原位生长在碳基材料上,可以提供丰富的边缘活性位点。第二,碳作为载体有效抑制了MoS2微球的堆叠团聚,增大了活性物质与电解质的接触面积,从而获得较高的储锂容量。第三,碳基材料的引入一定程度上会使MoS2的(002)晶格平面对应的层间距增大,在为锂离子的嵌入提供了更大的空间的同时也会加快锂离子扩散速度。第四,碳基材料可以强化体系结构,改善锂化过程中的体积膨胀问题,大大提高循环寿命。第五,碳基材料可以增强体系的导电性,提高离子、电子传输效率。
1.2 二硫化钼/非碳基复合材料
1.2.1 二硫化钼/锡基材料
锡及其氧化物具有理论容量大、资源丰富、环境友好等优点,是一种很有前途的负极材料[24]。单一的锡基材料最致命的缺陷是充放电过程中会出现巨大的体积膨胀效应。LU 等[25]以(NH4)6Mo7O24·4H2O和SnCl2·2H2O 为原料,采用两步溶剂热法合成了锡掺杂二硫化钼纳米花,并在Ar(H2)气氛中退火处理,生成Sn/MoS2复合物。Sn/MoS2复合材料作为锂离子电池负极材料,在电流密度为200 mA/g 时,经过100 次循环后,放电容量达到1 000 mA·h/g 以上,库伦效率接近100%。与未掺杂Sn 的MoS2相比,具有更高的可逆容量和更好的循环性能。
1.2.2 二硫化钼/Mxenes复合材料
Mxenes 是一种新型二维过渡金属氮化物、碳化物或氮碳化物纳米材料的统称,比表面积大、导电性能好、层间距大、储锂容量较高[26-27]。Mxenes 可以与MoS2复合,构建良好的导电网络,加快离子、电子运输效率。复合材料可以抑制MoS2在循环过程中的体积膨胀问题,表现出优异的电化学性能。CHEN等[28]采用液相混合法在Mo2TiC2Tx片层之间掺入S 颗 粒,在 惰 性 气 氛 中500~700 ℃加 热,使Mo2TiC2Tx表面的Mo-O 基元转化为MoS2,同时去除残留的硫,形成MoS2/Mo2TiC2Tx异质结构。经500 ℃热处理后,Mo2TiC2Tx的层间距为1.4 nm,表面覆盖着(002)晶面间距为0.69 nm 的少层甚至单层MoS2。随着热处理温度升高至700 ℃,MoS2层间距略微扩大至0.7 nm。MoS2/Mo2TiC2Tx-500 复合材料有较大的层间距,为嵌锂-脱锂过程提供了充足的缓冲空间,作为锂离子电池负极材料时可以大幅度提高循环稳定性,在100 mA/g充放电500次后的充电、放电容量可达554、646 mA·h/g,容量保持率为86%。MOON 等[29]采用射频磁控溅射沉积法制备出MoS2-TiN负极材料,初始放电容量为789.2 mA·h/g,300次循环后容量保持在700 mA·h/g,说明氮化物的引入降低了MoS2转化反应引起的体积变化,有助于电极材料的改进。但氮化物易与电解质反应,生成钝化膜,使电池容量降低,限制了其实际应用。
1.2.3 二硫化钼/过渡金属氧化物复合材料
过渡金属氧化物如TiO2、Co3O4、NiO等理论比容量高(500~1 000 mA·h/g)、成本低、安全性高、循环性能好[30]。TiO2作为负极材料结构稳定,有利于Li+快速的嵌入和脱出[31]。近年来,研究人员发现MoS2/TiO2复合材料在可充电锂离子电池方面显示出巨大的潜力[32]。ZHANG 等[33]采用简单水热法制备出无粘结剂的MoS2-TiO2复合电极材料,经煅烧处理后在800 mA/g的电流密度下循环300次后的容量保持在361.5 mA·h/g,容量保持率为88.0%。这种良好的性能可能来自于分散良好的MoS2纳米颗粒以及煅烧处理后TiO2与MoS2之间的紧密连接构建的特殊三维网络结构。ZHOU等[34]采用自支撑的TiO2复合界面路线,提出了在Ti基板表面生长垂直排列的MoS2纳米片,可以在电流密度为1 000 mA/g 下循环600次后,提供高达1 189 mA·h/g 的放电容量。一些含氧的金属盐类化合物,如TiNb2O7、LiTiNbO5、Li3VO4等,由于其中的金属原子具有多个氧化还原状态Ti4+/Ti3+、Nb5+/Nb4+、Nb4+/Nb3+和较低的体积膨胀率,也常作为MoS2电极材料的基体。PHAM-CONG 等[35]采用水热法用TiNb2O7纳米纤维和超薄MoS2纳米片制备出分层的纳米复合结构,在1 A/g的电流密度下循环200次后的容量为740 mA·h/g,4 A/g的电流密度下循环200次后的容量为611 mA·h/g。ZHANG等[36]采用简单的溶剂热法制备出一种新型的Li3VO4/MoS2复合材料,在100 mA/g电流密度下循环100次后的放电容量为789.1 mA·h/g;在500 mA/g 电流条件下,Li3VO4/MoS2复合物的容量保持在632 mA·h/g,表现出高比容量以及优异的循环稳定性。LI等[37]采用传统三步法依次制备出聚吡咯纳米管PPy、PPy@MoS2以及C@MoS2@TiO2三元复合材料。TiO2层的引入既能适应S向Li2S转变过程中的体积变化,又能缓解长链锂多硫化物溶解引起的“穿梭效应”。C@MoS2@TiO2复合物作为锂离子电池负极时,在2 000 mA/g 的电流密度下循环1 000次后比容量可达455.2 mA·h/g,具有良好的倍率特性以及循环稳定性。
1.2.4 二硫化钼/过渡金属硫化物复合材料
二维过渡金属硫化物有类石墨烯结构,与碳基材料低能量密度、金属氧化物的低电导率相比较,二维过渡金属硫化物如SnS2、Co9S8具有更高的比容量和优异的倍率性能[38]。硫化钴就是一种具有优良锂电性能的负极材料,且在MoS2的形成过程中,充足的硫源可以直接硫化硫化钴系前驱体,得到Co9S8与MoS2的复合材料。基于这个思路,刘瑜琳[39]采用水热法,成功地在石墨纸上制备了MoS2/Co9S8复合纳米结构,从而实现了整体结构导电性和稳定性的提高,100次循环后的比容量为677 mA·h/g,约为单独MoS2电极的4 倍。FOLEY 等[40]制备出由有机金属直接硫化形成的硫化铜(CuxS)碳纳米线复合材料,结果表明,纳米线的性能取决于CuxS 相和晶体形态,Cu1.8S/C-500 材料展现的性能最好,在200 次循环后的比容量为220 mA·h/g。
MoS2与过渡金属硫化物的复合也存在一些问题。硫化物的类石墨烯层状结构的比表面能较大,在晶粒生长过程中容易堆叠、团聚,长循环过程中会使负极材料粉化、失活;其作为半导体材料,电导率相对碳基复合材料低。更为严重的是,过渡金属硫化物经转化反应生成的硫元素极不稳定,易溶解到电解质溶液中,降低了活性物质含量。目前改善MoS2/金属硫化物复合材料的方法也多采用纳米化和复合化。LIU 等[41]提出采用rGO 包覆Co9S8/MoS2复合物,构筑金属硫化物杂化纳米结构的方法,成功制备出Co9S8/MoS2@rGO纳米管。图6显示出该类型电极具有良好的电化学性能:其初始比容量高达1 140 mA·h/g,在100 mA/g的电流密度下循环180次后比容量仍可维持在807 mA·h/g。双金属硫化物的协同效应改善了锂离子反应动力学,保证了结构完整性。还原石墨烯的导电性可以促进电子转移,提高电子稳定性,并适应循环过程中的应变,大幅度改善了双金属硫化物在结构和性能上的缺陷。

图6 Co9S8/MoS2@rGO纳米管样品的电化学性能[41]Fig.6 Electrochemical properties of Co9S8/MoS2@rGO nanotube samples[41]
以上是二硫化钼基复合材料的研究进展情况,各种材料的制备工艺与样品的电化学性能数据列于表1。从表1看出,目前二硫化钼复合粉体的主要制备方法以水热/溶剂热为主。在电化学性能方面,纯MoS2循环性能极差,即使制备成为纳米片状,其充放电性能衰减仍然很快。从目前的研究来看,二元复合体系中二硫化钼与碳材料复合能够得到较高的比容量,但其长期循环稳定性数据较为缺乏,当前的研究大多为100次循环充放电数据,有少量200次循环数据。而MoS2与过渡金属化合物进行复合后尽管比容量较与碳复合低,但多具有良好的库伦效率和循环稳定性。三元体系结合了碳和过渡金属材料的优点,如C@MoS2@TiO2、SnO2@C@MoS2、Co9S8/MoS2@rGO等具有更好的综合电化学性能。另外,因泡沫石墨烯、碳纳米管等第二相本身分散性能较好,与MoS2复合可得到较大的层间距,有利于脱/嵌锂过程。
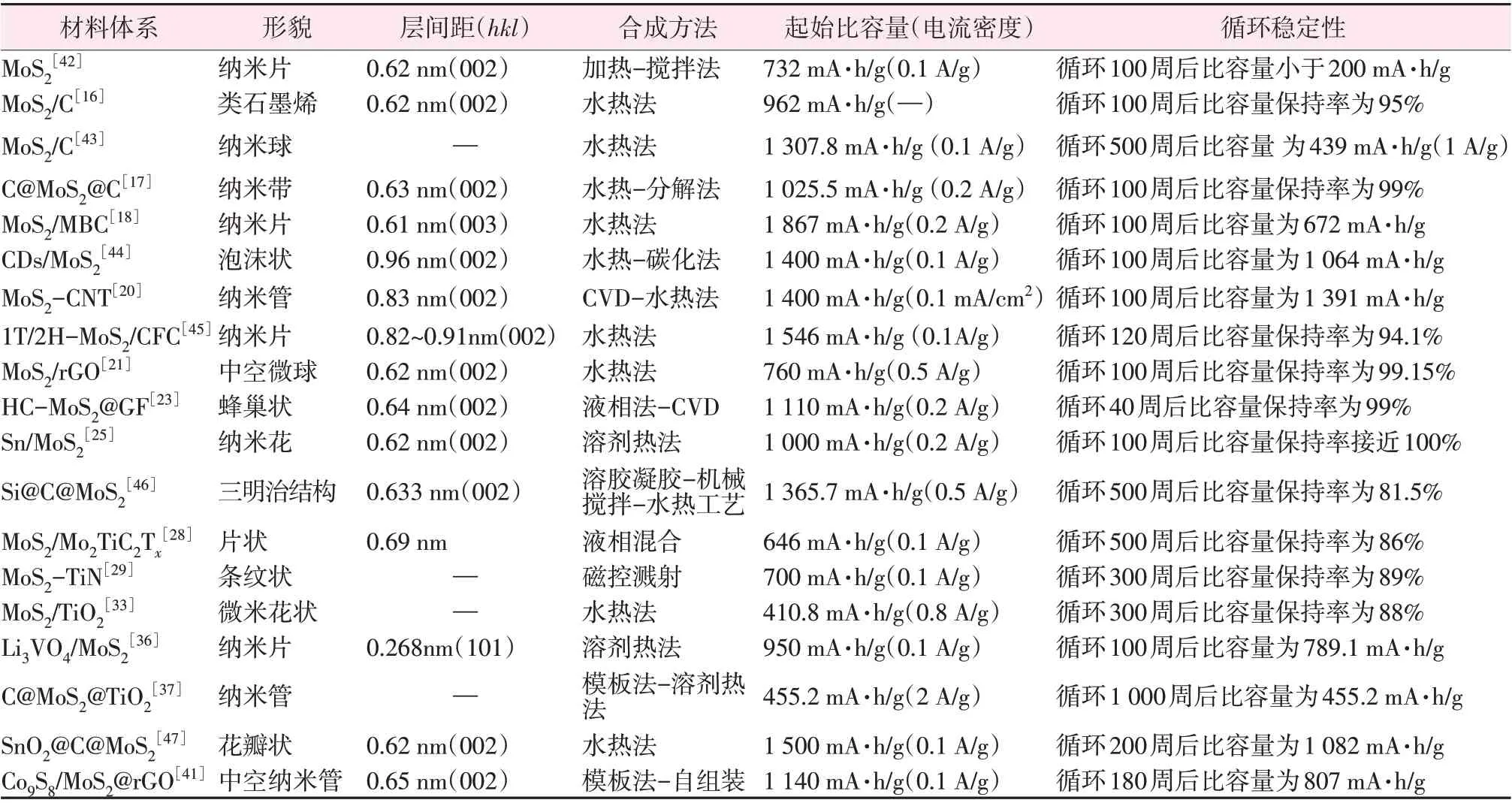
表1 MoS2及典型MoS2基复合材料作为锂离子电池负极材料时的电化学性能数据Table 1 Electrochemical performance data of MoS2and typical MoS2based composite as anode materials
2 结语与展望
负极材料对锂离子电池的性能有着重大影响,MoS2复合材料的本征电化学性质决定了负极的容量与电势,而电极与电解质的稳定接触面积决定了电池的循环寿命。将MoS2与碳基材料、非碳基材料复合,优势互补,得到高比容量、高循环寿命的电极材料成为当下研究趋势,这使得新型锂离子电池能够更广泛应用于便携式电子设备、新能源汽车等行业。
结合二硫化钼材料的结构以及其锂化反应的特点,未来提高MoS2作为锂离子电池负极材料的性能可以从以下方面进行研究。
1)优化二硫化钼纳米材料形貌结构。MoS2自身表面能大,易堆叠团聚,从而降低负极材料中的活性物质与电解液的接触。可选用模板剂作为MoS2前驱体的辅助用料,选择性地调控MoS2的形貌,同时利用复合第二相物质或表面活性剂稳定其纳米形貌、减少团聚,从而稳定电极与电解质的接触面积,有效提高离子运输效率,达到快速充电的效果。
2)通过复合化提高MoS2电极材料的结构稳定性。二元复合物并不能完全解决MoS2作为负极材料体积膨胀严重、循环稳定性差等问题。二硫化钼与碳材料复合能够增强导电性,缓解循环过程中的体积膨胀问题,但碳的库伦效率低,循环100次晶体结构即发生膨胀、剥落,致使锂离子电池寿命急剧下降;二硫化钼与过渡金属氧化物复合能够显著提高比容量,但过渡金属氧化物相比于碳材料电导率低,体积膨胀严重;过渡金属硫化物有类石墨烯结构,与二硫化钼复合能获得与氧化物相比更大的比容量,但仍然不能解决体积膨胀以及循环稳定性差等问题。因此,多元复合物的开发与利用必将成为MoS2作为负极材料的研究热潮,推动锂离子电池向更大型化、工业化的领域拓展。
3)探索新的复合材料体系。富勒烯C60作为碳的同素异形体,具有结构精确、衍生可控、溶解性好、丰富的活性位点等诸多有利于电池应用的独特特性,但与MoS2复合的研究却甚少。原因在于C60作为“嵌入型”储锂材料具有电负性,Li+在C60分子之间形成LixC60,破坏了原本的分子结构,导致其可逆容量差,因此纯C60理论上不适合作为单一负极使用。并且,与一维碳纳米管(CNTs)和二维石墨烯相比,富勒烯基负极材料的合成工艺复杂、成本高,这无疑限制了富勒烯基负极材料在LIBs中的大规模应用。随着科学研究的发展,PARK 等[48]以扭曲六苯并芴烯(cHBC)为有机共晶体,合成了C60/cHBC共晶的柱状结构,有利于提供Li+存储空位,在没有导电剂的情况下实现了C60在锂离子电池负极材料上的应用。该共晶结构在100 mA/g的电流密度下循环600次后的比容量可达330 mA·h/g,为进一步开发MoS2/C60负极材料的研究提供了新的思路。
4)合成机理研究。水热或溶剂热法是目前制备MoS2基复合材料最为常用的工艺,但当前对于硫化钼在高温高压体系中的结晶过程和复合材料的生长规律缺乏系统研究,基本未见晶体生长动力学的文献报道,各种添加剂对产物形貌的控制机理也存在较大分歧。未来,应结合压强、温度等对晶体生长热力学与动力学进行研究,探索不同水热/溶剂热体系中钼及添加元素的析出规律及复合机制,为高品质MoS2基负极材料的可控/可重复合成提供指导。
