NaOH-HCl酸碱法制备超纯煤的实验研究
2022-10-12李伟
李 伟
(浙江煤炭地质勘查院,杭州 310000)
0 引言
超纯煤技术是目前煤炭深加工新技术之一,也是时代发展对煤炭产品要求越来越高的体现。超纯煤是指尽可能地脱除煤中无机矿物质,使其灰分小于1%或2%的高附加值煤产品[1]。超纯煤用途广泛,大致可分为以下几类[1-2]:①直接燃烧,可降低颗粒污染物、SO2、CO2、NOx等污染物排放量、减少污染;②制备精细水煤浆,不仅能提高燃烧效率,还易于调控、方便管理;③炼焦,采用此焦碳进行炼钢可减少焦炭消耗,降低冶炼成本;④研制煤基新型复合材料,可提高活性炭和碳纳米管等产品性能。显然,广泛应用超纯煤有助于实现环境友好和经济效益双赢,对煤炭清洁加工和综合利用具有重大意义。
目前,超纯煤的生产方法主要有物理法和化学法,其中化学法主要有酸洗法、酸碱法、氢氟酸法、化学煤技术和油团聚-浮选等方法[3-5],其中常规酸碱法应用最广泛[6-7],除用于煤炭深度脱灰外,还用于石墨精制、煤矸石和非金属矿的深加工以及常规水煤浆开发[8]。目前该技术已基本成熟,澳、美、印度等已建成设有酸碱再生、复用、副产物回收工段的中试厂。该方法包括NaOH-HCl、NaOH-H2SO4、NaOH-HCl-HNO3等体系[9-11],以NaOH-HCl法最常见。
NaOH-HCl法属于常规酸碱法,条件也比较成熟。查阅大量相关资料后,发现此法具有产品纯度高、一次性投入少、工艺适应性强等优点,但也存在工艺较为复杂,反应过程中所需高温高压条件对反应设备要求严格,易于腐蚀设备,实际操作危险性大,且副产物难于回收等缺点[2]。为了解决操作繁琐、反应条件苛刻和成本较高的问题,已有研究采用碱低温常压焙烧工艺,对传统酸碱法进行了改良,得到灰分小于0.5%的超纯煤[6]。另外,肖劲等研究了中温条件下酸碱脱灰对煤炭结构变化及热解特性的影响,发现中温条件下采用酸碱法处理煤样,亦能达到很好的脱灰效果,使煤样灰分降至0.5%以下[12-13]。基于此,研究了相对温和的反应条件下,采用NaOH-HCl酸碱法对煤进行脱灰处理工艺,以期对传统的酸碱法制备超纯煤工艺进行改进。
1 试验部分
1.1 试验仪器
XL-2000型马弗炉,SDDH315型电热鼓风恒温干燥箱,BS124S型电子天平,B型玻璃仪器气流烘干器,WS70-1型红外线快速干燥器,JJ-1型精密定时电动搅拌器,KDM型控温电热套,HH-S2型电热恒温水浴锅,SHB-B95型循环水式多用真空泵,HC-TRII-10型普通药物天平,79-2型磁力加热搅拌器,傅立叶变换红外分光光度计,玻璃皿(5个),注射器(20mL),灰皿(10个),玻璃烧杯(250mL,5个),酸碱滴定装置(一套),布氏漏斗(3个),聚四氟乙烯烧杯(50mL,4个),抽滤瓶(3个),石棉网,三口烧瓶(250mL,3个),球型冷凝管(3个),容量瓶(100mL,10个),温度计(200℃,1个),锥形瓶(250mL,3个)。
1.2 试验药品
氢氧化钠(NaOH,分析纯AR),盐酸(HCl,分析纯AR),邻苯二甲酸氢钾(分析纯AR),溴化钾(KBr,分析纯AR),硫酸(H2SO4,分析纯AR),生石灰,酚酞指示剂,去离子水,定量滤纸(中速),pH值试纸(广泛)。
1.3 煤样选择、制备及分析
由于化学脱灰法适用于灰分低的优质煤[14],以低灰、低硫、低磷、高发热量的内蒙古太西无烟煤为研究对象。为了制备具有代表性的煤样,首先对手选块煤用锤式破碎机进行破碎,然后采用二分器法进行缩分,并用搅拌磨进行超细磨矿,最后筛分获得> 0.5mm、0.5~0.25mm、0.25~0.125mm、0.125~0.074mm、0.074~0.045mm和<0.045mm等粒级试验样品,并分袋保存。称取适量<0.074mm煤样进行工业分析和元素分析(表1)。碳元素含量较高,氧含量极低,所以可判断表面含氧官能团很少。
为了分析不同粒度级煤样对原煤灰分的影响,采用煤的工业分析方法(GB/T212—2008)中规定的缓慢灰化法对各粒级煤样进行灰分分析(表2)[15]。对于同一磨矿细度下的太西煤来讲,随着粒度变细,灰分逐渐降低,但达到<0.045mm时又提高,说明该煤样煤质较硬,高灰分的煤岩组分在粗颗粒尤其是在>0.5mm粒级中富集。
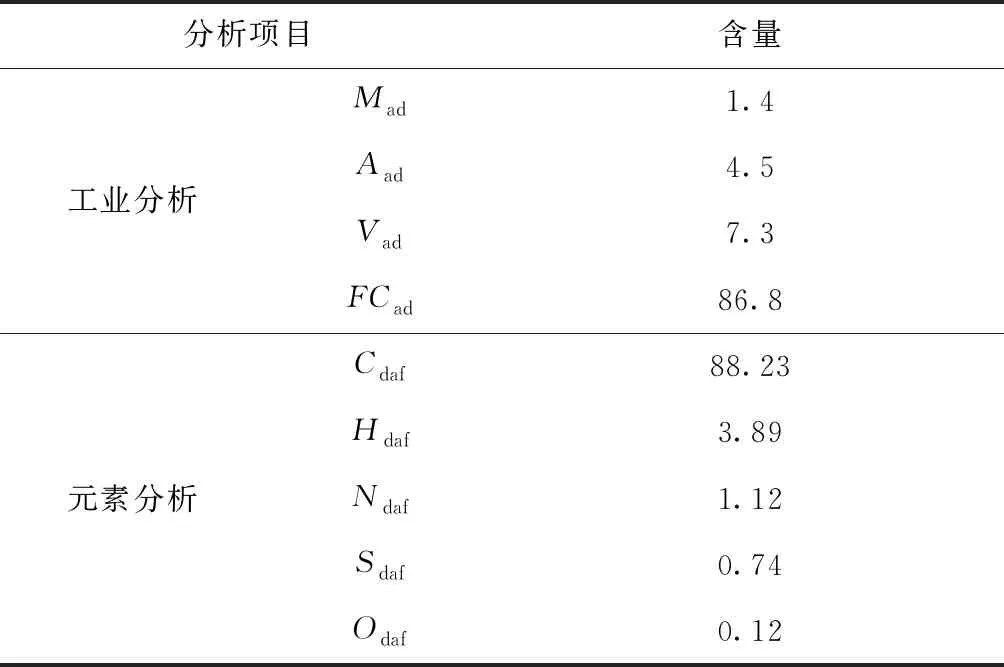
表1 太西煤的工业分析和元素分析数据
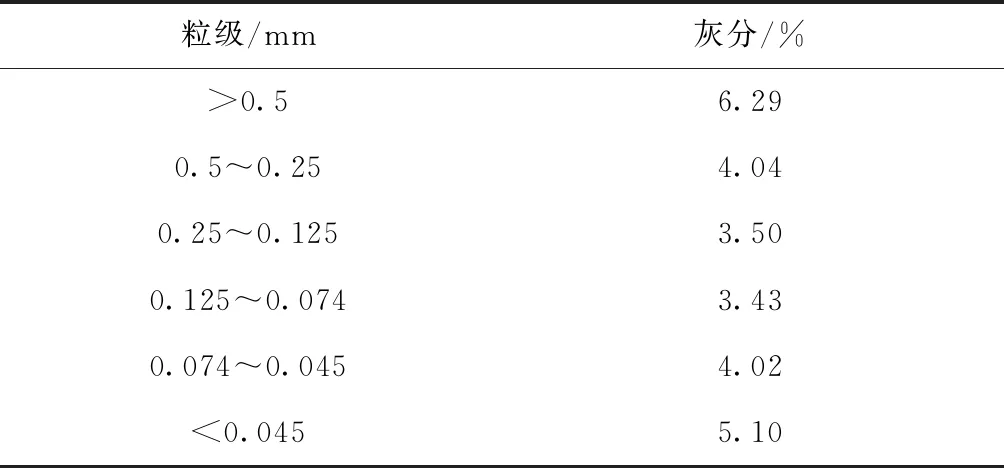
表2 粒度对原煤灰分的影响
另外,红外光谱法是研究有机化合物结构的最重要方法之一,为了分析太西煤的化学结构,取适量<0.074mm煤样进行红外光谱分析(图1)。红外数为3 400cm-1附近的吸收峰主要波是酚羟基(—OH)和胺基,这些基团是氢键化的,峰面积较小,OH含量也较少。3 030cm-1附近的吸收峰为面积较小的芳氢(ArH)吸收峰,可知芳氢含量较少。900~700cm-1有三个主要的吸收峰,它们是多重取代芳烃的面外弯曲振动和取代芳烃的骨架振动峰。2 950cm-1附近的吸收峰表示煤中甲基(—CH3)的碳氢伸缩振动,环烷烃和脂肪烃的碳氢伸缩振动峰位于2 920cm-1和2 860cm-1处。1 610cm-1附近处是煤的强特征峰(O-Ar),主要是氢键缔和的羰基和有氧取代的芳烃骨架振动造成的。1 200cm-1附近处是煤中含氧官能团C—O的吸收峰。综合以上分析可知,太西煤中甲基的含量少,氢键缔和的羟基含量少,含氧官能团含量也少,只有芳烃和取代芳烃含量大。

图1 原煤样的红外光谱图
1.4 NaOH和HCl对煤样的处理过程
1.4.1 NaOH处理过程
本阶段的处理步骤如果没有特别说明,将按以下操作进行。①称取10g细磨后的煤样于三口烧瓶中,然后再倒进30mL 6mol/L的碱溶液,液固比为3∶1; ②将烧瓶在恒温水浴锅中加热至100℃,边加热边搅拌,反应过程中通水冷却,在100℃这个温度下保持60min即可;③将反应溶液冷却至室温,于布氏漏斗上进行减压抽滤, 反复洗涤至刚刚洗出的滤液呈中性,收集滤液待用回收;④把滤饼放进105℃的恒温干燥箱中干燥,称重,然后装进样品袋中留待分析(图2)。
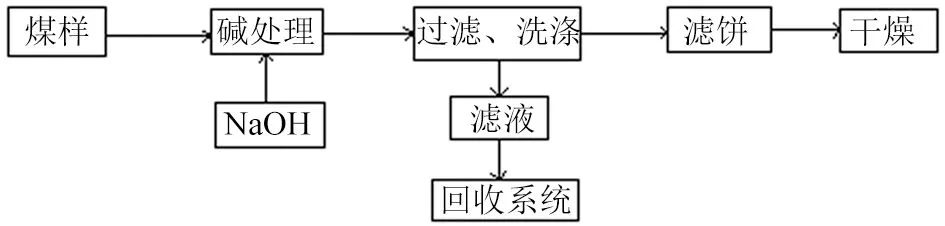
图2 NaOH处理阶段脱灰流程
1.4.2 HCl处理过程
处理步骤与氢氧化钠处理阶段的步骤相同。如没有特殊说明,将按以下配比进行:盐酸溶液浓度为1mol/L,反应温度为90℃,反应时间规定为120min,液固比仍为3∶1。两个阶段的反应现象也一样,随着反应温度的升高以及反应时间的增加,煤样与液体逐渐混合均匀,此阶段要注意的是对HCl的冷凝回流。
此实验阶段,影响灰分的因素也很多,不过主要影响因素和前述碱处理阶段的影响因素是相同的,即浓度、时间和温度这三个因素,不过它们与灰分的关系和碱处理阶段是有所不同的。
2 试验结果
2.1 NaOH处理阶段
该处理阶段可以观察到,由于煤的天然疏水性,在处理开始时,煤层与水层界面明显,反应体系分成两层,随着反应温度的持续升高以及搅拌的不断进行,煤样将会逐渐溶解,形成乌黑液体。
2.1.1 碱液浓度的影响
在本阶段实验中,首先考察碱液浓度这一因素的影响,配制以下浓度的碱溶液:1mol/L、2mol/L、3mol/L、4mol/L、6mol/L。按照上面介绍的步骤,逐一进行实验(表3)。
由于实验条件的限制,在所有煤样的检测中只测定产品煤中的灰分。从表3看出,煤灰的颜色呈砖红色,表明灰中Fe2O3含量较高,说明在温和条件下是NaOH参与了黄铁矿的反应,在生成Fe(OH)2之后,Fe(OH)2又迅速地与空气中存在的O2反应,生成了Fe(OH)3,这样Fe(OH)3就残留在了经过碱处理阶段的煤样中,碱处理过的煤样经过高温灼烧后,Fe(OH)3转化为Fe2O3存在于煤灰中。NaOH在与黄铁矿反应的同时,又与其他矿物质如硅铝酸盐等反应,生成可溶或不溶的物质,实现降低灰分的目的。
随着NaOH浓度的增加,灰分逐渐降低,这说明碱液浓度大,增加了碱液与煤相互作用的机会,提高了反应的强度,从而达到进一步降灰的目的(图3)。但碱液浓度有一个最佳数值,碱液浓度越高,需要冲洗次数越多,反而增加产品的成本,因此碱液浓度不要太高,从实际效果来看6mol/L比较合适。

表3 碱液浓度对灰分与脱灰率的影响
脱灰率=(1-处理后煤的灰分/原煤灰分)×100%。
2.1.2 碱液反应温度的影响
由于本实验研究环境是在温和反应条件下,所以设计温度不能太高,据此设计反应温度分别为60℃、70℃、80℃、90℃、100℃。依照上述步骤,分别在不同的温度下进行实验,所得结果见表4和图4。
可以看出,在60~100℃,随着碱处理温度的升高,所产煤的灰分逐渐降低,但是幅度不大。在90~100℃的曲线较为陡峭,即继续升高温度,灰分的降低特征会非常明显,这就是使用高温高压条件的原因。反应温度对脱灰效果的影响机制如下:随着碱液反应温度升高, 化学反应速度逐渐加快, 温度提高了碱液的渗透能力以及溶剂扩散、吸附、浸出速度,从而使碱液有最大机会与无机矿物质接触,从而降低灰分。
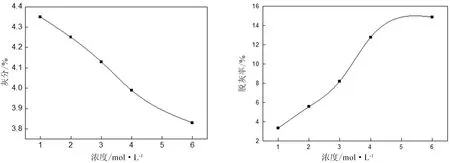
图3 NaOH浓度对灰分和脱灰率的影响
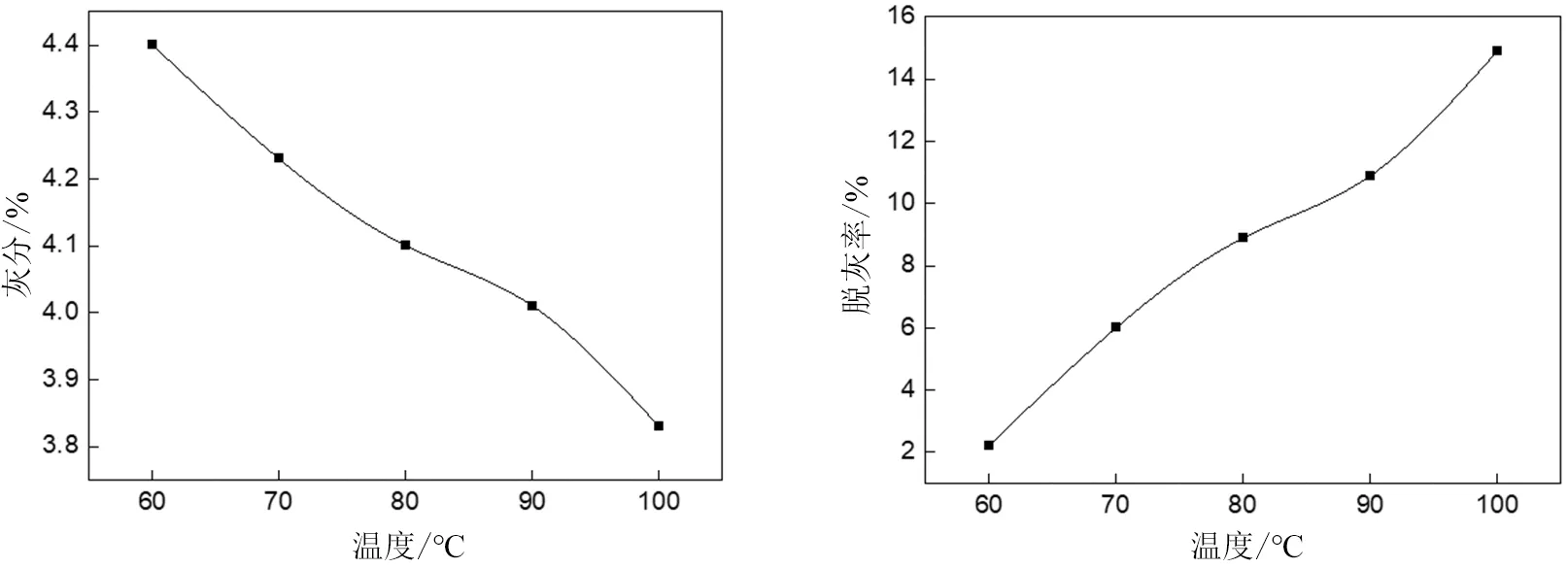
图4 碱液反应温度对灰分和脱灰率的影响
2.1.3 碱液反应时间的影响
设计的反应时间分别为10min、30min、60min、90min、120min。可以看出:在选定的时间范围内,随着反应时间增加,产物煤灰分先急剧下降,后略微上升,最佳反应时间为50~60min(表5、图5)。
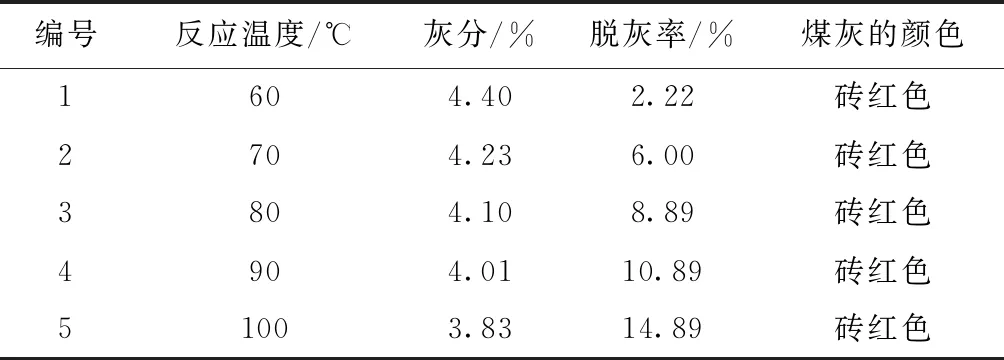
表4 碱液反应温度对灰分的影响

图5 碱液反应时间对灰分和脱灰率的影响
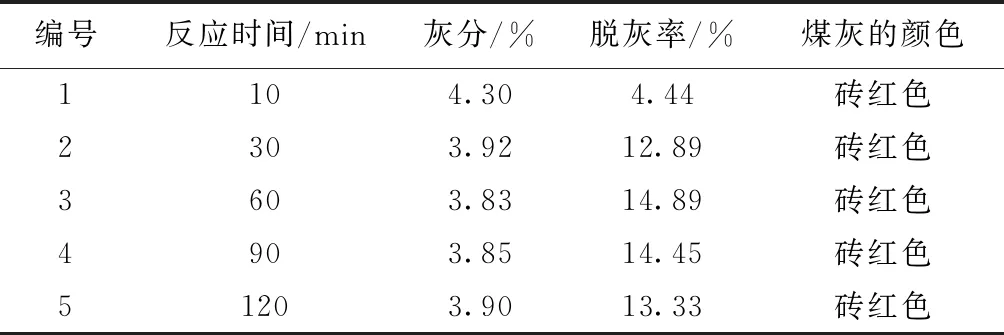
表5 碱液反应时间对灰分的影响
2.1.4 红外光谱分析
选择产煤中灰分最低的煤样进行红外光谱分析得到图6,对比图6和图1可以看出:3 425cm-1处形成一个鲜明的峰,3 646cm-1处的峰变弱,1 588cm-1和1 557cm-1处的两个峰变为一个1 572cm-1峰;两个谱图中不变的只是在700~900cm-1间的三个峰。
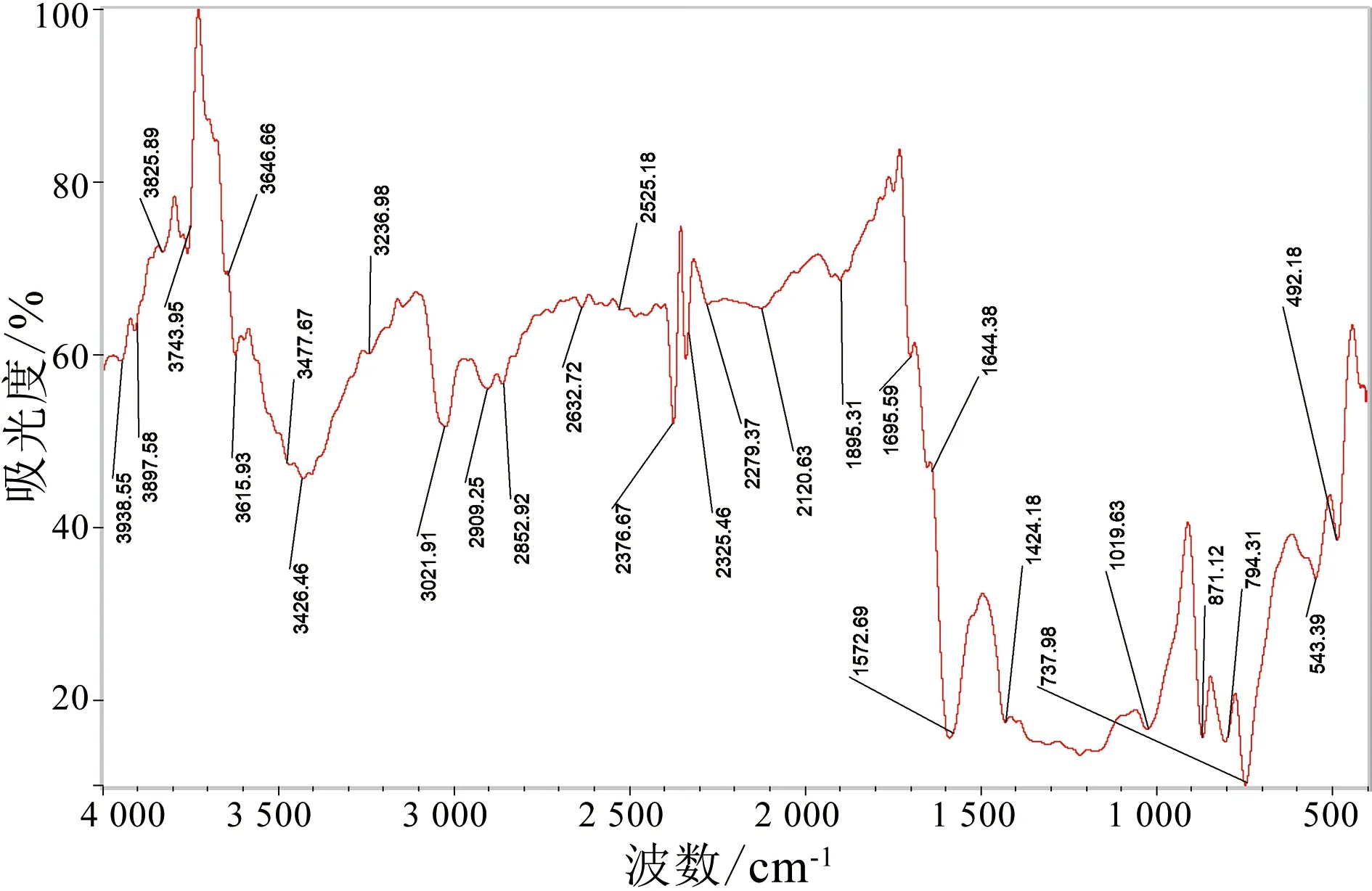
图6 6mol/LNaOH,100℃,60min产煤红外光谱图
2.2 HCl处理阶段
2.2.1 酸液浓度的影响
首先考察浓度的影响,可配制以下浓度的盐酸溶液:1mol/L、2mol/L、3mol/L、4mol/L、6mol/L、8mol/L。按照上述规定骤进行实验,所得结果见表6和图7。
可以看出,盐酸浓度在2~8mol/L时,随着盐酸浓度增加,产煤灰分升高,脱灰率下降;煤灰颜色随着盐酸浓度增加而加深,表明煤灰中Fe2O3的含量不断增加。分析可知,脱灰率主要集中在50%~55%,显示盐酸脱灰最佳浓度为2mol/L。

表6 盐酸浓度对灰分的影响
2.2.2 反应温度的影响
选择温度分别为60℃、70℃、80℃、90℃、100℃,其余条件不变,逐个进行实验,结果如表7和图8。在60~100℃的温度范围内,随着温度升高,灰分逐渐降低,但降灰幅度随着温度的升高而减小,综合考虑各方面因素,实验确定盐酸脱灰最佳反应温度为90℃。
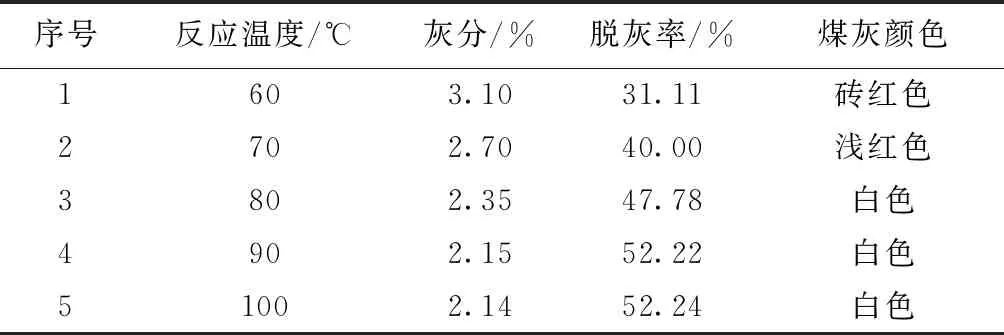
表7 盐酸反应温度对灰分的影响
2.2.3 反应时间的影响
设定四个反应时间:30min、60min、90min、120min。不同的反应时间对应不同的结果(表8、图9)。
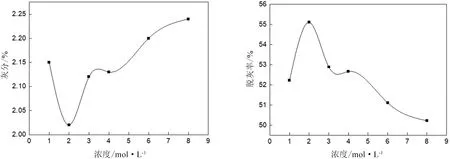
图7 盐酸浓度对灰分和脱灰率的影响
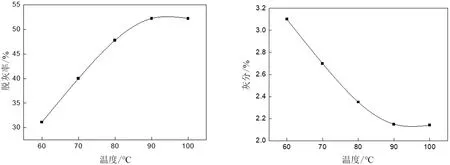
图8 盐酸反应温度对灰分和脱灰率的影响
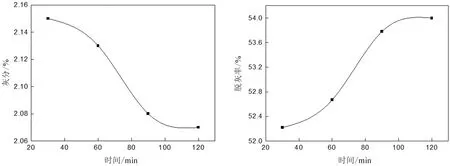
图9 盐酸反应时间对灰分和脱灰率的影响
可以看出:在30~120min中,随着反应时间延长,灰分逐渐降低,但降灰幅度随着时间增加而减小,与温度因素影响趋势相似,但在100~120min区间,曲线逐渐趋于水平,表明反应时间达到一定数值(本实验为120min)后,灰分变化不大,故确定盐酸脱灰最佳反应时间为120min。
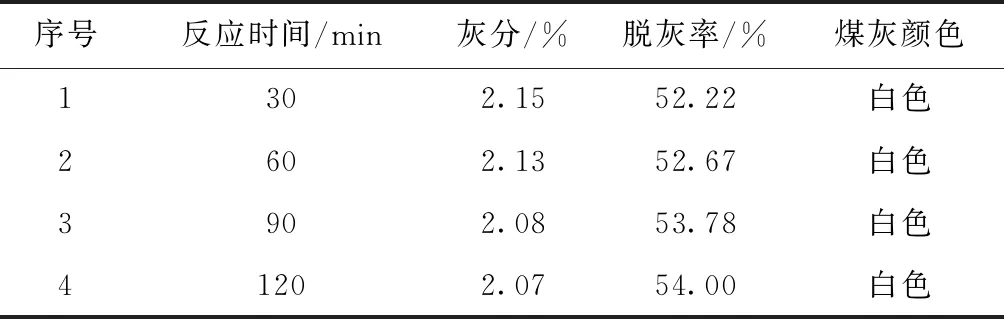
表8 盐酸反应时间对灰分的影响
2.2.4 红外光谱的分析
选取本实验阶段HCl浓度为2mol/L,反应温度为90℃,反应时间为120min的成品煤样进行红外分析得到图10。
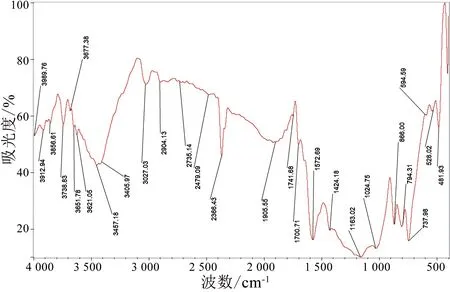
图10 产煤红外光谱图(2mol/LHCl,90℃,120min)
将图10与图1对比可以看出红外光谱图发生了一些改变,如1 163cm-1强峰的生成、3 457cm-1强峰的形成等。因为在上面的测定中,已经发现随着HCl浓度的升高灰分也升高,但是幅度不大。
为了探明HCl浓度对有机质的影响,需要选择两个灰分相差较大的煤样进行分析对比,考虑到HCl浓度对灰分的影响,选择HCl浓度为8mol/L,经过处理后的煤样红外谱图如图1
所示,对比图10和图11,可以看出:两者图谱极为相似,表明HCl浓度达到一定数值后,再增加浓度,对煤中有机质几乎不产生影响;影响有机质变化的主要因素为反应温度。

图11 产煤红外光谱图(8mol/LHCl,90℃,120min)
3 结论
1)对NaOH处理阶段和HCl处理阶段去灰作用机理进行分析表明:煤中碳酸盐与HCl发生反应去除,煤中游离SiO2和大部分硅酸盐与NaOH生成可溶性硅酸钠而被去除。
2)在温和反应条件下,NaOH单处理脱灰率不是很高,但却对煤中的有机质造成了破坏。增加碱液浓度或者反应温度都可以降低灰分。
3)HCl处理阶段,随着HCl浓度增加,灰分逐渐升高;但随着反应时间延长和反应温度升高,煤中灰分都是降低的。
4)本次试验表明,NaOH-HCl酸碱法制备超纯煤的优化反应条件为NaOH阶段碱液浓度6mol/L、反应温度100℃、反应时间60min;HCl阶段酸液浓度2mol/L、反应温度90℃、反应时间120min。
