不同浓度阿托品延缓近视儿童等效球镜度及眼轴长度效果的Meta分析
2022-10-10谷志明兰长骏钟维琪李小禹向小玲
谷志明,兰长骏,钟维琪,李小禹, 向小玲, 廖 萱
0 引言
近视是一种常见的屈光状态异常,多与眼轴长度(axial length,AL)改变有关,可增加黄斑变性、视网膜脱离、白内障、开角型青光眼等疾病的风险,甚至严重损害视力[1]。近年来,近视在全球范围有广泛流行的趋势;预计到2050年近视人口将达到全球总人口的50%,其中高度近视患者将占全球总人口的9.8%;每年用于矫正近视及治疗其并发症的经费巨大,极大地增加社会经济负担。因此,控制近视发展以降低其所致视力损伤显得尤为重要[2]。最近的一项荟萃分析表明,多种手段均可通过抑制AL变化而有效控制近视发展,尤其以抗胆碱药物效果明显[3]。而作为控制近视常用的抗胆碱药物,阿托品的疗效倍受关注。后续研究发现0.01%阿托品具有较好的近视控制效果,且副作用和反弹最小,因此开始应用于临床[4-8]。
然而,近视发生年龄、初始近视度数及父母是否患有近视等多种因素均可影响近视控制的效果。最近研究发现0.01%阿托品对初始近视度数较低以及父母没有近视的儿童效果较好;初始近视度数较高或者父母患有近视可能导致其效果下降,近视年龄较小的儿童需要更高浓度的阿托品才可以达到接受较低浓度的大龄儿童类似的功效[9-11]。Yam等[12]在比较了0.05%、0.025%和0.01%阿托品控制近视的效果后,发现0.05%阿托品优于0.01%及0.025%阿托品,且儿童对其具有较好的耐受性。但目前多处于小样本的临床探索阶段,其应用效果尚缺乏系统的评价。本文采用Meta分析的方法对已发表的关于0.01%、0.025%和0.05%阿托品控制近视效果的临床研究进行定量评价,以期为临床实践提供循证依据。
1 资料和方法
1.1资料检索PubMed、Embase、Cochrane Library、Web of Science、中国知网、万方数据库、维普网、中国生物医学文献数据库中从建库至2022-05期间发表的关于0.01%、0.025%和0.05%阿托品进行近视控制的研究。语言限定为中文及英文。英文检索关键词包括myopia、atropine、axial、refractive error的主题词、副主题词及自由词。中文检索关键词包括:近视、阿托品、眼轴长度、屈光度的主题词及自由词。纳入标准:(1)研究选取随机对照试验(randomized controlled trials, RCT)及病例对照研究;(2)研究对象年龄<18岁;(3)干预措施包括0.01%、0.025%与0.05%三种浓度阿托品的其中任意两种;(4)结局指标为等效球镜(SE)和AL,且基线数据与干预后的变化值等指标完整;(5)随访周期≥12mo。排除标准:(1)仅进行了0.01%、0.025%或0.05%其中一种浓度的研究;(2)无法获取全文或无法提取数据的文献;(3)会议报告文献。
1.2方法
1.2.1文献筛选流程和资料提取文献检索由两位独立的研究人员进行。初筛时,研究人员通过阅读文献题目及摘要,剔除重复文献、会议论文、病例报告、综述等与研究目的不符的文献。后续对剩余文献进行全文阅读,依据纳入及排除标准进行二次筛选。最终根据两名研究人员所筛文献进行交叉比较,确定最终纳入本研究的文献,并进行资料提取。如果数据提取过程中出现异质性较大的文献,则交由第三位研究人员确定是否提取相关数据。资料信息包括作者、国家及地区、出版年份、研究类型、研究对象年龄、样本量、干预措施、研究时长、基线SE及AL、干预后SE及AL相关数据。
1.2.2文献质量评价利用《Cochrane干预措施系统评价手册》从随机分配方法、分配方案隐藏、盲法、结果数据完整性、选择性研究报告及其他偏倚来源等方面对文献的偏倚风险及质量进行评价。
统计学分析:采用Revman5.4软件完成Meta分析。根据文献中提取的计量资料均值±标准差,计算加权均数差(weighted mean differences,WMD)和95%置信区间(confidence intervals,CI)作为不同浓度阿托品对AL和SE的变化效应值指标,检验水准为α=0.05。使用Q统计量及I2值判断不同研究间的异质性;若P>0.05或I2≤50%表明各项研究间的异质性不具有统计学意义,使用固定效应模型进行分析;若P<0.05或I2>50%表明各项研究的异质性具有统计学意义,使用随机效应模型进行分析。采用STATA12.0软件进行Egger检验对纳入文献潜在的发表偏倚进行评价,并用漏斗图体现。
2 结果
2.1文献检索结果在8个数据库中,共检索出相关文献2699篇,其中英文文献1253篇;中文文献1446篇。先剔除重复文献,再阅读标题和摘要,排除综述、会议论文、病例报告、无法获取全文以及无法进行数据提取等与纳入标准不符的文献,最终纳入6篇文献,其中英文文献4篇,中文文献2篇。文献筛选流程图见图1。
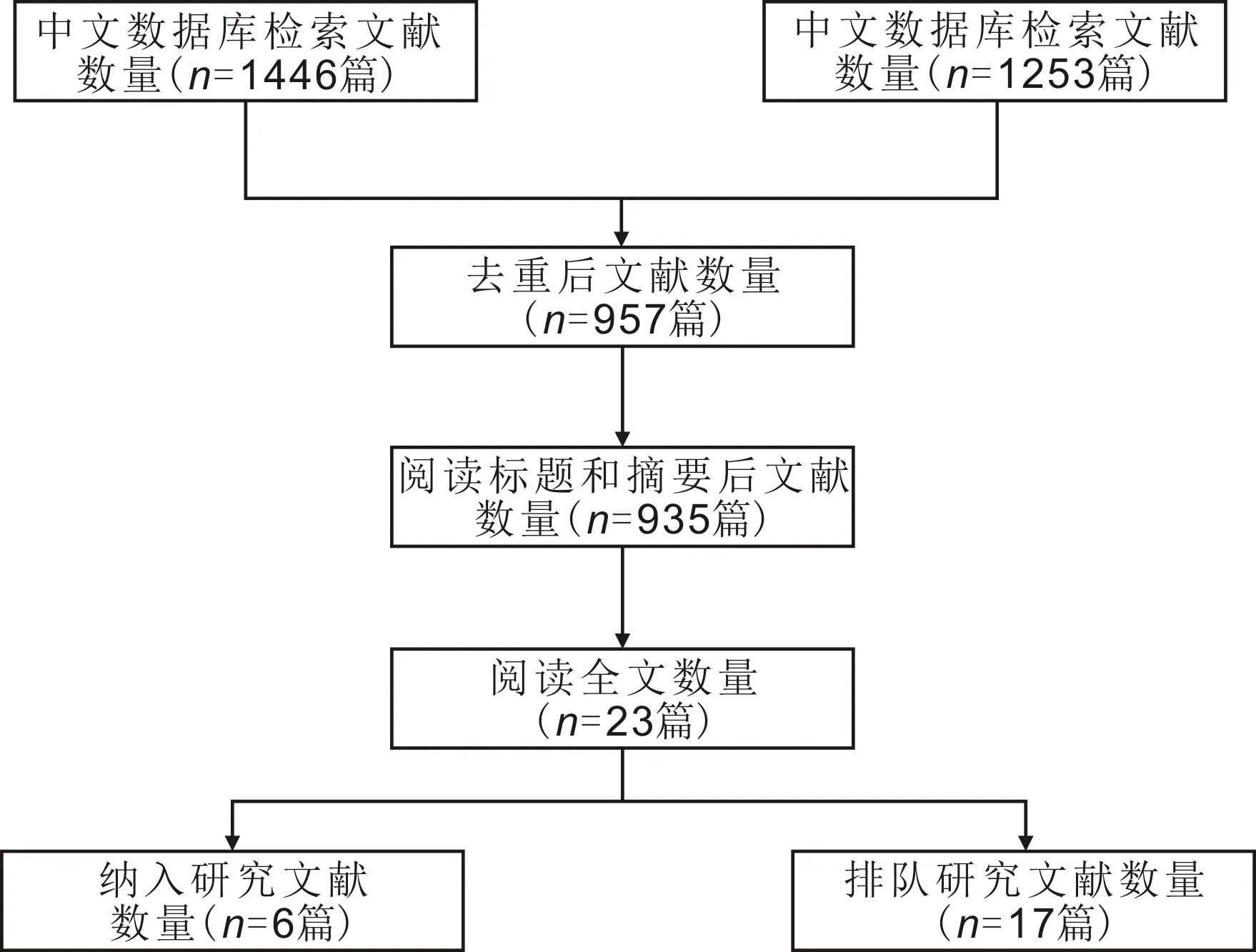
图1 文献筛选流程图。
2.2纳入研究基本特征及文献偏倚质量评价符合纳入标准的6篇文献[12-17]中,5篇为RCT[12, 14-17],1篇为病例对照研究[13]。研究基本特征见表1。

表1 纳入研究基本特征
文献质量评价图2结果显示,5项RCT均采用了随机分配原则,并排除失访病例对结局指标的影响,结局报道完整,因此偏倚风险较低[12, 14-17]。而Tsai等[13]采用病例对照研究,且治疗方式由患者或其监护人了解清楚研究目的后自行选择,因此导致出现较高的偏倚风险。
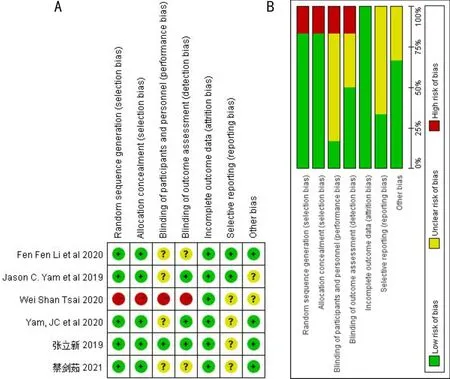
图2 文献质量评价图 A: 偏倚风险总结图;B: 偏倚风险百分图。
2.3Meta分析结果
2.3.10.01%及0.025%阿托品对SE及AL影响的Meta分析共3项研究[12, 14, 16]对0.01%及0.025%阿托品用药后SE的变化进行研究,各项研究间无异质性(P=0.86,I2=0%),采用固定效应模型进行分析。Meta分析结果表明0.025%阿托品对SE抑制效果优于0.01%阿托品,差异有统计学意义(WMD=-0.15, 95%CI:-0.23~-0.06,P<0.001),见图3A。
共4项研究[12, 14, 16-17]对0.01%和0.025%阿托品用药后AL变化的进行研究,各研究间无异质性(P=0.98,I2=0%),采用固定效应模型进行分析。结果显示0.025%阿托品比0.01%阿托品更能有效抑制AL增长,差异有统计学意义(WMD=0.07, 95%CI: 0.03~0.10,P<0.001)。其中,3项研究[12, 14, 16]的随访周期为12mo,2项研究[14, 17]的随访周期为24mo。亚组分析显示,用药12mo亚组无异质性(P=0.97,I2=0%),固定效应模型分析显示AL变化差异有统计学意义(WMD=0.07, 95%CI: 0.03~0.11,P<0.001);用药24mo亚组无异质性(P=0.53,I2=0%),固定效应模型分析显示AL变化差异无统计学意义(WMD=0.07, 95%CI: -0.01~0.15,P=0.09),见图3B。

图3 0.01%及0.025%阿托品对SE及AL影响的Meta分析 A: SE;B: AL。
2.3.20.01%及0.05%阿托品对SE及AL影响的Meta分析共3项研究[12, 14-16]对0.01%及0.05%阿托品用药后SE变化的进行研究,分析发现各研究间无异质性(P=0.09,I2=50%),采用固定效应模型进行分析。结果显示0.05%阿托品比0.01%阿托品更能有效抑制SE增加,差异有统计学意义(WMD=-0.35, 95%CI:-0.44~-0.26,P<0.001)。其中4项研究[12, 14-16]随访周期为12mo,1项研究[14]随访周期为24mo。亚组分析结果表明,12mo组无异质性(P=0.21,I2=34%),采用固定效应模型分析显示SE变化的差异有统计学意义(WMD=-0.32, 95%CI:-0.41~-0.23,P<0.001);24mo组无异质性(P<0.001),固定效用模型分析表明SE变化的差异有统计学意义(WMD=-0.57, 95%CI:-0.82~-0.32,P<0.001),见图4A。
共5项研究[12-16]对0.01%及0.05%阿托品用药后AL变化的进行研究,异质性检验表明各研究间无异质性(P=0.73,I2=0%),采用固定效应模型进行分析。结果显示0.05%阿托品比0.01%阿托品更能有效抑制近视AL增加,差异有统计学意义(WMD=0.16, 95%CI:0.12~0.20,P<0.001)。其中5项研究[12-16]随访周期为12mo,2项研究[13-14]随访周期为24mo。根据随访时间进行亚组分析显示,12mo组无异质性(P=0.58,I2=0%),采用固定效应模型分析表明AL变化差异有统计学意义(WMD=0.15, 95%CI:0.11~0.19,P<0.001);24mo组无异质性(P=1.00,I2=0%),固定效应模型分析表明AL变化差异有统计学意义(WMD=0.20, 95%CI:0.10~0.30,P<0.001),见图4B。

图4 0.01%及0.05%阿托品对SE及AL影响的Meta分析 A: SE;B: AL。
2.3.30.025%及0.05%阿托品对SE及AL影响的Meta分析共3项研究[12, 14, 16]对0.025%及0.05%阿托品用药后SE变化的进行研究,异质性检验提示无异质性(P=0.98,I2=0%),采用固定效应模型进行分析。结果表明0.025%阿托品对SE抑制效果差于0.05%阿托品,差异有统计学意义(WMD=-0.20, 95%CI:-0.28~-0.11,P<0.001),见图5A。
共4项研究[12, 14, 16-17]对0.025%及0.05%阿托品用药后AL变化的进行研究,各研究间无异质性(P=0.93,I2=0%),采用固定效应模型进行分析。结果显示0.05%阿托品比0.025%阿托品更能有效抑制近视AL增加,差异有统计学意义(WMD=0.09, 95%CI:0.06~0.12,P<0.001)。其中,3项研究[12, 14, 16]随访周期为12mo,2项研究[14, 17]随访周期为24mo。亚组分析显示,12mo组研究间无异质性(P=1.00,I2=0%),采用固定效应模型进行分析,结果显示AL变化差异有统计学意义(WMD=0.09, 95%CI:0.05~0.13,P<0.001);24mo组研究间无异质性(P=0.37,I2=0%),固定效应模型分析显示AL变化差异有统计学意义(WMD=0.08, 95%CI:0.00~0.16,P<0.001),见图5B。
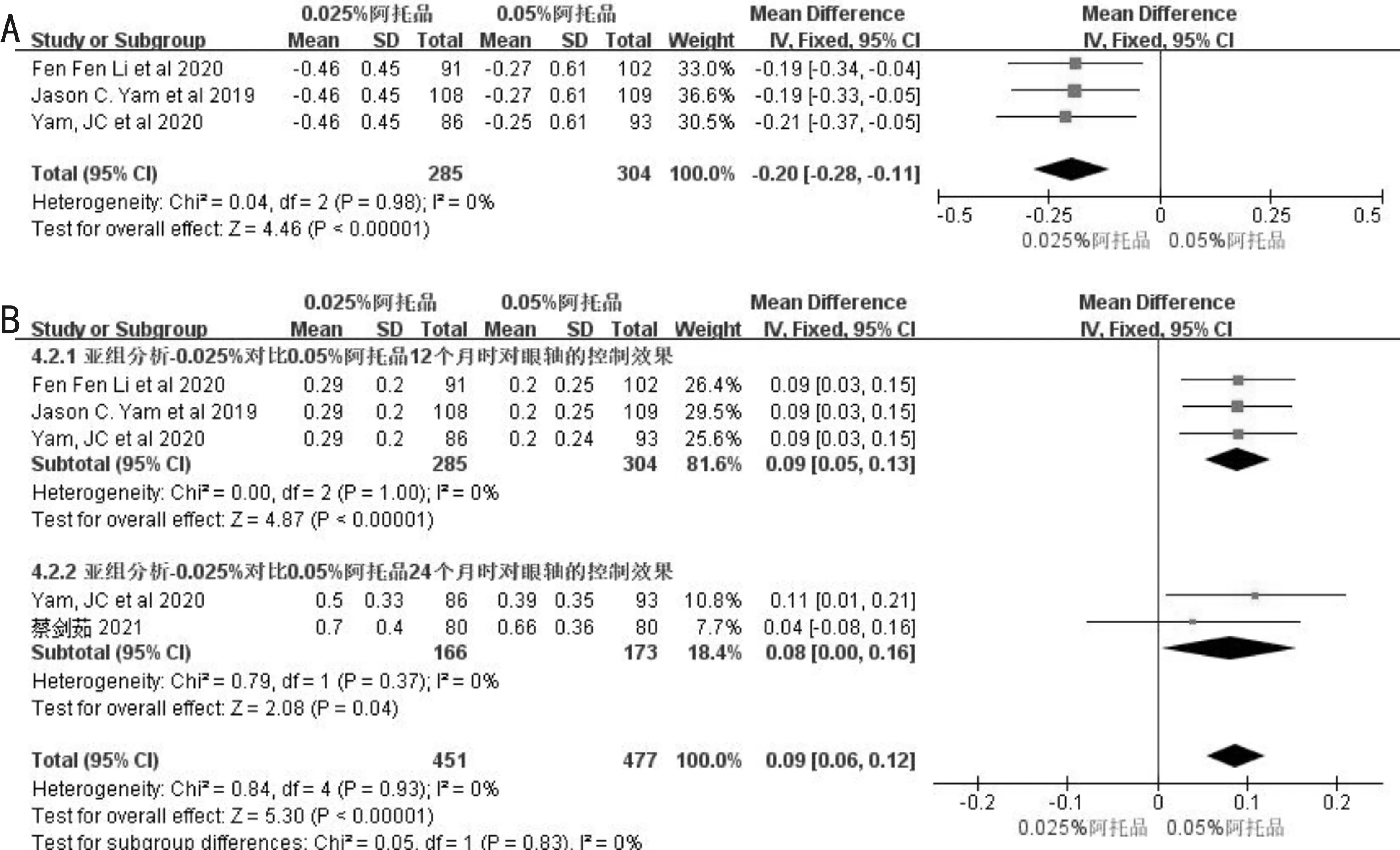
图5 0.025%及0.05%阿托品对SE及AL影响的Meta分析 A: SE;B: AL。
2.4敏感性分析对纳入本研究的6项研究[12-17]中SE及AL变化进行敏感性分析,逐一剔除后对比剔除前的研究结果显示SE的合并效应量较为稳定,仅有Li等[16]和Yam等[12, 14]的研究在删除后导致AL合并效应量异质性增加,但所有变化差异均无统计学意义(表2)。

表2 不同结局指标的敏感性分析
2.5不同结局指标的发表偏倚采用STATA12.0软件进行Egger检验对SE和AL变化差值的发表偏倚进行分析。结果显示,0.01%与0.025%阿托品组SE及AL变化差值均不存在发表偏倚(SE:t=-1.11,P=0.467;AL:t=-1.59,P=0.253)。0.025%与0.05%阿托品组SE及AL变化差值也不存在发表偏倚(SE:t=-1.16,P=0.454;AL:t=0.85,P=0.55)。0.01%与0.05%阿托品组SE变化差值不存在发表偏倚(t=1.94,P=0.192),而AL变化存在发表偏倚(t=-3.88,P=0.03),见图6,原因可能是由于部分研究样本量较少,且纳入研究的基线数据差异较大所致。
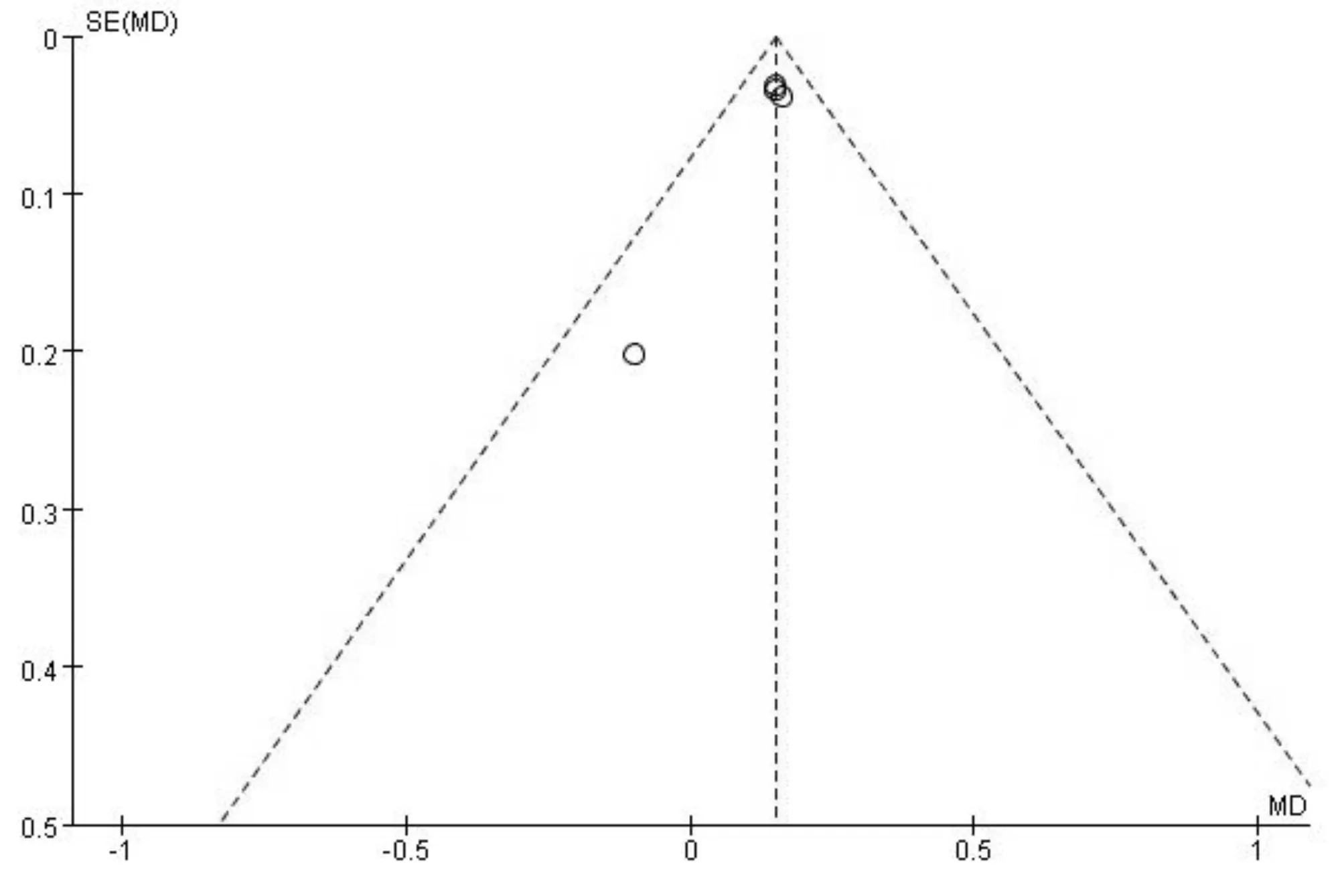
图6 漏斗图所示AL变化差值发表偏倚。
3 讨论
目前控制近视的方法如框架眼镜、角膜接触镜和药物中,以阿托品为代表的毒蕈碱受体拮抗剂被认为是比较有效的手段[3]。自上世纪70年代发现阿托品对近视的控制作用以来[18],已有多项临床研究对其控制近视的效果进行了观察。早期研究发现不同程度近视儿童在使用1%阿托品后,SE和AL增速均明显放缓,近视进展速度减慢[4, 19]。后续研究证实阿托品眼液呈浓度依赖方式控制近视,其近视的控制疗效与浓度正相关。Tong等[20]应用1%阿托品眼液于近视患者2a后,发现其可以有效抑制SE和AL增加;但在停药后1a内,阿托品组的SE进展(-1.14±0.80D)明显高于安慰剂组(-0.38±0.39D),表明停药后可引起近视反弹。Chia等[21]使用0.01%、0.1%和0.5%的较低浓度阿托品后,观察到阿托品的近视控制效果与浓度正相关,但停药后1a内AL分别增加了0.19±0.13、0.33±0.18和0.33±0.20mm,进一步提示阿托品浓度也是影响近视反弹效应以及不良反应发生率的主要因素。一项为期5a的研究证实了阿托品眼液以浓度依赖性方式减缓近视的进展,而只有0.01%阿托品在有效控制近视的同时,并未引起眼压增高、过敏、调节力及瞳孔大小改变等无法耐受的不良反应出现[22],表明低浓度阿托品可能是控制近视发展的较好选择。后续大量研究也证实在不同时长内使用0.01%阿托品均显示出优于框架眼镜的近视控制效果,且未导致眼压增高以及干眼等不良反应出现[5, 7, 23-26]提示局部使用0.01%阿托品可在有效抑制近视发展的同时减少不良反应发生,因此被推荐用于临床[6, 21-22, 27]。
然而,近年来的部分研究发现近视年龄过早、初始近视度数较高以及遗传等多种因素均可导致0.01%低浓度阿托品的近视控制效果下降[9-11],表明0.01%阿托品可能对于部分近视儿童并非最佳选择,因此寻找近视控制效果更好,适用人群更广的阿托品浓度则显得尤为重要。符爱存等[28]发现0.02%阿托品的近视控制效果优于0.01%阿托品,且不良反应发生率并无明显差异。随着阿托品临床实验的大量开展,0.025%及0.05%低浓度阿托品的近视控制效果也受到学者关注。Yam等[12, 14]观察了0.01%、0.025%、0.05%三种浓度阿托品的疗效,发现0.05%阿托品在控制近视青少年的SE增加及AL增长方面均优于其他两个浓度的阿托品,且未导致明显影响生活的不良反应,表明儿童对于0.05%阿托品也具有较好的耐受性。尽管目前已有许多研究对0.01%阿托品控制近视的功效进行了观察,并发现其可以有效延缓近视发展,但未对其他低浓度阿托品以及更长时间干预后的近视控制效果进行分析。此外,关于0.01%、0.025%及0.05%阿托品的研究样本量较小,应用效果尚缺乏系统的评价。因此本研究对已发表的关于0.01%、0.025%、0.05%阿托品控制近视效果的临床研究进行Meta分析,且随访周期最长至24mo。通过合并研究数据后发现,0.05%阿托品对近视儿童SE及AL抑制效果均优于0.01%及0.025%,且差异均具有统计学意义(P<0.001),浓度越高则近视增幅越小;进一步亚组分析发现,随着干预时间的延长,阿托品的近视控制功效也得以增强。
但本研究存在一定的局限性:(1)目前关于0.01%、0.025%及0.05%阿托品控制近视效果的相关文献较少,一定程度上影响结论的准确性;(2)病例对照研究可能出现选择性报告结论,导致结果可靠性降低;(3)纳入研究的样本量差异大,可能引起结果改变;(4)有报道发现使用0.01%、0.025%、0.05%阿托品后均出现了瞳孔散大、调节能力变化等不良反应[29],但现有研究关于相关药物副作用的报告数量较少,对其不良反应的发生率未进行明确叙述,因此无法纳入不良反应进行分析。
综上所述,现有证据支持局部使用0.05%阿托品抑制近视儿童SE及AL增长的效果优于0.01%及0.025%阿托品,但在评价其他结局指标方面缺乏足够的证据,尚需更多设计严格的研究以增加证据的强度。因此,后续还需要足够数量的大样本量随机对照试验,对使用不同浓度阿托品控制近视疗效及副作用等进行全面的综合评价,充分避免目前存在的局限性,才能为近视防控提供更有意义的循证医学证据。
