废三元锂离子电池锂优先浸出技术
2022-10-09周文斌彭茜茜石秋成唐晓寒
周文斌,彭茜茜,陈 龙,石秋成,廖 杰,唐晓寒
(珠海格力绿色再生资源有限公司,广东 珠海 519000)
发展新能源汽车是国家保障能源安全及改善生态环境的重要战略部署。新能源汽车的大规模推广将带动动力电池(通常为三元锂离子电池)的大幅增长,而退役的动力电池如不妥善处理将会造成社会隐患。废旧动力锂电池中含有大量有价金属元素资源,如钴5%~20%,锂5%~7%,镍5%~10%,锰5%~15%()。回收这些金属元素可在很大程度上缓解我国的资源紧缺现状,预计2020~2030年整体市场规模将达1 468亿元。我国锂资源非常紧缺,而锂作为重要的战略资源,从退役动力电池中对其进行回收再生十分重要。
在废三元锂离子电池材料的回收工艺中,锂常作为副产品在最后进行回收,主要回收流程为电池材料通过酸浸出后进行置换除铜和沉淀除铁、铝,再进行萃取深度除杂,然后萃取分离锰、镍、钴,最后进行溶液中锂的沉淀回收。该工艺锂的回收流程长,回收过程易造成锂的分散流失,最终导致其综合回收率低,只有80%左右。
本研究采用熔盐焙烧后碱性浸出的方法优先选择性浸出锂,以实现锂的高效浸出和镍钴锰的低损失,考察了熔盐种类和添加量、焙烧温度、氢氧化钠溶液pH对浸出效果的影响,并运用XRD技术对浸出机理进行了分析。
1 实验部分
1.1 实验材料
镍钴锰酸锂(NCM)三元正极粉:由市场回收的银隆新能源股份有限公司66160型钛酸锂电池经拆解、分离、破碎、研磨、筛分(过120目筛网,取筛下粉末)后得到。NCM三元正极粉的主要成分见表1(其他成分还包括导电炭黑、黏结剂等)。

表1 NCM三元正极粉的主要金属成分 w,%
1.2 实验方法
1.2.1 直接碱性浸出
配制pH为8~14的氢氧化钠溶液50 mL,加入三元正极粉10 g(固液比为1∶5),在60 ℃水浴锅里反应120 min,反应过程保持搅拌,转速400 r/min。
1.2.2 焙烧后碱性浸出
将三元正极粉置于马弗炉中,在设定的温度下焙烧120 min后取出,冷却至室温备用。称取焙烧后的三元正极粉进行碱性浸出实验,氢氧化钠溶液的pH为11,其他条件与1.2.1相同。
1.2.3 熔盐焙烧后碱性浸出
将三元正极粉与一定量的氯化钙/氯化钠/氯化钾混合均匀,置于800 ℃的马弗炉中焙烧120 min后取出,冷却至室温备用。称取焙烧后的三元正极粉进行碱性浸出实验,氢氧化钠溶液pH为11,其他条件与1.2.1相同。
1.3 分析方法
采用ThermoFisher公司iCAP-6200型等离子体发射光谱仪测定浸出液中锂和其他金属元素M(M=Ni,Co,Mn)的质量浓度,计算锂浸出率和镍钴锰总浸出率;采用Rigaku公司600型X射线衍射仪进行样品的物相分析;采用雷磁公司PHS-3C型pH计测定溶液的pH。
2 结果与讨论
2.1 直接碱性浸出结果
不同pH下直接碱性浸出的浸出率见图1。由图1可见,锂的浸出率高于镍钴锰,但锂和镍钴锰元素的浸出率均很低。这表明,回收的三元正极粉中游离的Li很少,绝大部分锂仍镶嵌在NCM材料的层状结构内,不能自由解离。因此,Li虽易溶于碱液,但回收的三元材料中的锂未能解离进入到碱液中。同时,镍钴锰元素形成的氧化物在碱性条件下不溶或难溶,同样不会被溶解到浸出液中。
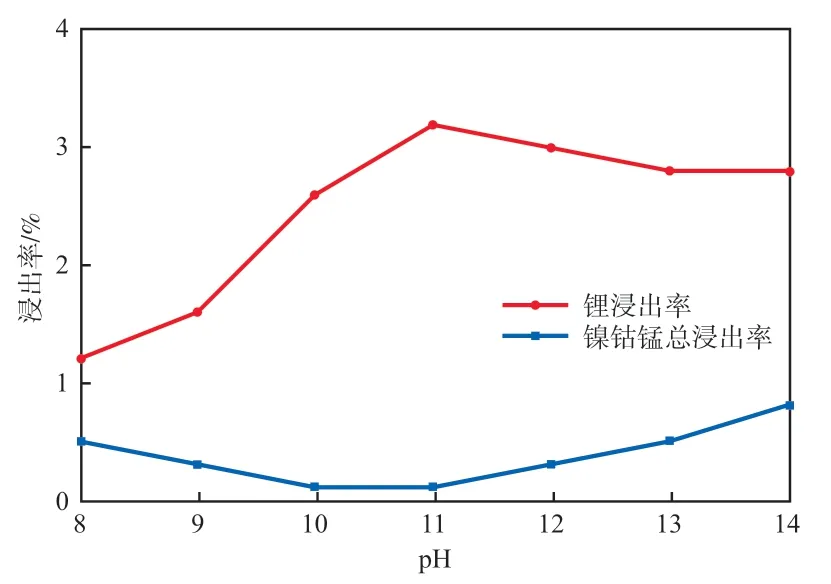
图1 不同pH下直接碱性浸出的浸出率
由图1还可见,随着氢氧化钠溶液pH的升高,锂的浸出率先升高后降低,镍钴锰的浸出率先降低后升高。这可能是因为:随着pH的升高,碱性增强,Li与OH结合率增加,使得浸出液中锂元素浓度增加,但Ni,Co,Mn在碱性条件下的氢氧化物不溶于水,导致浸出率减小;pH继续升高,溶液碱性继续增强,OH与Ni形成可溶性氢氧化物,消耗部分OH,导致锂浸出率达到最大后出现下降。pH为11时分别得到了最高的锂浸出率和最低的镍钴锰总浸出率,因此,选用pH为11的氢氧化钠溶液进行后续实验。
2.2 焙烧后碱性浸出结果
不同焙烧温度下的浸出率见图2。经过高温焙烧后,锂元素的浸出率明显上升,500 ℃的锂浸出率达7.9%,800 ℃的锂浸出率最高,达10.6%。与文献报道的锂浸出率为92%~99%相比,10%左右的锂浸出率仍处于较低水平,说明经过单纯高温焙烧后NCM材料的层状结构可能仍较完整,析出的自由锂离子量较少。经高温焙烧后,镍钴锰总浸出率有所降低,为0.1%~0.3%。

图2 不同焙烧温度下的浸出率
2.3 熔盐焙烧后碱性浸出结果
不同熔盐种类和添加量(与正极粉的质量比)下的浸出率见图3。由图3可见:添加氯化钙进行熔盐焙烧时的锂元素浸出效果最好,其添加量为30%时的浸出率最高,达99%以上,同时镍钴锰总浸出率在1%以下;而添加氯化钠、氯化钾进行熔盐焙烧时,锂的浸出效果不理想,最高浸出率只有7.7%。出现这种现象的原因可能是熔融的氯化钙解离出的氯离子能够更有效地进入到NCM材料内,与锂离子、镍离子等结合,破坏原来材料的内部结构,而氯化钾、氯化钠则达不到较好的熔融和氯离子解离效果。在碱性条件下Li高效地进入到溶液中,而Ni,Co,Mn则留在渣相中。
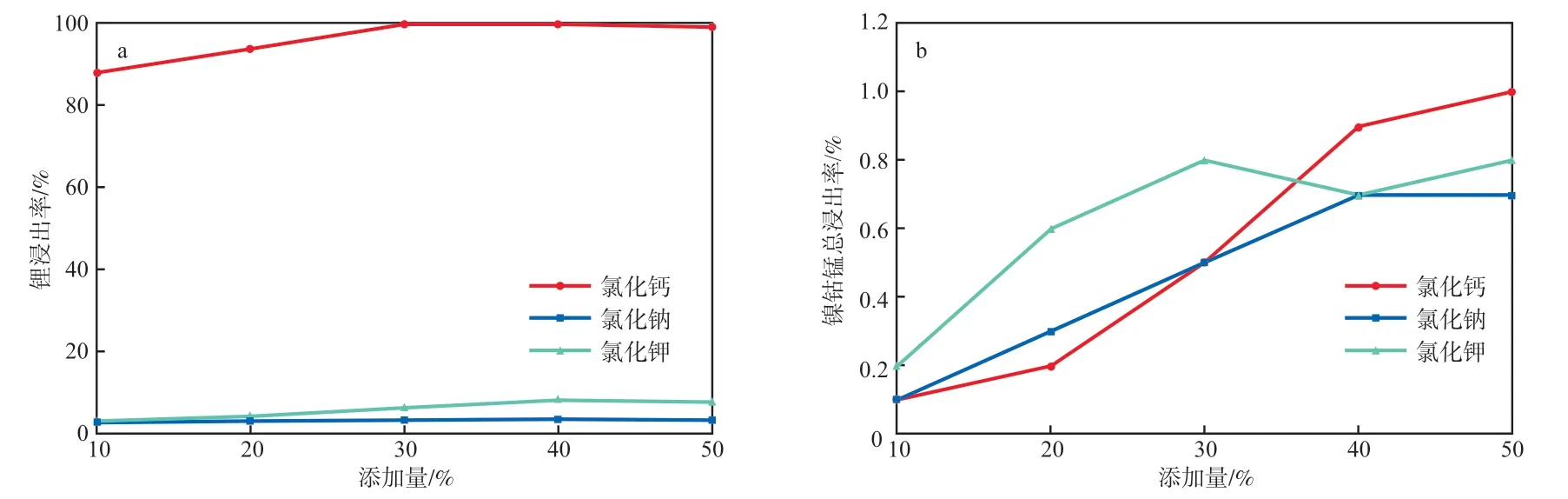
图3 不同熔盐种类和添加量下的锂(a)和镍钴锰总(b)浸出率
2.4 pH对熔盐焙烧后碱性浸出效果的影响
在最优氯化钙添加量30%、最优焙烧温度800 ℃的条件下,研究了添加氯化钙焙烧后不同pH条件的浸出效果,结果见图4。由图4可见,锂的浸出率在pH为11时达到最大值99.5%,在pH为8时锂浸出率最低,但也可达85.6%,且镍钴锰总浸出率均低于1%,说明氯化钙作为焙烧剂能够较好地选择性浸出锂元素。
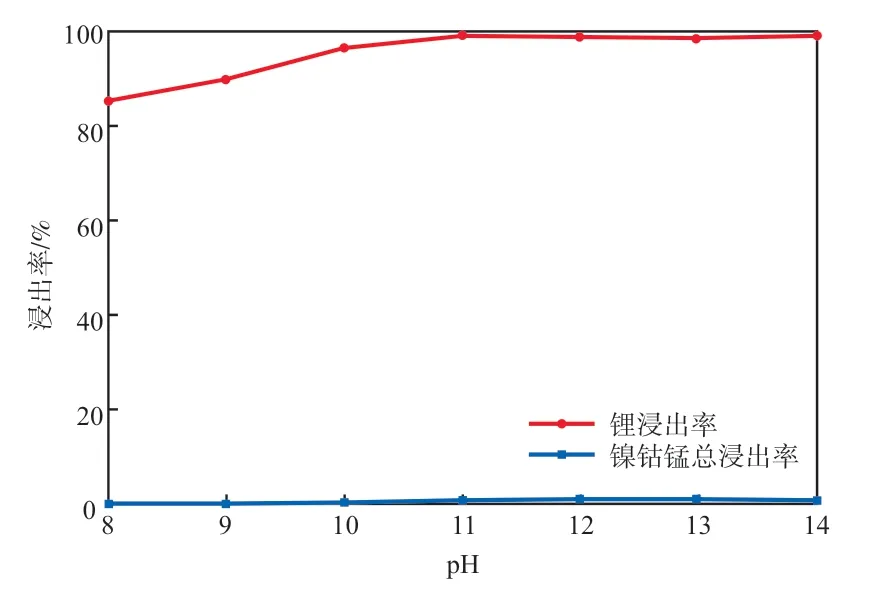
图4 pH对熔盐焙烧后碱性浸出效果的影响
2.5 NCM正极材料的晶体结构分析
锂电池NCM正极材料的晶型结构为六方晶系,属R3m空间群,具有层状α-NaFeO结构,其晶体结构见图5。
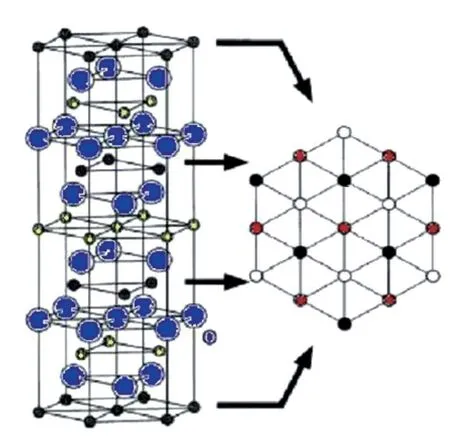
图5 NCM正极材料的晶体结构
焙烧前后NCM正极材料的XRD谱图见图6。
由图6可见:NCM正极材料的特征衍射峰尖锐,说明其结晶程度较高;(006)/(102)及(108)/(110)峰明显分开,说明NCM材料为层状结构;(003)和(104)的峰强比值大于1.2,说明材料中阳离子的有序程度较高。从焙烧后材料的XRD谱图可以看出:特征衍射峰的位置与焙烧前基本吻合,峰型较尖锐,层状结构特征峰明显,说明热处理后的NCM材料层状结构较稳定,结晶度较高,这也解释了单纯高温焙烧后再浸出时不能有效浸出锂元素的原因;但003峰的强度减小,说明阳离子的有序程度变差。

图6 焙烧前后NCM正极材料的XRD谱图
熔盐焙烧前后NCM正极材料的XRD谱图见图7。
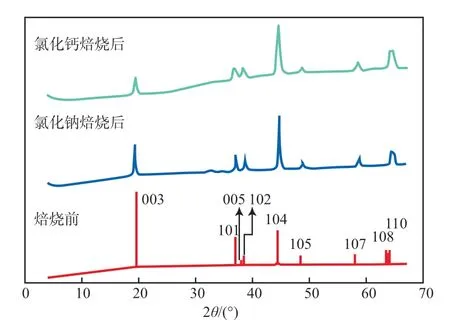
图7 熔盐焙烧前后NCM正极材料的XRD谱图
由图7可以看出,焙烧剂为氯化钙时:衍射峰较宽,说明结晶程度低;(006)/(102)及(108)/(110)峰明显未分开,说明层状结构被破坏;(003)/(104)比值远小于1,说明阳离子已无序排布,NCM材料的晶体结构被破坏。而氯化钠为焙烧剂时,衍射峰与未焙烧前的NCM材料基本相同,整体晶体结构相对稳定。这可能是因为:氯化钙为典型的离子型卤化剂,同时也是助熔剂,在与NCM材料进行高温焙烧时,可降低材料的晶体结构转变温度,熔融的氯化钙解离出的Cl能够渗入到材料的晶体结构内与Li、Ni等结合,破坏原有晶体中的原子组合,达到Li游离的目的(碱性条件下游离出的Ni等又形成沉淀);而其他的氯化钾、氯化钠则达不到较好的熔融和Cl解离效果,对NCM的晶体结构破坏力小,Li释放量有限。因此,添加氯化钙焙烧时可实现Li的选择性高效浸出。
3 结论
a)虽然Li易溶于碱性溶液中,但由于NCM正极材料晶型结构的特点,Li不能直接或单纯焙烧后碱性浸出。
b)添加氯化钙进行熔盐焙烧后再碱性浸出,能够有效地选择性浸出锂元素,在焙烧温度800 ℃、氯化钙添加量30%、固液比1∶5、氢氧化钠溶液pH 11、浸出温度60 ℃、浸出时间120 min的最优回收条件下,锂浸出率可达99.5%,镍钴锰总浸出率低于1%。
c)XRD分析结果表明,添加氯化钙进行高温熔盐焙烧时,氯化钙能够解离出Cl,使Cl与Li等金属离子结合,破坏NCM的晶体结构,释放出Li,有利于锂的浸出。
