基于T2WI影像组学模型可预测低级别胶质瘤1p/19q的缺失状态
2022-10-08刘书涵刘晓欢苏侨勇付国丽姜聪明许燕塔
刘书涵,刘晓欢,苏侨勇,付国丽,姜聪明,许燕塔
厦门大学附属第一医院放射科,福建 厦门 361003
2021年世界卫生组织(WHO)中枢神经系统肿瘤分类将成人弥漫性低级别胶质瘤分为星形细胞瘤和少突胶质细胞瘤,其诊断标准是异柠檬酸脱氢酶突变,伴或不伴染色体1p/19q共缺失[1]。因此,星形细胞瘤和少突胶质细胞瘤的主要鉴别点在于是否发生1p/19q共缺失[2-3]。该缺失是1号染色体短臂和19号染色体长臂之间易位导致的(1;19)(p10;q10)染色体联合缺失,在肿瘤分级、诊断治疗、预后评估中具有重要价值[4]。目前,鉴别1p/19q共缺失的金标准仍为有创性的病理检查,存在着出血、癫痫、神经功能障碍的风险[5]。随着“组学”概念的提出,影像组学作为无创预测肿瘤分子分型和评价肿瘤异质性的新手段,广泛应用于临床科研中。但由于1p/19q共缺失在胶质瘤中属于比较少见的基因丢失事件[6],故国内外研究相对较少。本研究通过T2加权成像(T2WI)构建影像组学模型,对低级别胶质瘤1p/19q状态进行预测研究。
1 资料与方法
1.1 一般资料
回顾性分析2018年1月~2021年12月经本院病理诊断为低级别胶质瘤的患者资料。纳入标准:肿瘤均为单发;术前4周内行常规MRI检查,包含完整的T2WI序列,且图像质量较好;MRI检查前均未进行任何医疗手段干预治疗;术后均行荧光原位杂交法检测1p/19q缺失状态。排除标准:轴位T2WI图像质量不佳,影响肿瘤分割及特征采集。最终共有154例患者纳入本次研究(表1),其中男性81例(52.59%),女性73例(47.41%),年龄19~84(42.08±13.58)岁。低级别胶质瘤两组间(1p/19q共缺失与1p/19q非共缺失)的一般资料(年龄、性别)差异均无统计学意义(t=1.501,P=0.135;χ2=1.480,P=0.224)。本研究通过厦门大学附属第一医院医院伦理委员会的批准。
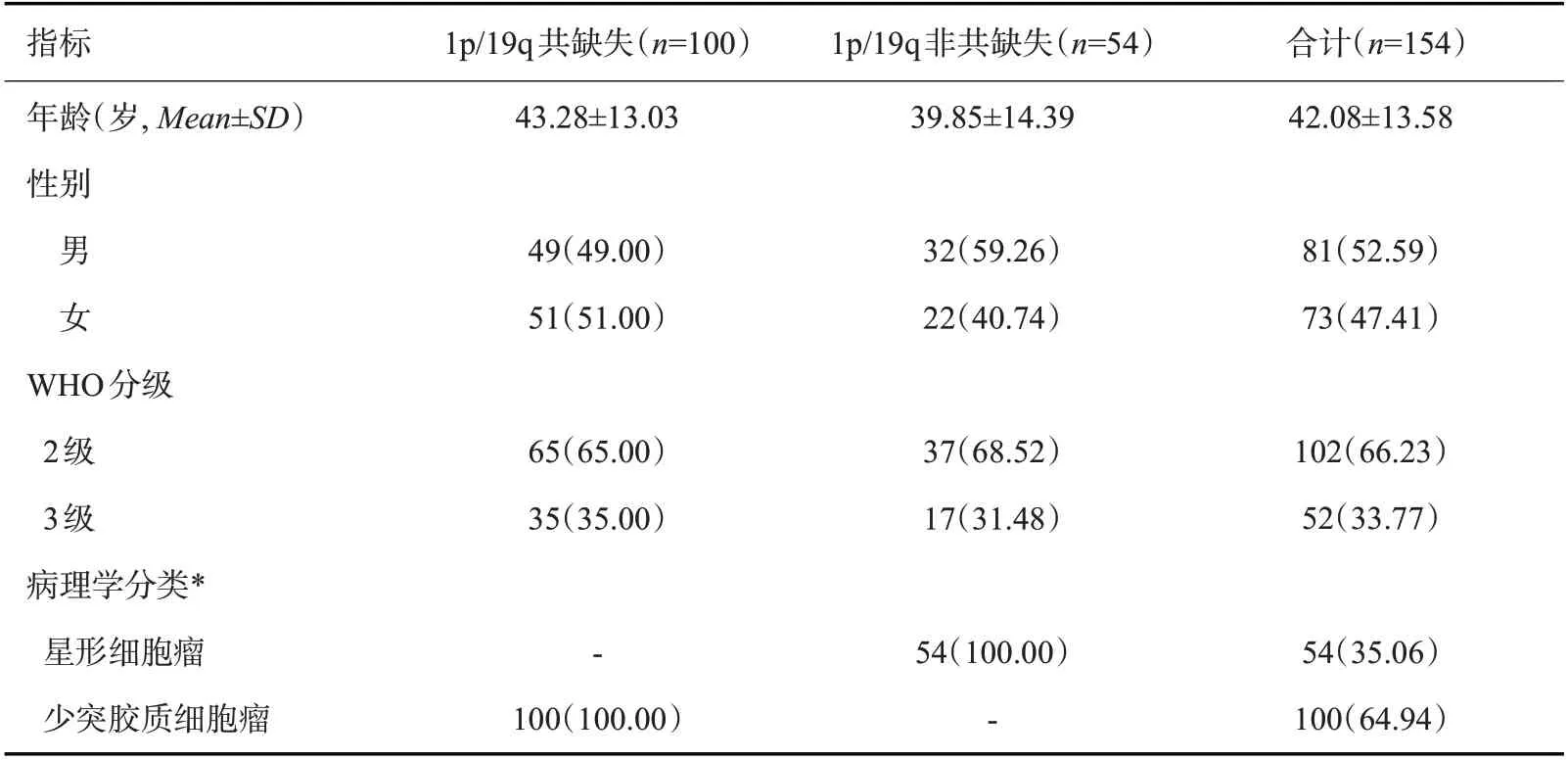
表1 患者临床信息及染色体1p/19q共缺失状态Tab.1 Clinical information and chromosome 1p/19 co-deletion status[n(%)]
1.2 扫描仪器及参数
所有患者术前均行常规MR 检查,使用Siemens 3.0T MR扫描仪,8通道相阵线圈。T2WI序列扫描参数:TR 5800 ms,TE 110 ms,视野220 mm×186 mm,反转角120°,激励次数1,矩阵256×512,层厚5.0 mm,层间距1.0 mm。
1.3 图像分割
由2名本院高年资主治医师(工作经验>12年)采用单盲法在T2WI 轴位图像上使用3D-Slicer 4.11 软件(https://www.slicer.org/)分别对肿瘤进行手动分割。由于WHO 3 级属于间变性肿瘤,其水肿区域可能出现肿瘤细胞浸润,因此勾画肿瘤感兴趣区(ROI)除肿瘤实质外,还应包含瘤周水肿区。当2位医师勾画肿瘤范围存在偏差时,由第3位资深的神经放射学医生(工作经验>20 年)对其ROI(包括目标病灶的T2WI原始图像)审查评估,最终经过二次勾画调整,以达成分割共识。
1.4 特征提取及筛选
使用pyradiomics进行特征提取,对每组ROI均提取851个影像组学特征,包括一阶统计量、灰度共生矩阵、灰度相关矩阵、灰度游程长度矩阵、灰度尺寸区域矩阵、邻域灰度差矩阵、形状、2D 形状及基于小波的特征。使用方差法,将方差低于设定阈值的特征筛选掉;剩余特征再使用10折交叉验证的最小绝对收缩和选择算子(LASSO)方法,引入惩罚因子,将不显著特征的权重系数降为0,从而筛选出重要的影像组学特征。
1.5 影像组学模型构建及评价
所有数据资料按分层抽样6:4分成训练集和验证集,训练集108 例(1p/19q 共缺失72 例,非共缺失36例),验证集46 例(1p/19q 共缺失28 例,非共缺失18例)。所有定量特征及模型构建均使用python 3.9.7分析处理。用LASSO筛选的特征分别构建支持向量机(SVM)、高斯朴素贝叶斯(GNB)、K-近邻(KNN)和逻辑回归(LR)模型。通过ROC 曲线下面积(AUC)及sklearn分类报告中的参考指标(准确度、敏感度、特异性、F1分数)评价模型的预测效能。
1.6 统计学分析
采用SPSS26.0软件进行统计学分析,计量资料以均数±标准差表示,两两比较采用独立样本t检验;计数资料为非连续性变量,采用卡方检验进行比较。以P<0.05为差异有统计学意义。
2 结果
2.1 影像组学特征筛选
851个特征分别标记为feature1~feature851。使用方差法对进行初步筛选,当方差阈值设为0.16时,筛选出108个特征。再通过10折交叉验证的LASSO算法,当惩罚因子=0.008时,筛选出14权重系数不为0的特征(图1),其特征贡献及权重系数(图2、表2),特征的关系热图(图3)。

表2 LASSO筛选的影像组学特征Tab.2 Radiomics features screened by LASSO algorithm
2.2 影像组学模型及效能评价
筛选出的影像组学特征分别构建SVM、GNB、KNN及LR模型,其训练集及验证集的ROC曲线(图4)。这4种机器学习模型在训练集中的AUC分别为0.95、0.81、0.92、0.91,在验证集中的AUC分别为0.91、0.77、0.86、0.88,其中SVM模型表现最佳;sklearn分类报告显示,各指标中表现最佳为KNN,其准确度、敏感度、特异性及F1分数分别为0.87、0.97、0.70、0.91,且各指标均高于模型平均值;其次为SVM,各项指标与模型平均值相当(表3)。
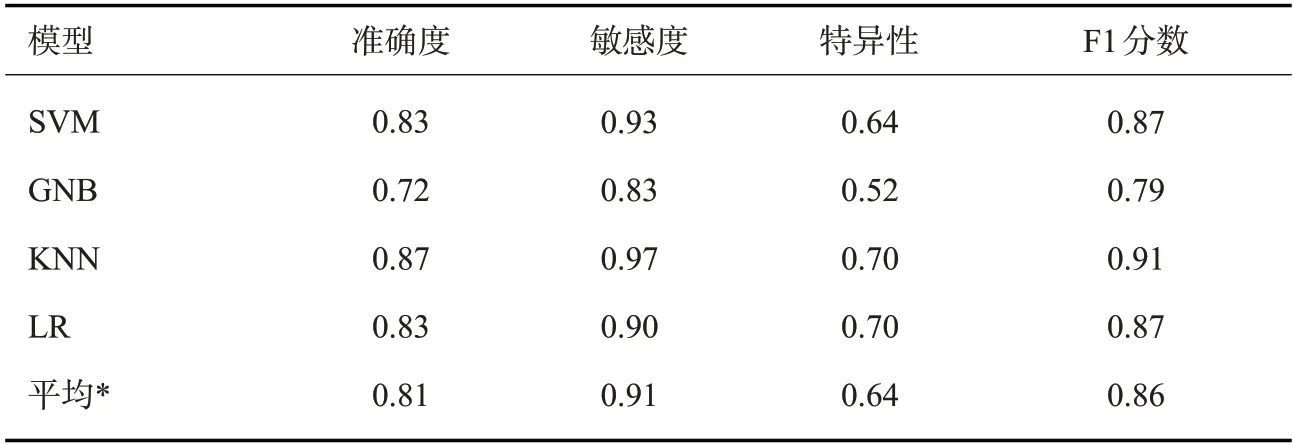
表3 机器学习模型的效能评价指标Tab.3 Effectiveness evaluation index of machine learning models
3 讨论
本研究通过提取T2WI 影像特征,构建SVM、GNB、KNN、LR 模型。用方差法和10 折交叉验证的LASSO算法对特征筛选,最终纳入14个与1p/19q共缺失显著相关的特征,包括4个一阶特征(即firstorder),主要反映所测体素的对称性、均匀性以及局部强度分布变化;10个纹理特征(包括4个glcm、3个gldm和3个glszm),主要反映图像体素灰度之间的空间排列关系。
在一阶特征中,偏度表示测量体素关于平均值的不对称性,偏度越大,说明肿瘤内部体素分布越不对称。该特征的纳入可能与文献[7-8]中描述1p/19q共缺失胶质瘤更容易出现钙化、囊变和水肿有关,肿瘤内成分的密度/信号跨度增大,会导致偏度增高。峰度是图像ROI中数值分布在平均值处峰值高低的特征数,它与偏度一样,是数据分布的重要描述性统计量,较高峰度表示ROI数值分布的质量集中在尾部,而较低峰度表示分布的质量集中在平均值附近的尖峰处。该特征的纳入提示胶质瘤1p/19q共缺失与1p/19q非共缺失之间存在体素分布质量集中的差异。在纹理特征中,集群阴影是衡量偏度和均匀度的指标,集群阴影越高,说明平均值的不对称性更大,集群阴影从纹理维度上加强了偏度识别的准确性。区域熵是测量区域大小和灰度级分布的不确定性和随机性,较高的值表示肿瘤纹理的异质性更高,该特征的纳入表明胶质瘤1p/19q共缺失与否之间存在异质性的差异。其余纹理特征的纳入,分别从能量强度、灰度级别、依赖强调等高维层面对全肿瘤异质性的差异作出评价。
在本研究4种模型中,SVM的AUC值最高,其在训练集和验证集中分别为0.95、0.91;而KNN在准确度、敏感度、特异性及F1分数上表现最佳,其次为SVM,均高于4种模型的平均值。因此,SVM模型在低级别胶质瘤1p/19q 状态的预测上具有良好的综合诊断效能,KNN模型具有较高的准确性和敏感度,而GNB和LR的稳健性及准确性相对较低。有学者通过分析98例弥漫性较低级别胶质瘤的FLAIR序列,从107个影像组学特征中筛选出8个显著特征建立SVM模型,其训练集和验证集AUC值分别为0.89和0.82[9];本研究与之比较,T2WI比FLAIR构建的SVM模型具有更高的AUC值,这可能与本次研究扩大了样本数、增加了训练集被试量及纳入了基于小波滤波的高阶纹理特征有关。此外,有研究发现超过半数1p/19q非共缺失的胶质瘤会发生T2/FLAIR不匹配(即T2呈高信号,FLAIR呈较低信号)[10];本研究结合该特征,提示在单独序列的影像组学中,T2WI比FLAIR可能更具有研究价值。有学者通过对157例WHO 2级胶质瘤患者进行T1WI、T2WI、对比T1加权图像采集,使用10折交叉验证LASSO法筛选影像组学特征,构建弹性网络和具有径向基函数核的SVM模型,其预测模型的AUC和准确度分别为0.81和0.76,F1分数为0.67[11]。该研究在特征筛选和模型构建上与本文存在共性,但文献中模型的诊断效能偏低,这可能与只纳入胶质瘤(WHO 2级)有关。有学者对96例WHO 2~3级胶质瘤进行磁共振图像采集,包括三维增强T1 和T2WI,使用LASSO 特征筛选并构建随机森林模型,其训练集和验证集的准确率分别为0.89 和0.83[12],与本研究使用的SVM、LR模型准确率相当,但低于KNN模型;AUC分别为0.94和0.89,均低于本研究的SVM模型。这说明随机森林模型在做同类研究时并不是最优模型,SVM较随机森林具有更好的稳健性,但值得注意的是不同机构所使用的数据结构有可能存在差异。也有学者采用与文献[12]相同的MR序列做特征提取,分别用5种机器学习模型进行纹理分析,发现神经网络、朴素贝叶斯、SVM、随机森林和随机梯度下降的预测效能差异没有统计学意义,5种算法平均AUC值为0.77~0.87,其中神经网络表现最佳,其AUC值为0.87[13]。本研究4种算法验证集中平均AUC值为0.86,SVM模型的AUC值高达0.91。虽然神经网络作为深度学习的经典应用,理论上应具备较高的诊断效能,但神经网络需要对大量的样本数据进行训练[14],而对类似于本研究的小样本数据来说,是否依然具有同样高的应用价值,还需要进一步比对研究。
本研究存在的局限性包括:(1)研究序列单一:据目前文献中对1p/19q缺失状态诊断有价值的序列[15-16],如T2WI、FLAIR、三维增强T1加权成像、表观扩散系数、体素内不相干运动等联合应用提取特征,会更全面的评价肿瘤异质性;(2)模型效能偏低:使用一些效能评价高、算法更为复杂的模型,如极端梯度提升、轻量级梯度提升机、卷积神经网络等,会有利于提高效能和综合评价;(3)单中心数据:扩大研究样本量的同时,应投入多机构、多中心的测试集中,进一步验证其预测效能。
综上所述,基于T2WI影像组学模型可以有效地预测低级别胶质瘤1p/19q的缺失状态。这种无创性技术为个性化治疗评估和诊断预测提供了可靠、有用的信息,在未来的临床科研中会有更广阔的应用前景。