经皮支架置入术与胆道引流术治疗肝门部恶性胆道梗阻的比较研究
2022-09-26姜小庆李明明徐家晨李思茵倪才方
姜小庆,李 智,李明明,胡 波,徐家晨,李思茵,倪才方
经皮穿刺介入治疗和逆行内镜治疗都是解除胆道梗阻的有效方法,但各有利弊[1-6]。介入治疗有外引流、内外引流、胆道支架3种模式。文献报道,外引流仅适用于一般状况差、预期生存期短或外科术前减黄的患者,如条件允许应选择胆道支架[7-9]。关于3种介入治疗模式的比较研究鲜见报道[10]。本研究收集介入治疗的恶性胆道梗阻(malignant billary obstruction,MBO)患者的临床资料,从引流效果、生存时间、并发症发生率等方面比较了不同介入方法治疗MBO的效果。
1 资料与方法
1.1 一般资料
回顾性分析苏州大学附属第一医院2016年1月至2020年12月接受介入治疗的MBO患者临床资料。纳入标准:①年龄18~85岁;②临床或病理诊断为MBO;③伴有MBO相关症状(黄疸、瘙痒、胆管炎、疼痛);④影像学检查Bismuth-Corlette分型为Ⅰ型或Ⅱ型;⑤不能手术切除或拒绝手术者;⑥ECOG评分0~3分。排除标准:①良性胆道梗阻;②术中造影发现Bismuth-CorletteⅢ或Ⅳ型患者;③既往行胆肠吻合术或内镜下胆管引流术者;④行胆道放射性粒子植入术者;⑤胆道支架置入后未拔除引流管者;⑥数据不完善或治疗后失访。患者选择流程见图1。
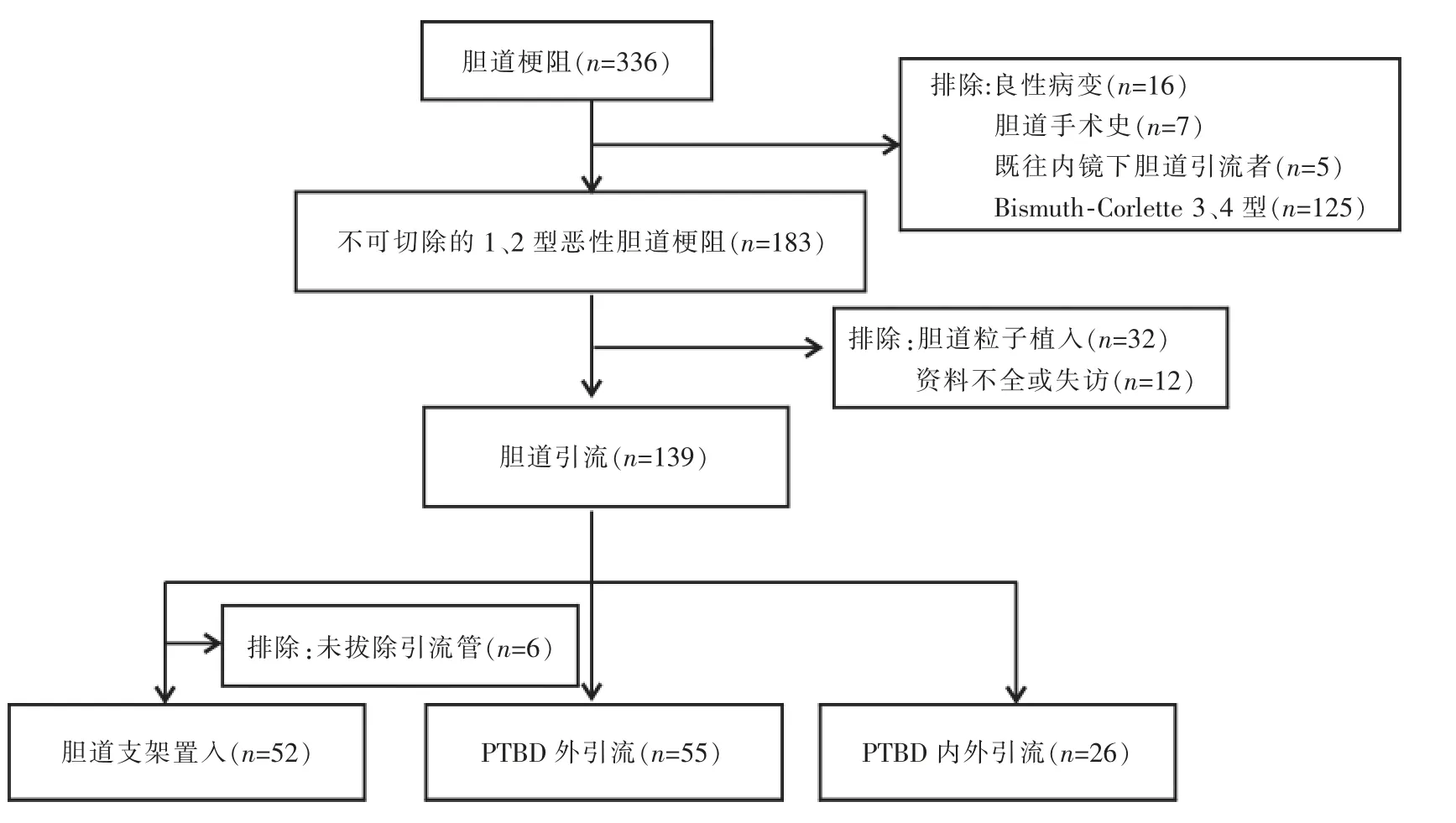
图1 患者选择流程图
根据引流方式不同将患者分为3组,其中胆道支架置入为A组(n=52),PTBD外引流为B组(n=55),PTBD内外引流为C组(n=26)。行支架置入术的患者因再梗阻或其他原因改变引流方式仍归为支架置入组,部分患者在支架置入前一期行PTBD外引流也归为支架置入组。
1.2 操作方法及术后处理
①胆道支架置入:在X线透视或超声引导下经皮肝内胆管穿刺,在狭窄段通过支架输送系统放置一枚自膨式金属裸支架,支架直径为8~10 mm,长度为6~10 cm,支架放置后,在支架内置入一根8~10 F猪尾巴引流管,部分有胆道感染的患者,一期行胆道外引流术,待感染症状改善后二期行支架置入术。②PTBD外引流及内外引流组:同样使用经皮肝内胆道穿刺方法,根据患者意愿在梗阻的上方(外引流)或十二指肠腔内(内外引流)置入8~10 F的猪尾巴引流管,部分行内外引流的患者为实现通畅引流需要另加侧孔,置入引流管的患者需体外固定引流管并连接引流袋。
胆道支架置入术后留置的引流管酌情开放或关闭,术后3 d复查胆红素,7~10 d后造影观察支架通畅情况,如胆红素水平明显下降且造影示引流通畅则拔除引流管。PTBD外引流及内外引流组每3个月更换一次引流管,以避免感染和导管移位。
1.3 观察指标
主要观察指标为各引流组的生存时间,次要观察指标为技术成功率、临床成功率、胆道再梗阻情况与再次介入率、术后化疗及不良事件(包括出血、感染、胰腺炎、引流管或支架移位等)发生率。其中生存时间是指从引流术后至患者死亡;技术成功是指支架或引流管到达目标胆管的狭窄段且透视下可见对比剂顺利通过支架或引流管;临床成功指胆红素水平在两周内降低至治疗前的50%以下水平[11-12]。再次介入指需要重新建立穿刺通道进行胆汁引流,而不包括PTBD外引流和内外引流定期换管。不良事件的评价是根据常见不良事件评价标准(CTCAE)5.0版进行评估,1、2级为轻中度不良事件,指无需治疗或需要较小、局部或非侵入性治疗;3、4级为严重或危及生命的不良事件,导致住院时间延长或需要紧急治疗。通过电子病历、复检记录及电话随访的方式获取患者资料,随访时间截至2021年3月或患者死亡。
1.4 统计学分析
采用SPSS 21.0分析软件。连续性变量以中位数和范围表示,采用方差分析;分类变量用卡方、似然比或kruskalwallis检验;用Kaplan-Meier法绘制生存曲线,组间生存率比较采用Log rank法;Cox比例风险模型进行单因素和多因素分析评估影响生存率的相关因素。P<0.05为差异有统计学意义。
2 结果
2.1 基线资料
共纳入患者133例,其中男性89例,女性44例,年龄18~85岁。A组、B组及C组的术前基线资料见表1。3组患者的年龄、性别、直接胆红素和总胆红素水平、Bismuth-Corlette分型、原发病类型及有无术前化疗比较差异均无统计学意义(均P>0.05)。
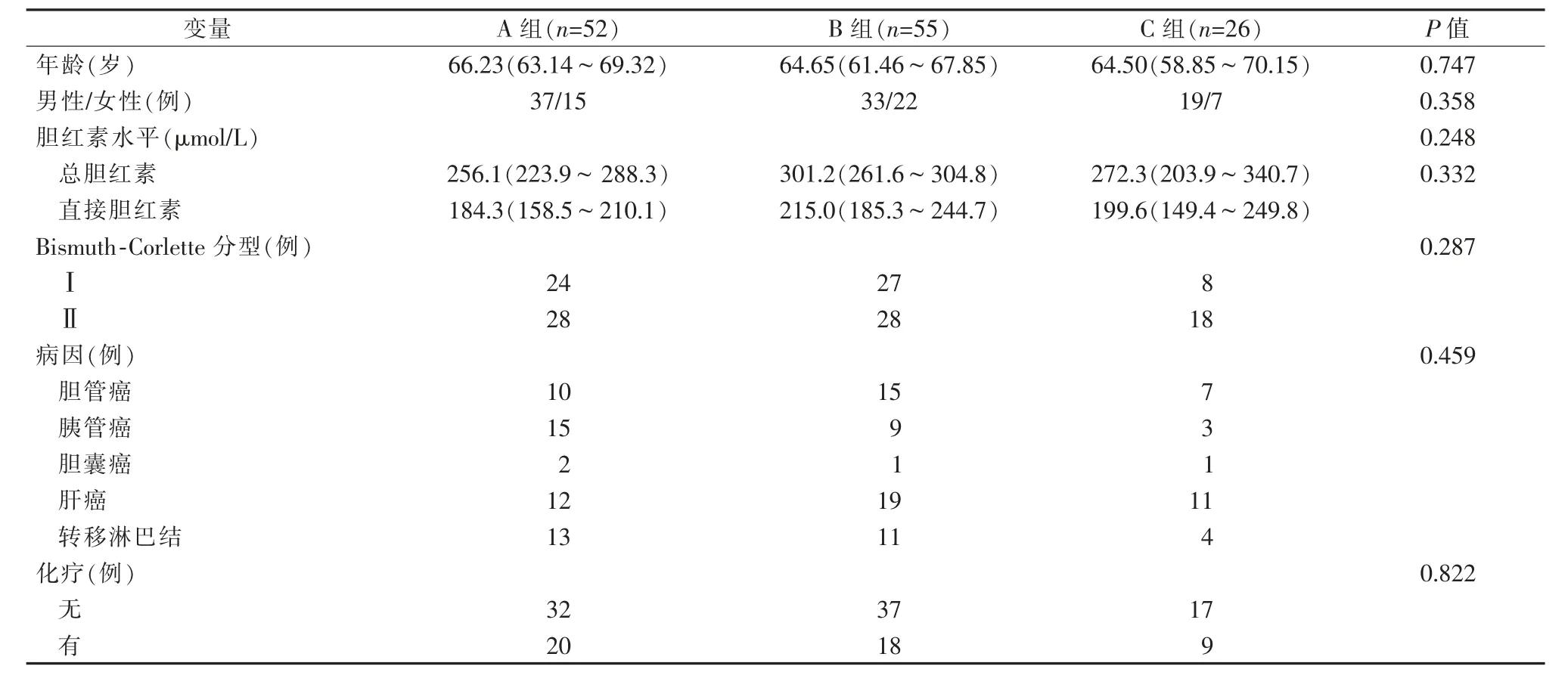
表1 A组、B组和C组患者术前基线资料对比
2.2 生存分析
至随访截止时间,有5例患者仍存活,包括1例胆道支架置入患者及4例PTBD外引流患者。A、B、C 3组患者的中位生存时间分别为64(59~69)d、95(30~160)d、42(36~48)d,B组患者的生存时间优于A组及C组。3组患者累积生存曲线见图2,A与B组、A与C组及B与C组比较差异均有统计学意义(均P<0.05)。

图2 支架组、外引流组和内外引流组恶性胆道梗阻患者的生存曲线
Cox单因素分析显示不同引流方式、性别、Bismuth-Corlette分型是影响患者OS的危险因素,进一步将单因素分析中差异有统计学意义的变量纳入多因素分析,结果显示不同引流方式和Bismuth-Corlette分型是影响患者OS的独立危险因素。见表2。

表2 影响恶性胆道梗阻患者生存期的单因素和多因素分析
2.3 技术成功率与临床成功率
3组患者技术成功率均为100%;临床成功率分别为73.1%、80%、50%,A与C组、B与C组比较差异均有统计学意义(P<0.05),而A与B组比较差异无统计学意义(P>0.05)。见表3。
2.4 胆道再梗阻与再次介入手术情况
A组患者中有10例在3个月内出现支架再梗阻,2例在半年之后出现了再梗阻,在再梗阻患者中,2例再次行支架置入术,4例行PTBD外引流术,2例行内外引流术;B组中有1例在3个月内出现再梗阻,考虑因胆汁粘稠所致,0.9%NaCl溶液冲管后症状好转,B组患者每3个月左右更换一次引流管,未改变引流方式;C组患者中有3例因严重胆道感染改为外引流,1例在术后半个月发生引流管堵塞,更换引流管后引流通畅,C组患者亦定期更换引流管。3组患者引流后有14例患者获得了化疗机会,其中A组4例(7.7%),B组10例(18.2%),而C组患者均未行术后化疗。见表3。

表3 A组、B组和C组恶性胆道梗阻患者术后情况对比 [例(%)]
2.5 不良事件
根据不良事件评价标准(CTCAE)5.0版评估,A、B、C 3组患者1~2级不良事件的发生率分别为19.2%、10.9%和11.5%,差异无统计学意义(P=0.425),而3~4级不良事件发生率为50%、30.9%和69.2%,差异有统计学意义(P=0.004),其中急性胆管炎是最常见的并发症,A、B、C组分别为16例(30.8%)、12例(21.8%)和11例(43.3%)。见表3。
3 讨论
对于无法手术治疗的MBO患者,支架置入及PTBD是缓解黄疸的有效手段,PTBD又可分为外引流和内外引流,这3种引流方式各有利弊。本研究结果显示,在生存期方面,PTBD外引流患者的中位生存期长于支架置入及PTBD内外引流的患者,3组间比较差异均有统计学意义,多因素分析结果显示不同引流方式和Bismuth-Corlette分型是影响生存期的独立危险因素。要提高胆道梗阻患者的生存期,引流胆汁量至少要达到肝容积的50%,这样可以减少胆管炎的发生,当黄疸减少到一定的程度时,患者可以进行化疗,进一步延长生存期[13]。有研究表明,黄疸与预后不良有关,当引流有效时,存活时间可从33 d提高到262 d[11]。因为肝代谢是大多数化疗药物的主要消除途径,化疗需要良好的肝功能和有效的胆汁清除。因此,有效的胆道引流是一个先决条件,不仅是为了患者的生活质量和营养稳定,也是为了进行化疗[14]。在本研究中,PTBD外引流组的临床引流成功率高于支架置入组及内外引流组;同时,PTBD外引流的3~4级不良事件发生率低于另外两组,主要不良事件包括感染和急性胰腺炎,而这些都是影响患者生存时间的重要因素。
从引流效果来看,3组的技术成功率均达到了100%,这可归因于近几年来临床医生胆道引流技术的提高。在既往研究中,PTBD外引流、支架置入的临床引流成功率分别为71%~97%、65%~100%[15-16],与本研究结果基本一致。关于临床引流成功的定义,目前尚无统一认识。一些学者认为,胆红素降至40μmol/L达到可化疗的水平即为引流成功,但并未说明多长时间内达到此水平,本研究中患者的病因不同,并非所有患者都适合化疗。内外引流的临床成功率仅为50%,与支架相比,内外引流管管径较细,粘稠的胆汁不易排出,与外引流相比,其导管头端位于肠道内易受肠道内压的影响,当肠道内压较大时肠内容物易逆流入引流管致其堵塞,这两点都在一定程度上影响了内外引流的效果。
一般认为,金属支架的通畅时间为6~12个月,若患者的预期生存时间大于3个月,则建议使用金属支架[1]。本研究支架置入组3个月、6个月的再梗阻分别为10例和15例,发生支架再梗阻的因素很多,除了肿瘤通过网眼向内生长或在支架两端生长、污泥或结石形成等原因外[17-18],支架本身也占据一定的空间,在一定程度上减小了胆道的内径,促进胆汁中有形成分的沉积,进而导致了胆道再梗阻。PTBD引流管虽然内径小于支架,但缺少像支架一样的网眼,所以因肿瘤压迫导致引流管梗阻的概率相对较低,此外,PTBD外引流及内外引流患者每3个月需要更换引流管,这在一定程度上也降低了再梗阻率。支架置入后再次梗阻的处理较PTBD更为复杂,手术风险也更高,需要重新穿刺建立通道。本研究中,15例发生支架再梗阻患者中有2例再次行支架置入术,4例改为外引流,2例改为内外引流。B组和C组各有1例患者在3个月内出现了胆道再梗阻,B组患者因胆汁粘稠所致,C组因引流管移位致胆汁不能有效引流。
本研究中共有14例在引流术后进行了全身化疗,主要包括胰腺癌和其他部位恶性肿瘤淋巴结转移致肝门部胆道梗阻的患者,部分肝癌和胆管癌患者进行了TACE治疗。外引流患者进行全身化疗的比例最高,可能是由于其临床引流成功率较高且术后并发症较少,达到可以化疗的的水平。
胆道支架和PTBD的常见并发症包括出血、感染、疼痛、胰腺炎、胆汁渗漏等。在本研究中,1~2级并发症主要是腹痛、出血及胆汁渗漏,3组之间没有显著差异;3~4级并发症为急性胆管炎、败血症、出血、急性胰腺炎及导管移位,B组与A、C组差异较大,A、C组间差异无统计学意义。主要的3~4级不良事件是急性胆管炎和败血症,内外引流组发生率最高,主要原因在于引流管头端位于肠道内,增加了胆道感染的风险,胆道压力高导致细菌入血引起败血症。外引流组有1例患者发生严重胆道出血,通过止血、输注血浆等保守治疗后好转。据报道,PTBD术后大出血的发生率为0.6%~12.0%,门静脉出血大多仅需保守治疗即可改善,而肝动脉出血则需要紧急栓塞[19]。术前需仔细评估胆管扩张的部位,减少血管损伤事件的发生。本研究中外引流组中有3例、内外引流组中1例患者出现导管脱落或移位,而支架置入组未发生移位,外引流或内外引流术后需妥善固定引流管和引流袋,发生移位的概率减少。对于不可切除的恶性胆道梗阻的患者,临床上多将胆道支架作为胆汁引流的首选,因为PTBD术需要外接引流管和引流袋,给患者的生活带来不便,但外引流可以方便观察胆汁颜色、性状及每日引流量,当出现变化时可尽早采取治疗措施。当然,PTBD术的弊端是长期的外引流造成胆汁流失,导致机体电解质、酸碱平衡紊乱,这可通过术后加强营养或进行胆汁回输来改善[20-22]。在本研究中,PTBD外引流可显著延长患者的生存期和减少3~4级不良事件的发生。但是在临床工作中,还需要根据患者的需求和病情选择对患者最有利的治疗方式。
本研究具有一定的局限性,首先,是一项回顾性研究,存在一定的选择偏倚;其次,是一项单中心研究,患者数量较少;第三,由于患者数量有限,没有对病因进行分层,可能导致每组患者病因分类不均一。
