用于凝血检测的声波传感器研究及应用进展*
2022-09-22王小丽庞义全侯立威何薪宇牟笑静
王小丽 庞义全 侯立威 何薪宇 葛 闯 牟笑静 徐 溢**
(1)重庆大学新型微纳米器件与系统技术重点学科实验室,光电技术与系统教育部重点实验室,重庆 400044;2)重庆大学光电工程学院,重庆 400044;3)重庆大学化学化工学院,重庆 400030;4)重庆大学肿瘤医院癌症转移和个体化治疗转化研究重点实验室,重庆 400030)
凝血检测对凝血相关疾病诊断、抗凝药物筛查、围手术期凝血状态评估具有重要的意义[1-4]。凝血过程是由内源性或者外源性的激活剂激活凝血因子而发生的一系列酶联反应(图1a)[5]。纤维蛋白生成期是凝血过程的核心,其本质是可溶的纤维蛋白原(凝血因子I)在凝血酶的作用下变成不可溶的纤维蛋白,纤维蛋白再聚合成纤维蛋白聚合物,随着侧向聚合程度加深,血块显得黏稠,由透明转向不透明。在Ca2+存在下,凝血因子XⅢ被迅速激活,能使聚合的纤维蛋白在邻近的肽链间形成桥键,从而形成稳定的交联纤维蛋白多聚体(图1b)[6]。在凝血过程中,血液的黏度、剪切阻力、密度等参数变化与凝血过程中凝血时间、血凝块的形成动力学及蛋白质分子含量等高度关联。在凝血检测中,凝血酶原时间(prothrombin time,PT)、活化部分凝血活酶时间(activated partial thrombin time,aPTT)、活 化 凝 血 时 间(activated coagulation time,ACT)、凝血酶时间(thrombin time,TT)是研究凝血疾病和药物监测最有效的测试指标[7]。
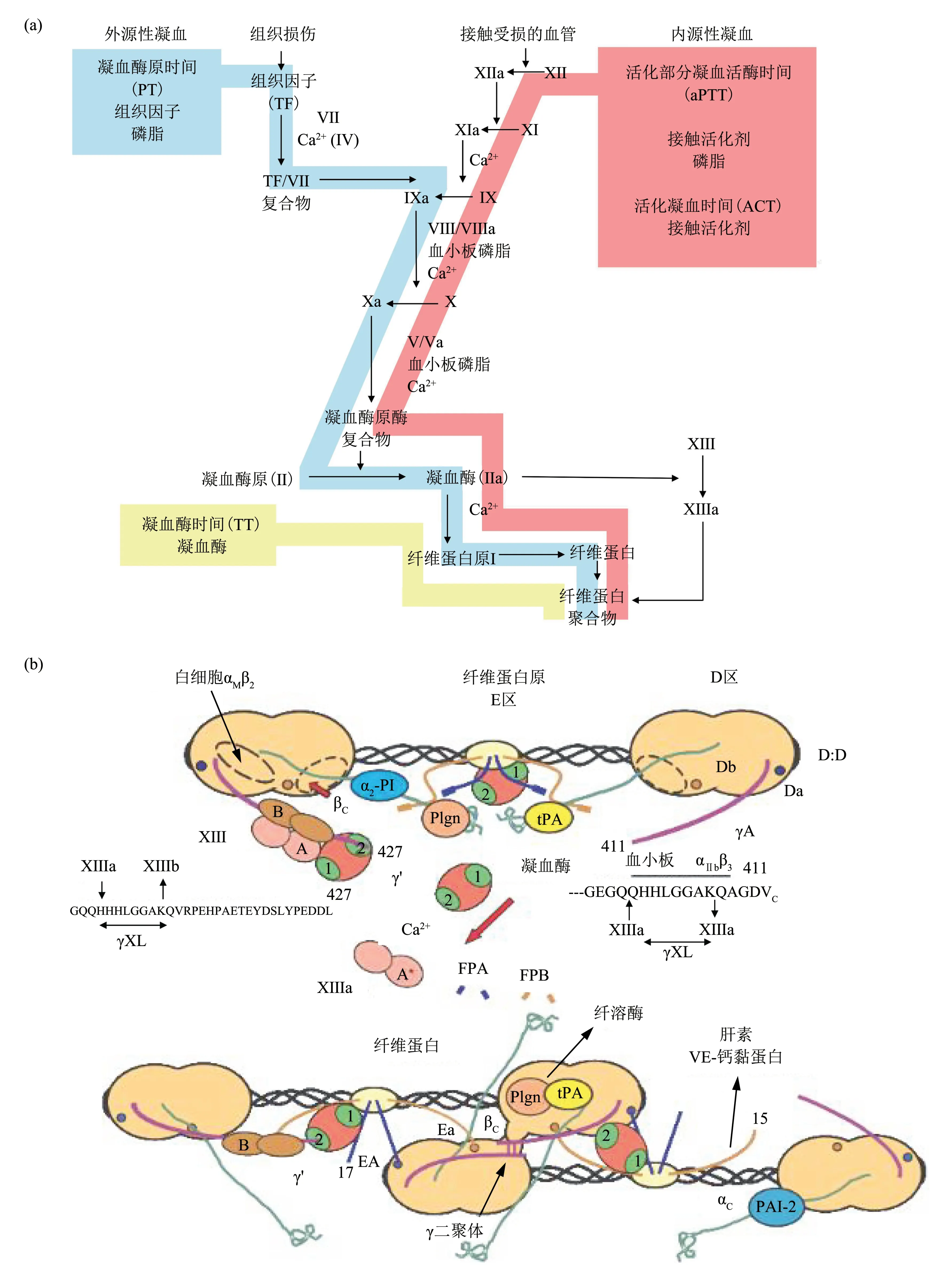
Fig.1 The coagulation cascade and clotting time(a)[5]and the major chemical reactions(b)[6]图1 凝血过程和凝血时间(a)[5]及发生的主要化学反应(b)[6]
传统的凝血检测方法包括光学法、机械法、电化学法等,存在易受样品本底干扰、操作过程复杂、需要专业技术人员和昂贵的大型仪器等缺点,越来越难以满足人们对快速、高灵敏的凝血检测要求[8-9]。床旁检测(point of care test,POCT)是指采用手持式或台式分析仪快速获取测试结果的方法,不受时间、场地环境的限制,开发准确、快速、高灵敏的POCT方法有利于快速做出医疗决策,已成为凝血测试方法研究的新趋势[10-11]。众所周知,生化传感器具有样品用量少、分析速度快、易于自动化、集成化和微型化等特点,由此发展起来的生化传感技术可为床旁(POC)凝血检测提供新的方法和技术途径。目前,已有许多生化传感器用于凝血检测,包括微悬臂梁传感器[12]、电化学传感器[13]、声学传感器[14]、介电常数传感器[15]、应变传感器等[16]。其中,声波传感技术在凝血检测中显示出独有的优势,比如不会破坏凝血进程,不易受黄疸、糜乳等异常样品的干扰,所需样品量仅几微升到十微升。同时,声波传感器具有抗电磁干扰能力强、可实时在线监测、快速准确、易于集成和微型化等优势,在凝血检测中备受关注。目前,石英晶体微天平(quartz microcrystal balance,QCM)、声表面波(surface acoustic wave,SAW)传感器、薄膜体声波谐振器(thin film bulk acoustic resonator,FBAR)、兰姆(Lamb)波谐振器、超声波传感器等声波传感器已在核酸、微生物、生物小分子的分析检测中多有应用[17]。本课题组也进行了相关研究[18-20],所研制的基于氮化铝(AlN)膜的双模态兰姆波传感器,在凝血检测显示出响应速度快、样品用量极少等优点[21]。研究发现,声波传感器由于可以感受凝血过程中多个参数的细微变化,可快速获得丰富的凝血信息,使得其在凝血检测方面具有极大的优势。
据此,本文在对凝血过程中发生的主要物理化学变化及相应参数进行简要介绍基础之上,分析总结声波传感器在凝血检测中的传感检测原理,重点对QCM、SAW传感器、FBAR和Lamb波传感器的设计及其应用进展进行分析与总结,对集成声波传感器的微流控芯片在凝血检测中的应用进展进行综述,并对声波传感器在凝血检测中面临的挑战及发展趋势进行讨论和展望。
1 凝血检测中的声波传感器研制进展
1.1 石英晶体微天平(QCM)
QCM是最常见的基于厚度剪切模式的压电晶体传感器,也是应用最为广泛的声波传感器件。QCM由夹在两个电极之间的压电材料组成,对其表面的质量(液体环境中的微克级)和黏度密度非常敏感[22]。
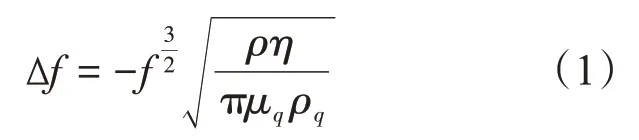
πμq ρq为石英本身的声学(机电)阻抗,ρ为血浆密度,η为血浆黏度。本课题组[23-25]在QCM气体传感器方面做了大量工作,并将其用于VOC、NH3等有毒气体的检测。QCM也用于各种基于液体的传感应用中,比如精液[26]、黄曲霉毒素B1[27]及凝血时间[28]等的检测。在晶体中传播的弹性横波与液体之间的耦合产生阻尼剪切-水平振荡,在横波穿透深度内呈指数衰减:

在水介质中,当谐振频率5 MHz、传感深度δ~250 nm时,波能阻尼(耗散)表现为动态电阻R[29-30]的增加:
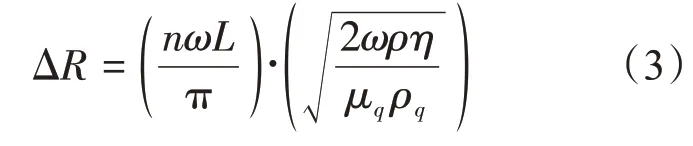
其中n为与液体接触的边数,ω为串联谐振的角频率,L为空载(干)传感器处的电感,然而这个理论仅支持亲水性表面无滑移边界条件。在血液凝固过程中,纤维蛋白原变成纤维蛋白,附着在QCM传感表面形成黏弹性膜,其深度超过QCM传感深度,使其不能完全随着晶体的振动而运动,部分能量会损耗在内摩擦中。因此,早期QCM对凝血检测的效果并不理想[28,31]。为此,有研究提出耗散型石英晶体微天平(dissipative quartz crystal microbalance,QCM-D),通过间歇地打开/断开电路,记录芯片频率的变化(Δf)以及基频从振荡到恢复静止的快慢,即耗散值(ΔD),可实现黏弹性吸附量的精确测量。根据Kevin-Voigt模型,QCM-D的耗散变化[32]可以表示为:

其中,f0、ρ0和h0是谐振频率、传感器的密度和厚度,h1、μ1、η1分别代表蛋白质层的厚度、剪切弹性和黏度,η是血浆黏度,δ是横波的穿透深度,ω是共振角频率。基于QCM-D的凝血过程及检测参数变化如图2a所示,除了QCM-D自身参数外,传感界面通过改变h1、μ1、η1等参数而影响传感器的响应速度和灵敏度[33]。
Hussain等[34]采用肝素分子对QCM-D电极表面进行分子印迹处理后,用于凝血时间的快速检测和抗凝剂肝素的治疗监测,测试所需血浆量为2 μl,测试时间较常规血凝仪分别缩短3倍和2.5倍。Oberfrank等[35]采用滴涂法在QCM-D传感电极表面上修饰一层来自受检者自身提供的贫血小板血浆,可在1 min内测得凝血时间,其值与凝血仪测试结果一致。此外,通过在QCM传感电极上修饰不同的配体和蛋白质,还可将其用于纤维蛋白原(1~6 g/L)、肝素、凝血因子VIII[36-37]等的检测,研究血小板聚集和组织因子对血液凝固的影响[38-39]。Kim等[40]通过镍钛诺/肝素/抗增殖药物修饰耗散型石英晶体纳米天平(quartz crystal nanobalance-dissipation,QCN-D),使QCN-D对负载在其电极表面的物质做出频率和耗散响应,将其用于研究支架表面动态条件下的凝血行为(图2b),能很好地模拟支架表面的血流动力学条件,为评估支架血栓形成风险提供了更加可靠的方式。总之,QCM-D结构更为简单、价格相对便宜,发展成熟,当前研究的重点主要集中在通过传感电极表面的修饰来加快检测速度和提高灵敏度。
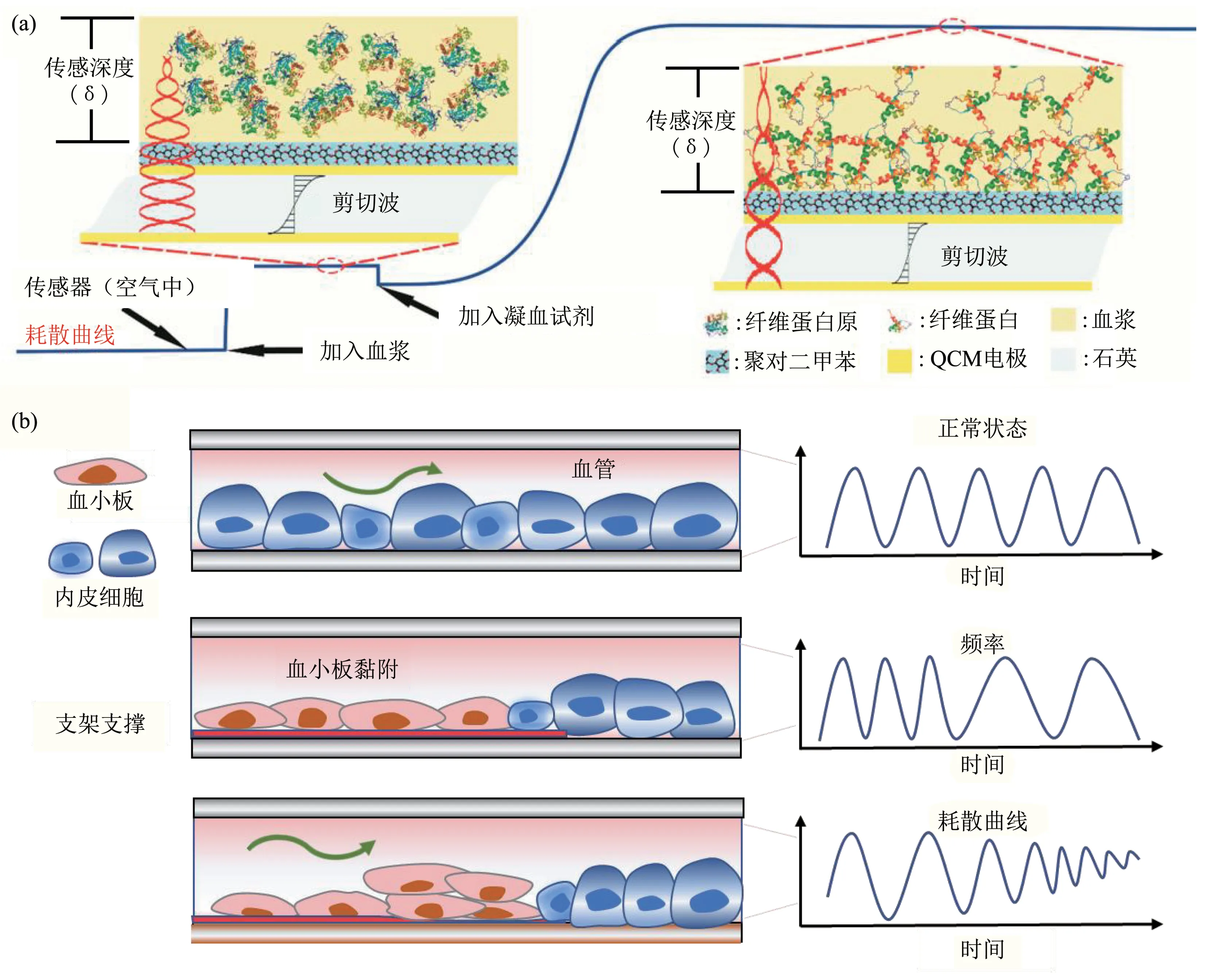
Fig.2 Principle of blood coagulation detection based on QCM and the signal it generates图2 基于QCM的凝血测试原理及信号响应
1.2 声表面波(SAW)传感器
SAW传感器已广泛用于蛋白质、核酸、细胞等的检测以及凝血过程的监测[41-43]。SAW传感器可将声波限制在传感表面传播,因而对表面质量变化高度敏感,其质量灵敏度为[17]:
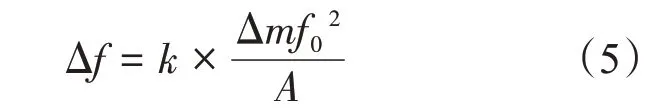
k为传感系统常数,Δm为质量荷载,f0为基频,A为传感面积。Guhr等[44]研制了以36°YX-LiTaO3为压电基底的单端口声表面波谐振器,其可对血液粘弹性变化做出频率响应。为排除电扰动对检测凝血过程中的机械变化的影响,Nagayama等[45]设计了以36°YX-LiTaO3为压电基底的双延迟线型结构的水平剪切型SAW(SH-SAW)声表面波传感器,以金属化传感界面为参比,自由化传感界面对微量质量变化做出相位响应[46]:

ΔPh为SH-SAW生物传感器相移(°),f为频率(Hz),l是传播长度(m),V0是加载前声波速度(m/s),加载后声波速度V1(m/s)。根据公式(5)可知,提高SAW传感器灵敏度的有效策略是增加工作频率f、传播长度l以及加载前后声波速度变化值。
基于Love模式的声表面波传感器在声表面波传感器压电基底上引入聚合物材料、玻璃或无定形石英等波导层,将声波限定在离传感表面更近的区域中传播,以减少能量损耗,可有效提高f、l值,从而提高灵敏度,同时保护电极不受生化液体的影响。本课题组[19-20]研制了多种声表面波生物传感器,在生化检测中展示出高灵敏、实时检测等优势。所研制基于单层石墨烯/纳米金的Love模式声表面波生物传感器,使核酸的检出限低至12.4 μg/L[18]。Hohmann等[47]通过将聚甲基丙烯酸甲酯(PMMA)和聚苯乙烯(PS)修饰到LiTaO3压电基底上,构建了双通道声表面波谐振器,采用差频信号处理技术,极大提升该传感器频率响应的稳定性。Rupp等[48]等构建了以LiTaO3为基底、以玻璃为波导层的基于Love模式的声表面波免疫传感器,通过在波导层上修饰聚乙烯胺来固定抗体,实现了血浆、血清或者全血中纤维蛋白原的定量检测,其检出限为4 mg/L。Gronewold等[49]设计了以AT-石英晶体为压电基底的基于Love模式的声表面波传感器阵列,通过在传感电极表面上修饰适配体,实现凝血过程中的凝血酶和凝血酶抑制剂的定量检测。研究表明,大多数用于凝血检测的基于Love模式的声表面波传感器为延迟线型结构,其通过感应传感界面上的微弱质量变化而作出相位响应。
一种新的基于Love波模式的单端口谐振型声表面波传感器在POC凝血检测中展示出极大的优势和发展潜力,其可以对凝血级联反应中微弱质量变化作出频率响应[50]:
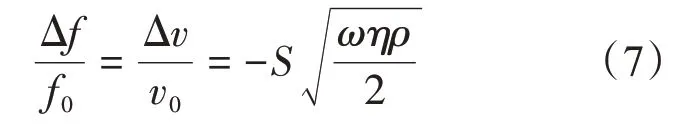
f0是加载前工作频率,Δf是加载后的频移,ν0为加载前的声速,Δv为加载后的声速差,ω为角频率,ρ为密度,η为黏度。Chen等[51]将研制的基于Love模式的单端口声表面波(single-port lovemode surface acoustic wave,SLSAW)谐振器,用于凝血时间的检测以及凝血动力学研究,且SLSAW谐振器件被设计成可一次性使用的即插即用型结构(图3)。与其他声波传感器相比,SLSAW传感器显示出更强的频率响应,测试结果与标准TEG分析仪测试结果具有很好的相关性。
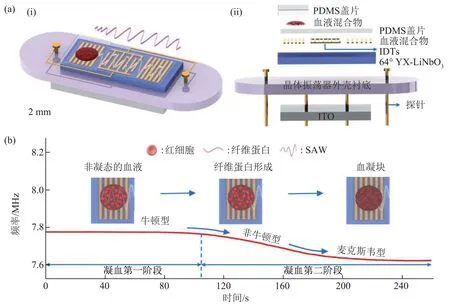
Fig.3 Structure and measurement principle of SLSAW sensor[51]图3 SLSAW传感器的结构和检测原理示意图[51]
可以看到,延迟线型SAW传感器在凝血指标测试中的灵敏度和稳定性还有待进一步提升,新发展的谐振型SAW传感器有望突破了这一局限。
1.3 薄膜体声波谐振器(FBAR)
FBAR由两个金属层以及夹在金属层之间的一个压电薄膜构成[52-54]。压电薄膜(100 nm至几μm)使FBAR可实现GHz工作频率,常见的压电薄膜包括AlN[55]、ZnO[56]、Pb(Zr,Ti)O3[57]、BaxSr1-xTiO3[58]等。在液体环境中,FBAR共振状态会受到相邻介质阻尼的影响,使其可以有效监测生物反应过程中的粘弹性变化[59-60]。FBAR在牛顿型液体中的频率响应为[61]:

ΔfN为牛顿型流体中的频移,fR是空气中的共振频率,ρ0和μ0分别表示压电层的密度和弹性模量,ρl为加载液体密度,ηl为加载液体的黏度。在麦克斯韦黏弹性流体中的频率响应为[62]:
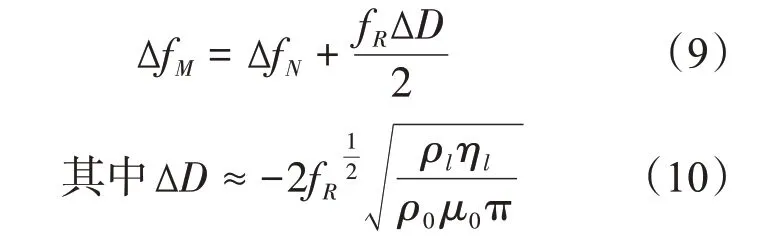
ΔfM为在麦克斯韦黏弹性流体中的频移,ΔD为高黏弹流体引起的耗散变化。FBAR的Q因子的计算公式为[63]:f为液体介质中的工作频率,FWHM为半峰全宽。因此,工作频率和Q因子是FBAR谐振器的核心。
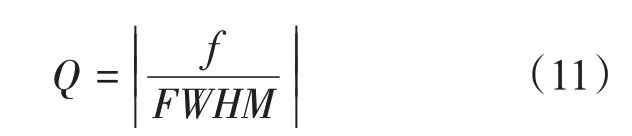
较早用于凝血检测的FBAR谐振器是countermode FBAR(C-FBAR)[60]。C-FBAR通 过 压 电AlN悬浮环形成径向共振模式,在半无限深度液体中的Q因子较低(水中为189和人全血中为77),难以满足凝血测试要求[64]。为提高FBAR在液体环境下的灵敏度,研究者提出研制C轴倾斜的压电薄膜,并与位于薄膜相对两侧的两个电极耦合[65]。通过共面电极,使用横向场激发C轴取向的压电薄膜,是产生厚度剪切模式的有效方法[66]。Chen等[67]研制了用于实时监测血液凝固过程和测量凝血参数的FBAR谐振器。该谐振器由Au/ZnO/Si3N4薄膜叠层制成(图4a),其传感表面修饰了有利于纤维蛋白原吸附的聚乙烯薄层,可产生1.42 GHz的剪切模式共振,在血液中的品质因数高达342。在血液凝固过程中,FBAR谐振器共振频率随血液黏度的变化而降低,呈现明显的阶梯曲线,凝血酶原时间(PT)测试结果与标准凝血测定方法具有良好的一致性。Chen等[68]采用类似的FBAR谐振器对凝血过程动力学进行研究,通过拟合时间-频率曲线,获得酶联反应时间、凝血速率、凝血时间和凝血程度等丰富的凝血信息。Chen等[14]研制了具有声学布拉格反射器的AlN基FBAR谐振器,工作频率高达1.9 GHz(图4b),SiO2/W反射器表面更光滑,使波散射减少,FBAR的Q因子从313提高到了430。在凝血测试中,FBAR谐振器的黏度检测灵敏度高达-337 kHz/cP,样品用量低至1 μl。
可见,FBAR具有很高的灵敏度,但结构相对复杂、工艺难度比其他声波传感器大,FBAR谐振器在凝血测试中极具优势,有可能发展为微型化、在线、自动化凝血检测工具。
1.4 兰姆(Lamb)波谐振器
Lamb波谐振器(Lamb wave resonator)的基频由平面内尺寸决定,制造采用MEMS技术平台,具有CMOS工艺兼容性,可成批地在同一个芯片上制造出不同谐振频率的微谐振器阵列,已用于生物化学检测中[67]。Lamb波谐振器最初在凝血检测中应用不起传感作用,而是代替SAW作为声波流发生器。Nam等[69]通过Lamb波产生声波流,快速混合血液和凝血试剂,混合液滴中的荧光颗粒随着声波流运动,随着血液的凝固,荧光颗粒逐渐停止运动,根据荧光颗粒的运动状态,判断凝血酶原时间PT。
Lamb波谐振器具有极高灵敏度和低信号衰减,在凝血检测中已展示出极大的优势。当Lamb波谐振器浸入液体中时,其传感界面上会产生渐逝波层。在血液凝固过程中,渐逝波的穿透深度会随着血液的凝固而发生变化,从而引起频率偏移。渐逝波的穿透深度[70]为:
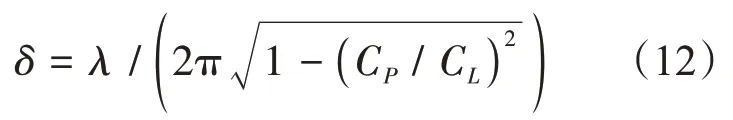
其中λ和CP分别为兰姆波的波长和相速度,δ消逝波层厚度,CL为液体的体声速,而CP由频率f决定)(CP=λf)。图4c显示了Lamb波谐振器监测凝血过程的原理。随着纤维蛋白的产生,消逝波层厚度发生变化,影响Lamb波的传播速度V,从而引起频率发生偏移。
Kong等[71]研制了聚乙烯-C修饰的Lamb波传感器(P-Lamb波传感器),使其在aPTT检测中的稳定性和灵敏度得到有效改善,其频率变化值大约是QCM的200倍。本课题组[21]通过研制双模态Lamb波传感器,设计了以AlN为压电晶体的双模态Lamb波传感器,其谐振频率为860 MHz,瑞利波模式的谐振频率为444 MHz。由于Lamb波对血浆黏度和温度都敏感,而瑞利波只对温度有频率响应,可以获取更加丰富的凝血信息,Lamb传感器在凝血检测中初步展示出很高的灵敏度,作为后起之秀具有较好的发展前景。
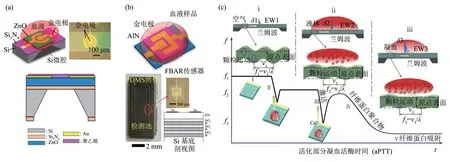
Fig.4 FBAR and Lamb wave sensor for coagulation detection图4 用于凝血检测的FBAR谐振器和Lamb波谐振器
综上所述,表1列出了用于凝血检测的各种声波传感器、物理参数及其在凝血测试中的应用。QCM和SAW传感器通过感知传感界面上凝血过程中的微弱质量变化而实现凝血检测,QCM还能对血液的黏弹性做出响应。FBAR谐振器和Lamb波传感器则通过感应血液的黏度变化而产生共振频率的移动。

Table 1 Summary of acoustic sensors for blood coagulation measurement and their main parameters表1 用于凝血检测的声波传感器及其关键参数
可以看到,声波传感器在凝血时间及其相关蛋白质的检测、凝血过程动力学研究、抗凝药物评估与筛选中展示出快速准确、高灵敏、样品用量少等优势。其中,QCM发展最早,其工艺及配套设备也较为成熟,SAW传感器对质量响应灵敏度相比QCM更高,FBAR谐振器和Lamb波传感器,具有很高的工作频率和灵敏度,且传感器体积极小,样品用量为1至几微升,未来极有可能发展为临床POC凝血测试装置。然而,要将声波传感器用于POC凝血测试中,还需要进一步提高灵敏度、稳定性和抗干扰能力等。
2 集成声波传感器的微流控芯片在凝血检测中的应用进展
微流控技术以样品和试剂消耗量低、反应速率快速等受到人们的广泛关注,微流控芯片因具有小型化、便携性及高效性等优势,在POCT的应用上展示出极大优势[74]。集成原位传感技术的微流控芯片已应用于凝血检测[75],这类微流控芯片上集成的检测模式包括荧光、电化学、微悬臂梁传感器、FBAR传感器等[76-78],也是未来微流控技术与传感检测技术融合研究的趋势和热点之一。Dos Santos等[79]设计了集成声表面波(SAW)混合功能的凝血检测小型装置,通过位于检测区域下方的SAW芯片可使血浆和激活剂迅速混合而发生凝血反应,采用图像相关分析法对血栓形成动力学进行了量化。Ohashin等[80]设计了集成声波技术的微流控电化学阻抗芯片,通过其底层的8YX-LiNbO3声波芯片调控传感层温度,使其与人体温度尽量保持一致。在早期用于凝血检测的集成声波技术的微流控芯片中,声波主要实现混合和控温等功能。Chen等[14]研制了集成FBAR传感器的微流控芯片用于凝血检测,通过设计微流控芯片的微通道,控制血液样本与传感器表面的有效接触和液体深度,从而提高凝血检测的灵敏度和准确性。虽然集成声波传感技术的微流控芯片在凝血检测中的研究还不足,但在分子构象研究、癌症标志物和细胞的检测中已显示出良好的应用前景[81-83]。
可以看到,集成声波传感器的微流控芯片的研究重点将主要聚焦于微流控芯片结构与功能设计,以保证凝血测试条件的一致性和稳定性,提高凝血测试的稳定性和重现性[79,84];针对POCT的应用需求,研发一体化微流控芯片,将血细胞分离、孵育、混合和衍生等多种功能集成到微流控芯片中,以期提高检测效率;同时,研发集成声波传感器的仿生芯片,模拟体内外凝血过程以及血管尺寸及表面性质、血液流动条件等因素对凝血过程的综合影响[85-86],以进一步提高凝血检测的准确性和可靠性,深化凝血过程的研究。
3 总结与展望
声波传感器具有灵敏度高、快速准确、种类多、传感器体积小、测试所需样品量少,易于集成和批量生产等特点,在凝血检测中展示出极大的优势。尽管当前用于凝血测试的声波传感器发展还面临诸多挑战,但因其可适应人们对健康管理的需求,适合于门诊和自检的POC凝血测试应用需求,有望发展为适用于临床诊断和研究的POC凝血专门系统和设备。目前,开发新原理、新结构和新材料是实现新型声波传感器的研发主流,相关传感器及装备的发展呈现出微型化、智能化和仿生化的趋势。
