索拉非尼/超支化聚(酰胺-胺)载药体系的构建及其体外药物释放动力学研究
2022-09-20何桂金李顺戚轶昕
何桂金,李顺,戚轶昕
(浙江大学 化学系,浙江杭州 310058)
面对某些恶性肿瘤的临床治疗效果不理想的问题,通过筛选新型药物组合方案、采用有针对性的纳米药物载体等手段,可以为恶性肿瘤治疗提供新策略,提升临床疗效[1]。索拉非尼是一种分子靶向药物,可用于肝细胞癌等多种恶性肿瘤的治疗,主要通过诱导肿瘤细胞铁死亡来抑制肿瘤生长[2]。肿瘤单药靶向治疗的效果可通过构建适当的纳米药物载体来增加药物在生物体内的稳定性与有效循环时间,提高内部的药物投递效率,从而有效增强药物的治疗效果。
超支化聚酰胺-胺(PAMAM)是一类分子内部富含酰胺键和胺键、端基为胺基的超支化聚合物,结构如图1所示[3]。特殊的结构赋予了其优良的水溶性与生物相容性,独特的单分子胶束也可以起到药物增溶的效果[4]。因此,PAMAM是理想的药物载体,通过适当的改进,可以有效增进所搭载药物的治疗效果;基于PAMAM的药物载体可以促进药物靶向投递,增强肿瘤区域药物浓度,增强治疗效果,减轻药物副作用[5]。
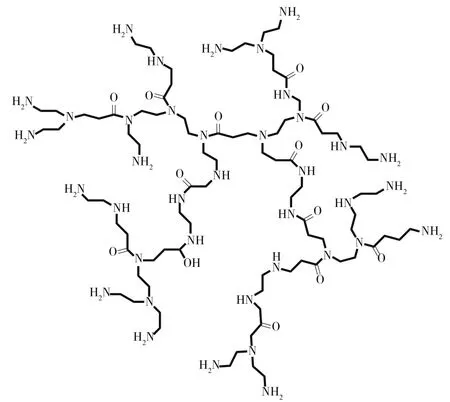
图1 超支化聚合物PAMAM的结构示意图
药物释放效果是载药体系的重要考评指标之一,高效液相色谱法(HPLC)利用高压泵对流动相施加高压,可有效提高物质的分离与分析的效率,具有应用范围广、灵敏度高等优点,在高沸点、大分子、强极性、热稳定性差化合物的分离分析方面具有独特的优势[6]。因此,HPLC配合在线检测的方式,可快速获取靶向载药体系的载药量与体外释放过程的相关参数,对靶向载药体系的深入研究有积极意义。
1 材料与方法
1.1 仪器与试剂
AVANCE Ⅲ 400型核磁共振波谱仪,德国Bruker公司;Nicholet iS10傅里叶变换红外光谱仪,美国Thermo Fisher公司;PL-GPC-50凝胶渗透色谱仪,美国Waters公司;Nano ZS纳米粒度电位分析仪,美国Malvern公司;LC 1100高效液相色谱仪,美国Agilent公司;Luna 5u C8(2)100A(250 mm×4.6 mm, 5 μm),美国Phenomenex公司。
乙二胺、甲醇、丙烯酸甲酯、乙醚、三氯甲烷,分析纯,国药集团化学试剂有限公司;索拉非尼(SRF),98.0%,上海麦克林生化科技有限公司;用于高效液相色谱的甲醇、三氟乙酸、十二烷基硫酸钠,色谱纯,Sigma-Aldrich试剂有限公司;磷酸缓冲溶液(PBS)7.4,阿拉丁试剂(上海)有限公司;透析袋,截留分子量3 000 Da,杭州辰通生化科技有限公司。
1.2 PAMAM的合成
乙二胺溶于甲醇后转移至三口烧瓶中,搅拌条件下滴加丙烯酸甲酯(控制乙二胺与丙烯酸的摩尔比分别为1∶3、1∶2和1∶1,所得产物分别命名为PAMAM-1、PAMAM-2、PAMAM-3),室温下搅拌48 h后停止反应,在减压条件下分别于60 ℃、80 ℃蒸馏1 h;100 ℃、120 ℃蒸馏1.5 h;140 ℃蒸馏3 h。缩合反应最后得到黏稠的黄色液体,颜色随着相对分子质量的提高由橘黄色变成黄绿色。
黏稠的黄色液体粗产物趁热用50 mL甲醇稀释,冷却至室温后倾入300 mL乙醚中搅拌0.5 h,静置分层后分去上层乙醚,再分别用100 mL乙醚洗涤两遍,将黄色产物转移至适合容器中,于40 ℃下真空干燥6 h得到黄色透明黏稠液体。
1.3 载药体系SRF@PAMAM的构建
PAMAM与SRF分别配制成水溶液和三氯甲烷溶液,混合后高速磁力搅拌1 h,旋蒸除去三氯甲烷;水相部分经抽滤除去不溶物后,转移至透析袋中充分透析3天以除去游离的SRF及杂质。充分冻干后即可获得SRF@PAMAM的体系。
1.4 HPLC条件
流动相为甲醇-水(含0.05%三氟乙酸和0.14%十二烷基硫酸钠),体积比为75∶25;流速1.0 mL/min;检测波长252 nm;柱温25 ℃;进样量10 μL。
1.5 SRF标准曲线的建立
取SRF溶于甲醇中,进一步稀释为0.625 μg/mL、1.250 μg/mL、2.500 μg/mL、5.000 μg/mL 和10.000 μg/mL的系列标准溶液。在1.4条件下,SRF保留时间为8.84 min。测定上述系列标准溶液对应的峰面积,以浓度为横坐标,峰面积为纵坐标拟合标准曲线。
1.6 SRF@PAMAM包封率的计算
以PAMAM-3作为包封SRF的模板。准确称取SRF,溶于三氯甲烷,另取PAMAM-3溶于超纯水。充分搅拌混合,待分层后取三氯甲烷层10 μL用甲醇按需要倍数稀释,进行HPLC分析,根据稀释倍数推算搭载后三氯甲烷相中的SRF含量C1(mg/mL),从而获得未包埋的SRF含量,包封率计算公式如(1)所示:

其中,Rload为包封率;m0为准确称取的SRF质量,mg;C1为搭载后三氯甲烷相中的SRF含量,mg/mL;V0为三氯甲烷的体积,mL。
1.7 药物释放曲线
将SRF@PAMAM-3加入到5 mL含40%乙醇的PBS中并转移到透析袋中,在50 mL含40%乙醇的PBS中透析,在不同时间点取样5 mL,同时补上5 mL含40%乙醇的PBS。检测样品中SRF的浓度,作SRF释放曲线。药物释放率计算公式如(2)所示:

其中,Rrelease为释放率;C’SRF为释放出来SRF的浓度,mg/mL;mSRF为载药体系中SRF的质量,mg。
2 结果与分析
2.1 PAMAM的结构表征
PAMAM的核磁共振氢谱如图2所示,各类氢的特征峰归属如下:δ=1.5~ 2.5,CO-CH2;δ=2.5~ 3.0,COCH2CH2NH、NH(CH2)2NH、NH(CH2)2;δ=3.2 ~ 3.5,NCH2;δ=3.5~ 4.0,CH3O。
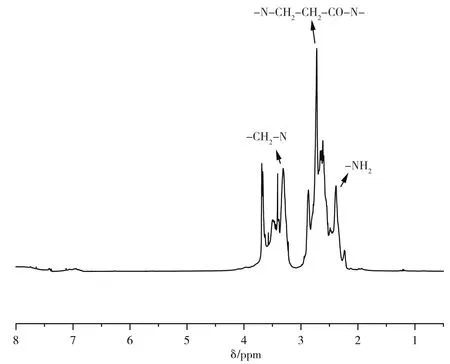
图2 PAMAM的核磁共振氢谱
图3为PAMAM的红外谱图。其中,伯胺N-H的反对称伸缩振动出现在3 388 cm-1处,而其对称伸缩振动出现在3 266 cm-1处;仲酰胺基的N-H的弯曲振动峰出现在3 099 cm-1,2 941 cm-1与2 843 cm-1处为饱和碳氢的伸缩振动峰,1 725 cm-1处是典型的酯羰基C=O的特征峰,而1 555 cm-1处可归属为C-N的伸缩振动峰。
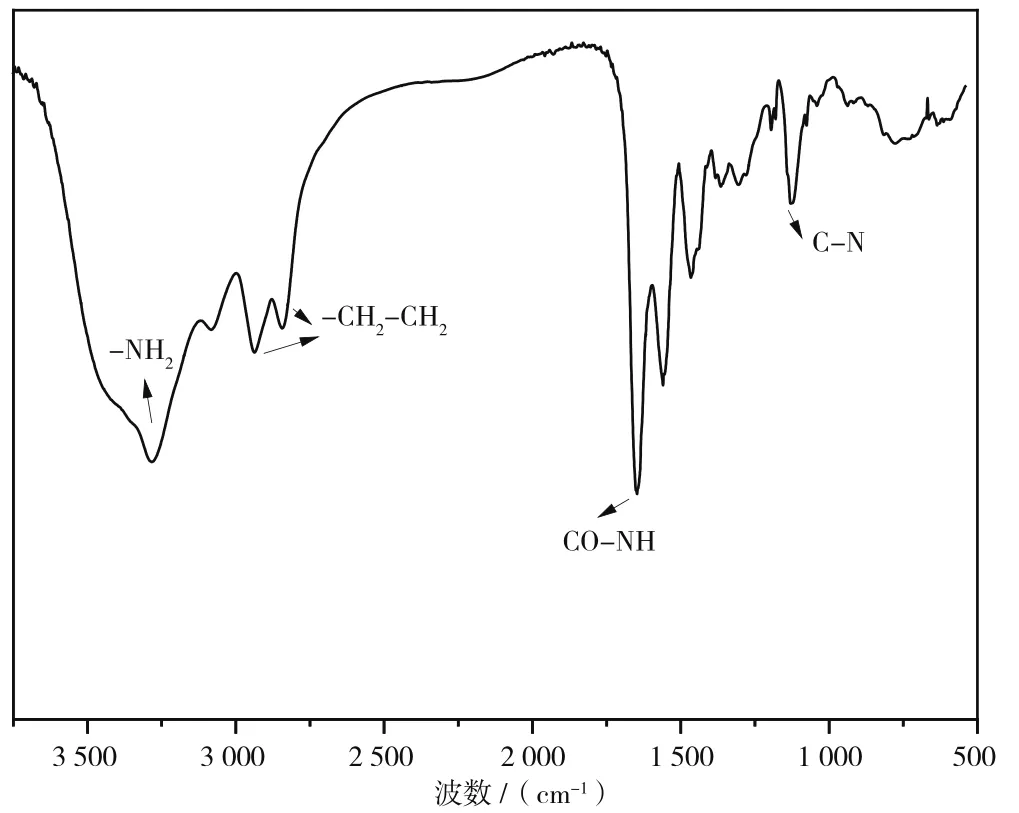
图3 PAMAM的红外谱图
2.2 投料比对PAMAM的影响
表1的数据表明,投料比可用来控制合成的PAMAM的相对分子质量,随着丙烯酸投料量的减少,所得聚合物的相对分子质量从5 300增加到26 800。此外,在乙二胺和丙烯酸甲酯的Michael加成反应中,一个乙二胺分子只与一个丙烯酸甲酯分子配对反应,因此1∶1的比例更有利于原料利用的最大化,有利于提高聚合物的相对分子质量。通过DLS技术测出的PAMAM平均粒径的大小与其相对分子质量密切相关,其最大平均粒径可达11.25 nm。
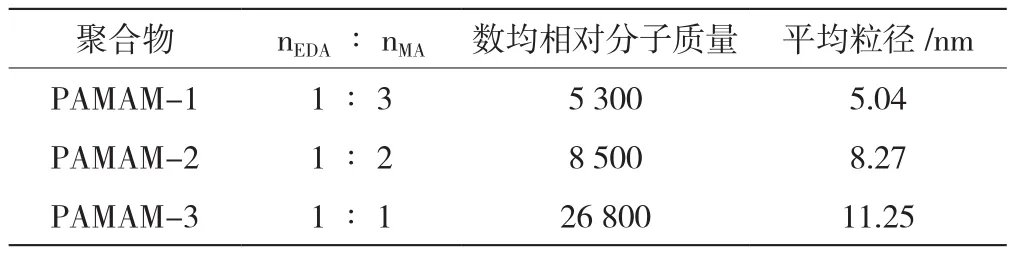
表1 PAMAM的相对分子质量及相关物理性质参数
2.3 标准曲线及PAMAM-3对SRF包封率
整理峰面积(A)与浓度(C)数据,经过线性拟合得到索拉非尼标准曲线,见图4。标准方程为A=40.065C-8.484,R2=0.999 7。线性范围 2.052~104.370 μg/mL。经过计算,PAMAM-3对SRF的包封率达42.3%。

图4 索拉非尼的标准曲线
2.4 药物释放曲线
SRF@PAMAM-3的药物释放动力学曲线如图5所示。可以发现,SRF@PAMAM-3在40%乙醇的磷酸缓冲液中的释放过程表现出先快后慢的趋势:在0~12 h内,其释放率上升较快;随着释放时间的进一步增加,释放率逐步趋于稳定。其释放率与时间的关系可通过公式(3)来表示:
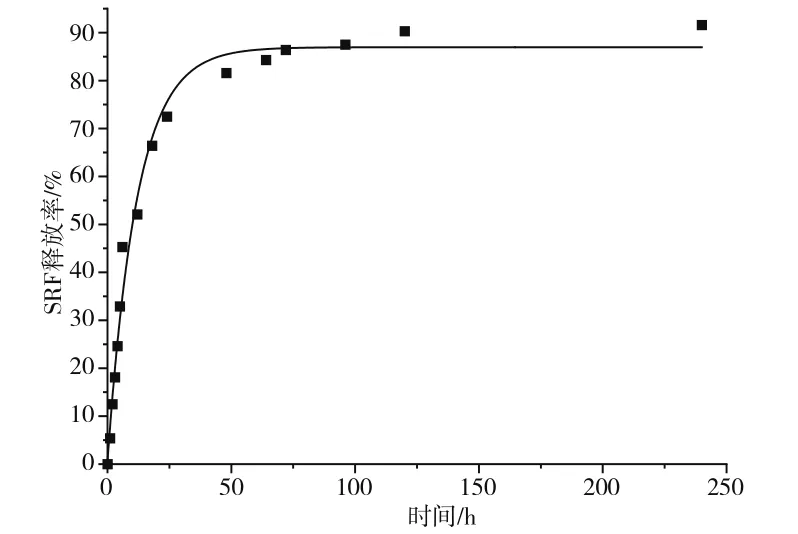
图5 SRF@PAMAM-3的药物释放过程及动力学拟合

其中,R为SRF@PAMAM-3体系不同时间内的释放率,t为释放的时间。
该动力学模型与药物释放动力学研究中提出的Gompertz曲线相一致[6]。该模型描述的药物释放曲线在一开始急剧增加,然后缓慢收敛至最大药物释放量,即药物总量。从测试得到的释放曲线可看出,一开始药物的释放较为迅速,可快速起效形成有效浓度;随后通过扩散控制缓慢释放到溶液中,直至最大溶出度。
3 结论
本文开发了SRF@PAMAM的载药新体系,利用HPLC法研究了抗癌药物索拉非尼在PAMAM载药体系中的体外释放过程,可准确、高效地获得其动力学参数,对未来进一步开发新的靶向药物缓释体系有一定参考价值。
