不对称催化胺化法制备CGRP 受体拮抗剂瑞美吉泮含氟手性片段的合成技术初探
2022-09-05林韦康
林韦康
(宿迁市科莱博生物化学有限公司,江苏 宿迁 223800)
偏头痛是一种以严重头痛为特征的偶发性疾病,全球偏头痛患者超过10 亿人[1],被列为全球第六大致残原因[2],也是导致世界上50 岁以下人群因残疾而失去工作的主要原因之一[3]。偏头痛虽然是全球第三大常见疾病,但人们对其发病机制的研究却少之又少[4]。目前该病症的治疗方案通常分为两种:预防性治疗和急性治疗。预防性治疗通过用药降低发作频次或疼痛程度,如瑞玛奈珠单抗(Fremanezumab)作为一种选择性靶向降钙素基因相关肽(CGRP)的人源化单克隆抗体,已被批准用于成人偏头痛的预防性治疗[5];急性治疗通过用药缓解发作时疼痛症状造成的不适,如CGRP 拮抗剂在偏头痛急性治疗中已显示出巨大的应用前景[6]。偏头痛是一种反复发作的单侧头痛为特征的严重疼痛状态[7],发作时病人痛不欲生,目前市场上既能用作预防又能用作急性治疗该疾病的药物仅有瑞美吉泮[8]。
有研究表明,偏头痛过程中CGRP 含量会显著提高,故CGRP 是偏头痛的生物标志物及促进因子[9-12],要想治疗偏头痛,要么阻止CGRP 的合成和释放,要么降低CGRP 释放后的浓度,要么阻止释放出的CGRP 激活其受体[13]。而瑞美吉泮作为一种选择性的、竞争性的口服CGRP 拮抗剂,能够迅速发挥、有效阻止CGRP 的受体被激活,进而起到缓解偏头痛的效用[14]。
瑞美吉泮(Rimegepant),也称BMS-927711,其显著特点是耐受性与安慰剂相当[15],剂型服用方便,不良反应少[16],不会引起血管收缩,安全性和耐受性较好[17],可用于孕妇治疗[18],其分子结构见图1。

图1 瑞美吉泮分子结构式
由图1 可知,瑞美吉泮分子结构中含有一含氟手性片段(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇,分子结构见图2。
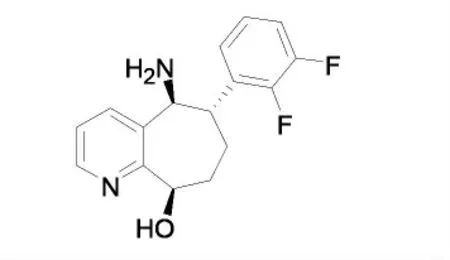
图2 瑞美吉泮的含氟手性片段分子结构式
图2 所示的化合物,共含有3 个手性中心,化学合成难度较大,Ma 等[19]报道可以用转氨酶为生物催化剂将(6S,9R)-6-(2,3-二氟苯基)-9-羟基-6,7,8,9-四氢-5H-环庚烷[b]吡啶-5-酮转化为该化合物,但是底物可接受性较差,转氨酶在合成空间位阻较大的手性胺时难以工业化,不适合工业化规模生产,转氨酶催化示意图见图3。

图3 瑞美吉泮含氟手性片段的转氨酶制法示意图[19]
本研究在Ma 等[19]的研究基础上,参考Malhari 等[20]的研究成果,采用不对称还原胺化方法替代生物酶催化,该方法以(6S,9R)-6-(2,3-二氟苯基)-9-羟基-6,7,8,9-四氢-5H-环庚烷[b]吡啶-5-酮为起始原料,工业氢气为还原剂,在AlⅢ/EDTA 络合催化剂的作用下,与简单氨源直接反应生成目标化合物。
1 实验方法
1.1 试剂与原料
(6S,9R)-6-(2,3-二氟苯基)-9-羟基-6,7,8,9-四氢-5H-环庚烷[b]吡啶-5-酮(工业级,99.5%,中锎米克化学过程(江苏)有限公司);AlⅢ/EDTA络合催化剂(工业级,中锎米克化学过程(江苏)有限公司);左旋樟脑磺酸铵(工业级,99.5%,浙江云涛生物技术股份有限公司);氨水(工业级,20%,聊城市华通化工产品有限公司)。
1.2 仪器与设备
气相色谱仪(9790,浙江福立分析仪器股份有限公司);液相色谱仪(1200,安捷伦科技(中国)有限公司);电子分析天平(XS205,梅特勒-托利多科技(中国)有限公司);微量水分测量仪(WS-3000,山东淄博正工仪器有限公司);集热式恒温磁力搅拌器(DF-101S,常州润华电器有限公司);旋转蒸发仪(YRE,巩义市予华仪器有限责任公司);真空干燥箱(KZ-50G,广州市康恒仪器有限公司);无油隔膜真空泵(XZ-1,郑州耀勒仪器科技有限公司);低温冷却液循环泵(DLSB-5L/25,巩义市予华仪器有限责任公司)等。
1.3 反应原理
(1)不对称还原胺化制备(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3)
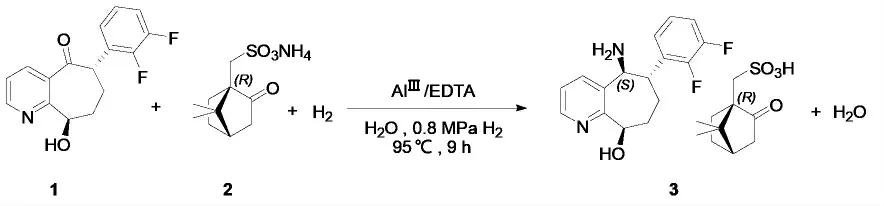
(2)(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3)的氨解

1.4 实验过程
先将水(350.00 g,19.42 mol)加入1 L 哈氏合金高压釜中,随后投入左旋樟脑磺酸铵(2,80.00 g,0.32 mol)并搅拌至溶清,最后一次性投入(6S,9R)-6-(2,3-二氟苯基)-9-羟基-6,7,8,9-四氢-5H-环庚烷[b]吡啶-5-酮(1,80.00 g,0.28 mol)和AlⅢ/EDTA 络合催化剂(4.00 g)。投料毕,此时反应体系呈悬浊状,升温至95 ℃~98 ℃,缓慢向高压釜中通入0.8 MPa 工业氢气并保温保压约9.5 h。保温保压完毕,反应体系呈浅黄色澄清液体,降温至10 ℃以下并继续搅拌养晶1 h。养晶毕,抽滤,滤饼为(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3,湿品重137.55 g),呈白色晶状固体,滤液中含有AlⅢ/EDTA 络合催化剂,不经任何处理,直接或浓缩后用于下一批不对称还原胺化。
将前述所得滤饼湿品(3)一次性投入已加水300.00 g(16.65 mol)的1 L 搪玻璃反应釜中,升温至溶清,溶清时反应体系约90 ℃,用20%氨水21.55 g(0.25 mol)调节反应体系pH=8,搅拌降温至25 ℃以下,抽滤,滤液为左旋樟脑磺酸铵(5)的水溶液,浓缩到一定体积后用于下一批不对称还原胺化;滤饼呈白色片状固体,为目标产物(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇(4),烘干后重65.25 g,摩尔收率为81.27%(以1 计),光学纯度为99.61%。
2 结果与讨论
2.1 催化剂的选取
由于催化剂的适用范围小,用普通氨源(氨气或铵盐)对酮进行不对称催化还原胺化直接制备相应手性伯胺一直是此类反应的研究热点。本研究使用手性有机酸氨源,胺化物可在反应体系中与手性酸形成复盐,故并不需要选用诸如二茂铁双膦配体、手性铱络合物、手性钌等昂贵、复杂、回收难度大的催化剂,只要选取一个能有效将酮羰基有效转化为氨基的催化剂即可。因AlⅢ/EDTA 络合催化剂具有价廉易得、可在水相中进行反应、可回收使用等优点,故适用于本文所述反应。
2.2 溶剂水量的选取
溶剂水量过多不利于后期析晶而影响收率,水量过少搅拌不均匀且反应后期也得不到均相反应液,故水量选择为起始原料底物酮重量的4.3 倍较为合适。当将(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3)或目标产物(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇(4)的滤液作为溶剂水进行循环利用时,也是通过前述建议水量来控制滤液的浓缩程度。
2.3 氢气压力选取
氢气压力过低不利于反应进行,氢气压力过 高会产生如图4 所示杂质。

图4 氢气压力过高可能产生的杂质
控制其他工艺参数不变,仅改变氢气压力,考察反应情况,结果见表1。

表1 不同氢气压力条件下的反应结果
根据表1 的结果可以看出,随着氢气压力的增高,目标产物收率不断提高,且在氢气压力为0.8 MPa 达到峰值;当氢气压力达到0.6 MPa 时开始有杂质1 产生;当氢气压力达到0.9 MPa 时,除了杂质1 以外还出现了杂质2 和杂质3;杂质1、杂质2 和杂质3 的含量与氢气压力正相关。当氢气压力高于0.9 MPa 时,氢气压力越高,杂质1、杂质2 和杂质3 的含量越高。考虑到杂质1 有水溶性,可以方便地与目标产物(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇(4)分离,故氢气压力选取为0.8 MPa 为宜。
2.4 滤液回收利用对目标产物收率的影响
在 (6S,9R)-6-(2,3-二氟苯基)-9-羟基-6,7,8,9-四氢-5H-环庚烷[b]吡啶-5-酮(1)的不对称还原胺化过程进行HPLC 中控发现,起始原料(1)已基本转化完全,但最终根据所得目标产物(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇(4)的干品重量计算,并达不到理论摩尔收率。为此,分别对(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3)滤液和目标产物(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇(4)的滤液进行浓缩,发现目标产物摩尔收率达不到理论量的原因是(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3)在水中有一定的溶解度。因此,当将(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3)滤液作为溶剂水用于下一批不对称还原胺化时,目标产物收率显著提高,达到93.00%以上。
3 结论
以左旋樟脑磺酸铵(2)为普通氨源,0.8 MPa氢气为还原剂,(6S,9R)-6-(2,3-二氟苯基)-9-羟基-6,7,8,9-四氢-5H-环庚烷[b]吡啶-5-酮(1)于95 ℃的水相中在AlⅢ/EDTA 络合催化剂的作用下,可被不对称催化还原胺化得到(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇的左旋樟脑磺酸复盐(3),复盐(3)经20%氨水氨解即可得到目标产物(5S,6S,9R)-5-氨基-6-(2,3-二氟苯基)-6,7,8,9-四氢-5H-环庚[b]吡啶-9-醇(4)。
最佳反应条件:反应温度为95 ℃,反应压力为0.8 MPa,投料比例是n(底物酮):n(普通氨源)=1:1.14,催化剂添加量为底物酮重量的5%,溶剂水的用量为起始原料底物酮重量的4.3 倍。
AlⅢ/EDTA 络合催化剂和普通氨源左旋樟脑磺酸铵(2)均可循环利用,生产成本较低,反应过程不涉及有机溶剂,安全性和环保性较佳,适用于规模化工业化生产。
