基础化学原理与前沿研究领域的契合
——以功能纳米材料的合成为例
2022-09-03张东凤朱英
张东凤,朱英
北京航空航天大学化学学院,北京 100191
基础化学是许多高校针对理工科专业学生在大学一年级开设的一门基础课,教学目的不仅在于让学生了解化学的知识体系,学习化学的基础原理和基本方法,更为重要的是要实现“学以致用”的目标,通过掌握化学原理来解决相关领域一些实际问题的方法,培养学生的学科交叉能力,增强学生的创新能力。然而,对于大一的新生来讲,他们的知识积累还不够丰富,视野还不够开阔,对于化学基础原理与各学科之间的相互联系认识不足,不仅无法实现用基础知识解决实际问题的教学目标,还容易让学生失去对化学学科的学习热情。显然,在基础知识的教学过程中引入化学原理在相关学科前沿研究领域的应用案例不仅可以激发学生的学习兴趣,还是拓展学生视野、培养学生创新意识的有效方法。
21世纪是学科高度交叉融合的时代,新兴学科不断涌现。比如,纳米科技就是一门交叉性很强的综合学科,在医药、生物、信息、电子、能源及环境等诸多领域都有广泛的应用。纳米材料的性质与其表面结构、几何构造和成分分布密切相关,使得纳米材料的制备成为整个纳米科技应用的基础。实际上,纳米材料的制备在很大程度上都依赖于化学原理的应用。在教学过程中,有针对性地引入化学原理在功能纳米材料合成中的应用,并简单介绍功能纳米材料在相关前沿研究领域中的应用,不仅可以丰富教学内容,加深学生对于基础知识的理解,还可以建立联系基础化学与多学科交叉融合的纽带,切实培养学生运用基础知识解决实际问题的能力。近年来,如何在化学基础知识教学过程中有机引入科学前沿研究内容也是大家在教改过程中关注的一个问题[1-3]。笔者认为,在课堂教学中引入化学学科自身的前沿研究进展是必要的,但更重要的是能引入一些化学原理在交叉学科前沿研究领域应用的实例。基于笔者多年的教学科研经验,本文介绍几种基础化学原理在功能纳米材料制备中应用的典型实例。
1 沉淀溶解平衡与介孔氧化物的合成

显然,在平衡状态下,An+离子浓度的大小取决于Kθsp和Bm−的大小。换句话说,An+在溶液中的浓度大小可通过选择具有不同溶度积的难/微溶物作为前驱体,或改变溶液中Bm−浓度的大小得到调节。
对于纳米材料的合成来说,动力学调控是实现材料结构和形貌控制的重要手段。其中,目标产物组分离子的浓度显然是动力学调控过程中的一个重要因素。从沉淀溶解平衡可见以包含目标产物组分离子的沉淀为前体是实现离子缓释的重要方法,因而在纳米材料的可控制备方面发挥了重要的作用。下面,我们以过渡金属氧化物有序介孔材料的可控制备为例来进行说明。
过渡金属氧化物有序介孔材料由于在电池、传感、光电及催化等领域有着广泛的应用,成为了物理、化学、生物、医药、材料、信息等多学科领域的宠儿。软模板法是合成有序介孔材料的重要方法,其基本原理是一定浓度的表面活性剂在溶液中组装成长程有序结构而作为软模板,目标产物组分前驱体均匀吸附或沉淀在这种长程有序结构表面(有些情况下,长程有序结构的形成是在目标产物组分离子的协同作用下完成的),通过后续反应得到在软模板表面附着的目标产物或目标产物前体,然后通过高温煅烧除去软模板,最终得到具有有序介孔结构的目标产物(图1)[4]。
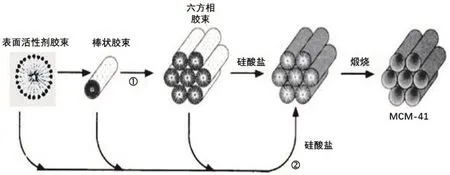
图1 软模板法合成SiO2有序介孔材料的液晶模板示意图[4]
当目标产物是氧化物介孔材料时,附着在液晶模板表面的一般是相应金属离子的水解产物,水解产物经过凝聚、脱水形成目标氧化物。从化学的角度来讲,金属离子水解-凝聚过程可以由以下方程式表示:

水解-凝聚得到的多羟基金属化合物Mx(OH)x+y(xn−x−y)+附着在液晶模板表面,在焙烧脱模过程中原位脱水生成氧化物。
金属离子的水解凝聚速度对于有序介孔结构的成功构建至关重要。若水解速度过快,则水解产物还来不及在液晶模板表面均匀沉积就已经自发聚集,模板起不到作用;若水解速度过慢,则水解产物在液晶模板表面的覆盖度低,不能有效融合形成完整的结构。由于金属阳离子的水解速率比较快,难以控制,人们不得不寻求非水溶液体系、活性更低的金属醇盐为前驱体等方法来实现过渡金属有序介孔材料的合成,这不仅提高了合成成本,也造成了环境污染。水溶液中过渡金属氧化物有序介孔材料的合成一直以来都是一个挑战。
通过分析方程(2)、(3)可以知道,决定金属离子水解凝聚速率的关键因素是自由金属离子浓度和溶液的pH。自由的金属阳离子水解速率很快,为了实现对水解速率的控制,在反应过程中对金属离子进行缓释,使其在溶液中保持一个相对低且恒定的浓度是一个有效策略。显然这可以通过沉淀溶解平衡原理可以实现。比如,我们利用沉淀溶解平衡原理成功制备了Cu2O有序介孔球[5,6]。
各项治理措施的实施,将有效地减缓降水下冲力,提高地表渗透性,经分析计算,项目实施后增加蓄水能力3.50万m3。
Cu2O一般通过Cu2+在碱性介质中的还原来合成,可以表示为以下反应方程式:

由于Cu+在水中的易歧化性和CuOH的不稳定性,Cu2O的生成速度很难被控制,即便是在表面活性剂能组装成液晶相的条件下也很难形成有序介孔结构。根据无机物沉淀溶解平衡原理,若使还原Cu2+得到的Cu+先生成其他难溶物,然后通过沉淀转化生成CuOH,则Cu2O的生成速度会得到极大控制。我们课题组应用该原理在Cu2O有序介孔纳米球制备方面获得了成功。
我们以抗坏血酸作为还原剂,聚吡咯烷醇(P123)为表面活性剂进行了实验。当以CuAc2或CuSO4作为铜源时,得到的是Cu2O无序多孔球状聚集体。若向溶液中添加一定量的Cl−离子,则可以成功获得Cu2O有序介孔纳米球。Cl-离子的用量是有序介孔结构能否形成的重要因素。当溶液中有Cl−存在时,还原生成的Cu+会与Cl−首先生成CuCl,生成的CuCl水解生成CuOH,CuOH分解得到Cu2O,如方程式(6)、(7)所示:

根据平衡移动原理,当Q = c(H+)c(Cl−) < KθEq(6)时,平衡向右移动;当时,平衡向左移动。显然,若H+和Cl−的离子积太小,则平衡向右移动太快,没办法控制Cu2O的生成速度,若H+和Cl−的离子积太大,则生成的CuCl又无法完成向CuOH的转变。设,实验表明,当ξ <<0.1时,得到的产物为Cu2O小颗粒球状聚集体,说明在该条件下,生成的Cu2O速度太快,来不及与P123胶束进行组装,为了降低体系能量,发生了球形聚集;当ξ ≈ 0.1时,产物为Cu2O有序介孔纳米球,说明在此条件下,生成Cu2O小颗粒的速度合适,与P123胶束有充分的相互作用时间,从而确保了有序介孔结构的形成;当ξ继续增大时,CuCl的水解速度进一步降低,溶液中会同时存在CuCl和Cu2O,ξ越大,CuCl的比例越大,CuCl在溶液中的溶解-重结晶甚至会诱导原位生成的Cu2O进行组装,在1 < ξ < 1.7的区间内,得到了以Cu2O有序介孔球为结构基元的规整多面体组装体。当ξ继续增大时,CuCl的水解非常缓慢,导致在相当长的时间内,得到的产物都以CuCl为主。
2 氧化还原反应与金属纳米材料的合成
根据电池反应热力学,对于两个半电池反应:

这是基础化学学习中需要掌握的一个重要原理。该原理在纳米材料尤其是贵金属及其合金纳米材料的可控合成方面有着广泛的应用。比如人们运用金属间置换反应合成了具有多面体、核壳结构、空心结构等多种构型的单组分或多组分金属纳米材料。其基本步骤为:向含有预先合成的A粒子的分散液中,加入一定量的Bn+离子(EAm+/A< EBn+/B),若Bn+与A的氧化还原反应在A粒子的表层均匀发生,且还原生成的B在A粒子表面原位沉积,则得到了以A为核B为壳的A@B核壳结构粒子;如果对基底纳米粒子进行一定的表面处理,使某些暴露面被保护,则金属间置换反应从边角或未被保护的暴露晶面处开始,还可以获得空心结构、凹面结构等多种特殊形貌材料。若A、B易于合金化,则B在沉积的过程中还可以与尚未反应的A形成AB合金。
美国华盛顿大学华裔科学家夏幼南课题组在这方面做出了开创性的工作[7]。他们向分散有Ag纳米立方体的溶液中,加入一定量的HAuCl4溶液,由于

研究表明,氧化还原首先从Ag立方体的某个边角部位开始,生成的Au则会在立方体表面均匀分布,且与Ag形成AuAg合金。随着反应的持续发生,内部的Ag基底不断地被消耗,形成AuAg空心结构材料。空心结构的厚度可以通过调节AuCl4−(aq)的加入量得到控制。若AuCl4−(aq)用量足够多时,AuCl4−(aq)会进一步与AuAg合金壳层中的Ag反应,发生脱合金化,从而生成多孔框架结构(具体机理如图2所示)。更为重要的是,结构的调变可以使Au的等离子共振峰在600-1200 nm范围内得到调节,这为Au在生物检测、药物传递、热疗等生物医学领域的应用提供了重要的物质基础。
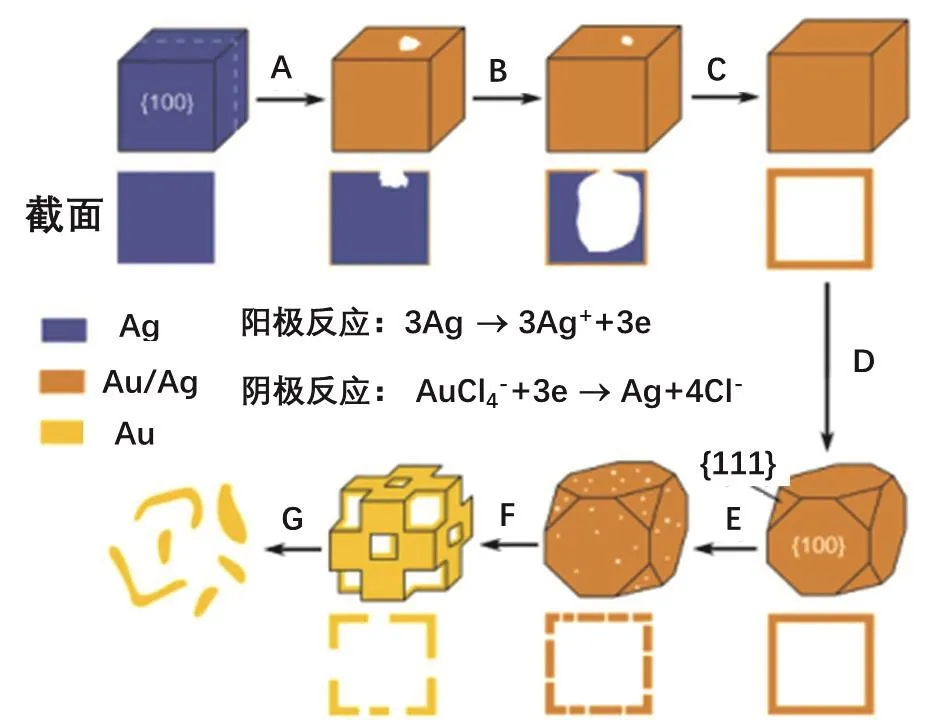
图2 Ag纳米立方体和AuCl4−发生氧化还原反应生成AuAg合金笼及至Au框架结构的过程示意图[7]
以Pt、Pd、Ru、Rh等为代表的贵金属材料催化性能优异,在工业应用中发挥着无可替代的作用。然而,昂贵的价格和较低的地壳丰度严重桎梏了它们的广泛使用。低贵金属含量催化剂的开发是能源、环境、化工等领域科学家普遍关心的问题。因为催化反应一般在催化剂表面发生,以过渡金属(M)为核,贵金属(NM)及其合金为壳的核壳结构材料显然可以有效降低贵金属的用量。另一方面,贵金属与过渡金属之间的协同作用还可以进一步优化活性组分的电子结构和几何构型。由于贵金属的氧化还原电势一般高于过渡金属的氧化还原电势,所以金属间置换反应也是贵金属基壳层结构制备过程中的一个重要原理。
3 配位解离平衡与特定形貌纳米材料的合成
在配位化学基础一章的学习过程中,我们知道过渡金属原子/离子(M)由于具有部分填充的d轨道,可以与具有孤对电子的配位体(L)形成配合物。为了陈述简便,我们以Pd2+与X−形成的配合物PdX42−为例。按照配位解离平衡原理,体系中存在以下平衡:

在一定温度下,达到平衡时,各离子浓度之间关系如下:

即溶液中Pd2+离子的浓度与的数值及的浓度成正比,而与X−浓度成反比。
从配位解离平衡中解离常数的表达式可以知道,配位解离平衡与沉淀溶解平衡相似,也是实现离子缓释的重要途径,因此也是调控纳米材料的成核-生长速度的常用手段。同时,从配位解离平衡中解离常数的表达式我们还可以知道,达到平衡时,离子的浓度还与配体的不稳定常数有关。比如,若向含有一定浓度Pd2+的溶液中,分别加入不同种类的卤素离子使它们的浓度相同,则由于不同卤素离子与Pd2+离子形成的配合物离子稳定性不同而导致溶液中自由Pd2+离子的浓度不同。当体系中发生涉及到Pd2+离子的化学反应时则会有不同的动力学反应速度。因此配位络离子的种类也是控制纳米粒子生长方式的重要因素。
影响配位单元稳定性的因素也是配位化学基础一章的重要知识点。当中心离子相同时,配体中配位原子的电负性越小,给电子能力越强,配位化合物越稳定。Br−的电负性小于Cl−的电负性,因此稳定。按照能斯特方程,

在含有相同浓度Pd2+离子的溶液中,分别加入过量的Br−和Cl−时,显然Br−体系中钯的氧化还原电势比Cl−体系中更低,遇到相同还原剂时,Pd2+在Br−体系中被还原的速度比Cl−体系中更慢。近期,美国华盛顿大学的夏幼南课题组利用这个原理,成功调节了Pd在Au纳米框架结构内外表面的沉积方式(图3)[8]。
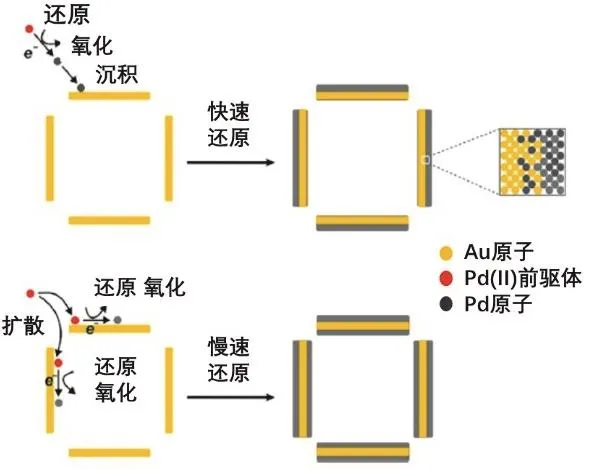
图3 以Au框架结构为基底,通过选用具有不同稳定性的 (X = Cl, Br)络离子来调节其氧化还原动力学从而得到不同Pd沉积方式的Pd@Au核壳结构和Pd@Au@Pd三明治结构的过程示意图[8]
他们首先将一定量具有超薄微孔壳层的Au纳米框架结构和抗坏血酸、聚吡咯烷酮混合均匀,当向其中加入一定量的时,得到的产物为在Au纳米框架结构外表面沉积有Pd壳层的Pd@Au核壳结构;当向其中加入的是等量的时,则Pd不仅在Au纳米框架结构的外表面沉积,而且在内表面也有沉积,形成了Pd@Au@Pd三明治结构。在该体系中,Au纳米框架结构为基底,抗坏血酸(AA)作为还原剂还原形成Pd。同时,由于Au基底具有超薄微孔壳层结构,Br)还有扩散进入Au纳米框架结构内部的倾向。扩散过程和被还原过程相互竞争。如前所述,的被还原速度比的快,因此在还没有来得及进入Au纳米框架结构内表面的时候就被还原生成Pd,因而得到在Au基底外表面沉积有Pd壳层的Pd@Au核壳结构。对于来说,其被还原速度大大降低,因此PdBr42−有足够的时间进入Au纳米框架结构内部,当其被还原后在Au基底的内外表面都有沉积,因此得到了Pd@Au@Pd三明治结构。
4 结语
基础化学是多个理工科专业的基础课,而纳米材料的应用是多个学科的前沿研究领域。本文中总结了几种重要的基础化学原理:沉淀溶解平衡、氧化还原反应、配位解离平衡在几种重要的功能纳米材料合成中应用的典型实例,并深入分析了化学基础知识点与纳米材料结构和形貌控制之间的内在联系。此类事例在《基础化学》课程教学中的引入有助于消除化学原理的“距离感”,让学生体会到化学不仅仅是一门课程,而且与兴趣专业研究前沿联系密切。这对于激发学生的学习兴趣,拓展学生视野,培养学生的学科交叉和科教融合能力,切实发挥基础化学的基础学科作用具有重要意义。
