不同温度对钚在北山地下水中溶解行为的影响
2022-09-01龙浩骑周舵王波姜涛包良进
龙浩骑,周舵,王波,姜涛,包良进
(中国原子能科学研究院,北京 102413)
高放废物是一种放射性强、毒性大、含有的核素半衰期长并且发热的特殊废物,对其进行安全处置难度极大,面临一系列科学、技术、工程、人文和社会学的挑战。目前公认最可行的高放废物处置方案是深地质处置,其核心内容是放射性核素的包容、阻滞和迁移。一般认为高放废物中放射性核素进入环境中的主要途径为:处置库一旦受到人为破坏或地质运动,使地下水渗入废物库中,包装容器被腐蚀,废物固化体受到地下水的作用,开始降解并释放出放射性核素,进入地下水的核素由此迁移进入环境[1]。因此,研究高放废物中关键核素在处置条件下的化学/物理行为,掌握关键核素在地下水中的迁移规律对于安全处置高放废物非常重要。溶解度是高放废物固化体中浸出核素在地下水中迁移的浓度上限和源项,是高放废物地质处置安全和环境评价中的关键参数,一直受到国内、外学者的高度重视。
239Pu 因半衰期长(t1/2=2.41×104a),毒性大,形态复杂,是高放废物深地质处置研究中的关键核素,其常温下的溶解度数据国内外学者已多有报道[2-18],但关于温度对钚溶解行为影响的研究却不多[2,9-10]。考虑到放射性核素的释热会导致处置库中心温度达到较高水平[2,19-20],且多数物质溶解度是温度的函数,测定核素溶解度时应探究温度对其影响。目前我国已将甘肃北山地区确定为高放废物地质处置重点预选场址,针对北山预选场址安全评价的相关研究工作已经开展。因此,本工作拟通过测定不同温度下钚在北山地下水中的溶解度,探究温度对钚溶解行为的影响规律,以期为我国高放废物深地质处置库的安全分析和环境评价提供可靠数据。
2 实验部分
2.1 试剂与仪器
同位素指示剂239Pu(239Pu>99.9%),中国同辐股份有限公司;闪烁液,Optiphase Hisafe 3(PE life and analytical science. U.S.A);NaOH、HClO4、HNO3和NaClO4,国 药 集 团 化 药 试 剂 公司;TTA、HEDHP、PMBP、二甲苯和甲苯,阿法埃莎(中国)化学有限公司。
QUANTULUS 1220 型超低本底液闪谱仪,美国P.E 公司,239Pu 检测下限3×10-13mol·L-1;低氧工作箱(氧浓度小于5×10-6,二氧化碳浓度为300×10-6),上海米开罗那有限公司;2000D 型超纯水机,北京长风仪器仪表公司;LM-123 型超滤装置,北京旭邦膜设备有限责任公司;TDL-80-2B 型低速离心机,上海安亭科学仪器厂;干式恒温器,杭州奥盛公司,温度范围介于30~90℃之间,控制精度±1 ℃;HI8424 型pH 计,配 置HI2930pH 电 极 和HI3131Eh 电极,意大利HANNA 公司;超滤离心管,截留分子量10 000 道尔顿;针头式过滤器,0.45 μm,美国Millipore公司;Zeta电位激光粒度分析仪,美国贝克曼公司,测量范围0.6 nm~7 μm。
2.2 实验方法
本实验按照国际上对胶体和溶解度的定义,将溶液中溶解的微粒定义为两部分,一部分是指含有能通过450 nm 过滤膜而被截流分子量为10 000 道尔顿滤膜所阻挡的微粒,将其定义为胶体;另一部分是指能通过截流分子量为10 000 道尔顿的滤膜的微粒,将其定义为真溶液,在一定温度和条件下,真溶液中溶质的浓度称为溶解度。
2.2.1 北山地下水的预处理
将北山地下水(北山04)经过0.45 μm 滤膜过滤后,备用。水样送清华大学环境质量检测中心分析其主要组分;另用Zeta 电位激光粒度分析仪对经预处理的北山地下水进行胶体分析。
2.2.2 实验方法
在氩气氛围的低氧工作箱中([O2]≤5×10-6),取预处理后的北山地下水50 mL 于聚乙烯试管中,并在溶液中加入2.0 mL 制备好的浓度为1×10-3mol·L-1的Pu(NO3)4储 备 液,用NaOH或HClO4调节溶液中的pH 值。将试管置于金属域恒温控制器上,保持温度为(30±1)、(45±1)和(60±1)℃。定时取2.0 mL 样品,分别用孔径为0.45 μm 的针头式过滤器和截留分子量为10 000 道尔顿(10 kDa)的超滤离心管进行溶液中钚的固-液相分离,取1.0 mL 滤液用超低本底液闪谱仪测量其放射性活度,直至体系中固-液两相钚的放射性活度达到稳定,用TTA-二甲苯、HEDHP-甲苯、PMBP-二甲苯分析溶液中钚的价态分布情况,并测量试管中剩余水相的pH 和Eh 值。
3 结果与讨论
3.1 北山地下水的组成和胶体分析
3.1.1 北山地下水的成分分析
清华大学环境质量检测中心对北山地下水(北山04)分析结果见表1。与国外处置场预选区的地下水相比[9],北山地下水中离子强度大(离子强度约0.1 M,美国J-13 地下水离子强度约为4 mM),尤其是氯离子浓度高达12.5 mmol·L-1。考虑到氯离子对不锈钢的腐蚀,我国在处置容器材料选择时,应当重点考虑对氯离子的防护。此外,离子强度对于热力学数据也有较大影响,在安全评价时也应考虑对数据的校正。
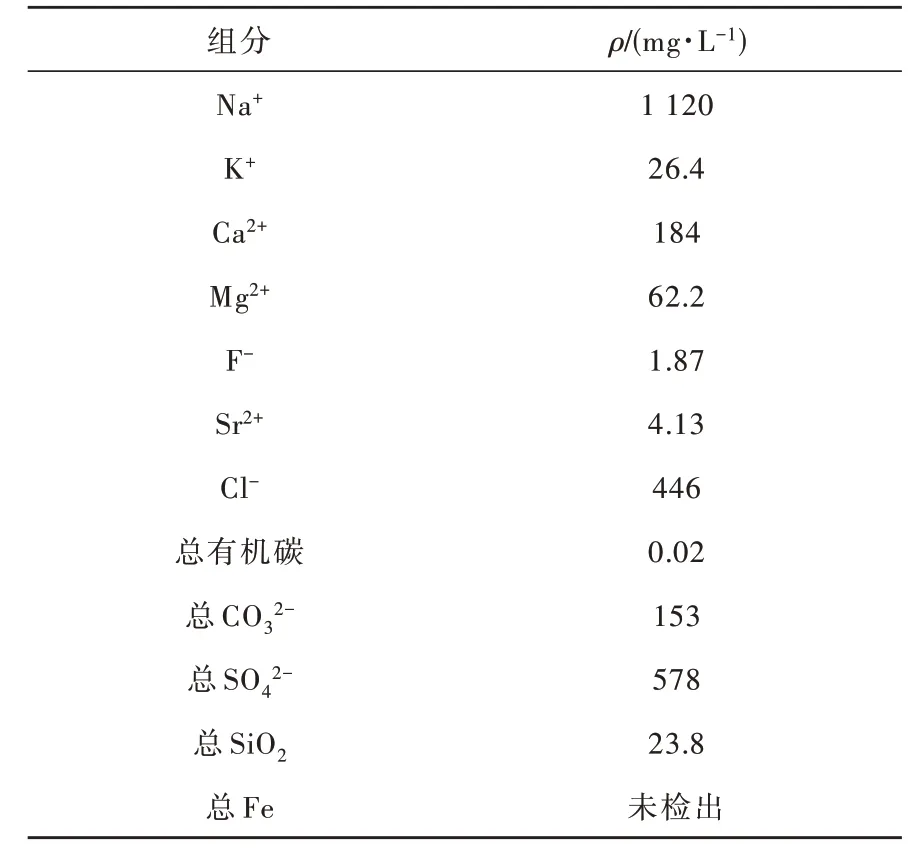
表1 北山04 井地下水的主要成分Table1 groundwater composition in Well-04,Beishan
3.1.1 北山地下水的胶体分析
胶体的存在对核素溶解行为有较大影响,微小的胶体颗粒能够吸附核素导致其溶解和迁移行为发生变化。地下水中存在的胶体通常分为无机胶体和有机胶体,无机胶体主要包括黏土矿物胶体和水合氧化物胶体,而有机胶体主要是腐殖质胶体。用Zeta 电位激光粒度分析仪测量地下水中的胶体粒径和Zeta 电位,结果见表2。

表2 北山地下水中的胶体粒径分布和Zeta 电位Table 2 Colloid partical size distribution and Zeta potential in Beishan groundwater
本次实验所采用的是北山深层地下水(深度超过500 m),水体中总有机碳的含量比较低(约为0.02 mg·L-1),因此地下水中的胶体多为无机胶体,其产生的原因可能是花岗岩表面被风化后形成了胶体粒径范围内的颗粒,随后矿物颗粒被裂隙中的水流转化为胶体。从胶体粒径分布来看,北山地下水中的胶体粒径分布介于250~450 nm 之间,使用10 KDa(粒径约为4 nm)的超滤膜进行固-液分离可以完全消除胶体对钚溶解度测定的影响。Zeta 电位的分析结果可以看出北山地下水中的胶体不太稳定(一般Zeta 电位的绝对值大于40 认为胶体稳定),易于凝聚沉淀,这对于阻滞钚的迁移是有利的。
3.2 溶液中钚的价态分布
当钚在溶液中的浓度达到溶解-沉淀平衡后,采用TTA-二甲苯、HEDHP-甲苯、PMBP-二甲苯溶剂萃取法对样品溶液中钚的价态分布进行了分析,萃取流程详见表3,具体实验结果详见表4。

表3 不同价态钚的萃取方法Table 3 Extraction method used for Pu oxidation of different valance in this work
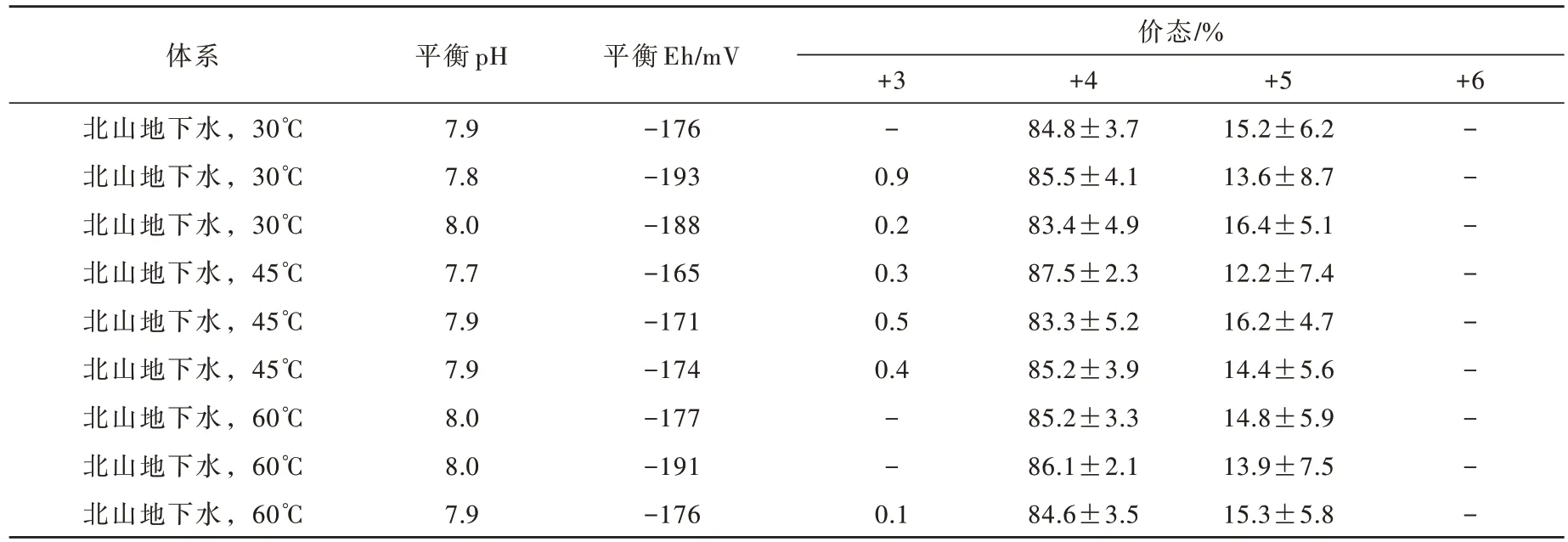
表4 平衡后钚在溶液中的价态分布Table 4 Valence of plutonium in solution after dissolution-precipitation balance
由表4可见,在体系达到溶解-沉淀平衡后,钚的主要存在价态是+4 价,有少量的+5 价,而+3 价和+6价则基本不存在,体系不同温度变化对钚的存在价态影响不大。根据理论计算(图1,使用phreeplot绘制)表明,还原条件下钚在溶液中的存在价态为+4价,这与实验结果有一定的差别。这表明在实际环境中,钚在溶液中的存在价态比理论计算复杂得多。Neck[7]在对已发表的Pu(OH)4(am)溶解度数据进行评估时认为,钚的歧化和Pu4+的氧化导致溶液中钚存在可疑的氧化-还原状态,从而造成各溶解度数据巨大的差异性。由于+5价钚的溶解度要比+4价钚的溶解度更高,因此,从保守的角度出发,以高价态钚的溶解度作为核素迁移初始源项数据应引起安全评价的重视。
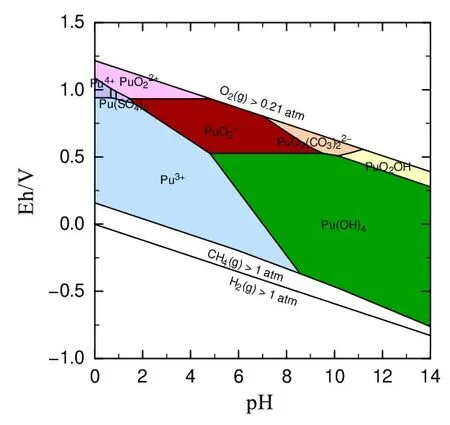
图1 钚的价态随pH-Eh 变化图Fig.1 Valence change of plutonium with pH-Eh
3.3 钚在北山地下水溶解行为的研究
实验进行了600 d,最终钚在溶液中达到溶解-沉淀平衡,试管底部均出现绿色絮状沉淀,体系温度高的沉淀产物颜色略深,实验结果见图2。
由图2 可见,在反应初始,溶液中钚的浓度下降很快,60 d 后钚浓度开始缓慢下降,大约在360 d 时浓度趋于稳定。体系达到平衡后,(30±1)、(45±1)和(60±1)℃条件下,钚在北山地下水体系中的溶解度分别为(3.06±0.97)×10-8、(3.16±1.27)×10-10和(1.34±0.67)×10-10mol·L-1。从分级过滤的结果来看(表5),溶液中大部分的钚都能通过截流分子量为10 kDa 的超滤膜,这表明在北山地下水中,钚主要以离子形态存在,只有极少量的钚是以胶体形态或者是吸附在地下水中的胶体上,考虑到钚离子比钚胶体更容易与膨润土、岩石发生吸附作用,该结果对于阻滞钚的迁移是有利的。

表5 不同粒径过滤后地下水中钚的浓度Table 5 Concentration of plutonium in groundwater after filtration of different sizes
由图2 还可见,当体系温度升高,钚的溶解度进一步降低,这与美国在研究温度对钚在J-13 地下水中的溶解度的影响结果一致[9-10]。为了进一步分析该现象产生的原因,将达到溶解-沉淀平衡后的实验样品继续进行以下实验(图3)。

图2 不同温度下钚在北山地下水中的溶解度Fig.2 Solubility of Pu in Beishan groundwater at different temperatures
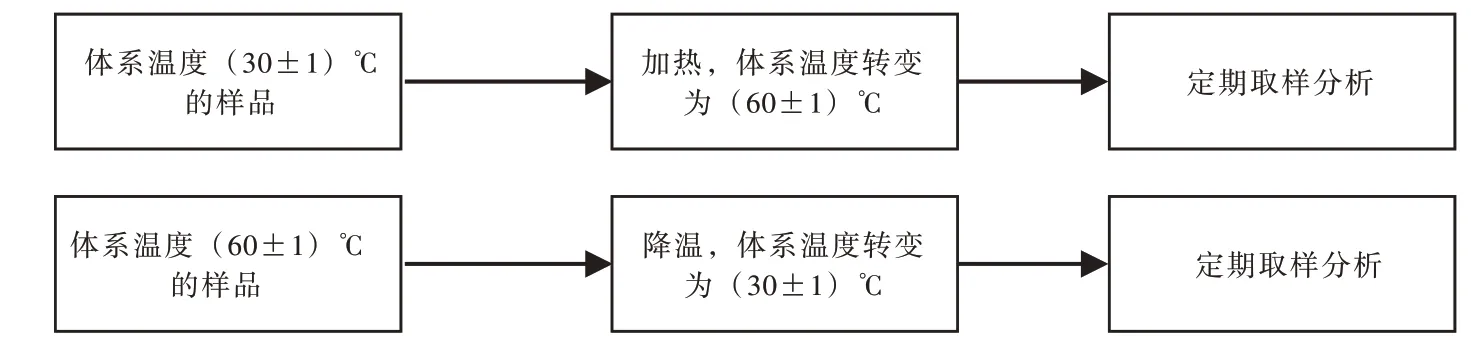
图3 体系温度变化对钚溶解度的影响实验流程Fig.3 Experiment procedure of the influence of temperature change on Pu solubility
实验将体系温度由(30±1)升高到(60±1)℃后,发现样品溶液中钚的浓度迅速降低(图4),在90 d 内,钚在北山地下水中的溶解度由原 来 的3.06×10-8下 降 到3.68×10-10mol·L-1;而将体系温度由(60±1)℃降低至(30±1)℃的样品溶液中,钚的溶解度基本没有变化。结合表4 的结果,判断产生该现象的原因是随着体系温度的升高,钚的溶解度控制固相发生了相应变化。Efurd[9]等人使用XRD 对25 和90℃钚的溶解度固相产物进行分析时发现,25℃时钚溶解度固相产物的布拉格衍射峰分布宽泛且强度不高,表明存在无定形的Pu(OH)4或者是Pu4+胶体,而90℃时钚溶解度固相产物的衍 射 峰 则 更 接 近 于PuO2(s)。由 于PuO2(s)比Pu(OH)4的溶解度更低,因此随着体系温度的升高,钚的溶解度进一步降低。此外,溶解产物含水率的不一致,也被认为是钚溶解度存在较大差异的原因[7]。

图4 体系温度变化对钚溶解度影响实验结果Fig.4 Experimental result of the influence of temperature change on Pu solubility
Fujiwara[15]在研究钚的溶解产物随时间变化时,认为随着实验时间的深入,钚的溶解产物 会 由 最 初 的 无 定 形Pu(OH)4慢 慢 向PuO2·xH2O 转变,并给出了相应的聚合过程(图5)。在常温下钚溶解产物的聚合过程非常缓慢,体系温度的升高会加速该过程。

图5 钚的溶解产物转变过程示意图[15]Fig.5 Schematic diagram of the transformation process of dissolved Pu product[15]
4 结 论
1)在达到溶解-沉淀平衡后,钚在溶液中的主要存在价态为+4价,+有少量5价;
2)体系温度为(30±1)、(45±1)和(60±1)℃时,钚在北山地下水的溶解度分别为(3.06±0.97)×10-8、(3.16±1.27)×10-10和(1.34±0.67)×10-10mol·L-1;
3)随着体系温度的升高,钚在北山地下水中的溶解度下降,这可能是因为溶解度控制固相发生了变化,溶解度控制固相由原来的无定形Pu(OH)4向PuO2·H2O转变;体系温度升高使钚溶解度减小,有利于阻滞钚的迁移。
