麻醉苏醒室患者术后低氧血症的危险因素分析及护理对策
2022-08-10陈赟赵晶张军王昕
陈赟,赵晶,张军,王昕
随着手术量的不断增加,麻醉后苏醒室(Post-Anesthesia Care Unit,PACU)作为围术期麻醉过程中的重要一环,承担了全麻后患者的复苏与拔管,因而是术后低氧血症的高发地[1]。特别是在拔除气管插管早期,呼吸道并发症发生率高,其中低氧血症是常见的呼吸道并发症[2]。Siddiqui等[3]研究表明,从手术室转运至PACU的过程中,有19.12%患者术后出现低氧血症,69.8%患者在转入PACU 30 min后发生低氧血症,在PACU期间有35%~55%的成人患者至少发生1次低氧血症。王云姣等[4]研究显示,PACU内10.02%患者发生了低氧血症。严重的低氧血症可增加机械通气时间,影响术后伤口愈合,引发多种类型的心律失常、异常血压变化及神经系统损伤,是患者术后发生病情变化的预警信号,严重者可发生呼吸心跳骤停[5-7]。因此,苏醒室护理人员早期发现高危患者,积极采取相应保护措施,对降低PACU内患者低氧血症的发生率尤为重要。研究显示,多种围术期因素,如高龄、吸烟、肥胖等是患者术后出现低氧血症的高危因素[8],但目前对于低氧血症危险因素的研究尚未有统一定论。因此,本研究对全麻术后患者进行术后低氧血症影响因素分析,并提出相应护理对策,旨在为采取针对性措施降低患者低氧血症提供参考。
1 资料与方法
1.1一般资料 选取本院麻醉科2021年3~9月收入PACU的全身麻醉术后患者,监护仪每5分钟自动记录1次生命体征,将监护仪的SpO2报警值设置为0.90,实时上传至麻醉复苏信息系统。排除标准:数据缺失者;在PACU内未脱氧及未完成动脉血气分析者;因术后寒战、体温偏低导致SpO2监测出现偏差者。共纳入1 028例患者。
1.2方法
1.2.1观察指标 本研究将患者呼吸空气时SpO2低于0.90[9],持续15 s以上作为判断低氧血症的标准;术后血红蛋白低于90 g/L作为判断贫血的标准。全部数据通过医院电子病历系统和麻醉复苏系统获得,由2名麻醉科护士同时录入数据,并确保数据的一致性和准确性。研究对象的主要观察指标包括:SpO2、性别、年龄、BMI、ASA分级、术后自控镇痛泵(Patient Controlled Analgesia,PCA)使用情况、吸烟史、术后PACU内测得的血红蛋白、入PACU状态(有无拔除气管插管)、术前合并呼吸系统疾病、手术部位。
1.2.2统计学方法 采用SPSS22.0软件进行分析,采用χ2检验及logistic回归分析,检验水准α=0.05。
2 结果
2.1PACU患者资料 1 028例患者中,男342例,女686例;年龄17~89(53.75±13.30)岁;BMI 15.18~40.48(23.29±3.32);有吸烟史298例;术后贫血147例;入PACU有气管导管762例;术前有呼吸系统疾病史53例。
2.2PACU低氧血症发生情况 1 028例患者中发生低氧血症224例(21.79%),持续时间1 min以内82例,1~min 66例,2~min 69例,5~min 5例,超过30 min 2例(此2例曾尝试多次脱氧、多次复吸氧,SpO2始终只能维持在吸氧0.90左右,转入ICU进一步观察)。
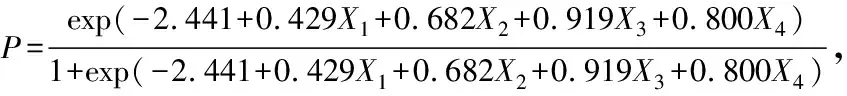
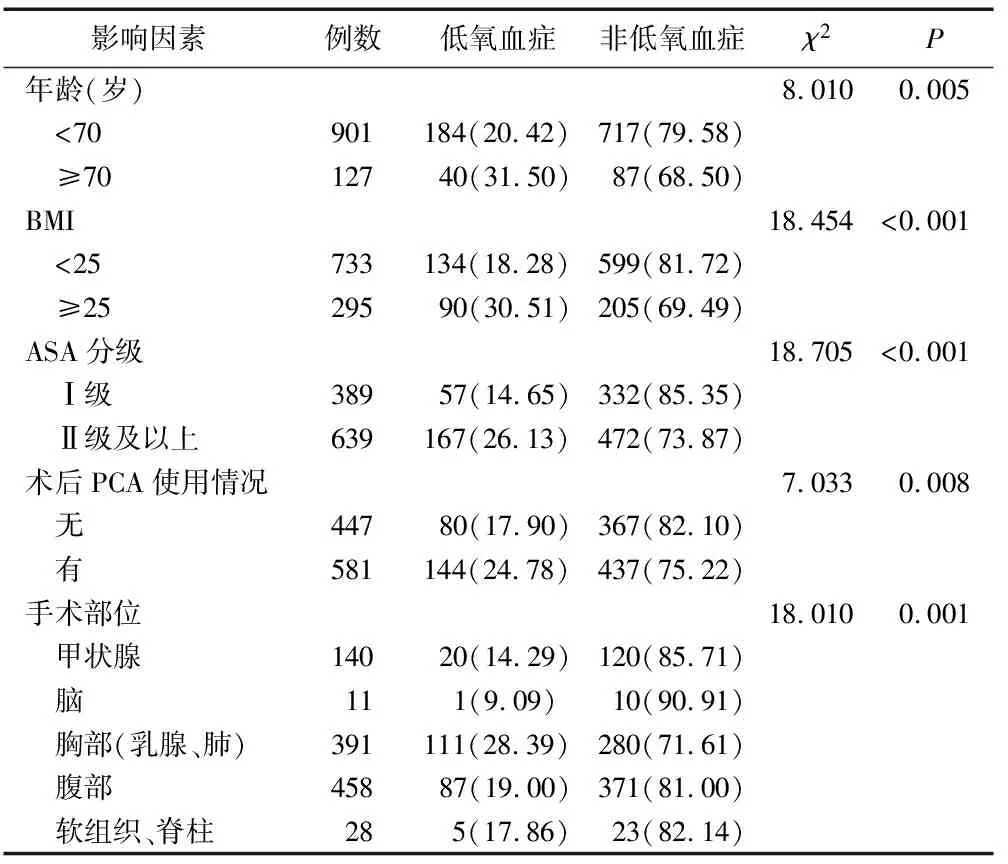
表1 PACU全身麻醉患者术后低氧血症的单因素分析 例(%)
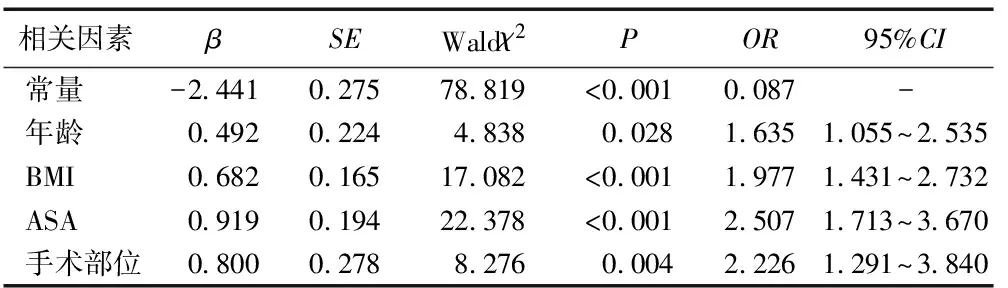
表2 PACU全身麻醉患者术后低氧血症的回归分析
3 讨论
3.1PACU患者术后低氧血症的发生率较高 本研究结果显示,PACU 21.79%患者发生了低氧血症,低于Siddiqui等[3]的报道,高于王云娇等[4]的报道,可能与纳入的研究对象不同有关,但均表明患者在PACU低氧血症的发生率较高。研究表明,导致低氧血症的主要原因是患者肺内右向左分流增加,通气与血流比下降[10]。
3.2低氧血症的影响因素及护理对策
3.2.1年龄 廖礼平等[11]研究显示,2 938例患者全麻术后苏醒期老年组以低氧血症、高血压、苏醒延迟发生率偏高。周琪[12]在对上腹部手术后546例患者低氧血症的发生情况研究中发现,70岁以上患者低氧血症发生的风险比达3.782。既往研究表明,高龄患者全麻苏醒期低氧血症发生率高达22.90%[13],是术后呼吸衰竭死亡的主要危险因素之一。本研究中高龄(≥70岁)患者术后低氧血症的发生率为31.50%,风险比为1.635。Geraldes等[14]研究表明,随着年龄的增加,小血管病变会造成血管反应性降低、灌注不足,从而出现低氧血症,因此年龄是术后低氧血症的危险因素。护理对策:适当延长高龄患者的苏醒和拔管时间,在拔管前行血气分析了解患者的呼吸功能及酸碱平衡状态,及时吸出口咽和气道内分泌物。拔管后实时监测呼气末二氧化碳,及时准确地发现呼吸抑制等情况,及早干预。
3.2.2BMI 刘熠等[15]研究表明,低氧血症发生的独立危险因素包括BMI、年龄、俯卧位、术中应用灌洗液,其中肥胖患者发生低氧血症的概率是超重患者的2.692倍。张胜利[16]研究发现,肥胖是发生呼吸系统并发症的独立危险因素,同时合并阻塞性睡眠呼吸暂停低通气综合征的肥胖患者发生低氧血症的频率更高(89%比11%)。Kendale等[17]研究显示,BMI正常范围内的患者术后低氧血症的发生率仅为16%,而BMI>30、>40的患者低氧血症的发生率分别为28%和35%。本研究中BMI≥25的患者术后低氧血症发生率为30.51%,是BMI<25患者发生低氧血症的1.977倍。Steier等[18]研究结果发现,肥胖影响膈肌及胸腹部运动,进而导致功能残气量降低、区域性肺不张和肺内分流增加,因此BMI的增加与术后低氧血症发生率、持续时间和严重程度密切相关。护理对策:在本研究发生低氧血症的肥胖患者中,有19例患者因肌力未完全恢复,导致术后低氧,针对术中肌松药使用情况,肌松药使用顺式阿曲库铵患者给予新斯的明1 mg和阿托品0.5 mg拮抗,使用罗库溴铵患者给予布瑞亭200 mg拮抗后,均恢复正常氧饱和度。因肥胖患者容易发生麻醉药物蓄积,所以在肥胖患者气管导管拔除期间和拔除后的早期均应充分评估肌松药残余情况和患者肌力恢复情况,除了观察患者可抬头时长和握拳力度来判断肌力恢复情况外,可借助神经刺激器来进行肌松药的监测,减少因肌松药残留、拔管不当造成的低氧血症,并在医生的指导下拔除气管导管。另外,有14例患者因拔管后出现呼吸遗忘及舌后坠导致低氧,因此麻醉护士在医生指导下拔管前后应落实好呼吸道管理措施,发生舌后坠时应立即将患者头偏向一侧,或给予合适的口咽通气道或鼻咽通气管来辅助肥胖患者通气,低氧严重者可采用托下额法,行面罩通气来改善低氧情况。
3.2.3ASA分级 本研究中ASA分级Ⅱ级和Ⅲ级的患者术后低氧血症发生风险是Ⅰ级患者的2.507倍,与有关研究结果类似[19-22],低氧与器官功能障碍有关。护理对策:麻醉医生应充分做好手术患者的术前麻醉评估,了解患者的整体状况,制订合适的麻醉方案;苏醒室护士在患者入PACU后,应与麻醉医生做好交接班,对拔管期间患者血流动力学的维持,以及拔管后的并发症制订针对性措施。通过观察患者的血压、心率、意识、呼吸等变化,给予针对性处理,降低术后患者发生低氧血症的风险。
3.2.4胸部手术 有研究显示,胸外科患者术后低氧血症发生率为41.2%[22]。Xue等[23]研究发现,低氧血症的发生及严重程度与手术部位有着密切联系,其中胸腹联合手术和上腹部手术与低氧血症的相关性最高。Shirakami等[24]研究发现,乳腺癌手术后夜间发作性低氧常发生,其中低氧患者BMI较高,PACU需氧治疗次数较多。本研究发现,胸部手术(乳腺、肺)的患者术后低氧血症的发生率为28.39%,风险比为2.226。有研究认为胸外科手术由于术中单肺通气[25],术侧肺萎陷,健侧肺不张及肺内分流增加,可导致低氧血症。除此之外,乳腺手术伤口包扎过紧会导致肺呼吸活动受限,引起肺有效通气量降低。在大多数开胸和乳房切除术后,约50%患者可能会出现术后疼痛,而疼痛和反射性腹部肌张力增加会使功能残气量较术前降低20%[26]。肺呼吸活动受限以及疼痛都是导致术后低氧血症发生的因素。护理对策:可配合麻醉医生给予镇痛药,或行肋间神经阻滞来缓解疼痛,改善患者通气情况。护士应加强胸外科手术患者的术后监护,拔管前及时进行肺复张,拔管后鼓励患者进行有效咳嗽咳痰,及时清理痰液,降低因肺不张导致的低氧血症。而乳腺手术后因手术部位包扎过紧导致的低氧,护士也应及时做好患者的术后宣教,指导患者进行有效呼吸。
4 小结
本研究结果显示,全麻术后患者PACU中低氧血症发生率为21.79%,高龄、肥胖、ASA分级Ⅱ级以上、胸部手术是术后低氧血症的危险因素。对低氧血症的深入研究也有助于苏醒室护士更好地预测和识别低氧血症,为患者提供安全舒适的围麻醉期护理。本研究样本量仅来自1所医院,纳入研究的低氧血症风险因素相对较少,导致分析不够全面;手术种类过于单一,手术类型的数量分布不均,在一定程度会对研究结果造成影响。在今后的研究中,需纳入更多的风险因素、更均衡的手术类型,进一步完善研究。
