铜绿假单胞菌注射液联合顺铂、地塞米松及利多卡因治疗肺癌合并恶性胸腔积液患者的效果
2022-08-04闫振华潘春玲任永佳
闫振华,潘春玲,任永佳
(汝州市中医院 呼吸内科,河南 平顶山 467500)
肺癌为常见的肿瘤,其病死率在全球肿瘤中居首位。肺癌患者早期无明显症状,确诊时多处于中晚期,预后较差。有研究指出,临床约有15%的肺癌患者首次确诊时合并恶性胸腔积液(malignant pleural effusion,MPE)[1]。药物胸腔灌注为临床治疗肺癌合并胸腔积液的主要手段之一,可达到控制MPE、改善预后的目的。有研究指出,铜绿假单胞菌(Pseudomonasaeruginosa,PA)注射液治疗非小细胞肺癌患者MPE可取得理想效果,且具有一定安全性[2]。为明确其具体治疗效果,本研究选取118例肺癌合并MPE患者进行分析,现报告如下。
1 资料与方法
1.1 一般资料本研究经汝州市中医院医学伦理委员会审核批准。选取2018年2月至2020年5月汝州市中医院收治的118例肺癌合并MPE患者,依照随机数字表法分为两组,各59例。对照组:男37例,女22例;年龄43~65(54.19±5.07)岁;临床病理分型鳞癌20例,腺癌39例;肺癌分期Ⅰ期9例,Ⅱ期35例,Ⅲ期15例。观察组:男34例,女25例;年龄43~65(55.26±4.86)岁;临床病理分型鳞癌24例,腺癌35例;肺癌分期Ⅰ期7例,Ⅱ期33例,Ⅲ期19例。两组患者一般资料(年龄、临床病理分型、性别、肺癌分期)均衡可比(P>0.05)。
1.2 纳入及排除标准
1.2.1纳入标准 (1)经病理学检查确诊为肺癌,经影像学检查合并胸腔积液,且为恶性;(2)预计生存期>3个月;(3)就诊时伴有胸痛、胸闷、呼吸困难等症状;(4)对本研究知情,签署知情同意书;(5)卡氏功能状态(Karnofsky performance status,KPS)评分>60分。
1.2.2排除标准 (1)肝、肾功能异常;(2)先天性呼吸循环系统解剖结构异常;(3)研究药物禁忌证;(4)血液系统疾病;(5)近1 a内接受放化疗、靶向治疗等相关治疗;(6)不能配合研究或中途退出;(7)精神疾病、认知障碍。
1.3 治疗方法
1.3.1用药前 两组均接受胸腔闭式引流术治疗。B超定位,在其引导下引流MPE,引流过程中严格控制速率,B超确认引流情况,完毕后行药物胸腔内灌注治疗。
1.3.2对照组 接受顺铂注射液(云南生物谷药业股份有限公司,国药准字H20043888)、地塞米松磷酸钠注射液(成都倍特得诺药业有限公司,国药准字H32021561)及盐酸利多卡因注射液(成都倍特药业股份有限公司,国药准字H32023421)治疗。顺铂30 mg·m-2及50 mL生理盐水,混匀,经导管注入胸腔,之后注入10 mL地塞米松及20 g·L-1的利多卡因,以避免发生化学性胸膜炎。
1.3.3观察组 在对照组基础上接受PA注射液(北京万特尔生物制药有限公司,国药准字S20043022)联合治疗。5 mL PA注射液及50 mL生理盐水,混匀,经导管注入胸腔。
1.3.4用药后 两组灌注后封管,嘱患者每15 min变换1次体位,促使药物充分接触胸膜脏层、壁层,治疗过程中密切关注不良反应,并及时给予患者针对性处理;治疗后1周,B超复查胸部,并再次给予药物灌注,每次1周,连续治疗4周,之后根据具体治疗情况确定拔管时间、定期复查时间。
1.4 疗效评估标准(1)完全缓解,胸部B超检查显示MPE完全消失,临床症状消失;(2)部分缓解,MPE体积减小>50%,无恶化、复发;(3)稳定,MPE体积减小25%~50%;(4)进展,未达以上标准。总有效包括完全缓解、部分缓解。
1.5 观察指标(1)疗效。(2)治疗前后KPS评分。量表总分100分,得分越高表示患者生活质量越高[3]。(3)治疗后肺癌细胞增殖活力及凋亡率,包括NCI-H1395细胞、95-D细胞。分别于治疗前后取处于对数生长期的肺癌NCI-H1395细胞、95-D细胞,胰酶消化处理后制成细胞悬液,接种培养,采用MTT比色法测定细胞增殖活力,采用AnnexinV/PI双染法测定凋亡率。(4)治疗前后免疫功能,包括T淋巴细胞亚群(CD3+、CD4+、CD8+)、免疫球蛋白(IgA、IgM)。于治疗前后采集患者空腹静脉血约5 mL,使用流式细胞仪(美国Beckman公司,型号EPICS-XL)测定CD3+、CD4+、CD8+水平;离心(3 500 r·min-1,10 min,10 cm)取上清液,使用酶联免疫吸附法测定IgA、IgM水平。(5)两组不良反应。
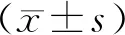
2 结果
2.1 疗效观察组治疗总有效率高于对照组(P<0.05),见表1。

表1 两组疗效对比[n(%)]
2.2 KPS评分治疗后,两组KPS评分均提升,且观察组高于对照组(P<0.05),见表2。
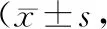
表2 两组KPS评分对比分)
2.3 肺癌细胞增殖活力及凋亡率治疗后,观察组NCI-H1395细胞、95-D细胞增殖活力低于对照组,NCI-H1395细胞、95-D细胞凋亡率高于对照组(P<0.05),见表3。
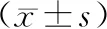
表3 两组肺癌细胞增殖活力及凋亡率对比
2.4 免疫功能治疗后,观察组CD3+、CD4+、IgA、IgM较对照组高,CD8+较对照组低(P<0.05),见表4。
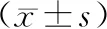
表4 两组免疫功能对比
2.5 不良反应两组消化道反应、骨髓抑制、发热、白细胞减少发生率对比,差异无统计学意义(P>0.05),见表5。

表5 两组不良反应对比[n(%)]
3 讨论
临床目前对于肺癌尚缺乏特效治疗手段,MPE的出现,使得患者病情进展更加迅速,同时会引起呼吸、心血管等系统出现并发症,加大治疗难度[4]。胸腔灌注属于局部治疗手段,能缓解患者胸腔积液引起的不适症状,还能促进脏层、壁层粘连,提升局部药物浓度,促进癌细胞凋亡[5]。本研究结果显示,观察组治疗总有效率较对照组高,且治疗后KPS评分也较对照组高,表明PA注射液联合顺铂、地塞米松及利多卡因治疗肺癌合并MPE的效果较好,能有效提高患者生活质量。PA注射液为近年常用的抗肿瘤辅助治疗药物,不仅能抵抗肿瘤生长,还能改善胸腔积液。PA注射液具有双向免疫调节作用,其有效成分通过与高甘露糖表达型癌细胞特异性结合,改变癌细胞结构、功能,促进其凋亡,增强癌细胞抗原信号,刺激抗原递呈细胞,恢复免疫监视作用,从而能抑制癌细胞生长[6-7]。作为人体异源性物质,PA注射液还能诱导胸腔产生无菌性炎症,促使胸膜血管壁增加,胸腔纤维蛋白增生,从而达到胸膜闭锁效果。化疗作为有效治疗手段,能抑制肿瘤进展,但其在杀死癌细胞的同时还会杀死部分正常细胞,骨髓抑制等可引起T淋巴细胞功能改变[8-9],加之肺癌合并MP患者免疫功能较差,接受化疗使细胞免疫功能进一步降低。同时,细胞免疫功能抑制可影响肿瘤转移、复发[10]。本研究结果显示,治疗后,观察组T淋巴细胞亚群水平、免疫球蛋白水平均优于对照组,可见肺癌合并MPE患者在接受顺铂、地塞米松及利多卡因治疗的同时辅助PA注射液治疗,能在一定程度上减轻免疫功能抑制。其主要原因为:PA注射液通过促进树突状细胞等抗原提呈细胞成熟,增强其协同刺激分子表达,强化其对肿瘤抗原的加工提呈能力,可诱导Th1类细胞因子产生,从而活化并刺激T淋巴细胞,增强特异性细胞免疫功能;PA注射液还能直接诱导跨菌属抗体产生,增强机体对病原体的免疫防御功能[11-12]。
本研究结果显示,治疗后,观察组NCI-H1395细胞、95-D细胞增殖活力较对照组低,NCI-H1395细胞、95-D细胞凋亡率较对照组高。PA注射液通过凋亡途径抑制癌细胞增殖,其主要作用机制可能为,菌毛上甘露糖结合蛋白特异性结合于高甘露糖表达型肿瘤,能加快癌细胞微绒毛除极、电荷消失、流动性改变,抑制癌细胞增殖,并通过改变其结构和功能降低增殖、侵袭、转移能力,从而启动凋亡程序,诱导癌细胞凋亡[13]。本研究结果还显示,两组消化道反应、骨髓抑制、发热、白细胞减少发生率对比,无明显差异,提示PA注射液联合顺铂、地塞米松及利多卡因治疗肺癌合并MPE,不会明显增加患者不良反应。
综上所述,PA注射液用于辅助治疗肺癌合并MPE化疗患者,效果确切,能有效抑制癌细胞增殖活力,促进肺癌细胞凋亡,改善机体免疫功能,提高患者生活质量。
