UV/PMS/H2O2体系对他汀类药物的去除作用及机制研究*
2022-08-01赵孟雷袁守军
赵孟雷,袁守军
(合肥工业大学土木与水利工程学院,安徽 合肥 230009)
随着社会经济的发展,人类的寿命得到了延长,但同样,高龄人口的患病率也随之上升。据统计,2019年全球有5.23亿人口患有心血管疾病[1],各类治疗心脑血管疾病药物的使用量逐年增加,其中,他汀类药物因在调血脂、降胆固醇等方面作用显著而被广泛应用,在2017~2019年,瑞舒伐他汀的销售额位居全球第43位,而阿托伐他汀的销售额则位于全球第68位。这些药物被服用后大部分被排出,再经由市政管网进入污水厂,但现有污水处理工艺对大部分药物的去除效果不佳,每年有大量残留药物随着污水厂尾水进入环境水体,从而对水生生物及生态环境造成潜在威胁[3]。
紫外线(UV)消毒因具有杀菌效果优良、不产生新的消毒副产物等特点而被用作污水厂尾水的消毒工艺,以此为基础的UV光催化的研究也一直受到人们的关注[4]。过硫酸氢钾(PMS)和过氧化氢(H2O2)常作为氧化剂被用于有机物的降解。本研究构建了UV/PMS/H2O2体系,开展了典型他汀类药物的降解实验,研究不同实验条件对于他汀类药物去除的影响作用,探讨其降解机理,从而为该类药物的进一步去除提供技术支持。
1 材料与方法
1.1 试剂和设备
瑞舒伐他汀钙(ROSC,99%)和阿托伐他汀(ATV,99%),Aladdin公司,甲醇、N,N-二甲基甲酰胺(DMF)等有机溶剂,均为HPLC级,上海安谱实验科技股份有限公司;其他药物均为分析纯,国药集团化学试剂有限公司。
GC-MS(Clarus 680+Clarus SQ 8 T),美国PerkinElmer;高效液相色谱(1260 Infinity),美国Agilent;TOC分析仪(UltiMate),美国DIONEX。
1.2 实验方法
1.2.1 实验设计
降解产物分析实验。分别取10 mg/L的ATV和ROSC各 200 mL置于恒温水浴中,加入适量PMS(1 g/L)和H2O2(1 g/L)储备液配成10 mg/L的氧化剂(PMS: H2O2=1:1)浓度,立刻打开UV灯进行氧化,反应分别进行120 min(ATV)、10 min(ROSC)后取反应液10 mL于20 mL棕色瓶当中,过0.22 μm滤膜。用GC-MS分析其降解产物;用TOC分析仪分析其矿化效果。
1.3 样品预处理及分析方法
1.3.1 HPLC方法
水样中的ROSC和ATV浓度由HPLC进行检测,色谱柱型号为Wonda Cract Ods-2,柱温30 ℃,进样量20 μL。ROSC的液相条件:流动相0.1%三氟乙酸:水:乙腈(V:V:V)=1:49:50,流速0.9 mL/min,检测波长245 nm;ATV液相条件:流动相:1%甲酸:乙腈(V:V)=25:75,流速0.9 mL/min,检测波长:242 nm。
1.3.2 水样预处理和降解产物分析方法
样品预处理。取出1 mL样品,经冷冻干燥后加入2 mL甲醇溶解,然后经轻柔氮气吹干,用600 μL N,N-二甲基甲酰胺(DMF)重新溶解,然后通过0.45 μm混合纤维素酯膜过滤。加入体积为100 μL的衍生试剂BSTFA,用非极性三甲基甲硅烷基取代酸性氢;最后,在70 ℃下衍生化1 h后,使用GC-MS分析衍生化的样品。
GC-MS条件:色谱柱:HP-5MS毛细管柱(Agilent,30.0 m×320 μm×0.25 μm);升温程序:50 ℃保持5 min,然后以 5 ℃/min升高至200 ℃并保持2 min,再以20 ℃/min升高至300 ℃并保持1 min;进样器温度250 ℃;进样量1.0 μL;离子源温度250 ℃;传输线温度250 ℃;载气为高纯He,气体流量1.0 mL/min。
2 结果与讨论
2.1 不同氧化体系对他汀类药物的降解作用
Litvic等发现瑞舒伐他汀是一种光敏性有机化合物在可见光条件下就可以产生两种光产物。William在研究中发现,紫外催化镁钛基催化剂对于ATV最大去除率不超过20%。为了进一步探究不同氧化体系对他汀类药物的降解效果,实验中分别研究了PMS、H2O2、PMS/H2O2、UV、UV/PMS、UV/H2O2和UV/PMS/H2O2七种氧化体系对ATV和ROSC的降解作用。ATV和ROSC在各体系中的降解效果如图1所示。在H2O2体系中,ROSC的去除率最仅为10.13%(180 min);在PMS体系中,ATV的最高降解率为20.45%。而在UV催化条件下,ATV和ROSC降解速率明显提升,这是由于紫外线激发PMS及H2O2产生活性自由基,系统氧化性能增强。

图1 不同氧化体系下他汀类药物的降解情况

临床痊愈:中医临床症状、体征消失或基本消失,证候积分减少≥90%;显效:中医临床症状、体征明显改善,证候积分减少≥70%;有效:中医临床症状、体征有所改善,证候积分减少≥30%;无效:中医临床症状、体征无明显改善,证候积分减少<30%。
2.2 淬灭剂实验
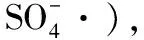
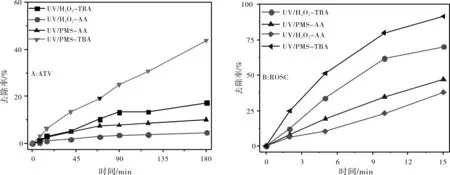
图2 不同淬灭剂条件他汀类药物的降解实验
2.3 实验条件及环境因素影响
2.3.1 pH影响

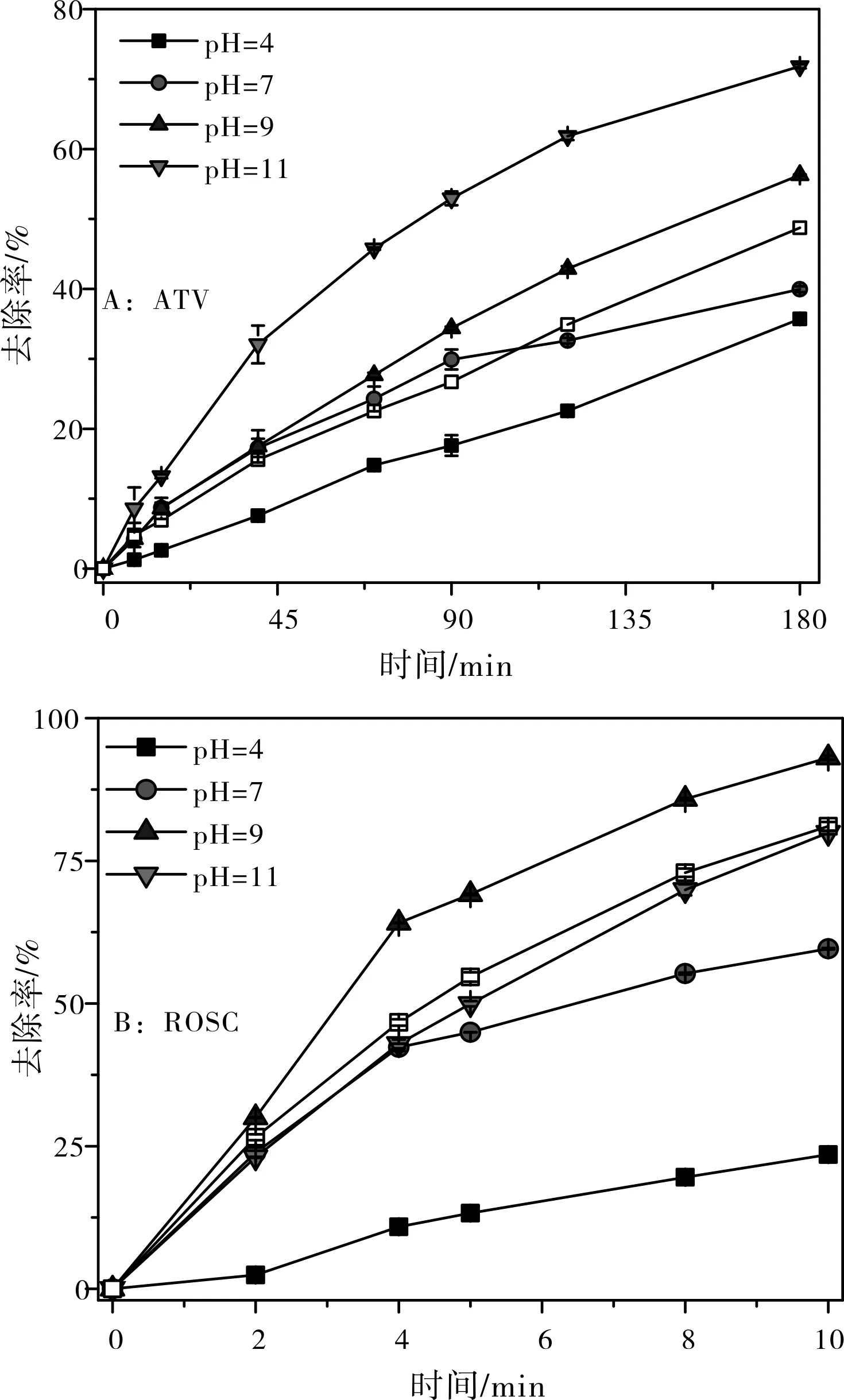
图3 不同pH条件降解效果
(1)
(2)
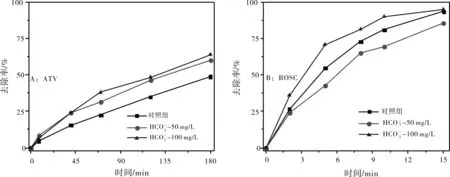
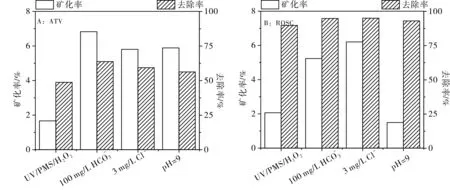
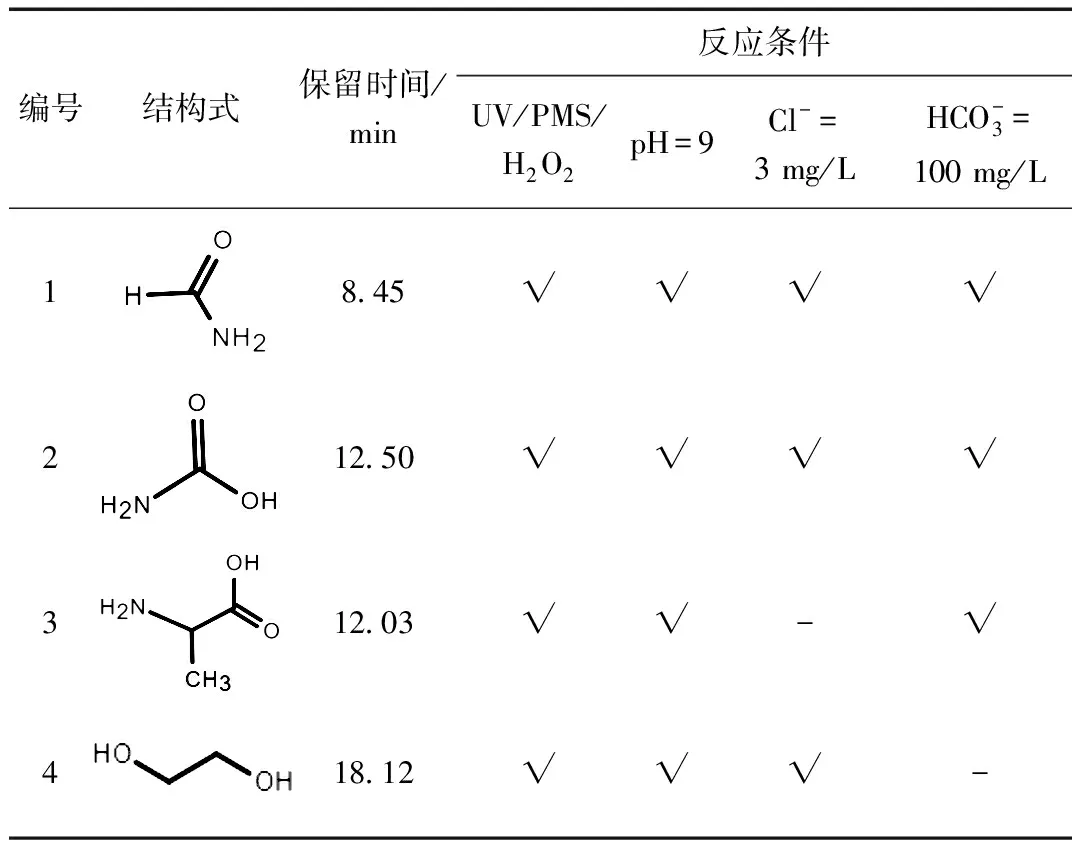
在酸性条件下,羟基自由基受到氢离子消耗,同时过硫酸氢钾在酸性条件下活化受到抑制,氧化基团减少导致了两种他汀类药物的降解速率大幅度下降,ROSC的动力学常数kpH=4(0.0268 min-1) 2.3.2 碳酸氢根影响 图4 碳酸氢根离子对他汀类药物降解的影响 (3) (4) (5) (6) (7) 2.3.2 氯离子影响 当氯进入体系时,发生如式(8)~式(11)的反应[11];在诸多反应的综合作用下,随着氯离子浓度的增加,他汀类药物的降解过出现抑制和促进交替呈现的规律(图5)。 图5 氯离子对于他汀类药物降解的影响 (8) (9) (10) (11) 2.3.2 腐殖酸影响 图6 腐殖酸对于他汀类药物降解的影响 在UV/PMS/H2O2体系各反应条件下,ATV的去除率在48.7%~63.7%之间,矿化率在1.66%~6.82%之间;ROSC的去除率在89.7%~95.0%之间,矿化率在1.49%~6.21%之间(图7)。这表明他汀类药物虽然有较好的去处效果,但系统中仍残留较多有机物。结合GC-MS的分析结果可知(表1),系统中仍存在大量小分子有机物,如含羧基、酰胺基团的化合物。这些小分子有机物的环境效应进一步关注。 图7 不同体系对他汀类药物去除效果和矿化效果 表1 ATV降解产物分析 本文主要对两种他汀类药物的高级氧化降解进行进行了研究。结论如下: (1)相对单独的UV/PMS和UV/H2O2体系,UV/PMS/H2O2体系对他汀类药物表现出更好的去除效果,但系统中仍存在大量含有羧基、羰基和酰胺基团的小分子有机物。两种他汀类药物的降解过程均符合伪一级动力学。


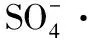

2.4 矿化率及降解产物分析
3 结 论