借助思维导图促进学科知识的结构化
——以《物质结构与性质》模块整合为例
2022-07-29河北廖淑芳
河北 廖淑芳
(作者单位:河北省张家口市第四中学)
《中国高考评价体系》提出的高考评价要求为“基础性、综合性、应用性、创新性”,随着新课标、新教材、新高考的步步推进,以核心素养为宗旨的高考命题对学科复习提出了新的要求。新高考化学试题凸显出以化学知识为工具,解决真实情境下的实际问题这一导向,这就要求在复习过程要将化学学科知识梳理,转化为学科核心素养,落实为熟练的认识解决实际问题的能力。
一、借助思维导图促进学科知识的结构化
在实践过程中,考前复习中存在的问题大多是因时间紧任务重,有偏重练习轻视知识系统再梳理的倾向。如何将知识体系再构建与题目练习有效结合,实现化学学科知识向化学学科核心素养的最终转化,是考前复习的主题之一。实践证明,利用思维导图结合典型例题进行专题复习,是突破考前复习难点的有效途径。
思维导图是进行归纳总结、建立知识框图、厘清内在逻辑的有效工具。选取适当的角度,引导学生从典型例题中提取核心要素,进行特定中心知识、规律、方法的思维导图结构化整理,能够在宏观层面,用简明扼要的表达方式厘清关系,有助于跳脱出题目本身,而提炼并牢固建立认知模型,从而达成熟练运用模型认识、解决实际问题的目标。在角度选择上,针对不同主干知识的特点,抓住核心问题,是实际操作的关键。
以《物质结构与性质》模块为例,其知识体系并不复杂,但概念较多、知识抽象、理论性强,逻辑严密但内在联系建立较为困难是学习的特点。一轮复习时可采用以教材章节为依据的梳理方式进行整合,突出“微观结构决定宏观性质,宏观性质反映微观结构”这一化学学科核心观念的结构化,建立思维导图基本框架如图1。

图1
复习时则需要转换视角,以高考真题的设问方向为依据,引导学生进行基于模块综合试题问题认识解决思路的结构化再梳理,构建问题解决模型,促进证据推理与模型认知的学科核心素养目标达成。
二、教学实例
研究高考真题,将《物质结构与性质》模块综合题目考向归纳为“描述”“比较”“判断”与“计算”四角度,分为2至3课时完成。以其中“比较”与“判断”考向为例,教学设计如下。
【课前准备】研习以下习题,试归纳其核心考点及涉及的一般规律与方法。
【真题体验1】(2020·全国卷Ⅰ·35)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为________。
(2)Li及其周期表中相邻元素的第一电离能(I1)如表1所示。I1(Li)>I1(Na),原因是________________。I1(Be)>I1(B)>I1(Li),原因是____________。
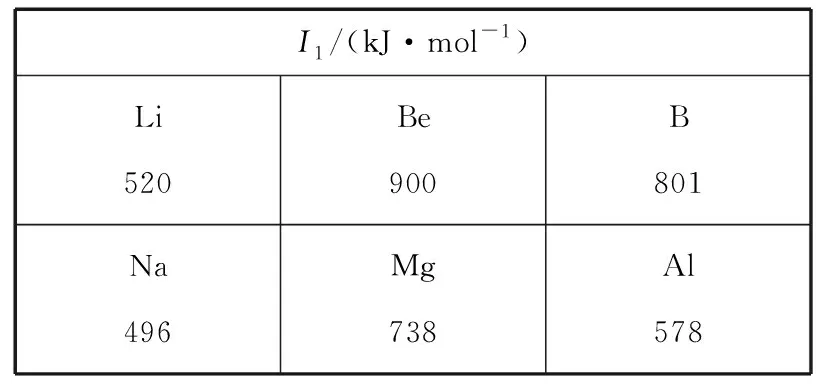
表1
(3)磷酸根离子的空间构型为________,其中P的价层电子对数为________、杂化轨道类型为________。
(4)LiFePO4的晶胞结构示意图如图2(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有________个。

图2
电池充电时,LiFeO4脱出部分Li+,形成Li1-xFePO4,结构示意图如(b)所示,则x=________,n(Fe2+)∶n(Fe3+)=________。

(2)Na与Li同族,Na电子层数多,原子半径大,易失电子,电离能小 Li、Be、B同周期,核电荷数依次增加,Be为1s22s2全满稳定结构,第一电离能最大,与Li相比,B核电荷数大,原子半径小,较难失去电子,第一电离能较大。
(3)正四面体 4 sp3

【真题体验2】(2020·山东卷·17)CdSnAs2是一种高迁移率的新型热电材料,回答下列问题:
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为________,其固体的晶体类型为________。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为________(填化学式,下同),还原性由强到弱的顺序为________,键角由大到小的顺序为________。
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图3所示,1 mol该配合物中通过螯合作用形成的配位键有________mol,该螯合物中N的杂化方式有________种。
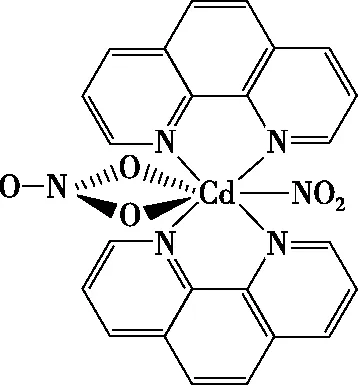
图3
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图4所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表2所示。

表2

图4
一个晶胞中有________个Sn,找出距离Cd(0,0,0)最近的Sn________(用分数坐标表示)。CdSnAs2晶体中与单个Sn键合的As有________个。
【参考答案】(1)正四面体形 分子晶体
(2)NH3、AsH3、PH3AsH3、PH3、NH3NH3、PH3、AsH3
(3)6 1
(4)4 (0.5,0,0.25)、(0.5,0.5,0) 4
【设计思路与意图】对于普通高中而言,在集中综合训练之前学生解决此类综合题目可能存在一定困难,故采用课前自主体验的方式为课堂讨论做出准备,同时节省课堂时间,突出整合过程这一教学重点。这里解题不是教学的重点,而是要通过高考真题的分析、比较与归纳,明确考法、厘清思路,从而构建此类问题的解题模型和解决模型。在课前将答案给出,让学生发现自己认知上的不足,为课堂个性化问题的解决提供方向指导,同时有助于引导学生把课堂关注点放在解决“为什么”而不是简单追求“是什么”。
【课堂探究】以上述两题为依据,设置探究问题,引导分析、讨论与归纳。
设问1.《物质结构与性质》模块综合题命题有什么特点?
发现1.《物质结构与性质》模块综合题以生产生活、科学技术等真实情境为依托,选择不同考点分别设问,从而确定本题的解决策略为:化整为零,各个击破,互不干扰。
发现2.《物质结构与性质》模块综合题立足主干知识,关注常规考点、考法,从而确定解题时对问题应精准识别,灵活运用一般规律与方法。
设问2.可以将《物质结构与性质》模块综合题按照设问方向分为哪几类?
归纳1.大致可以归为描述、比较、判断、计算四大考查方向,描述类主要包括书写、绘制、表述等,主要集中于对原子结构相关问题的考查,计算类主要是以晶体结构为中心的晶胞计算及相关问题,绘制思维导图框架如图5。
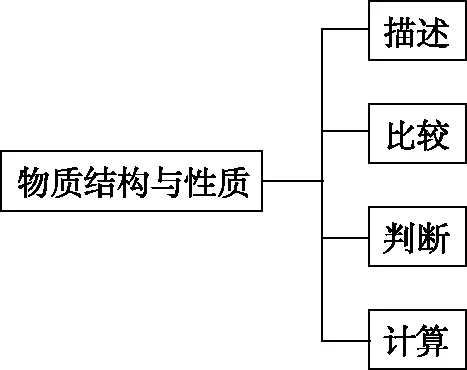
图5
同时,教师应在课堂上指出,描述类问题一二轮复习解决情况较好,留为课下自主梳理内容,计算类问题是难点,会在下次课集中解决;本课重点解决比较类与判断类问题。
设问3.找出上述两题中的比较类问题,分组讨论总结比较的一般方法与思维过程。
结论1.元素的电离能比较,关注一般规律和特殊。如【真题体验1】(2)同主族Na比Li电子层数多,金属性强,失电子能力强,电离能较小,符合一般规律;Li、Be、B同周期自左而右,非金属性增强,失电子能力减弱,但Be原子2s层电子全充满,原子结构稳定,导致其电离能增大,故I1(Be)>I1(B)>I1(Li),在一般规律下同时考虑特殊。拓展至第二电离能、第三电离能的比较,总结为图6。

图6
结论2.物质熔沸点或硬度的比较,按先看晶体类型用一般规律、同晶体类型按不同情况比粒子间结合力的思维顺序进行。如【真题体验2】(2)NH3、PH3、AsH3为分子晶体,组成结构相似,相对分子质量依次增大,范德华力依次增大,沸点依次升高。具体总结为图7。

图7
结论3.共价键键参数比较,键角比较规律为一般孤对电子对对成键电子对的排斥力比成键电子对对成键电子对的排斥力大,所以孤对电子对越多成键电子对之间就越紧凑,键角越小;孤电子对影响相同再看成键电子对,半径越小,成键电子对间斥力越大,键角越大。如【真题体验2】(2)NH3、PH3、AsH3孤电子对数相等,看成键电子对,半径增大,成键电子对间斥力减小,键角减小。具体总结为图8。

图8
设问4.找出上述两题中的判断类问题,分组讨论总结判断的一般方法与思维过程。
结论4.分子构型判断,依据价层电子对互斥理论、杂化轨道理论进行。二者之间的联系总结为图9。

图9
典型实例列表如表3:

表3

结论5.晶体类型判断,可依据构成粒子、粒子间作用力或性质特点进行,总结如表4所示:

表4
如【真题体验2】(1)常温常压下SnCl4为无色液体,熔沸点低,应为分子晶体,SnCl4空间构型与CH4相似为正四面体。
结论6.粒子间作用力判断,可总结如图10。

图10
【课堂小结】通过上述问题的讨论解决,形成如图11所示思维导图,明确正确识别题目设问模型,准确使用一般规律与方法模型,是突破《物质结构与性质》模块综合题的关键,构建应用体系,坚持有序思维是顺利应对变化的途径。

图11
【设计思路与意图】探究过程的设计采用了问题导引的组织模式推进。在教学的主干采用由果溯因的思路组织探究,体验证据推理的过程,在知识结构化整理的过程中同时达成设问规律与解题规律的双重建模,完成模型认知的核心素养的提升。
【真题再体验】(2021·全国甲卷·35节选)我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。单晶硅的晶体类型为________。SiCl4是生产高纯硅的前驱体,其中Si采取的杂化类型为________。SiCl4可发生水解反应,机理如下:

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为________(填标号)。
(2)CO2分子中存在________个σ键和________个π键。
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是______________________。
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图12所示。Zr4+离子在晶胞中的配位数是________。

图12
【参考答案】(1)原子晶体(共价晶体) sp3②
(2)2 2
(3)甲硫醇不能形成分子间氢键,而水和甲醇均能,且水比甲醇的氢键多
(4)8
【认识延伸】“配位数”在不同情况有不同含义。配位化合物中,配位数指化合物中中心原子周围的配位原子个数。如[Cu(H2O)4]2+、[Cu(NH3)4]2+中配位数为4,[Ag(NH3)2]+中配位数为2。此概念也可延伸至任何化合物,也就是配位数等同于共价键的数量,例如,可以说甲烷中碳的配位数为4。这种说法通常不计π键。金属晶体中,指一个金属的离子周围最近金属离子数。离子晶体中,指一个离子周围最近的异电性离子的数目。
【设计思路与意图】利用高考真题进行巩固练习,尝试利用课堂所得解决新问题,体会模型识别和逻辑推理的过程,印证模型的有效性。同时发现不同题目间的变与不变,了解题目的发展能力要求和适当拓展延伸,明确“量力而行,熟能生巧”的应对策略。
考前复习是学科知识体系在更高层次实现重构,核心素养得以大幅度提升的关键阶段。实践证明,将单纯的知识再梳理转化为对照高考真题的分析与归纳,将一味的数量化练习转化为比较提炼下的深度学习,同时借助思维导图这一得力工具,使知识规律方法间的复杂联系及思维过程得以外显,是实现问题解决模型建构、达成专题突破切实可行,且行之有效的方法。
