妇幼医疗机构药物警戒体系的运行模式与实践*
2022-07-27江永贤陈文文
江永贤,李 根△,陈文文,叶 曦,王 飞
(1.四川省妇幼保健院,四川 成都 610041; 2.电子科技大学医学院附属妇女儿童医院•成都市妇女儿童中心医院,四川 成都 611731; 3.四川省成都市药品检验研究所,四川 成都 610095)
2002年,世界卫生组织(WHO)将药物警戒定义为,发现、评价、认识和预防药品不良反应(ADR)或其他任何与药物相关问题的科学研究和活动[1]。药物警戒较传统的药品不良反应监测范围更广[2−3],旨在通过风险管理的方法和理念,对药品的全生命周期进行监管,保证患者的用药安全。2019年颁布的《药品管理法》和2021年颁布的《药物警戒质量管理规范》均要求建立健全药物警戒制度,加大用药安全监管。医疗机构作为药物警戒工作的主体之一应坚决执行。妇女儿童作为用药的特殊群体,用药安全尤为重要。成都市妇女儿童中心医院(以下简称中心医院)探索和构建妇幼医疗机构的药物警戒体系,同时尝试将从事ADR 监管的人员转变为全职的用药安全主管(MSO),通过结合质控管理方法,从药品角度、用药行为、安全意识3个维度开展工作,通过3 个等级的干预来实行日常监管,现总结该院妇幼药物警戒体系构建的工作经验,以供参考。
1 工作构架与内容框架
1.1 机构及人员架构
中心医院药学部成立药物警戒信息办公室(以下简称办公室),办公室成员包括1 名专职MSO 和4 名专职警戒药师。负责全院的药物警戒工作,办公室的工作由该院药事管理委员会下设的ADR 小组负责监管和协调,药学部主任对该办公室进行直接管理。
1.2 工作内容框架
办公室工作参考《美国用药安全总监手册》[4]并结合中心医院药学部实际情况开展工作,工作内容主要包括药品角度、用药行为、安全意识3大板块,其框架详见图1。
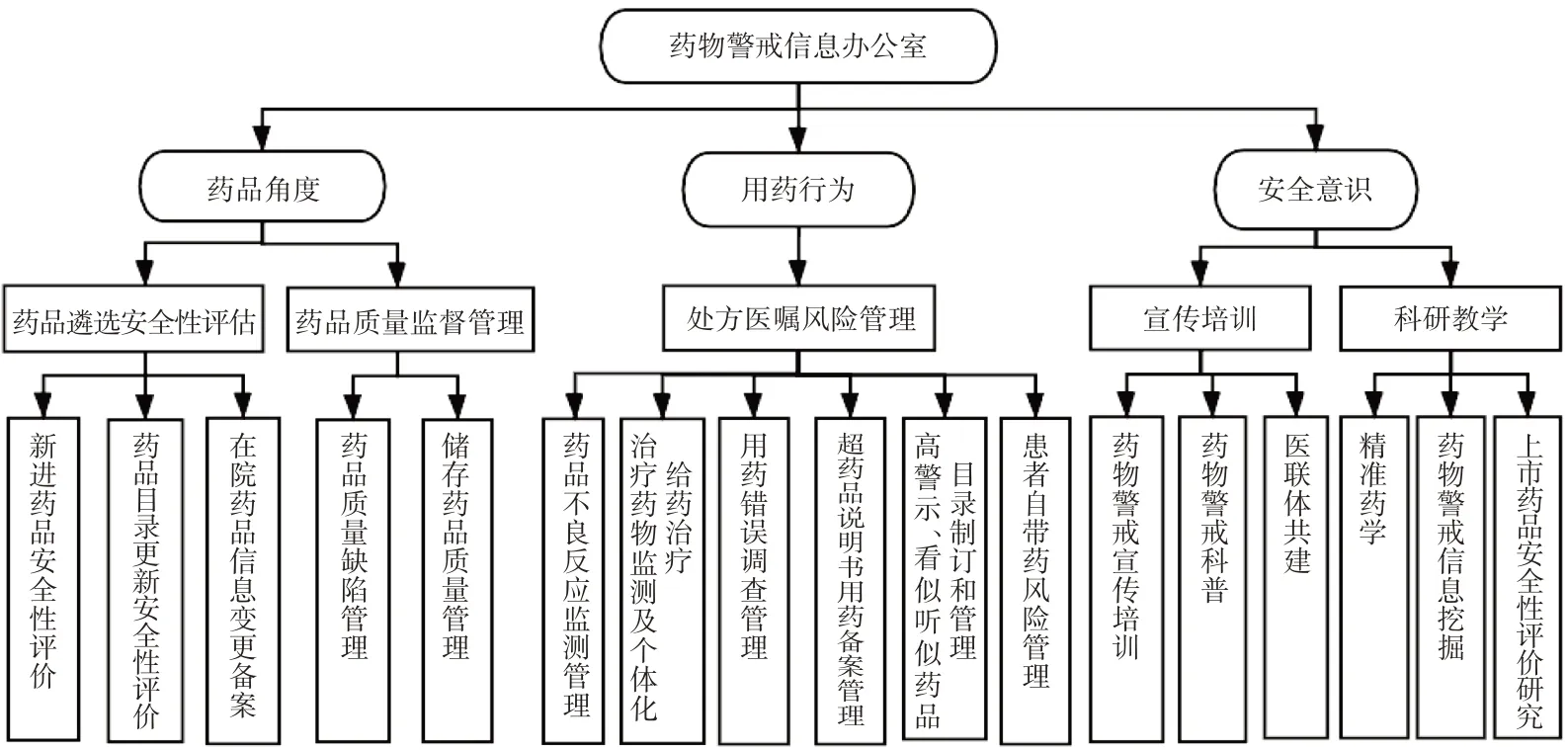
图1 成都市妇女儿童中心医院药物警戒信息办公室工作内容Fig.1 Work contents of Pharmacovigilance Information Office of the Chengdu Women′s and Children′s Central Hospital
2 工作模式
2.1 岗位设立及工作职责
MSO:美国的医疗机构招聘该岗位人员时会提出许多附加要求[5],但由于人员等各种条件的限制,我国的妇幼医疗机构多选择药学部内部实现岗位转变的形式,有利于MSO 岗位的设立。中心医院的MSO 由ADR专员岗位转变而来,有利于在ADR/ 药品不良事件(ADE)的基础上发现用药风险。其工作职责是制订年度用药安全计划,多维度拓宽对特殊人群安全用药的监管与服务,制订相应的日常药物警戒措施和风险控制策略,减少ADE发生[6]。
警戒药师:这是区别于临床药师的全新的岗位。警戒药师是风险干预的执行者,其在MSO 的带领和负责下,按既定工作流程和模式开展用药安全监管活动,该岗位的设立也是保障患者用药安全的有效措施之一[7]。警戒药师从日常工作中挖掘ADE 风险点,并进行风险评估及确认,并根据中心医院指定的药物警戒风险干预模式,执行不同级别的干预。
2.2 风险管理的流程和干预模式
流程:办公室的工作模式为风险隐患预警、实时监控及风险改进,并对全院的用药风险点进行梳理和日常监管,并按图2进行风险管理。一旦发现风险,MSO会组织科主任、警戒药师和质控药师使用风险数值(RPN)法进行风险评估[8]。RPN=S×O×D,其中S 为严重度,O 为风险发生频率,D 为风险是否能被发现的可侦测度,均计1~10分,风险数值越大越要进行风险干预。并采用鱼骨图和柏拉图分析导致风险的原因并选择风险干预策略,通过不同的干预措施进行风险管理,最后确认管理效果并持续追踪。
干预模式:根据RPN 和实际情况决定。RPN ≤100时,进行Ⅲ级干预;100 <RPN ≤150 时,进行Ⅱ级干预;RPN >150,或RPN ≤150但S值较高时,进行Ⅰ级干预。Ⅲ级干预为文件干预,如发布药物警讯、文件来督促改进;Ⅱ级干预是通过制订标准化流程,开展讲座、宣教形式干预或提醒谨慎使用某种药品;Ⅰ级干预为最重要的干预方式,是使用质控方法进行用药干预,利用信息化手段进行流程改进或药品清退。
3 工作实践
3.1 药品角度
3.1.1 药品遴选安全性评估
包括新进院药品的安全性评估、药品目录更新安全性评价及在院药品信息变更备案,主要围绕药品有效性、特殊人群的安全性、稳定性、经济性来开展首营和药品目录变更安全性审核工作,审核不通过的药物执行Ⅰ级干预,进行药品淘汰;对于正式进院的药品进行Ⅱ级干预(此处为对药学部的所有部门进行培训)及Ⅲ级干预(此处为通过医院内网、处方集等形式发布新药警讯)。用药风险管理流程见图2。

图2 用药风险管理流程Fig.2 Flow chart of medication risk management
3.1.2 药品质量监管
药品质量缺陷管理:主要针对患者投诉及使用过程中导致ADE 并发现疑似质量问题的药品首先及时停用,根据调查情况将该药品清退或更换批次,所有质量风险信号排除后,将调查情况反馈给相应部门,多角度消除药品安全隐患。2019 年至2020 年针对药品质量问题采取Ⅲ级干预89 次,主要涉及漏液、粉针剂溶解变色、片剂变色、胶囊融化、空盒等问题;Ⅱ级干预1 次,为药品说明书变更后限制新生儿科使用的处理;Ⅰ级干预3 次,其中对于多个胶塞脱屑的案例直接将该品种淘汰,对于夹杂毛发、不溶物的案例则予更换批次处理。
全院药品养护管理:即每月对全院进行药品质控检查后将检查结果以简报形式发至内网和护理部进行反馈。采取Ⅱ级干预23次,为针对冷链药品脱离冷链后保存时间、遮光避光药品的汇总和宣教;Ⅰ级干预1次,为针对查房中自制制剂的效期风险管理,MSO 组织进行效期管理的根因分析(RCA),排出了相关隐患,通过RCA 完善了自制制剂的效期管理、召回制度和药学部质量管理工作制度。
3.2 用药行为
3.2.1 用药错误调查管理
对于用药错误(ME)的管理,药物警戒主要依托ADR/ ADE 上报系统。参照美国用药安全规范研究所(ISMP)医院用药安全自我评估标准[9],办公室每季度通过对本单位报告及药品质控检查发现的潜在风险、或已发生的ME 进行分析评估,不断建立和改进工作体系和流程,以减少安全风险,并通过检索文献对其他医疗机构发生的ME 进行讨论,评价本机构是否可能发生类似错误并有针对性地进行改进。如对于妇科蛇毒类血凝酶所致血栓[10]及儿童自行更改自带药品使用剂量所致低血糖[11],均根据药物警戒工作模式和思路进行干预和改进,并已将干预思路和过程撰写文章并发表,有利于其他医疗机构借鉴参考,以减少ME 导致的风险。
3.2.2 ADR 管理
除月度、季度对ADR 报表的总结和分析外,对于本院发生的新的严重ADR[12−13],应汇总[14]并及时公告,并对多次引发严重ADR 的药品进行Ⅰ级干预,积极开展病区严重ADR 讨论,及通过医嘱系统信息提示的方式警示医务人员在使用该药品时应注意观察,一旦发生ADR应及时救治。
3.2.3 治疗药物监测(TDM)及个体化用药方案制订
TDM 通过样本检测,为患者制订个体化治疗方案及提供用药监护,是药物警戒工作的重点。警戒药师通过对患儿地高辛[15]、万古霉素的血药浓度监测,发现剂量过大等多个风险点并进行多重干预,最大限度地降低患儿的用药风险,保障其用药安全。
3.3 安全意识
构建用药安全文化氛围是建立药物警戒体系过程中非常重要的一环,不仅要让医务人员关注药物警戒,患者、公众也是用药安全文化建设的关键。
办公室会定期收集国际、国内、院内的妇幼相关药物警讯,并在内网上发布。每月组织1 次药物警戒相关内容的学习活动,带动更多的调剂药师、规培实习生参与并关注安全用药工作[16−19]。该活动充分调动了调剂药师对ADR 的关注,在合理用药窗口主动开展ADR 相关咨询服务。主动收集退药患者可能存在的ADR 信息,2020年医院ADR上报总数中调剂药师上报率从3.33%升至31.32%。
4 对比与思考
4.1 不同医疗机构药物警戒体系对比
查阅文献,PITTS 等[3]的药物警戒研究仅报道了政策层面的制度。欧洲药品管理局建立加强药物警戒的SCOPE 项目[20],提到了药物警戒工作开展的工作流程,为发布ADR 相关的警戒信息,发现及发布风险信号,风险最小化措施及协调沟通药物安全的工作。而BENINGER[21]认为,药物警戒工作的核心是个案管理、风险信号管理及效应风险管理,其中提及的药物警戒管理流程与中心医院的药物警戒工作内容及模式基本一致。
2013年,美国用药安全总监(ISMP)协会成立,美国大型医疗机构纷纷设立了MSO 或类似岗位[22]。我国在全国8家三级甲等医院和上海大部分二、三级医院开展设立MSO 岗位的试点工作[23]。2018 年,MSO 被列入ISMP 白皮书,强调MSO 需作为医疗保健团队的组成部分,如文献[5]提及,美国的MSO 与行政部门关系密切,需要每月在医院层面召开安全质量控制会议。与之相比,中心医院MSO 的工作准入和工作职责与国外MSO类似,但与行政部门沟通较少。
我国的药物警戒工作尚处于起步阶段,与发达国家相比,在法律法规、政策等方面存在较大差距[24]。药物警戒相关文章的发文量虽逐年递增[25],但研究机构多为国家,各省市药品不良反应监测中心,制药企业及医学院校,医疗机构数占比较低,且大部分文章的选题为药物警戒信号挖掘、ADR 监测[26]及开展药物警戒 工 作 的 理 论 思 路[27−29]等。仅 有 几 个 医 疗 机构[24,30−31]分享了对自身开展药物警戒工作的经验,其与本研究的对比情况详见表1。其中本研究中的药物警戒模式的特点是设定了风险评估流程和风险干预的三级管理。

表1 不同医疗机构开展药物警戒工作实践经验比较Tab.1 Comparison of practical experience of different medical institutions in pharmacovigilance
4.2 思考及建议
大多数医疗机构仅建立了ADR/ADE 监测与干预制度,未对药品安全的全生命周期监管建立全面、系统的监测体系。故开展药物警戒相关工作是医疗机构用药风险监测的必然选择[6,31−33]。
MSO 岗位建设:通过药物警戒体系建立的实践,对MSO 的工作职责、岗位隶属和资质准入有了更深的体会。首先,MSO 不应仅局限于药学部,应纳入院级管理体系,使其具有行政职能,才能更好地开展药物警戒工作;其次,MSO 的工作职责除上文提到的内容外,更应加强在药学部门的概念推广,增加认同感;再次,MSO 除应具备许多文献提及的学历及药事管理、临床药学、沟通协调能力外,更应有药学部各个部门的从业经历。
药物警戒规范化培训开展:中心医院的药物警戒体系的建立完全靠文献、讲座等方式摸索,殊为不易。建议我国参照临床药师培训体系,建立药物警戒培训体系,以利于医疗机构更好地开展培训。有研究显示[34],药师经过集中于MSO 的岗位职责,风险管理重要性,ADR 发生率和应用质控方法(RCA 和失败模型与效应分析)来解决风险问题的药品安全管理和MSO课程系统培训后,药物警戒知识与能力有了明显提升。
4.3 本研究的不足
一是现阶段药物警戒工作的主体仍以药师为主,医师、护士的参与较少。但建立一个全院药品全生命周期监管的药物警戒体系需要所有医务人员的参与,所以下阶段的目标是加大对医务人员的培训及增加参与风险干预的活动,提高医疗机构所有人员对药物警戒的认识。二是本研究中介绍的药物警戒体系仅在单一妇幼医疗机构建立及实践,未在其他妇幼医疗机构推广,故下阶段的目标是通过妇幼医疗体共建的形式,帮助更多的医疗机构建立药物警戒体系。
4.4 结语
妇幼专科医院是医疗机构中的重要组成部分,面对的患者均为特殊人群,在我国药物警戒体系中的地位不可替代。希望我国建立更多药物警戒体系及设立更多国家药品不良反应监测哨点机构时可考虑纳入更多妇幼专科医疗机构。实践证实,建立妇幼医疗机构的药物警戒体系有助于风险的预警与管控,从而保障临床用药安全有效。
