不同胚胎移植方案在体外受精—胚胎移植中的效果分析*
2022-07-23李蕊蕊
李蕊蕊
洛阳市妇幼保健院生殖医学研究所,河南洛阳 471000
不孕症为临床常见的疑难杂症,可分为女性不孕与男性不育,主要病因包括排卵障碍、精液异常、输卵管异常等,受环境因素、食品安全、生活节奏加快等诸多因素影响,不孕症发生率呈逐年递增趋势,对家庭和谐、社会稳定造成较大影响[1-2]。近些年,生殖医学工程是治疗不孕症而改变生物自然生殖的过程,利用现代技术来繁衍下一代,体外受精—胚胎移植(IVF-ET)是重要手段,越来越多的不孕症家庭从中受益[3-4]。IVF-ET是重要的人工生育技术,治疗不孕症效果较好,其中胚胎移植是最重要步骤,与患者临床妊娠关系密切[5]。据相关调查显示,既往IVF-ET临床妊娠率仅为40%左右,但患者即使妊娠仍存在流产率高的特点,导致整体效果并不理想[6]。经临床不断实践发现,通过对移植过程中的某些环节进行改进,或许能够提高胚胎种植率与妊娠率[7]。为提高胚胎移植成功率,越来越多的移植方案应用于临床,但关于哪种方案移植成功更高,预后更好尚存在较大争议。鉴于此,本研究进一步探讨不同胚胎移植方案在IVF-ET中的效果,现总结如下。
1 资料与方法
1.1 一般资料
回顾性分析2017年6月—2020年6月洛阳市妇幼保健院行IVF-ET治疗的患者临床资料,包括新鲜移植周期1 500个,解冻移植周期1 500个。根据内膜准备方法(激素替代周期、自然周期)、周期类型(新鲜周期、解冻周期)、移植胚胎发育天数(囊胚-D5、卵裂期胚胎-D3)进行分组。解冻周期中替代周期(H)准备内膜者又分为H-D3、H-D5,自然周期(N)分为N-D3、N-D5,新鲜周期(F)分为F-D3、F-D5。不同周期内不同移植胚胎发育天数患者年龄、体重指数、不育年限、子宫内膜厚度、移植胚胎数量等一般资料具有可比性(P>0.05),见表1。
表1 不同周期内不同移植胚胎发育天数患者一般资料对比(±s)

表1 不同周期内不同移植胚胎发育天数患者一般资料对比(±s)
组别周期数(n)年龄(岁)体重指数(kg/m2)不育年限(年)子宫内膜厚度(mm)移植胚胎数(个)新鲜移植周期F-D3 F-D5替代周期H-D3 H-D5自然周期N-D3 N-D5 1 190 310 30.35±3.97 30.54±3.94 22.61±3.08 22.74±2.99 4.15±1.01 3.97±1.19 10.55±2.13 10.43±2.28 1.89±0.31 1.92±0.29 550 440 30.78±4.06 31.02±3.86 21.89±2.97 22.17±3.05 3.94±1.25 3.86±1.03 10.24±2.17 10.37±2.25 1.88±0.35 1.94±0.33 270 240 30.69±3.99 30.76±4.05 22.56±2.45 22.64±2.85 4.05±1.17 4.21±1.22 10.54±2.36 10.71±2.24 1.96±0.27 1.92±0.25
1.2 入选标准
纳入标准:(1)所有入选的夫妻双方无遗传性疾病或家族性疾病史。(2)夫妻双方染色体检查正常。(3)由输卵管异常、子宫内膜异位症、排卵障碍、男方因素等原因或不明原因导致的不孕。(4)所有患者临床资料完整,未出现丢失情况。(5)既往无不良妊娠结局。排除标准:(1)夫妻双方任意一方伴有认知障碍或精神疾病。(2)女方子宫畸形或宫腔严重粘连。(3)伴有恶性肿瘤或重要脏器功能衰竭。(4)拒绝参与本次研究,或入选者存在视听障碍无法进行正常交流。(5)传染病检查结果为阳性。
1.3 方法
1.3.1 新鲜周期移植方案控制性促排卵采用黄体中期长效长方案,根据患者年龄、BMI、基础卵泡数(AFC)选择促性腺激素(Gn)剂量,用药剂量可视患者卵巢反应情况进行酌情调整。当直径≥18 mm卵泡数量占比超过优势卵泡数量的50%时,将5 000~10 000 IU人绒毛膜促性腺激素针(HCG)通过肌肉进行注射,诱发排卵,注射后间隔36 h实施取卵。第3 d移植卵裂期胚胎(1~2枚)或第5 d移植囊胚(1~2枚)。取卵后,由阴道置入黄体酮缓释凝胶(MERCK SERONO LIMITED,批准文号:H20140552),90 mg/d,另外口服20 mg/d地屈孕酮(Abbott B.V.,批准文号:H20150346)。
1.3.2 解冻周期移植方案 (1)替代周期内膜准备方案:对于既往自然周期子宫内膜较薄的患者或者无排卵患者,可采用激素替代周期。于月经第3~5 d口服4~6 mg/d雌二醇(昆明赛诺制药股份有限公司,国药准字H20041721),期间使用剂量可视患者内膜厚度调整,但不得超过8 mg/d,内膜厚度使用阴道B超观察。当子宫内膜厚度≥8 mm时可转化内膜,第5 d移植卵裂期胚胎,第7 d移植囊胚。(2)自然周期内膜准备方案:对于月经规律的患者,自然周期密切监测优势卵泡排出情况,于排卵日诱导内膜转化成分泌期,转化内膜后使用孕激素为第1 d,第3 d移植卵裂期胚胎,第5 d移植囊胚。替代周期、自然周期两种方案在转换内膜日均加用黄体酮,用法参照新鲜周期方案取卵后。
1.3.3 胚胎移植使用澳大利亚COOK 5000型移植管,移植过程需在腹部B超引导下进行,操作需轻柔,匀速、缓慢推注胚胎至宫底15~20 mm内膜最厚处,移植时随胚胎一起进入宫腔的液体量应<15μL,移植后平卧半小时。
1.3.4 妊娠判断胚胎移植2周后,进行血、尿妊娠试验检查,血βHCG阳性、尿妊娠试验阳性即可判定为生化妊娠。胚胎移植4~5周后进行B检查,见孕囊、胎心搏动为临床妊娠。若在宫腔以外的地方,如宫颈、宫角或附件区探及包块,且血βHCG阳性则可判断为异位妊娠。
1.4 观察指标
比较不同周期内不同移植胚胎发育天数的生化妊娠、临床妊娠、异位妊娠发生情况。
1.5 统计学方法
采用SPSS 22.0软件进行统计分析。计量资料以均数±标准差(±s)表示,组间比较采用t检验。计数资料以例数和百分比(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
解冻周期囊胚移植H-D5、N-D5生化妊娠率[70.22%(309/440)、69.17%(166/240)]、临床妊娠率[59.77%(263/440)、59.17%(142/240)]均高于H-D3[42.18%(232/550)、39.82%(219/550)]、N-D3[43.33%(117/270)、40.74%(110/270)],差异有统计学意义(P<0.05)。新鲜周期F-D3生化妊娠率(59.90)、临床妊娠率(52.02%)占比均高于H-D3(42.18%、39.82%)、N-D3(43.33%、40.74%),差异有统计学意义(P<0.05)。各组间异位妊娠发生率对比,差异无统计学意义(P>0.05),见表2。
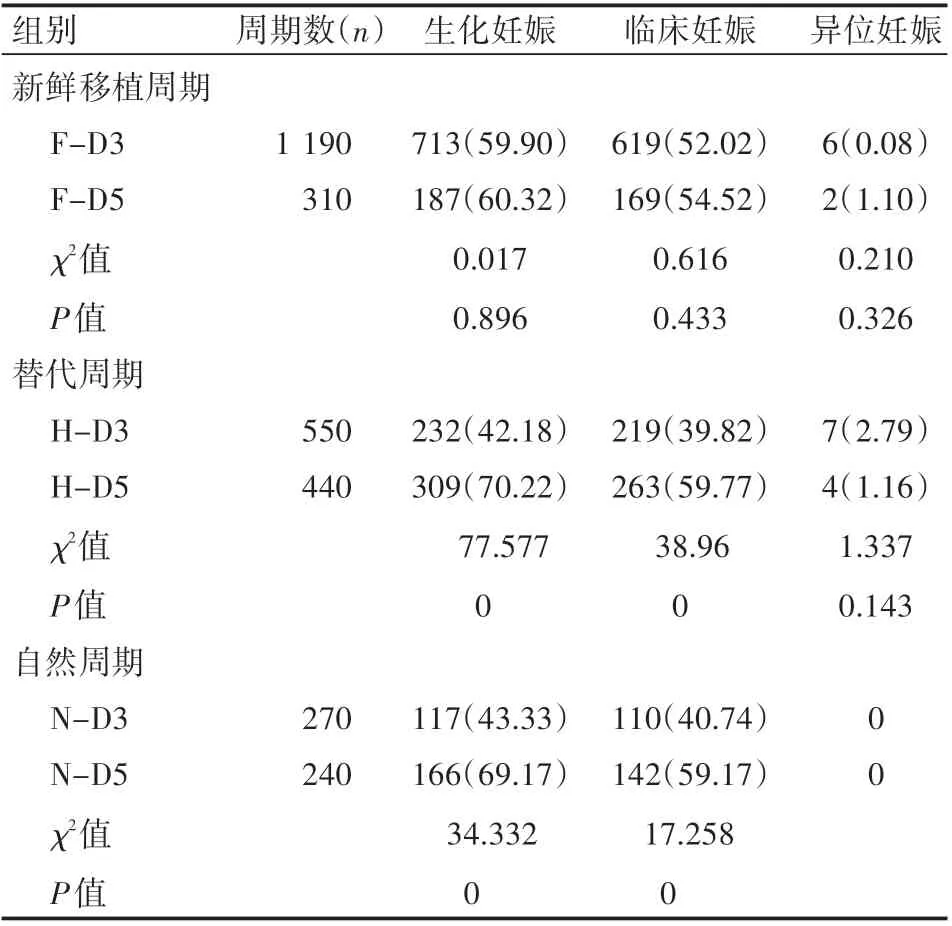
表2 各组间生化妊娠、临床妊娠、异位妊娠发生情况例(%)
3 讨论
近些年,IVF-ET技术得到全面发展,已呈现出个体化、多元化,能够满足不同原因导致的不孕症患者,制定针对性IVF-ET方案是生殖临床的重要内容[8-9]。但IVF-ET后能够成功妊娠受诸多因素影响,如胚胎质量、子宫环境、胚胎移植技术、内膜容受性等均会影响胚胎发育,导致患者出现不良妊娠结局[10-11]。异位妊娠是IVF-ET技术最常见且最严重的并发症,自然妊娠该并发症发生率为1.2%~1.4%,而IVF-ET妊娠异位妊娠发生率为2%~5%,远远高于自然妊娠[12-13]。IVF-ET发生异位妊娠的机制较为复杂,具体原因至今尚未完全明确,临床认为主要与激素环境、女性输卵管因素、操作方法等多方面因素相关,为降低并发症发生,提高妊娠率,IVF-ET患者选择合适的移植方案有重要意义[14]。
胚胎移植操作过程需在临床医师、实验室工作人员配合下进行,成功与否的关键在于胚胎防治情况,而此过程无法在直视下进行,稍有不慎易异位妊娠出现,导致妊娠失败[15-16]。为提高妊娠成功率,选择合理妊娠胚胎移植方案至关重要[17]。本研究结果显示,解冻周期囊胚移植H-D5、N-D5生化妊娠、临床妊娠占比均高于H-D3、N-D3,新鲜周期F-D3生化妊娠、临床妊娠占比均高于H-D3、N-D3,各组间异位妊娠发生率无明显差异。由此可见,新鲜周期与解冻周期临床妊娠率相当,但囊胚移植妊娠率明显高于卵裂期移植,为提高临床妊娠率,临床可选择囊胚移植。分析其原因为,正常受孕期间,胚胎发育往往在输卵管中进行,当发育至囊胚期才会进入子宫腔内[18]。IVF-ET将囊胚移植宫腔内能够缩短发育与着床之间的时间,是胚胎种植率提高,从而临床妊娠率也随之升高[19]。即使卵裂期移植成功,但在发育过程中可能因潜能差、染色异常等原因导致胚胎不能继续形成囊胚,临床可通过延长体外培养时间,直接在体外将胚胎培养至囊胚再发育,以降低胚胎损失,提高妊娠成功率,同时还利于降低异位妊娠发生风险,改善患者预后[20]。
综上所述,临床进行IVF-ET时选择新鲜移植周期或解冻移植周期妊娠率并不会出现较大差别,但囊胚移植妊娠率较卵裂期移植明显更高,临床应优先考虑该方案。
