细菌纤维素/功能化石墨烯复合材料的制备及抗菌研究
2022-07-22王学洋崔吉晓胡晓慧
王学洋,钟 成,崔吉晓,杨 颖,胡晓慧,辛 波,2
(1.天津科技大学 生物工程学院 工业发酵微生物教育部重点实验室,天津 300457;2.天津瑞普生物技术股份有限公司,天津 300308)
细菌纤维素(bacterial cellulose,BC)是一种新型的纳米纤维素材料,主要由细菌发酵形成。BC具有极细的纳米纤维网络结构、较高的持水性能、高比表面积、优异的力学性能、亲水性、良好的生物相容性等特征,在食品、生物医药、工业造纸、环境等领域具有较大的应用潜力[1]。然而,BC本身并不具备抑菌性能,在一定程度上限制了其实际应用。
氧化石墨烯(GO)是一种二维纳米片状材料,GO 及其衍生物最重要的特性是它们具有一定的抑菌性能和细胞相容性好等优点。作为石墨烯的衍生物,还原石墨烯(rGO)已经引起了相关学者极大的关注[2],其表面具有丰富的官能团,是吸附金属或其他无机前体的良好候选物,可以轻松地被各种有机小分子和聚合物功能化[3]。此外,具有抗菌活性的rGO基材料可用作生物医学设备和食品包装中的抗菌涂层材料[4]。二氧化锡(SnO2)纳米粒子具有优异的光催化性能、晶粒尺寸小、良好的稳定性等特点,可以充分利用其光催化性能对rGO进行功能化修饰,增强rGO的抗菌性能,从而达到协同抗菌的效果。
本文中,笔者首先采用氧化还原反应制备rGO-SnO2复合纳米粒子,然后通过匀浆共混法将纳米复合物填充到BC基质中,制备细菌纤维素/功能氧化石墨烯抗菌复合材料,然后测定复合材料的性能,为后续的应用提供基础数据。
1 实验部分
1.1 主要菌种及其来源
木糖驹形氏杆菌(Komagataeibacterxylinus,CGMCC 2955,由工业发酵微生物教育部重点实验室筛选),中国普通微生物菌种保藏管理中心(CGMCCC)保藏;金黄色葡萄球菌(Staphylococcusaureus)ATCC 6538、大肠杆菌(Escherichiacoli)DH5α,由笔者所在实验室保存。铜绿假单胞菌(Pseudomonasaeruginosa)PAK由天津科技大学生物工程学院杨洪江教授惠赠。枯草芽孢杆菌(Bacillussubtilis)CGMCC1.504由天津市畜牧兽医研究所提供。
1.2 培养基及溶液配制
发酵培养基(g/L):葡萄糖25、酵母提取物7.5、胰蛋白胨10、Na2HPO410;冰乙酸调节pH至6.0。
细菌培养基(g/L):蛋白胨10、NaCl 10、酵母提取物5。
2 mg/mL的GO溶液的配制:精确称取GO纳米片0.5 g,加入250 mL的纯水中,超声分散10 h,直至GO溶液充分分散溶解。
1.3 细菌纤维素的发酵培养
从培养皿上挑取K.xylinus单菌落,180 r/min、30 ℃振荡培养24 h后,向液体培养基中添加0.4%(体积分数)的纤维素酶,以6%(体积分数)的接种量接种培养,直至菌体OD600为0.5~0.6。离心收集菌体,洗涤后重悬于200 mL的液体培养基中,调节菌体OD600为0.02。在30 ℃下静置培养4 d后,使细菌纤维素膜厚度约为6 mm。
将得到的细菌纤维素膜浸泡在0.1 mol/L的NaOH溶液中直至膜中残留的培养基和菌体被完全除去,此时BC膜呈乳白色半透明状,用去离子水反复冲洗,直至膜表面水的pH呈中性。采用纤维疏解器将BC破碎处理,调制BC浆液质量浓度为10 g/L。
1.4 rGO-SnO2纳米复合物的制备
以GO为模板载体吸附金属离子前驱体,合成rGO-SnO2纳米复合物。通过GO和SnCl2在90 ℃下发生直接氧化还原反应得到SnO2修饰的rGO(rGO-SnO2纳米复合物),GO被SnCl2还原为rGO,与此同时Sn2+被氧化成SnO2纳米粒子沉积在rGO的表面。具体实验步骤如下:首先将64 mL 的2 mg/mL GO悬浮液用超纯水稀释至200 mL。然后将0.56 g的SnCl2·2H2O 加入200 mL的盐酸溶液(含4 mL 37% HCl),搅拌至溶解。将上述2种溶液混合超声分散10 min后,90 ℃磁力搅拌反应6 h。最后,再收集离心得到的纳米复合物,用超纯水离心洗涤若干次(10 000 r/min,10 min)后80 ℃真空干燥,即得rGO-SnO2纳米复合物。
1.5 BC/rGO-SnO2纳米复合材料的制备
分别将5、10和15 mg的rGO-SnO2纳米复合物加入10 mL的超纯水中,超声分散均匀,将得到的混合溶液加入一定量的细菌纤维素匀浆(10 g/L)中,搅拌均匀,超声分散,得到的混合物用醋酸纤维素膜抽滤成薄膜状,之后冷冻干燥,保存备用,得到不同复合比率(5%、10%和15%)的复合材料,分别命名为BC/rGO-SnO2-5%、BC/rGO-SnO2-10%和BC/rGO-SnO2-15%。
1.6 BC/rGO-SnO2复合材料膜光催化性能测定
以亚甲基橙(MO)为模型化合物,研究BC/rGO-SnO2复合膜对于甲基橙染料的光催化降解效率。首先将0.4 g BC、BC/GO、BC/SnO2、BC/rGO-SnO2样品浸没在100 mL配制好的MO溶液(10 mg/L)中,超声分散5 min后,在黑暗条件下搅拌1 h,达到吸附平衡后,用功率为250 W的紫外灯(波长254 nm)对MO溶液进行照射(光源距离为10 cm),之后每隔一段时间(0、20、40、60、80、100和120 min)取样测定1次。在甲基橙样品溶液测定前,10 000 r/min离心10 min去除溶液中的不溶杂质和沉淀后,用紫外-可见分光光度计测定甲基橙溶液的吸收光谱。
1.7 BC/rGO-SnO2复合材料的光催化抑菌实验
以金黄色葡萄球菌作为测试菌株,在近紫外光的催化下(365 nm,20 W),测定不同样品BC(对照组)、BC/SnO2以及BC/rGO-SnO2复合膜的抑菌活性。具体的过程如下:
金黄色葡萄球菌在LB液体培养基内37 ℃培养过夜,收集对数生长期的细菌,用0.1 mol/L的磷酸盐缓冲液(PBS)洗涤后重悬,调节OD600为0.5。取直径为90 mm的培养皿,每个培养皿中加入20 mL的菌悬液后,将BC膜和rGO-SnO2纳米复合物复合比率分别为5%、10%、15%的BC/SnO2以及BC/rGO-SnO2纳米复合膜圆片(直径约为90 mm,约0.5 g)分别加至有菌液的平板,在近紫外光(365 nm,20 W)激发下测定材料的光催化抑菌活性。辐照时间为6 h,取菌液进行梯度稀释,之后取100 μL的菌液涂布在准备好的LB固体平板上,37 ℃培养24 h后进行菌落计数,计算抑菌率。实验之前,复合材料要经过高温蒸汽灭菌(121 ℃,20 min)。
2 结果与讨论
2.1 透射电镜(TEM)分析
GO纳米片的TEM图像如图1(a)所示。由图1(a)可知:单层GO纳米片的TEM图成薄纱状,表面含有许多的褶皱。
图1(b)~(c)为rGO-SnO2的TEM照片。由图1(b)和(c)可知:SnO2纳米颗粒均匀地沉积在rGO薄片上,rGO薄片的整个表面都被蠕虫状的SnO2纳米颗粒所修饰。
图1(d)为rGO-SnO2的晶格照片。由图1(d)可知:晶格间距为0.33和0.26 nm,分别对应于金红石相SnO2的(110)和(101)晶格平面的d-间距。
图1(e)为rGO-SnO2的选区电子衍射(SAED)图像。图1(e)进一步证实rGO-SnO2复合物的形成,其中衍射环表示的是rGO-SnO2复合物,衍射斑点是石墨烯[5]。
图1(f)为负载在rGO薄片上的SnO2纳米颗粒的粒径分布图,是从rGO-SnO2纳米复合物的高倍TEM图中随机选取了50个SnO2纳米颗粒,通过Nano Measure软件分析[6]计算得到的。由图1(f)可知:在GO纳米片上,原位生长的SnO2纳米颗粒粒径为3~6 nm,平均粒径为4.5 nm。

图1 GO(a)、rGO-SnO2(b、c)膜的TEM图谱,rGO-SnO2(d)的HRTEM图谱,rGO-SnO2(e)的SAED图谱和SnO2 NPs在rGO片上的粒径分布(f)Fig.1 TEM images of GO sheets(a),rGO-SnO2 (b,c),and high-resolution TEM image of SnO2 nanoparticles on a rGO sheet(d),SAED pattern of rGO-SnO2(e),histograms and particle distribution of SnO2 nanoparticles on rGO sheets(f)
2.2 X线衍射(XRD)分析
图2为rGO-SnO2、BC/rGO-SnO2、BC/SnO2和BC的XRD图谱。由图2可知:BC的XRD图谱在2θ=14.9°和2θ=23.1°处有2个主要的结晶峰,为BC的特征衍射峰,分别对应于BC的(110)和(200)晶面;在2θ=17.2°处的峰是BC位于无定形区的非结晶峰。rGO-SnO2样品中未见层状GO的衍射峰,说明阳离子还原后GO的层状堆叠结构消失了。在2θ=26.6°、33.7°和52.2°处出现的衍射峰分别对应于金红石相SnO2的(110)、(101)和(211)晶格平面(JCPDS 41-1445)[7]。这些较宽的衍射峰表明在rGO纳米片上原位合成的SnO2的颗粒粒径较小,结晶性差。同时,在图中均未发现rGO衍射峰,可能是由于rGO含量过低未达到仪器检测水平造成的。
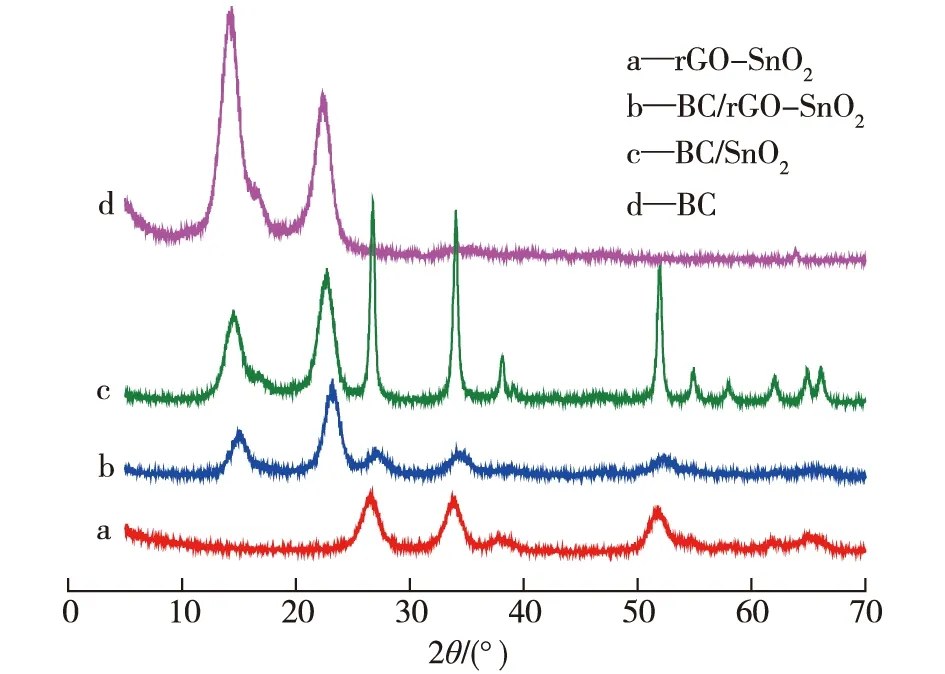
图2 rGO-SnO2、BC/rGO-SnO2、BC/SnO2和BC的XRD图谱Fig.2 XRD patterns of rGO-SnO2,BC/rGO-SnO2,BC/SnO2 and BC
2.3 扫描电镜(SEM)分析
图3为BC、BC/rGO-SnO2的SEM分析及BC/rGO-SnO2的能谱图。由图3可知:呈三维缠结网络结构的纳米纤维组成了BC膜,形成BC薄膜的单根纳米纤维的直径为30~100 nm;rGO-SnO2纳米复合物填充在细菌纤维素的间隙和孔洞中,使复合膜的表面结构更加致密,这是因为BC水凝胶具有天然多孔结构,因此以BC作为基质可以大量负载rGO-SnO2纳米复合物[8],而且rGO-SnO2纳米杂化物具有一定的团聚性;GO纳米片具有高密度的成核位点,这也导致了SnO2纳米颗粒在rGO片上大量的形成。BC/rGO-SnO2复合材料的能谱分析(EDS)结果表明,复合材料中含有C、O、Sn这3种元素,进一步证实了rGO-SnO2复合物的形成[9],而EDS图谱中出现的Au元素是复合材料进行扫描电镜前喷金处理引入的,Cl-的存在可能是rGO-SnO2复合物制备过程中未充分洗涤除去Cl-造成的。

图3 BC(a)、BC/rGO-SnO2(b、c、d) 的扫描电镜照片和BC/rGO-SnO2(e)的能谱图Fig.3 SEM images of BC(a)and BC/rGO-SnO2(b,c,d)and the EDS spectrum of the BC/rGO-SnO2 membrane(e)
2.4 热质量分析(TGA)
图4为GO和rGO-SnO2的TGA曲线。由图4可知:GO有2个主要的质量损失温度区,第一个快速失质量区(~20%)为室温到150 ℃,这可能是由于GO表面水分子的蒸发造成的;第二个快速失质量区(~18%)为150~200 ℃,这可能是由于GO表面含氧官能团的分解造成的[10]。与GO相比,rGO-SnO2纳米杂化复合物的热稳定性更高,rGO-SnO2的质量损失在200和400 ℃时分别只有6.5%和10.9%。

图4 GO和rGO-SnO2的TGA曲线Fig.4 TGA curves of GO and rGO-SnO2 under N2 atmosphere
2.5 复合材料的力学性能分析
表1显示了BC以及不同复合比率的BC/rGO-SnO2的力学性能。由表1可知:随着纳米填充物rGO-SnO2复合比率的增加,复合材料的拉伸强度和杨氏模量逐渐增大,当rGO-SnO2复合比率为5%时,拉伸强度和杨氏模量分别增加了15.9%和5.6%。当rGO-SnO2复合比率为15%时,拉伸强度和杨氏模量分别增加了48.2%和69.5%。这是因细菌纤维素纤维呈无规则的排布,导致纤维间空隙和孔洞的形成,当rGO-SnO2纳米复合物填充在细菌纤维素纤维的微孔当中,在纤维间起到了交联作用,从而增强了纳米复合材料的力学性能。
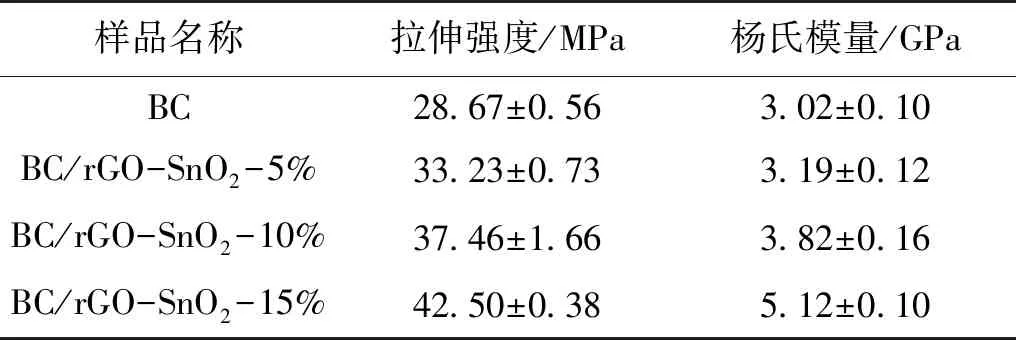
表1 BC及BC/rGO-SnO2的力学性能Table 1 Mechanical properties of BC and BC/rGO-SnO2
2.6 BC/rGO-SnO2复合材料膜的光催化性能
考察BC、BC/GO、BC/SnO2和BC/rGO-SnO2这4种材料对有机染料MO的光催化降解活性,结果如图5所示。由图5可知:MO的最大吸收波长为464 nm,随着UV照射时间的延长,BC/GO、BC/SnO2和BC/rGO-SnO2处理组MO溶液的峰值强度逐渐减小,说明MO在UV照射下被降解;BC/GO、BC/SnO2和BC/rGO-SnO2都具有不同程度的光催化性,与BC/GO和BC/SnO2相比,BC/rGO-SnO2具有更高的光催化活性,并且光催化效果随着光催化时间的延长而增强。这是因为石墨烯与半导体材料复合后,由于石墨烯良好的导电性能和巨大的比表面积,促进了光生电子和光生空穴的有效分离,抑制了电子-空穴复合反应的进行,因此提高了催化剂的光催化效率[11-12]。由于有效的电荷分离和转移,石墨烯纳米片的存在大大提高了金属氧化物在紫外光照射下降解MO的光催化活性,大约有93.4%的MO在2 h内被BC/rGO-SnO2纳米复合材料降解(图5(d)),这说明BC/rGO-SnO2对MO有较好的降解作用。光催化降解通常发生在光催化产物的表面,因此表面积是光催化的一个重要参数。此外,MO的降解遵循式(1)所描述的拟一阶反应动力学[13]。
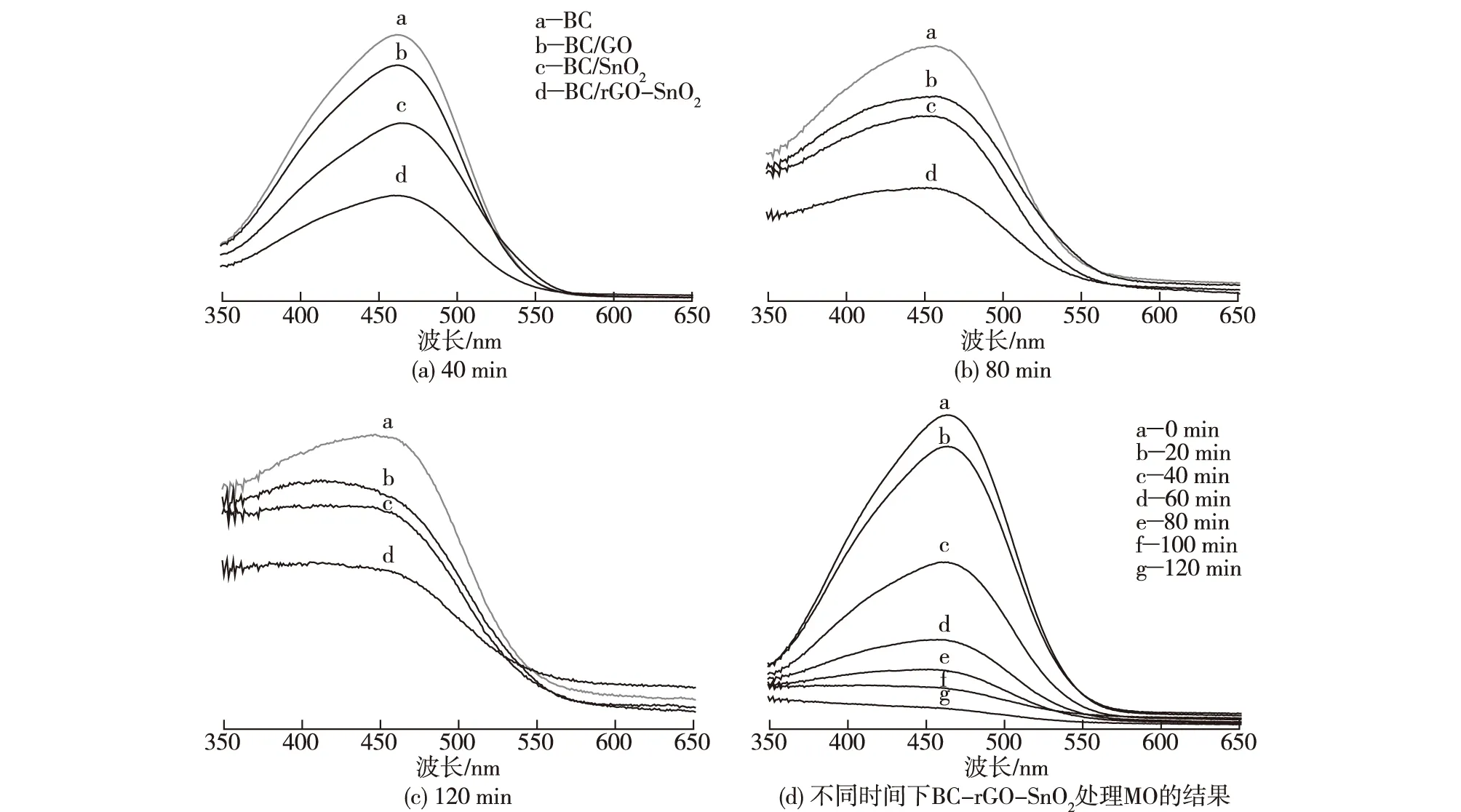
图5 纳米复合材料处理MO溶液在紫外线照射不同时间后的紫外-可见光谱及BC/rGO-SnO2处理MO溶液在紫外照射不同时间后的紫外-可见光谱Fig.5 UV-visible spectra of MO solution treated with nanocomposites at different UV-irradiation time,and photodegradation of MO with BC/rGO-SnO2
(1)
式中:c0和c分别对应于MO溶液的初始浓度和在t时刻的测量浓度,k为光降解速率常数。
由此计算得到BC/rGO-SnO2纳米复合材料降解MO的光降解反应的速率常数k为0.023 2 min-1。
2.7 BC/rGO-SnO2复合材料的光催化抑菌实验
以金黄色葡萄球菌作为测试菌株,将BC、BC/SnO2和BC/rGO-SnO2复合材料放入菌液中,紫外光催化6 h(预实验结果证明,在没有复合材料的培养基中,紫外线照射后金黄色葡萄球菌的CFU并没有明显的下降,这说明在低能量的UV-A光照下,光化学失活可以忽略不计),对BC/SnO2和BC/rGO-SnO2光催化复合材料的光催化抑菌性进行测定,结果如图6所示。由图6可知:与对照组相比,BC/SnO2和BC/rGO-SnO2组在紫外光诱导下的菌体活力都有不同程度的降低,复合比率为5%、10%和15%的BC/rGO-SnO2组菌体死亡率分别为24.77%、31.94%和52.12%,由此可见,随着rGO-SnO2纳米复合物复合比率的增加,其抑菌能力逐渐增强,复合比率为5%、10%和15%的BC/SnO2组的抑菌率分别为9.71%、12.26%和17.76%。BC/rGO-SnO2组的抑菌效果要优于BC/SnO2组,这与BC/rGO-SnO2组的光催化活性高于BC/SnO2组的结果一致,说明复合材料的光催化性能直接影响着它的光催化抑菌能力[14-15]。

图6 BC、BC/SnO2和BC/rGO-SnO2复合材料对S. aureus的光催化抑菌性Fig.6 Photocatalytic antibacterial activity of BC,BC/SnO2 and BC/rGO-SnO2 composites against S. aureus
2.8 BC/rGO-SnO2复合材料对微生物细胞内活性氧(ROS)的影响
为了探究BC/rGO-SnO2复合材料的抑菌机制,以S.aureus为对象测定紫外光照射6 h后、BC/rGO-SnO2材料处理后细胞内ROS[16]的含量,结果如图7所示。由图7可知:与对照组的结果相比,黑暗处理组的荧光强度无明显变化。在光照条件下,复合比率为5%、10%和15%的BC/rGO-SnO2材料在紫外光催化6 h后ROS的荧光强度分别为对照组的1.83、2.52和3.85倍,S.aureus胞内ROS的荧光强度与细菌死亡率的趋势一致。但随着rGO-SnO2纳米复合物复合比率的增加,BC/rGO-SnO2复合材料的光催化能力增强,复合材料处理后S.aureus胞内ROS的荧光强度逐渐增强,说明细菌的死亡率逐渐增加。由此初步推断:BC/rGO-SnO2复合材料在紫外光诱导下产生ROS,导致细菌受到氧化胁迫,造成细菌的氧化损伤,进而引起菌体的死亡[17-18]。
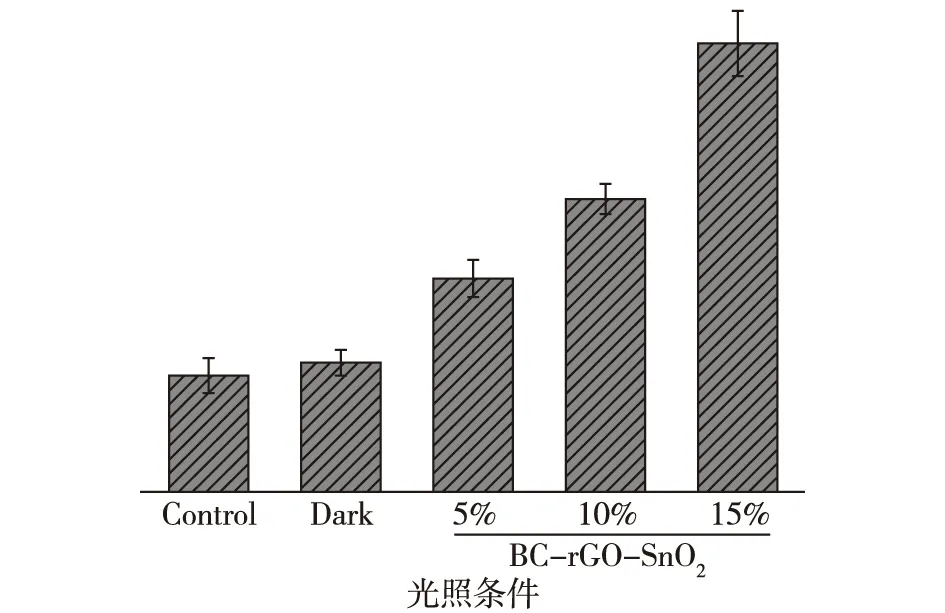
图7 S. aureus胞内ROS的荧光强度(光照6 h)Fig.7 Fluorescence intensity of intracellular ROS inS. aureus by contacting with 5%,10%,15% BC/rGO-SnO2 composites under UV-A light for 6 h
3 结论
通过TEM、XRD、SEM和TGA等技术手段对制备得到的BC/rGO-SnO2复合材料进行分析,结果发现:蠕虫状的平均粒径为4.5 nm 的SnO2NPs均匀地沉积在rGO薄片上,形成了rGO-SnO2纳米复合物;在rGO纳米片上原位合成的SnO2的颗粒粒径较小,结晶性差。SEM结果表明,rGO-SnO2纳米复合物填充在细菌纤维素的间隙和孔洞中,使复合膜的表面结构更加致密;与GO相比,rGO-SnO2纳米杂化复合物的热稳定性更高。rGO-SnO2纳米复合物填充在BC纤维的空隙和孔洞当中,在纤维间起交联作用,因此BC/rGO-SnO2复合材料的力学性能增强.
同时以具有光催化能力的SnO2NPs来修饰GO后负载在BC纤维中得到BC/rGO-SnO2纳米材料。复合材料在近紫外光催化下表现出较强的抑菌活性,这是因为BC/rGO-SnO2复合材料在紫外光诱导下产生大量的ROS导致细菌受到氧化胁迫,造成细菌的氧化损伤,进而引起菌体的死亡。
由此,BC/rGO-SnO2纳米复合薄膜不仅可以保持BC本身优异的材料性能,而且还附加了功能化氧化石墨烯和金属氧化物纳米粒子的抗菌特性及光催化性能,还具有优异的力学特征,为BC在抑菌、环境等领域的应用提供了新的思路。
