天然黏土矿物和腐殖酸对纳米乳化油吸持的实验研究
2022-07-19郭玉茹何宝南何江涛刘子榕王诗语
郭玉茹,何宝南,何江涛,刘 韬,刘子榕,王诗语
(中国地质大学(北京) 水资源与环境学院 水资源与环境工程北京市重点实验室,北京 100083)
作为一种新型缓释液态碳源(Leeetal., 2019; Dingetal., 2020),纳米乳化油因具有廉价、无毒、缓慢释放电子以及有效寿命长等优点(Dingetal., 2021),而被广泛应用于原位生物修复地下水硝酸盐、氯酸盐、高氯酸盐、六价铬、铀污染等(Bordenetal., 2019; Dongetal., 2019; Sarriaetal., 2019; Dingetal., 2020)。然而在实际场地修复过程中,受乳化油注入的影响,常出现含水层渗透性下降或堵塞的现象,从而导致修复效率降低(Coulibaly and Borden, 2004)。调研发现,除原位生物修复过程中微生物的增值代谢(Wenetal., 2017)以及产气(Borden, 2007)等造成的生物堵塞外,乳化油自身在孔隙介质中的滞留对渗透性的影响也不容忽视。对乳化油自身滞留行为的了解是进一步回答微生物效应的重要基础。
有研究显示乳化油滞留可造成砂质沉积物达40%的渗透性损失,且该损失与滞留比例呈显著正相关关系(Coulibaly and Borden, 2004)。为有效应对这一问题,何宝南等(2018)进行了纳米乳化油缓解多孔介质渗透性损失的实验研究,结果发现乳化油粒径大于多孔介质孔径产生的物理截留是乳化油滞留的一个重要原因,对此将乳化油粒径从微米降低至纳米级,极大程度上缓解了渗透性损失。然而,该结果是在纯石英砂的理想介质条件下获取的。相比之下,实际场地中除石英砂介质外,还存在大量的黏土矿物和有机质等(Jungetal., 2006; Coulibalyetal., 2006),而矿物和有机质会对乳化油产生吸附、凝聚及表面络合等作用,即吸持作用。Coulibaly等(2006)通过一维柱实验,发现高岭石的加入抑制了乳化油的迁移,并且随着高岭石含量的增加,抑制率会提高。Al-Maghrabi等(2016)发现黏土矿物会对乳化油产生附着作用。 Wu等(2015)和Saeedi等(2018)则发现腐殖酸及黏土矿物的复合会对吸附有机污染物产生促进作用。Wang和Xing(2005)的研究也发现,腐殖酸的加入对黏土矿物吸附有机污染物的行为及特征会产生影响。由此可以看出,环境介质组成也是影响乳化油滞留的一个重要因素,高岭石、蒙脱石和腐殖酸等天然黏土矿物和有机质的存在,在一定程度上增强了乳化油在多孔介质中的滞留作用。然而,天然黏土矿物及有机质对乳化油的吸持性能与作用机制到底如何,与物理截留作用相比,影响程度大小还不得而知。
为此,本研究选取典型的天然黏土矿物高岭石、蒙脱石和典型的天然有机质腐殖酸,开展了天然黏土矿物及有机质对纳米乳化油吸持的批实验研究,并对比单一黏土矿物(高岭石、蒙脱石)、有机质(腐殖酸)以及有机矿质复合体组分(高岭石-腐殖酸、蒙脱石-腐殖酸)对纳米乳化油的吸持情况,辅以比表面积全分析、扫描电镜(SEM)、X射线衍射(XRD)及红外光谱(FTIR)等表征手段,揭示吸持作用机理,为科学评估纳米乳化油原位修复过程中在多孔介质中的滞留行为提供基础依据。
1 材料与方法
1.1 实验材料
天然黏土矿物高岭石购于国药集团化学试剂公司,化学纯,CAS号: 1335-58-7;蒙脱石购于国药集团化学试剂公司,化学纯,CAS号: 1318-93-0;腐殖酸购于国药集团化学试剂公司,化学纯,CAS号: 1415-93-6;
纳米乳化油制备所需材料有市售金龙鱼大豆油、吐温80及斯盘80(食品级乳化剂),购于天津光复化工研究院。
1.2 实验方法
1.2.1 纳米乳化油制备
本实验所用纳米乳化油根据何宝南等(2018)的方法制备而成,将大豆油、吐温80、斯盘80和去离子水按照一定比例混合,然后以1 500 r/min的转速电动增力搅拌10 min,再借助升温相转变技术,超声仪超声处理25 min(温度55℃),静置48 h无破乳分层现象,则得到稳定的纳米乳化油,平均粒径大小为255.1 nm,稳定性动力学指数为0.5。
1.2.2 纳米乳化油浓度测试方法
纳米乳化油作为一种乳浊液,其浓度没有一个定量的表达,本文通过对有机碳含量的测定来表征其浓度。将纳米乳化油原液以不同浓度梯度进行稀释(400~3 000倍),得到不同体积分数的纳米乳化油,分别利用浊度仪与TOC仪测定各体积分数的纳米乳化油对应的浊度和浓度,建立浊度与浓度的关系曲线(y=1.079x+3.338,R2=0.999),以通过测定浊度来表征纳米乳化油浓度的大小。
1.2.3 固液比确定实验
分别用高岭石、蒙脱石和腐殖酸做固液比确定实验。设置纳米乳化油初始浓度为800 mg/L和70 mg/L分别代表高、低两种浓度条件,设置固液比(g/mL)为1∶150、1∶200、1∶250、1∶300、1∶350、1∶400及1∶450,准确称取相应质量样品于30 mL血清瓶中,每组均设置3个平行样,在恒温空气浴振荡器(25℃,175 r/min)中振荡48 h,取10 mL上清液,过0.45 μm滤膜,测试纳米乳化油浓度。固液比选取满足一定的吸持量且剩余量易于测试,最终固液比确定为1∶400,即0.075 g样品∶30 mL溶液。
1.2.4 吸附动力学实验
准确称取0.075 g高岭石、蒙脱石、腐殖酸于30 mL血清瓶中,加入400 mg/L的纳米乳化油,在恒温空气浴振荡器(25℃,175 r/min)中振荡,分别在0、2、4、6、8、10、12、16、24、32、48 h取10 mL上清液,过0.45 μm滤膜,测试纳米乳化油浓度,每个时间点均设有3个平行样。
1.2.5 等温吸附实验
准确称取0.075 g高岭石、蒙脱石、腐殖酸、高岭石-腐殖酸、蒙脱石-腐殖酸(复合物按质量比1∶1机械混合)于30 mL血清瓶中,加入不同初始浓度梯度(30、50、100、200、400、600、800、1 000 mg/L)的纳米乳化油30 mL,在恒温空气浴振荡器(25℃,175 r/min)中振荡24 h,取10 mL上清液,过0.45 μm滤膜,测试纳米乳化油浓度,每组均设置3个平行样。
1.3 分析测试
比表面积、孔径和孔体积表征: 采用BET氮气吸附法,通过全自动快速物理吸附分析仪(ASAP 2460,美国)测定,分析浴温度设置为-196 ℃,反应平衡时间为10 s。
Zeta电位表征: 由Zeta电位仪(Zetasizer Nano-Zs90,英国)测定,观察吸附剂与吸附质的带电情况,分析其静电相互作用。测量范围为1 nm~5 μm,测量角度为90°。
表面微观形貌表征: 扫描电子显微镜(SU8020,日本)用于观察样品吸持纳米乳化油前后,表面微观形貌的变化。测试条件的压强控制在1×105Pa,温度为21±0.5℃,湿度为46±1%。
官能团表征: 红外光谱(FTIR)的测定,由红外光谱仪(Nicolet IS10,美国),按1∶200的样品KBr比,采用压片法定性分析测得,测定分辨率为4.0 cm-1,测定波数为400~4 000 cm-1,分析反应前后官能团的变化及化学反应等。
晶体结构表征: X射线衍射(XRD)扫描,由X射线粉末衍射仪(D8 ADVANCE,德国)测试,衍射靶为铜靶,扫描速率为6°/min,扫描角度范围为5°~90°,矿物的晶面层间间距值由布拉格方程(2dsinθ=nλ)计算,观察吸持前后样品结构是否发生变化。
1.4 数据处理
1.4.1 吸附动力学拟合
对吸附动力学结果采用准一级(2)、准二级(3)以及颗粒内扩散方程(4)进行拟合:
qe=(Co-Ce)V/m
(1)
log(qe-qt)=logqe-k1t/2.30 (2)
(3)
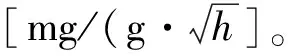
1.4.2 等温吸附拟合
等温吸附实验数据用Freundlich模型进行拟合:qe=KF·CeN(5)
式中:KF为Freundlich常数[(mg·g-1)/(mg·L-1)N],与吸附容量和吸附亲和力有关;N为指示等温吸附特性的参数。
不同平衡浓度下样品对纳米乳化油的分配系数Kd(L/kg)按下式计算:
Kd=qe/Ce=KF·CeN-1
(6)
1.4.3 吉布斯自由能
通过自由能的计算,可以判断纳米乳化油吸附反应的自发性以及吸附类型(Shin and Kim, 2016; Yangetal., 2019):
ΔG=-RTlnKd
(7)
式中,ΔG为吉布斯标准自由能(kJ/mol);R为理想气体常数8.314 J/(mol·K);T为热力学温度(K)。
1.4.4 理论叠加值以及协同率计算
假设样品在复合过程中,没有发生任何作用和反应,则纳米乳化油在复合体系中的吸持量应该等于纳米乳化油在对应质量比例的单一样品吸持量之和,即理论叠加值qe,cal:
qe,cal=0.5KF1·CeN1+0.5KF2·CeN2(8)
定义复合体系Freundlich拟合值和理论叠加值的差值与理论叠加值的比值为协同率r:
r=(qe,F-qe,cal) /qe,cal
(9)
式中,KF、N在单一样品吸持纳米乳化油时,按Freundlich方程拟合得到;qe,F为复合体系Freundlich拟合值。
2 结果与讨论
2.1 天然黏土矿物和腐殖酸对纳米乳化油的吸持特征
2.1.1 天然黏土矿物和腐殖酸对纳米乳化油的吸附动力学
高岭石、蒙脱石和腐殖酸对纳米乳化油的吸附动力学如图1所示,在起初的2 h,吸附量迅速增加,可达76%~81%,为快速吸附阶段;在2~16 h呈现出上下波动的态势,吸附速率逐渐减缓,为慢速吸附阶段; 24 h之后基本稳定,达到吸附平衡。准一级、准二级以及颗粒内扩散方程对纳米乳化油吸附动力学的拟合结果(表1)显示,准二级动力学方程拟合的实测值(qe,exp)与拟合值(qe,cal)非常接近,R2达0.99以上,说明纳米乳化油在高岭石、蒙脱石和腐殖酸上的吸附符合准二级动力学方程,吸附是一个物理化学过程,主要受化学键以及吸附剂与吸附质之间的电子共用或电子转移的影响(Jiaetal., 2018)。
2.1.2 纳米乳化油的等温吸附特征
高岭石、蒙脱石和腐殖酸单一体系以及复合体系对纳米乳化油的等温吸附结果如图2a所示。等温吸附拟合结果显示,单一及复合体系的吸附均符合Freundlich模型。样品的分配系数Kd计算结果(图2b)显示,在单一体系中,吸持能力大小为: 蒙脱石>腐殖酸>高岭石;复合体系中: 蒙脱石-腐殖酸>高岭石-腐殖酸,且均大于其所对应的单一样品,出现了“1+1>2”的现象,复合体系的实测值和理论叠加值结果进一步显示了这一特征(图2c、2d)。为量化复合体系对吸持的影响,依据公式(9)计算协同率r(图3),协同率越高代表其促进作用越显著,高岭石-腐殖酸随着纳米乳化油初始浓度的升高,促进作用增强 (r=-7%~32%),在乳化油浓度为30 mg/L时,表现为抑制作用,与整体规律相反,可能是由于实验误差所致。蒙脱石-腐殖酸与之相反,随着纳米乳化油浓度的升高,促进作用减弱(r=15%~76%),即便如此,从整体上看腐殖酸对蒙脱石吸持纳米乳化油的促进作用依然更强。以上现象表明,介质组成越复杂,对纳米乳化油的吸持滞留程度就会越大。除此之外,还说明腐殖酸与高岭石和蒙脱石之间发生了一定的相互作用,并且这种相互作用存在差异。
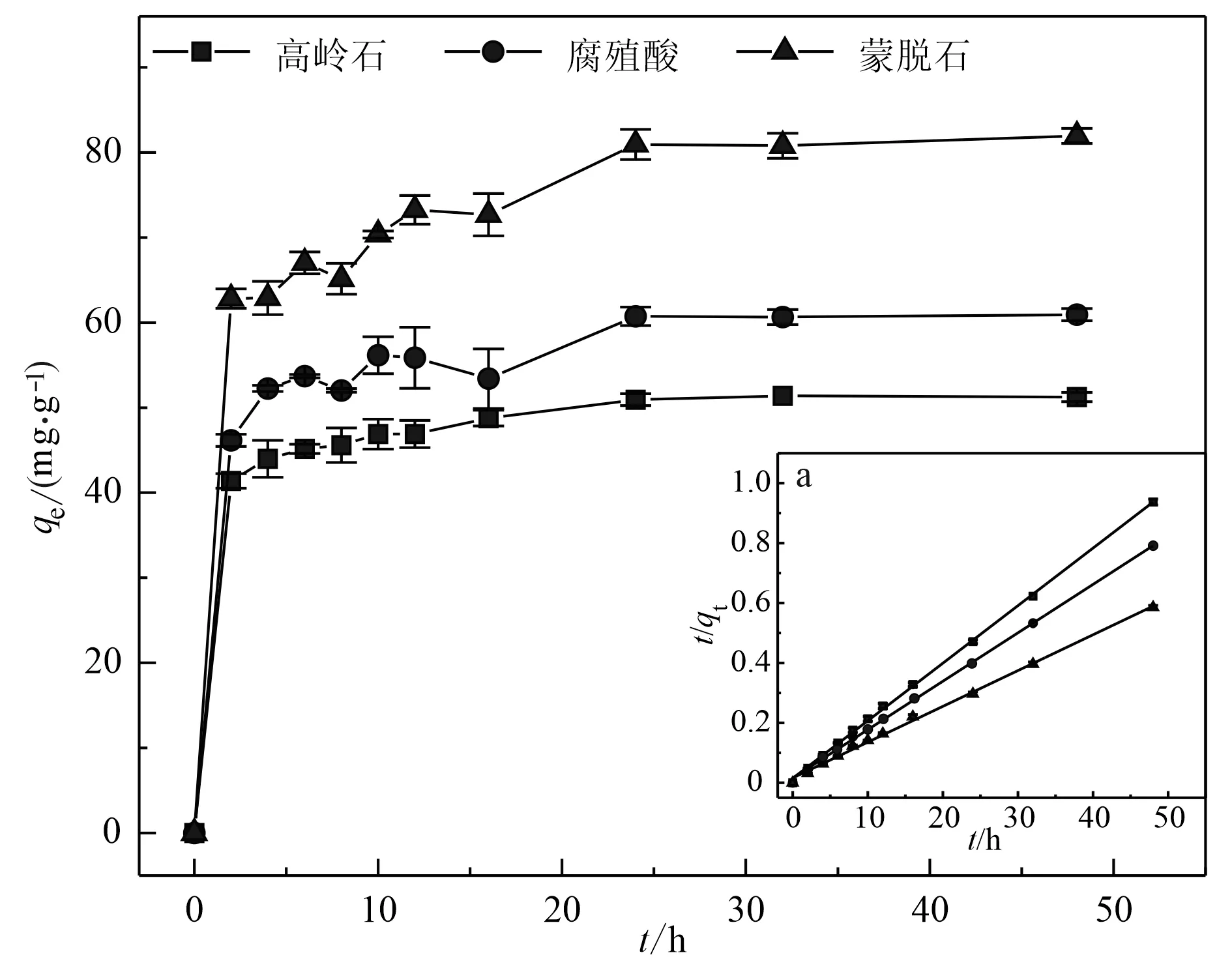
图1 纳米乳化油在样品上的吸附动力学(a: 准二级动力学拟合)Fig.1 Adsorption kinetics of nano emulsified oil on single samples (a: fitted with pseudo-second-order kinetic)
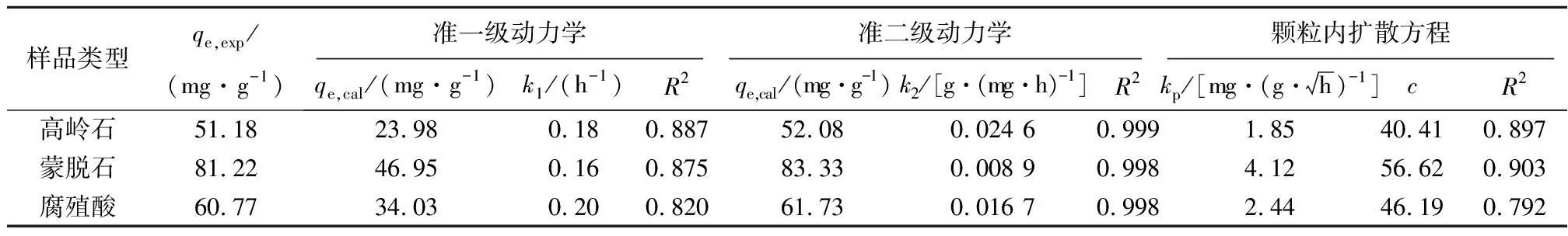
表1 动力学方程拟合参数Table 1 Fitting parameters of sorption kinetic equation
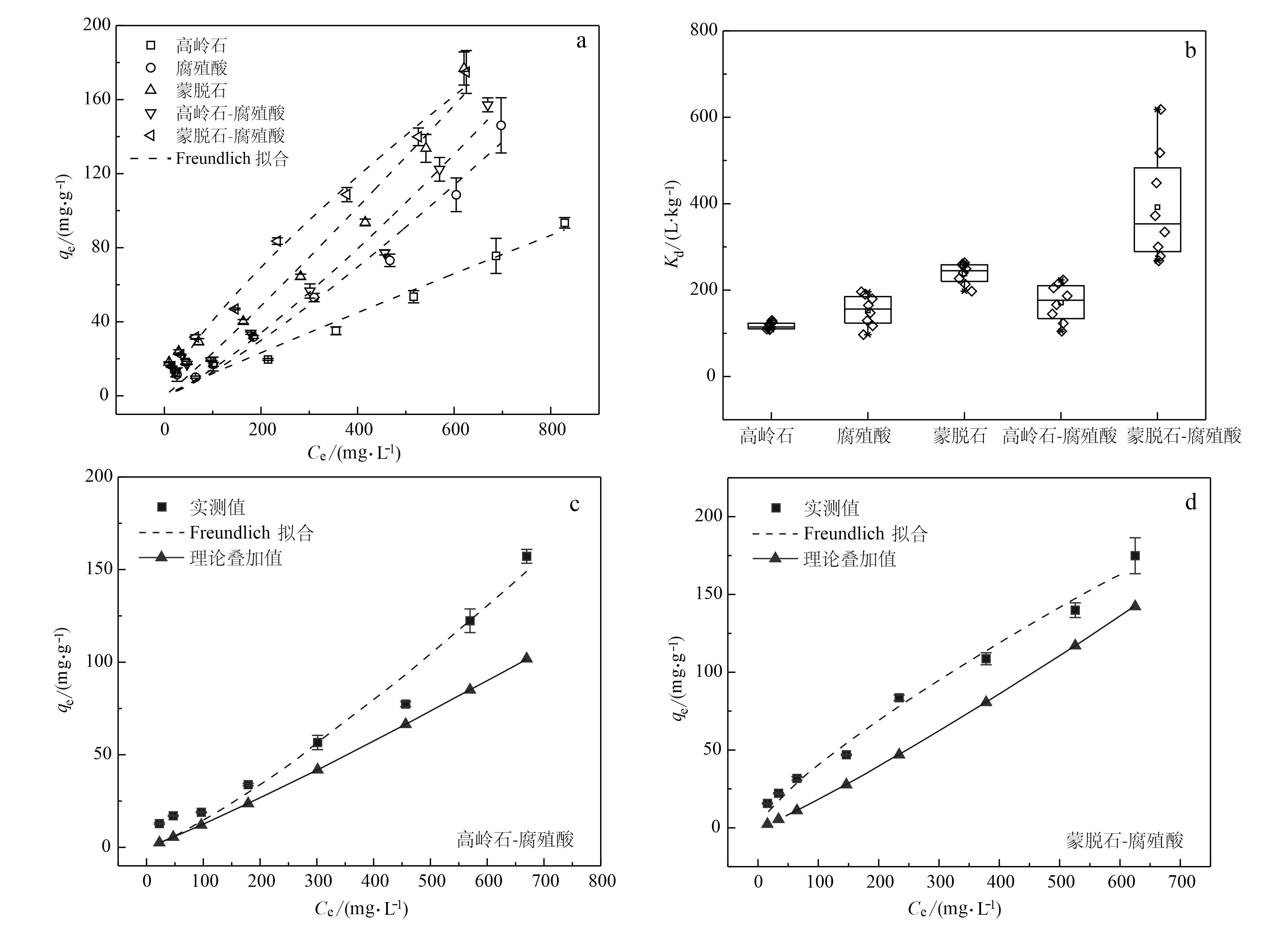
图2 样品对纳米乳化油的等温吸附结果(a)、样品的Kd值(b)、样品对纳米乳化油的吸持实测值与理论叠加值对比(c、d)Fig.2 Isotherms adsorption results of nano emulsified oil on samples (a), Kd values of samples (b) and comparison between actual and overlay values of nano emulsified oil sorption on samples (c, d)
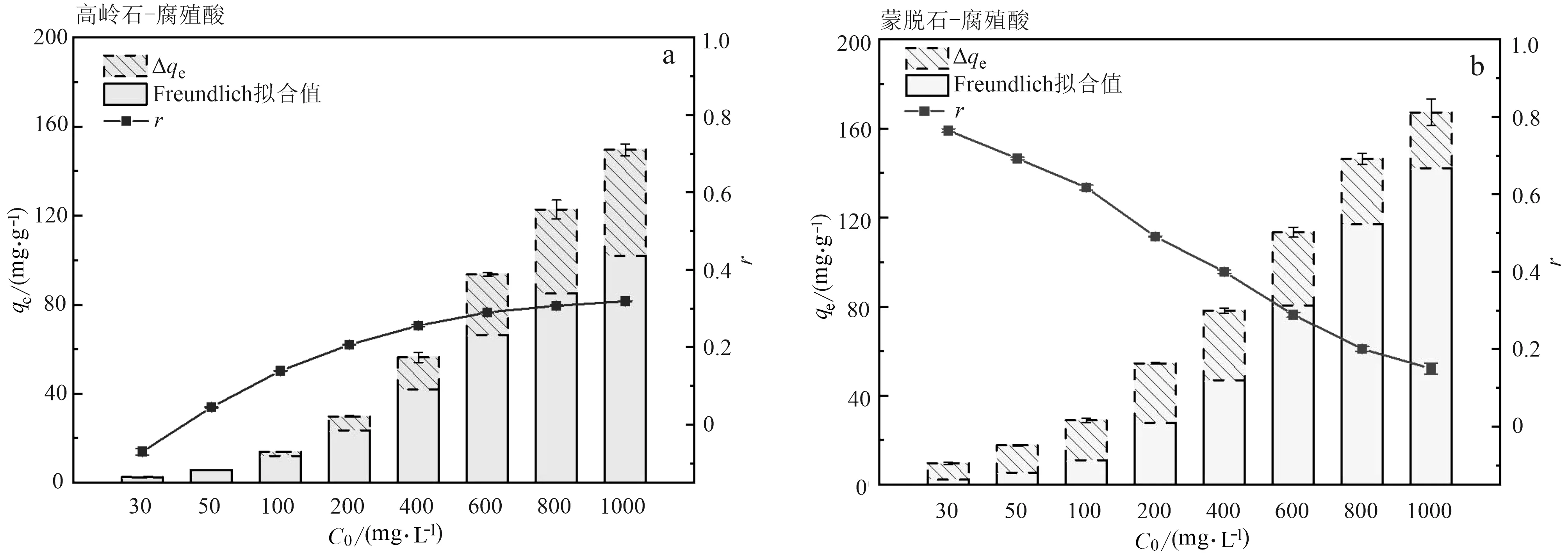
图3 复合样品协同率变化Fig.3 Change of synergetic efficiency of composite samples
为进一步说明天然黏土矿物及腐殖酸对纳米乳化油吸附反应的自发性及类型,在上述基础上,计算样品的热力学参数吉布斯自由能ΔG。结果显示,所有样品的ΔG均在-15.9~-11.3 KJ/mol范围内,为负值,表明吸附是自发的热力学过程(Yangetal., 2019)。一般认为,-40~-5 KJ/mol以物理吸附为主,-800~-40 kJ/mol以化学吸附为主(Shin and Kim, 2016),由此在动力学结果的基础上进一步可以看出,吸附过程是以物理吸附为主导的物理化学过程。
2.2 表面结构性质对吸持纳米乳化油的影响
吸持剂表面性质及结构是影响其吸持性能的重要因素,为探讨这一因素对纳米乳化油吸持的影响,采用扫描电镜及孔结构分析等手段表征了黏土矿物及腐殖酸吸持纳米乳化油前后的表面形貌特征。在高岭石、蒙脱石和腐殖酸的单一体系中(图4a),吸持后,一些孔隙被填平,结构更加紧密。有研究显示,黏土矿物中比表面积对吸持起着重要作用,比表面积越大,其吸持能力相应越强(Saeedietal., 2018)。从表3结果可以看出,蒙脱石的比表面积最大,与等温吸附结果中蒙脱石的Kd值最大一致,说明比表面积对蒙脱石的吸持起主导作用。然而表征结果显示,高岭石相较于腐殖酸具有更大的比表面积,但吸持结果却显示腐殖酸的吸持能力要强于高岭石,表明腐殖酸吸持除比表面积外还有其他主导因素。这和纳米乳化油及腐殖酸的粒径范围均属于纳-亚微米、二者更多地表现为与颗粒聚集作用有关。
相比于单一体系,高岭石、蒙脱石和腐殖酸复合后,其颗粒大小及表面形貌(图4b)、孔体积与孔径的值(表3)均更接近于黏土矿物,说明复合体是以黏土矿物为框架,腐殖酸相对均匀和分散地分布在黏土矿物表面(Zhuetal., 2016)。但对于表面电性和孔结构来说,单一及复合体系与纳米乳化油的Zeta电位(-13.1±1.6 mV)均为负,存在静电斥力;纳米乳化油的粒径(50~500 nm) (Heetal., 2018)远大于样品的平均孔径,表明表面电性和孔结构均不是影响其吸持的主要因素。值得注意的是,复合体系的比表面积均有减小,但实际结果表明其吸持能力不减反增,进一步表明天然黏土矿物与腐殖酸混合后发生了相互作用,这种作用与腐殖酸的性质息息相关。
2.3 晶体结构对纳米乳化油吸持的影响
吸持可能会影响吸持剂的结构,分析结构变化可以为揭示吸持机理提供依据。对于高岭石(图5a),强衍射峰2θ=16.400°和2θ=26.171°分别指向(110)和(210)晶面(Wangetal., 2020),吸持纳米乳化油后,峰的位置和形状均没有变化,在检测范围内,没有新的衍射峰出现,晶体结构没有发生改变,说明纳米乳化油并没有进入高岭石层间,只是附着在高岭石的基面和边缘表面(Jeevaetal., 2019)。
蒙脱石的特征衍射峰2θ=5.857 °指向(001)晶面(图5b),根据布拉格方程,计算此时的d(001)=1.5 nm。可根据d(001)值来判断蒙脱石的类型,一般认为,d(001)在1.2~1.3 nm为钠基蒙脱石,1.3~1.4 nm为钙钠基蒙脱石,1.5~1.6 nm为钙基蒙脱石(Li and Wu, 2010)。可以看出,本实验为钙基蒙脱石。吸持后,检测范围内同样没有观察到新的衍射峰,其中晶面衍射d(001)衍射峰出现了小幅度的左移,出现在2θ=5.311°的地方,此时的层间距平均距离为1.664 nm,与吸持前相比增加了0.164 nm。蒙脱石的两个相邻晶层之间没有氢键,单位晶层之间结合力微弱,水分子进入了蒙脱石片层间,从而引起晶格膨胀(徐玉芬,2008; Wuetal., 2015)。纳米乳化油未进入层间,结合在蒙脱石表面。

图4 样品吸持纳米乳化油前后的SEM图Fig.4 SEM images of samples before and after sorption of nano emulsified oil
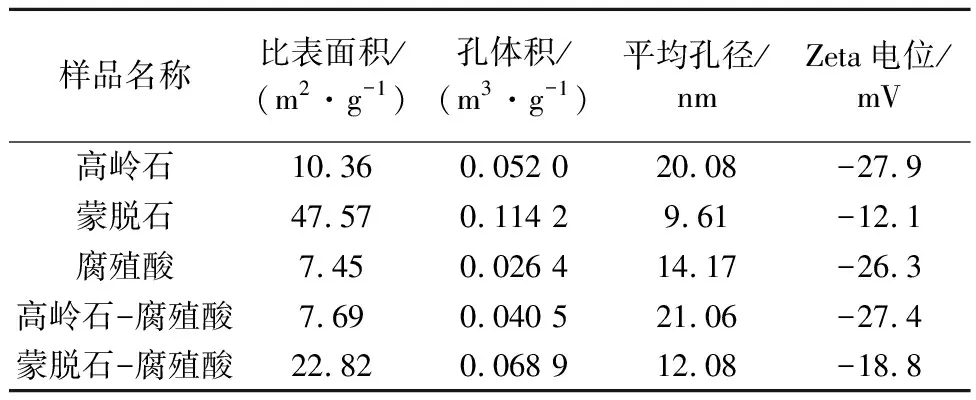
表3 样品的表面结构性质Table 3 The surface structure and properties of samples
复合体系相较于单一体系,其特征衍射峰几乎无偏移(图5),高岭石的层间氢键作用大,活性小(Chenetal., 2017),腐殖酸分子很难进入;而蒙脱石-腐殖酸的d(001)层间间距仅从1.5 nm增加到1.55 nm,表明腐殖酸分子仅少部分插入蒙脱石的Al—Si层,腐殖酸主要结合在矿物的边缘和外表面上。在吸持后,无新衍射峰出现,说明纳米乳化油主要吸持在复合体系的表面,未进入层间。
2.4 官能团对纳米乳化油吸持的影响
采用傅里叶红外光谱表征官能团对纳米乳化油吸持的影响(图6),各波数代表的化学键见表4。高岭石的 Al—OH、骨架外 Si—O—Al 以及骨架内Si—O—Al 这3个弯曲振动吸收峰在吸持前后分峰明显,峰形尖锐,位置形状均无明显变化,说明底面羟基基团结构比较完善(徐玉芬,2008; 魏青峰等,2019),纳米乳化油分子未进入高岭石层间。高岭石的羟基(3 442 cm-1)在吸持后少量富集,表明乳化油的羧基与高岭石的羟基形成氢键(Wangetal., 2020)。1 099 cm-1处指示高岭石Si—O伸缩振动(王菲等,2016)以及脂肪酸CO伸缩振动(Koliastasietal., 2020),吸持纳米乳化油后,吸光度变大,表明该处官能团的含量升高,而大豆油分子式为C56H100O6(连玉倩等,2018),属于长链脂肪酸,疏水性强,纳米乳化油应是通过疏水作用结合在高岭石表面。
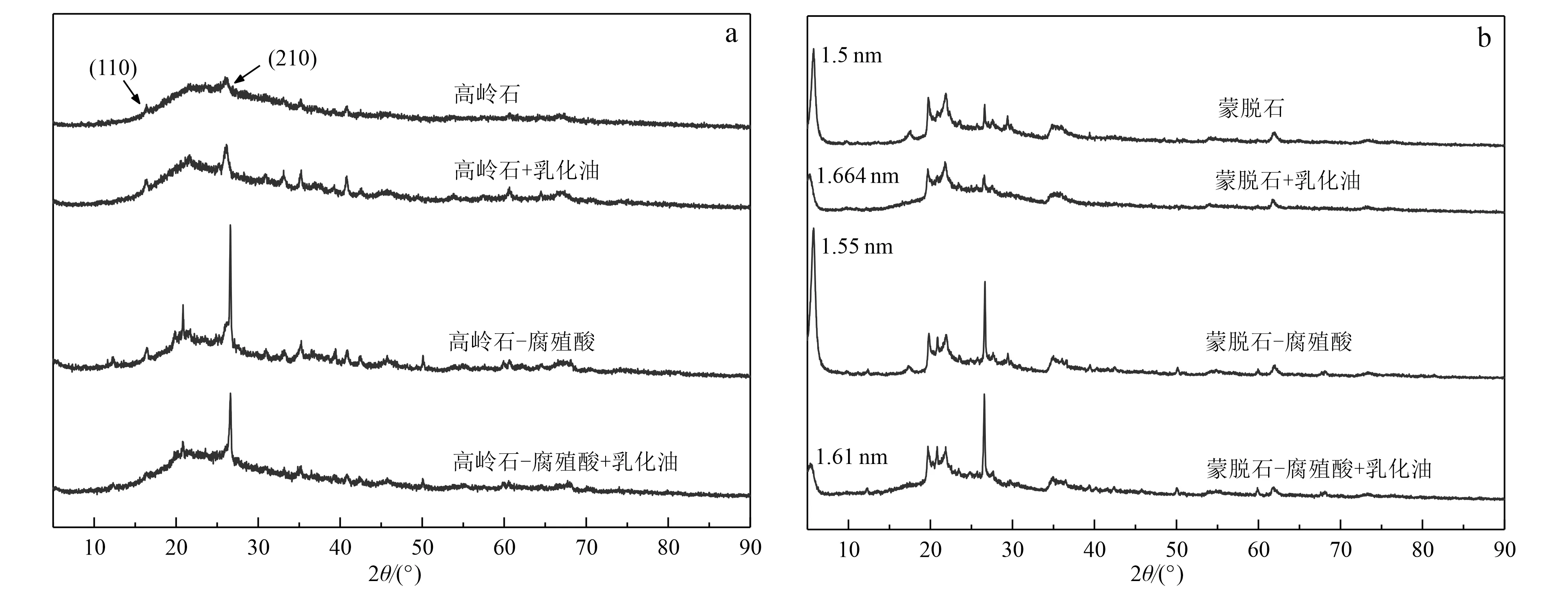
图5 高岭石、蒙脱石及复合体系吸持前后的XRD图谱Fig.5 XRD patterns of kalinite, montmorillonite and composite samples before and after the sorption of nano emulsified oil
蒙脱石的Si—O—Si伸缩振动以及Si—O—Al和Si—O—Fe弯曲振动吸收峰(魏青峰等,2019),在吸持纳米乳化油前后位置、形状及强度均未发生显著变化,说明整个吸持过程对蒙脱石的基础结构影响不大。吸持后,纳米乳化油的特征峰(1 741、2 925 cm-1)无显著变化与偏移,表明以物理吸持为主。蒙脱石结构羟基吸持前后强度几乎无变化,说明吸持过程对层间结构水分子影响不大。但游离水分子的羟基强度减弱,说明脱去了部分层间吸附水,蒙脱石表面的疏水性增强(张小亮等,2013),其羟基与纳米乳化油的羧基形成了氢键,使其附着在蒙脱石表面。
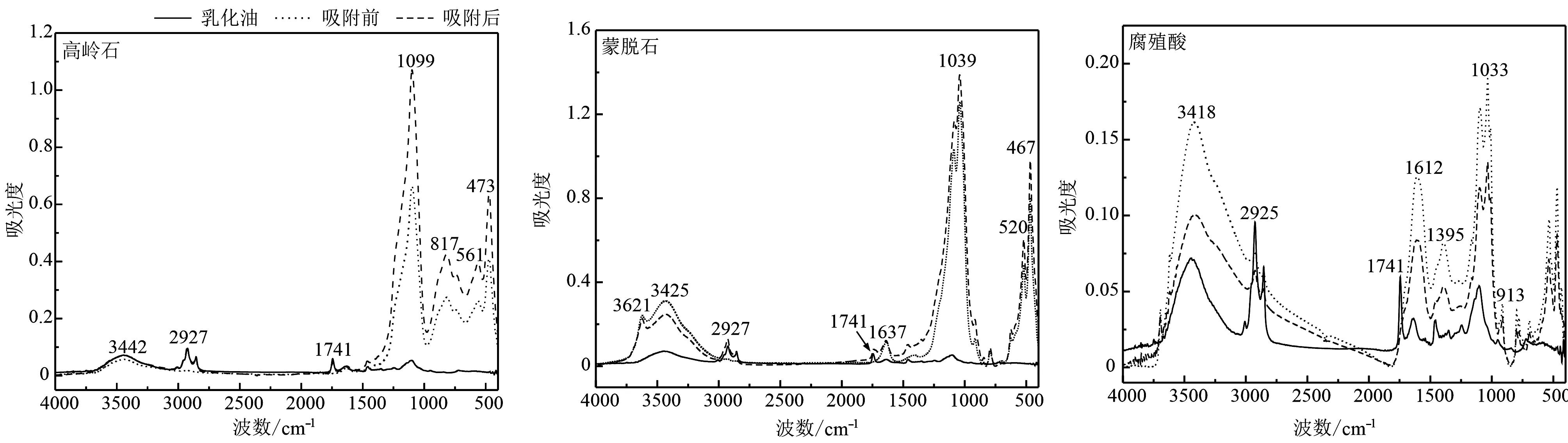
图6 单一样品吸持前后的FTIR图谱Fig.6 FTIR spectra of single samples before and after the sorption of nano emulsified oil
从表4可以看出,腐殖酸的主要结构单元有烷烃、芳香族与脂肪族化合物以及含氧官能团(羧基、羟基等)。在吸持纳米乳化油后,其特征峰的位置及形状基本无变化,说明整个吸持过程以物理作用为主。1 033 cm-1处CO键强度明显降低,指示腐殖酸表面极性降低,纳米乳化油的疏水基团与腐殖酸脂肪族、芳香族的疏水作用(夏绮文等,2020)增强。腐殖酸—OH的减少,表明与乳化油的羧基发生了氢键的结合,颗粒间分子作用力较强,主要为吸持作用,进一步印证了比表面积不是其吸持的主导因素。

表4 样品的红外光谱吸收峰位置Table 4 FTIR spectra absorbance peaks of samples
高岭石-腐殖酸复合组分的红外光谱如图7a所示,3 418 cm-1处的峰变宽,强度增加,表明分子间稳固的—OH增多。2 925 cm-1(脂肪族中C—H)、1 612 cm-1(芳环骨架中CC)以及1 395 cm-1(甲基C—H)处峰的增强,证明腐殖酸复合在高岭石的表面(黄仁龙等,2017),形成逐层叠加的腐殖酸“膜”(魏青峰等,2019),主要通过氢键及疏水作用结合(Fengetal., 2005)。此时在同一吸持位点上,纳米乳化油更多接触到腐殖酸,吸持后(图7b)各个官能团振动强度整体降低,变化规律接近于腐殖酸,吸持过程更多由腐殖酸主导。羟基和羧基峰强度的降低,表明与纳米乳化油发生了配体交换反应。小分子腐殖酸会代替高岭石表面的水分子,使得高岭石表面的疏水性增强(魏世勇等,2009),对吸持起到促进作用。纳米乳化油可以通过氢键或疏水作用结合在腐殖酸的表面,而腐殖酸又可以附着在高岭石上,增加的附着量也可归因于部分乳化油与腐殖酸结合后共吸附和累积吸附于高岭石表面。随着纳米乳化油初始浓度的升高,更多的乳化油与腐殖酸结合,共吸附和累积吸附作用增强,使高岭石-腐殖酸吸附的促进作用更强。
从蒙脱石-腐殖酸的红外光谱图(图7c)可以看出,1 629 cm-1处峰强增加并且出现蓝移,表明腐殖酸与蒙脱石产生了一定的反应,使得其CC变得不稳定,结构松散(黄仁龙等,2017)。3 350 cm-1~3 650 cm-1为水分子—OH伸缩振动,强度减弱,表明腐殖酸的负电基团与蒙脱石的羟基发生了配体交换反应(Zhangetal., 2012)。吸持后的红外光谱图(图7d)强度整体变化不大,915 cm-1指示羧酸或羧酸二聚体成键的—OH键的面外弯曲振动峰,此处吸收峰强度的增加,表明蒙脱石-腐殖酸与纳米乳化油发生了化学键合(张小亮等,2013),蒙脱石的结构羟基Al—OH与游离水分子羟基含量的减小,说明吸持不仅脱去了部分层间吸附水使亲水性减弱,同时也破坏了层间结构水,此时蒙脱石表面由于缺乏电荷补偿层间阳离子,可能会吸引水分子,而水分子可以和腐殖酸的亲水基团(羧基、羟基)形成氢键,从而在纳米乳化油与蒙脱石-腐殖酸之间起到桥梁的作用(Conteetal., 2011),促进其吸持。Wu等(2011)研究发现有机矿质的复合会引起蒙脱石表面的改性,并提供新的吸持位点,从而增加对纳米乳化油的吸持能力。随着纳米乳化油浓度的升高,可以起到“桥梁”作用的腐殖酸占比减小以及吸持位点的相对减少,使得蒙脱石-腐殖酸对纳米乳化油吸持的促进作用逐渐减弱。复合于内层的腐殖酸会受到“束缚”,结构致密,而结合在表面外层的部分较松散,因此蒙脱石-腐殖酸对纳米乳化油的吸持行为更加复杂。
2.5 天然黏土矿物和有机质对纳米乳化油的吸持机理
综合上述分析讨论,提出天然黏土矿物和腐殖酸吸持纳米乳化油的概念模型(图8)。高岭石、蒙脱石及腐殖酸的吸持过程均以物理吸持为主。高岭石和蒙脱石之间的表面结构性质差异导致其对纳米乳化油具有不同的亲合能力。蒙脱石作为2∶1型矿物具有相较于高岭石更为明显的层状结构以及较大的比表面积,从而具有更大的吸持容量。纳米乳化油主要通过氢键及疏水作用结合在矿物及腐殖酸表面。
相比于单一体系,复合体系对纳米乳化油的吸持滞留,主要通过氢键、配体交换及疏水作用实现。腐殖酸会引起矿物表面性质的改变,增加吸持位点,并增强矿物表面的疏水性,从而提升复合体系对乳化油的吸持能力。随着纳米乳化油初始浓度的升高,乳化油与腐殖酸在高岭石表面的共吸附和累积吸附作用增强,使高岭石-腐殖酸吸持的促进作用逐渐增强。而对于蒙脱石-腐殖酸,随着纳米乳化油浓度的升高,起到“桥梁”作用的腐殖酸以及吸持位点的相对减少,使得其促进作用减弱。复合体系对纳米乳化油的吸持能力相比于单一体系更强,而实际场地中的介质组成复杂,吸持滞留作用对纳米乳化油在多孔介质中迁移的影响更是不容忽视,实验结果将有助于进一步探明纳米乳化油在天然环境条件下的迁移行为。
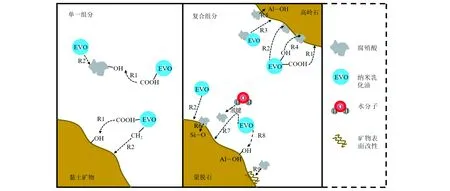
图8 矿物与腐殖酸对纳米乳化油吸持的概念性模型图Fig.8 The conceptual model of mineral and humic acid adsorbing nano emulsified oil R1为纳米乳化油羧基与矿物、腐殖酸羟基发生氢键作用; R2为纳米乳化油疏水性组分与矿物表面疏水结合; R3为纳米乳化油与腐殖酸发生共吸附和累积吸附作用; R4为纳米乳化油与高岭石-腐殖酸之间的配体交换作用; R5为高岭石与腐殖酸之间的氢键及疏水作用; R6为腐殖酸的亲水基团与蒙脱石上极性基团发生氢键、配位键作用; R7为水分子与腐殖酸形成氢键,在纳米乳化油与蒙脱石-腐殖酸之间起到桥梁作用; R8为纳米乳化油与蒙脱石水分子羟基和结构羟基发生氢键作用; R9为腐殖酸引起蒙脱石表面改性,提供更多吸持位点R1 represents that hydrogen bonding occurs between carboxyl group of nano emulsified oil and hydroxyl group of minerals and humic acid; R2 represents the hydrophobic binding between nano emulsified oil hydrophobic component and mineral hydrophobic surface; R3 represents that co-sorption and cumulative sorption between nano emulsified oil and humic acid; R4 represents the ligand exchange between nano emulsified oil and kaolinite-humic acid; R5 represents the hydrogen bond and hydrophobicity between kaolinite and humic acid; R6 represents the hydrophilic group of humic acid and the polar group of montmorillonite bind by hydrogen bond and coordination bond; R7 represents the hydrogen bond between water molecule and humic acid, which acts as a bridge between nano emulsified oil and montmorillonite-humic acid; R8 represents the hydrogen bond between nano emulsified oil and water molecular hydroxyl and structural hydroxyl of montmorillonite; R9 represents that humic acid induced surface modification of montmorillon-ite, providing more sorption sites
3 结论
(1) 天然黏土矿物及腐殖酸对纳米乳化油的吸附符合Freundlich模型,表明3种样品的表面吸附点位存在差异,吸持能力大小为: 蒙脱石>腐殖酸>高岭石; 蒙脱石-腐殖酸>高岭石-腐殖酸。复合体系对纳米乳化油的吸持起到了促进作用,出现了“1+1>2”的现象,表明腐殖酸的加入与黏土矿物产生协同作用,提高了复合体系对纳米乳化油的吸持滞留量。
(2) 高岭石、蒙脱石及腐殖酸对纳米乳化油的吸持过程以物理吸持为主。纳米乳化油主要通过氢键及疏水作用结合在矿物和腐殖酸表面,表面结构性质为高岭石和蒙脱石吸持过程中的主导因素,蒙脱石较大的比表面积,使其具有更强的吸持能力。而腐殖酸与乳化油颗粒之间的结合通过疏水作用、范德华力及氢键等强作用力,主要表现为发生凝聚作用。
(3) 两种复合体系对纳米乳化油吸持的促进作用随着纳米乳化油浓度的变化,呈现出相反的趋势。乳化油与腐殖酸在高岭石表面的共吸附和累积吸附通过氢键与疏水作用实现,随着纳米乳化油初始浓度的升高而增强,进而引起促进作用的增强。蒙脱石-腐殖酸由于乳化油浓度的升高,起到“桥梁”作用的腐殖酸和吸持位点相对减少,导致促进作用减弱。整体来看,蒙脱石-腐殖酸由于具有较大的比表面积,导致其对纳米乳化油吸持的促进作用更显著。
