子痫前期产妇右美托咪定胎盘转运及对新生儿安全性的影响
2022-07-18徐文平詹淑玉张素芹赵艳萍夏丰
徐文平 詹淑玉 张素芹 赵艳萍 夏丰
随着高龄初产孕产妇数量的逐年增高,子痫前期(preeclampsia,PE)产妇发病率约为18%。PE产妇剖宫产椎管内麻醉为首选,术中适当镇静带来的益处显而易见。右美托咪定(Dexmedetomidine,Dex)作为现代舒适化麻醉代表药物,以其独特的优势被用于PE产妇围术期,用于术前镇静辅助降压,术中镇静并辅助镇痛、减少寒战及术中牵拉反应等,术后镇痛、减少产后出血等。Dex对新生儿、早产儿的使用尚未发现不良反应,但缺少大样本的临床数据支持,亦并未超说明书使用,使得临床应用时普遍存在顾虑。有研究报道,Dex可以通过胎盘屏障经胎盘转运至胎儿循环。由于PE产妇孕期胎盘结构、血液灌注以及多种炎症因子影响胎盘转运体的表达等[1]。Dex在PE产妇中药物胎盘转运情况如何,未见相关报道[2]。笔者假设PE产妇腰硬联合麻醉下择期剖宫产术中静脉应用Dex可以通过胎盘屏障进入胎儿循环,且对新生儿无不良影响。该文旨在探明剖宫产中PE产妇Dex经胎盘转运的情况以及对新生儿安全性的影响,为临床优化用药提供参考。
1 资料与方法
1.1 临床资料 选择2019年10月至2020年10月在嘉兴市妇幼保健院行择期剖宫产术单胎孕产妇36例,其中非PE产妇(NPE组)和PE产妇(PE组)各18例。按照1∶1匹配,匹配条件为接受相同麻醉、手术方式及右美托咪定用药方式。(1)纳入标准:依据《妇产科学》(第8版)诊断为PE产妇,ASA I~II级,孕期35~42周,年龄20~45岁,体重61~89 kg。(2)排除标准:右美托咪定过敏者;椎管内穿刺禁忌;麻醉平面高于T4或更改为全身麻醉者;双胎妊娠、胎盘早剥、前置胎盘等合并症;术前胎儿宫内窘迫者;严重心、肝、脑、肺、肾功能障碍;酗酒或滥用药物;长期催眠药物或吸毒者;精神病产妇,语言障碍或无法正常交流者。本研究医院医学伦理委员会批准[2019(伦)-33] ,所有产妇均签署知情同意书。
1.2 研究方法 拟择期行剖宫产术单胎孕产妇均常规禁食禁饮。入室后,静脉给予羟乙基淀粉130/0.5(5 mL/kg),常规监护血压、心电图(electrocardiogram,ECG)、心率(heart rate,HR)。右美托咪定(国药准字:H20090248;批号:16040132;规格:2 mL:200 μg;江苏恒瑞医药股份有限公司)200 μg稀释至50 mL 0.9%NaCl溶液(4 μg/mL),两组产妇均采用0.5μg/kg输注10 min,体重采用标准体重(Kg)=(身高-70)(cm)×60%,随后以1μg/(kg·h)持续输注至胎儿及附属物取出。Dex给药后严密观察至少10 min,生命体征平稳方可实施腰硬联合麻醉。产妇取左侧卧胸膝位,以L3、L4间隙为穿刺点,蛛网膜下腔穿刺成功后缓慢注入0.5%布比卡因2.0 mL。硬膜外头侧置管3 cm,腰麻效果不满意时作为补救。麻醉穿刺完成立即翻身平卧,右臀部垫高。控制麻醉平面在T5~T6水平。当收缩压<90 mmHg或低于基础值的30%时,静脉注射麻黄碱6 mg或去氧肾上腺素50 μg,必要时可重复。心率<50次/min时静脉注射阿托品0.3~0.5 mg。
1.3 血标本采集、处理 胎儿取出后双向钳夹脐带,中间间隔不小于30 cm,采集脐动脉血(umbilical artery,UA)、脐静脉血(umbilical vein,UV)各3 mL,以及母体的无静脉输液上肢静脉血(maternal vein,MV)3 mL。脐动脉血进行血气分析,其余血标本以3,500 r/min离心10 min,采用高效液相色谱法(high-performance liquid chromatography mass spectrometry,HPLC-MS/MS)测定右美托咪定血药浓度。血液标本采集及检测者对产妇分组并不知情,血药浓度测定由同1名专业人员完成。
1.4 观察指标 (1)记录入室时(T0)以及给药后3 min(T3)、5 min(T5)、10 min(T10)、20 min(T20)、30 min(T30)的平均动脉血压(mean arterial pressure,MAP)、HR。记录母体药物暴露时间(TDex),Dex给药后至采集血标本期间心动过缓(HR<50次/min)、低血压、高血压等不良事件的发生情况。(2)测定取胎后脐动脉血气分析,以及母体静脉(CMV)、脐动脉(CUA)、脐静脉(CUV)中Dex浓度,药物胎盘转运(CUV/CMV),胎儿排泄率(CUA/CUV)。记录新生儿体重,娩出后1 min及5 min进行Apgar评分。Apgar评分法是以新生儿出生后1 min内的心率、呼吸、喉反射、肌张力和皮肤颜色5项体征为依据,每项为0~2分,满分为10分,8~10分属正常新生儿,4~7分为轻度窒息,0~3分为重度窒息。
1.5 统计学方法 采用SPSS16.0统计软件。计量资料符合正态分布以(±s)表示,采用t检验;不符合正态分布以[M(IQR)] 表示,采用Mann-Whitney U检验;计数资料以[n(%)] 表示,采用χ2检验或Fisher确切概率法。以P<0.05为差异有统计学意义。
2 结果
2.1 两组产妇的一般资料比较 两组产妇的年龄、身高、体重、TDex比较,差异均无统计学意义(P均>0.0.5)。NPE组孕周持续时间长于PE组,差异有统计学意义(P<0.05)。见表1。
表1 两组产妇的一般资料比较[n=18,(±s)]

表1 两组产妇的一般资料比较[n=18,(±s)]
组. 年龄(岁. 体重(kg. 身高(cm. 孕周[周,M(IQR)] TDex(min)NPE. 32.00±4.47 71.09±12.54 160.36±5.99. 38.55(0.90. 45.12±8.64 PE. 31.21±6.12 72.17±10.01 159.29±4.93 37.3(2.95. 43.90±11.87 t/Z. 0.38 -0.25 0.52 2.37 0.96 P. 0.70 0.80 0.61 0.02 0.34
2.2 不同时间点两组的MAP、HR比较 PE组各时间点的MAP与NPE组比较,均处于高水平(P<0.01);NPE组,与入室时(T0)比较,给药后T30显著降低(P<0.01)。PE组,与T0比较,给药后T20、T30均显著降低(P<0.01)。两组的心率比较,差异无统计学意义(P>0.05);NPE组,与入室时T0比较,给药后T10、T20、T30均明显下降(P<0.05);PE组,各时间点的心率比较差异无统计学意义(P>0.05)。见图1。
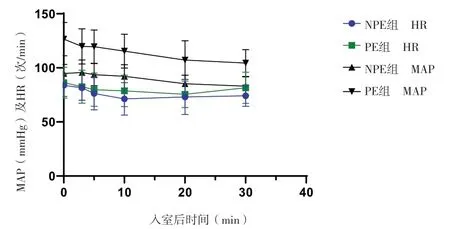
图1 不同时间点两组的MAP、HR比较
2.3 两组Dex血药浓度及胎盘转运情况比较 两组CMV、CUA、CUV的Dex血药浓度差异无统计学意义(P>0.05)。PE组产妇Dex经胎盘转运略有升高、胎儿排泄率处于低水平,但与NPE组比较差异无统计学意义(P>0.05)。见表2。
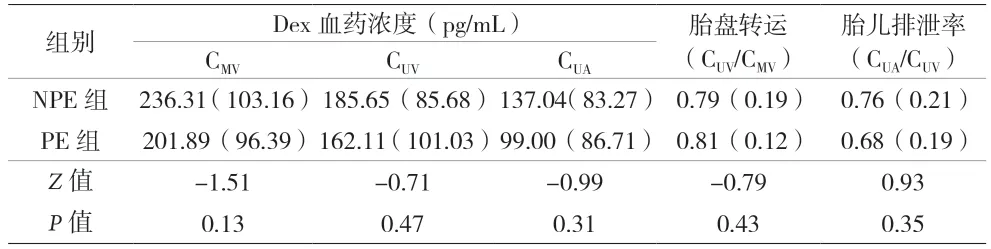
表2 两组血药浓度及胎盘转运情况比较[n=18,M(IQR)]
2.4 两组新生儿动脉血气、体重及Apgar评分比较 NPE组新生儿体重与PE组比较,差异有统计学意义(P<0.001)。见表3。
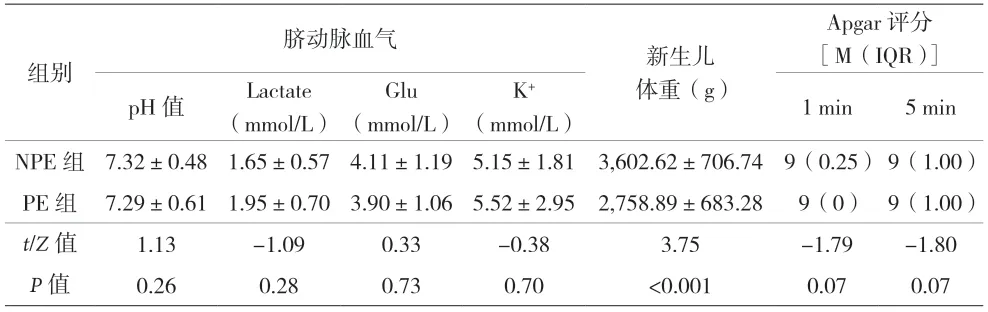
表3 两组新生儿脐动脉血气、体重及Apgar评分比较(n=18)
2.5 两组的不良事件发生情况比较 两组各出现1例心动过缓,给予阿托品后缓解。取胎后子宫体软收缩欠佳者,NPE组2例,其中1例是由胎盘黏连剥离困难影响子宫体肌肉收缩所致。NPE组有3例发生低血压,其中1例发生在缩宫素应用后,其余均发生在椎管内局麻药推注后10 min内,考虑为仰卧位综合征引起的一过性低血压,持续时间均<3 min。NPE组出现2例恶心呕吐,考虑由子宫体局部注射欣母沛药物所致。两组的不良事件发生情况比较,差异无统计学意义(P>0.05)。见表4。

表4 两组的不良事件发生情况比较 [n=18,n(%)]
3 讨论
目前,PE产妇终止妊娠仍以椎管内麻醉为主,Dex有协助镇痛镇静的作用机制,该研究显示静脉给予Dex后并维持20~30 min,可以有效降低术中MAP和NPE组产妇的HR,有利于维持循环稳定,而PE组的HR无明显降低,考虑可能与样本量偏少有关[3]。有报道,Dex用于先兆子痫产妇,与对照组比较,肿瘤坏死因子α(TNF-α)、白细胞介素-6(IL-6)、白细胞介素-10(IL-10)表达降低,β2-MG、KIM-1和尿蛋白含量均降低,对肾损伤有一定的保护作用[4]。在不良反应方面,该研究未发现右美托咪定PE组的高血压、低血压、恶心呕吐发生率高于NPE组。另外,Dex用于产科麻醉还有独特优势,作为一种高选择性a2受体激动剂,具有镇痛和抗交感神经作用,还有无呼吸抑制的有意识镇静,可以有效缓解产妇术中紧张焦虑情绪。术中寒战一直是临床麻醉棘手的问题,发病率约52%,严重的颤抖会干扰术中监测,Dex可显著降低并抑制其发生[3,5]。Dex还有助于子宫收缩,可降低术中出血的风险[6]。综上,Dex有望成为PE围术期及阴道分娩镇痛镇静的新选择。
临床上,几乎所有的麻醉药物都可以通过胎盘屏障。母体静脉应用右美托咪定同样可以通过胎盘屏障直达胎儿,但新生儿的脐动脉血气分析及1 min、5 min Apgar评分结果显示并无影响,表明Dex对胎儿的呼吸抑制和镇静作用不明显[7]。麻醉药物的胎盘转运与否及程度是胎盘的生理解剖、发育的不同阶段及胎儿循环共同作用的结果。脐静脉中约50%以上的血液流经肝脏,大部分药物被迅速代谢清除,剩余少量药物经体循环到达心脑等重要器官,这种特殊的结构一定程度上保护了胎儿重要器官免受高浓度药物的影响。高浓度、小分子量(<500 u)、离子化程度低、脂溶性高及蛋白结合率低的麻醉药物能够促进胎盘转运。另外,母体给药途径及暴露时间、合并用药、相关疾病、胎盘的成熟度、血流动力学的情况以及胎儿的成熟度均会对胎盘转运及胎儿排泄造成不同程度的影响。
本研究结果显示,NPE组产妇的胎盘转运率为0.79,PE产妇略高为0.81;NPE组产妇的胎儿排泄率为0.76(CUA/CUV),PE产妇略低为0.68,但两组的差异无统计学意义(P>0.05)。NPE组产妇的孕周、胎儿体重及成熟度均优于PE组,胎盘的通透性减弱,即胎盘转运率更低;PE组的胎儿体重小、产妇孕周小,胎儿排泄率相对越弱,胎儿体内药物聚集越多,产生的影响可能就越大。两组均未发现Dex对胎儿Apgar评分、动脉血气造成不良影响。既往研究中,1997年报道体外胎盘灌注Dex经胎盘转移为0.77,本研究正常产妇右美托咪定胎盘转移为0.79,与全麻中胎盘转移相似0.76[8-9],均显著低于可乐定(0.85)和瑞芬太尼(0.88),可能与Dex脂溶性高,更容易滞留在胎盘组织内有关。本研究PE组的血压在各时间点均处于高水平,显著影响胎盘灌注,产妇全身炎性介质的释放诱发血管内皮损伤致全身小血管痉挛、胎盘转运体的减少等[10],多种因素协同作用下,并未发现与NPE组在胎盘转运及胎儿排泄率方面有显著差异。本研究的局限性在于,仅排除了胎龄<35周的产妇,下一步研究应严格纳入标准,控制混杂因素,尽量减少孕周及胎儿体重对结果造成影响。
综上所述,PE产妇应用Dex有助于维持循环稳定,降低心脏后负荷,未发现对新生儿有不良影响,在PE产妇中胎盘转运为0.81,胎儿排泄率为0.68,与非PE产妇相似。
