恶性肿瘤患者术后PICC置管血栓形成和非计划拔管的危险因素分析
2022-07-18张健宋建文赵伯贤沈苑魏锋
张健 宋建文 赵伯贤 沈苑 魏锋
经外周置入中心静脉导管(peripherally inserter central catheter,PICC)是肿瘤患者化疗等治疗首选途径之一,近年来应用普遍,但随之而来的静脉血栓、静脉炎等并发症逐渐增多,其中静脉血栓是影响PICC继续使用的严重并发症之一,可导致患侧肢体胀痛、血栓脱落甚至心、肺、脑等重要脏器栓塞的严重后果,同时导管脱落、堵塞、置管感染等并发症还会导致非计划型拔管,加重患者负担。该研究旨在分析恶性肿瘤患者术后PICC置管血栓形成的高危因素以及导致非计划性拔管的相关因素,现报道如下。
1 资料与方法
1.1 临床资料 回顾性分析2014年1月至2019年12月在湖州市中心医院普外科行PICC置管的恶性肿瘤术后患者510例。(1)纳入标准:恶性肿瘤术后患者,经病理检查确诊;年龄≥18岁;在本院行PICC置管,临床资料完整。(2)排除标准:非肿瘤患者留置PICC导管;PICC置管临床资料缺失。
1.2 研究方法 (1)PICC置管:采用三向瓣膜式硅胶材质PICC管(规格:4Fr;型号:7745450;厂商:美国巴德公司),由本院PICC小组成员按规范操作置管。所有患者均按PICC标准实施护理,并规范实施化疗。收集并记录患者的一般临床资料和置管资料。(2)静脉血栓诊断标准:患者PICC置管侧上肢出现胀痛,彩超检查可见上肢置管静脉实质性低回声团块,血管管径扩张,同时确定血栓部位和范围。(3)非计划拔管标准:①导管堵塞或脱落,加压后无法注入0.9%NaCl溶液或人为意外部分或完全移除导管;②导管相关感染,依据《医院感染诊断标准》,发热≥38 ℃,排除其他感染,血培养或导管培养为阳性,拔管后体温恢复正常;③导管相关上肢静脉血栓。(4)血栓患者抗凝治疗:低分子肝素4,000 AxalIU(体重<60 kg)或6,000 AxalIU(体重≥60 kg)皮下注射,每12 h一次。出院后口服利伐沙班,3周内剂量为15 mg/次,2次/d;3周后剂量为20 mg /次,1次/d,连续口服3个月。
1.3 观察指标 患者的年龄、性别、BMI、吸烟史、基础疾病(高血压、糖尿病等)等一般资料,导管型号、置管次数、导管尖端位置等置管数据,用药情况、凝血酶原时间(PT)、纤维蛋白原(FIB)水平、D-二聚体水平、置管上肢活动时间等临床资料,统计患者发生血栓及非计划拔管情况。
1.4 统计学方法 采用SPSS20.0统计软件。计量资料符合正态分布以(±s)表示,采用t检验;计数资料以[n(%)] 表示,采用χ2检验;血栓形成和非计划拔管的单因素及多因素分析均采用Logistic回归模型分析。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 该研究共纳入恶性肿瘤患者510例,其中乳腺癌134例、结直肠癌182例、胃癌111例、胰腺癌83例;男311例、女199例;年龄(65.7±13.2)岁,置管时间(162.5±39.6)d。并发血栓者36例,血栓形成率为7.06%,其中并发肺栓塞者3例,均有临床明显症状;26例患者在抗凝后好转,继续使用PICC置管,另外10例患者因无法继续导致非计划拔管。
2.2 恶性肿瘤患者术后PICC置管并发血栓的危险因素分析 单因素Logistic回归分析显示,患者的BMI、高血压病史、糖尿病史、吸烟史、活动时间为导致血栓形成的危险因素(P<0.05)。多因素Logistic回归分析显示,BMI、糖尿病史、活动时间为血栓形成的独立危险因素(P<0.05)。见表1。
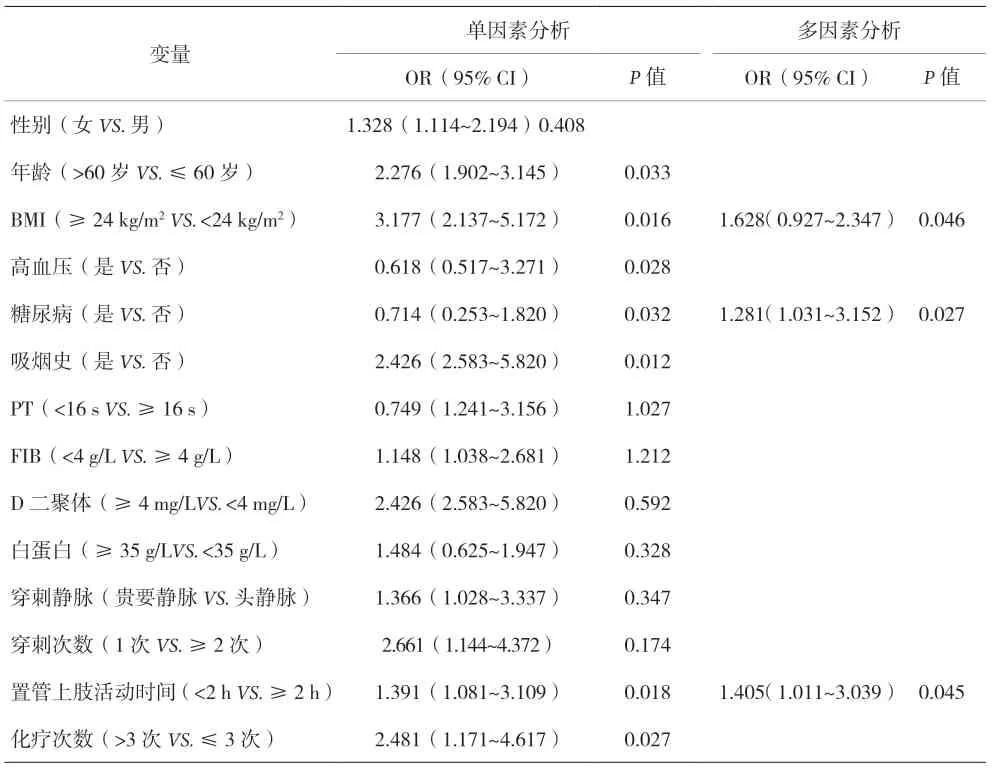
表1 恶性肿瘤患者术后PICC置管并发血栓的危险因素分析
2.3 恶性肿瘤术后患者PICC置管后非计划拔管的危险因素分析 PICC非计划拔管患者27例,占比5.29%,其中血栓10例、导管堵塞7例。导管相关感染5例、导管意外脱出3例、机械性静脉炎1例。单因素分析显示,BMI、导管堵塞和导管相关血栓是非计划拔管的独立危险因素。多因素分析显示,导管堵塞和导管相关血栓是非计划拔管的独立危险因素(P<0.05),见表2。

表2 恶性肿瘤术后患者PICC置管后非计划拔管的危险因素分析
3 讨论
PICC相关深静脉血栓形成(deep venous thrombosis,DVT)发生所需时间为13(95%CI:12~32)d,提示在PICC置入后前2周预防DVT形成的重要性[1]。无症状血栓占比约76.8%(43/56),其中腋静脉最易形成血栓,可能当浅静脉血液汇入深静脉(腋静脉)易产生湍流,或因肢体活动使得腋静脉处导管与血管壁之间接触摩擦造成血管壁损伤增加血栓形成风险[2]。
有研究指出,活动量少和肥胖是PICC相关血栓形成的危险因素[3]。本研究多因素分析显示,肥胖(BMI≥24 kg/m2)、活动减少、糖尿病史是肿瘤患者PICC血栓发生的高危风险因素[4]。肥胖患者可能是因为脂肪因子干扰血脂及糖代谢会增强凝血活性的同时降低纤维蛋白溶解,而致使血栓发生率增加[5]。糖尿病是静脉血栓形成的危险因素,糖尿病患者发生PICC相关DVT的可能性是正常人的3倍[6],机制可能为内膜和凝血酶原的损伤,高血糖、血小板异常会增加血液黏度,减缓血液流动[7-8]。血浆中自由基紊乱、血脂氧化水平升高可导致血管内皮细胞损伤。血小板的黏附聚集和负电荷磷脂暴露在血小板表面,血管内皮细胞损伤可引起凝血过程,上述一系列反应最终导致血栓形成[9]。另外,化疗是恶性肿瘤的重要治疗方法之一,化疗后患者常有恶心、呕吐等消化道症状,且存在一定心理压力,害怕导管脱落特意减少置管侧手臂运动会导致血流缓慢、血管壁损伤,最终形成血栓。
目前,肿瘤患者PICC留置时间可达3~6个月,完成预定治疗后给予拔管。多因素分析显示,导管相关血栓和导管堵塞是非计划拔管的独立危险因素(P<0.05)。Meta分析提示,血栓和药物(高浓度高营养)是导致PICC非计划拔管的主要危险因素[10],有血栓的患者非计划拔管增加2.93倍,定期彩超随访可降低PICC相关血栓导致的非计划拔管率[11]。放射科、超声科、血管外科和药剂科等多学科合作模式可提高PICC置管安全性和规范处理PICC相关并发症,从而降低非计划拔管率[12]。
导管开口方式和管腔直径是导管阻塞的主要因素。远端导管在咳嗽、便秘等情况下导致胸内压升高,容易导致血液回流。若没有及时冲洗导管,附在管壁上的血液会堆积,导致导管堵塞。管腔直径不同时,管腔直径越小则导管阻塞的几率越高。因此,应了解不同类型的导管、开放方式和规格,并及时冲洗导管。为减少堵塞,应加强操作技能,在超声引导下操作,肝素冲洗采用快-慢-快的冲洗方法[13]。
综上所述,PICC在普外科肿瘤患者术后广泛应用,BMI、糖尿病史和活动时间是导致PICC置管患者血栓形成的高危因素,预防导管相关血栓形成和导管堵塞可降低患者非计划拔管率。因此,应加强PICC小组对患者导管规范化管理,降低相关并发症发生率,更好地为肿瘤患者服务。
