纳米纤维基单向导湿抗菌敷料的制备及其性能
2022-07-18欧康康祁琳雅侯怡君范天华王宝秀王华平
欧康康,祁琳雅,侯怡君,范天华,齐 琨,王宝秀,王华平,3
(1.中原工学院 纺织服装产业研究院,河南 郑州 451191;2.东华大学 纤维材料改性国家重点实验室,上海 201620;3.国家先进功能纤维创新中心,江苏 苏州 215228)
创面愈合是一个复杂的动态过程,涉及到组织细胞间的相互作用,护理不当会影响愈合效果,因此,合理选择创伤敷料对于创面的愈合具有重要意义[1]。研究发现,湿润的微环境可促进创面愈合,这也推动了湿性敷料的快速发展,但传统的湿性敷料易在伤口处形成积液,影响创面的愈合[2],因此,亟需开发出具有单向导湿功能的创伤敷料,去除伤口周围过量渗出液,以实现创面的快速愈合。
近年来,基于传统织物和三维纳米纤维膜的单向导湿功能材料在吸湿排汗功能面料、生物医用材料、组织工程等方面展示出极大的应用前景[3-4],也有望用于创伤护理领域。静电纺纳米纤维膜具有纤维直径细、比表面积大、孔隙率高、易功能化加工以及质量轻等优点,且其内部的纤维形态结构还与生物体组织细胞外基质相类似,将其用于创伤敷料具有其他材料不可比拟的优势[5-6]。可将静电纺丝技术与单向导湿结构设计相结合,尝试构建具有单向导湿功能的纳米纤维创伤敷料。
聚氨酯纳米纤维柔韧性好,且具有高强高弹性、优异的疏水性能以及生物相容性,成为医用敷料中应用最为广泛的一种高分子材料[7]。聚丙烯腈(PAN)具有良好的亲水性和可纺性,其纳米纤维膜软而蓬松,吸水性较高[8]。但纯PAN纳米纤维膜的力学性能略差,但将聚氨酯(PU)与PAN混纺可显著增强PAN纳米纤维膜的力学性能,使纤维膜结构更稳定[9-10]。聚丙烯酸钠(SPA)具有优异的吸水保水性,可显著提升纳米纤维膜的吸水性能[11]。创伤敷料中引入SPA可吸收较多伤口渗出液,但湿润的微环境反而加速了细菌滋生易引发伤口感染,因此,对创面的有效处理成为降低创伤患者感染的重要手段。目前,研究者常采用杀菌快、广谱性强的有机小分子抗菌剂,但其易渗入伤口而危害人体健康。纳米银具有其他材料无可比拟的抗菌效果,但其价格昂贵,且有研究发现其对人体肺脏、肝脏等有一定损伤,生物安全性依然没有明确定论[12]。聚合物抗菌剂具有性能稳定、不会透过伤口渗入人体等优点,具有更持久的抗菌性,有望满足临床抗菌敷料的应用[13]。其中含胍基的阳离子型抗菌聚合物,如聚六亚甲基胍盐酸盐的结构与天然抗菌肽相似,具有较高的抗菌性和生物相容性[14]。
综上,本文基于聚合物材料固有的亲疏水特性,结合聚合物抗菌剂聚六亚甲基胍盐酸盐(PHGC),利用静电纺丝技术开发出内层为疏水性的PU-PHGC纳米纤维膜,外层为亲水性的PAN/PU-SPA纳米纤维膜,通过调控内外层纤维膜的厚度、孔隙结构以及亲疏水性,促使双层敷料内部形成润湿性梯度和差动毛细效应,以期制备出集单向导湿、抗菌等功能于一体的双层结构纳米纤维医用敷料。
1 实验部分
1.1 实验材料与仪器
材料:聚氨酯(通用级,1180A10),德国巴斯夫公司;聚丙烯腈(相对分子质量为700 000),苏州晖煌氟塑化有限公司;聚丙烯酸钠(医用级),杭州英博生物科技有限公司;四氢呋喃、N,N-二甲基甲酰胺、无水乙醇、盐酸胍、1,6-己二胺(分析纯),国药集团化学试剂有限公司;金黄色葡萄球菌和大肠杆菌(河南汇博医疗股份有限公司);胎牛血清(FBS),杭州四季青生物工程材料公司;人胃上皮细胞(GES-1),中国科学院上海生物化学与细胞生物学研究所;3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(MTT)、杜尔贝科改良伊格尔培养基(DMEM)、青霉素-链霉素双抗溶液、磷酸盐缓冲溶液(PBS),赛默飞世尔科技公司。
仪器:Handy型静电纺丝机(北京永康乐业科技发展有限公司);SIGMA-500型场发射扫描电子显微镜(卡尔蔡司光学有限公司);OCA35型光学接触角测试仪(德国Dataphysics公司);W3/031型水蒸气透过率测试仪、XLW(EC)型智能电子拉力试验机(济南兰光机电技术有限公司);YG461E-III型全自动透气量仪(宁波纺织仪器厂);Varian 640-IR型傅里叶红外光谱测试仪(安捷伦科技有限公司);TG209Fl型热重分析仪(德国耐驰公司)。
1.2 试样制备
1.2.1 PHGC抗菌剂的制备
将等量的1,6-己二胺(0.50 mol)和盐酸胍(0.50 mol) 加入三口烧瓶中,于120 ℃下搅拌2 h,至无氨气释放后调温至180 ℃,持续搅拌6 h,随后在真空干燥箱中将产物烘干得到PHGC抗菌剂。
1.2.2 PU-PHGC防黏抗菌内层的制备
室温条件下,将PU在质量比为1∶1的DMF和THF混合溶剂搅拌6 h,制得质量分数为18%的PU纺丝液,然后将0.06%的PHGC加入PU纺丝液中搅拌均匀,采用静电纺丝机制备防黏抗菌内层膜。纺丝工艺为:纺丝电压20 kV,接收距离18 cm,接收辊转速150 r/min,供液速度0.08 mL/min,纺丝时间(x) 分别为1、2、3 h。不同纺丝时间所制得PU内层纤维膜记为PU-x。
1.2.3 PAN/PU-SPA吸液外层的制备
室温条件下,将质量比为7∶3的PAN和PU在DMF溶剂中搅拌6 h,制得质量分数为12%的PAN/PU溶液;随后将占聚合物总质量10%的SPA粉末加入上述溶液中,混合均匀后得到纺丝液,静电纺丝8 h可制得吸液外层膜。纺丝工艺为:纺丝电压20 kV,接收距离18 cm,接收辊转速为100 r/min,供液速度为0.1 mL/min。
1.2.4 双层敷料的制备
在铝箔纸上先纺出PU-PHGC防黏内层,然后在防黏内层表面继续纺制PAN/PU-SPA吸液外层得到双层敷料,纺丝条件与单独制备内外层膜时保持一致,并将双层敷料的防黏内层标记为正面。
1.3 性能测试
1.3.1 微观形貌观察及直径测量
利用场发射扫描电子显微镜(SEM)观察纳米纤维膜的表面和截面形貌,采用Nano Measurer软件分析内外层膜中纤维直径分布和平均尺寸。
1.3.2 接触角测试
利用接触角测试仪表征2 μL大小的水滴在单层纤维膜和双层敷料表面的接触角。将样品粘在载玻片上置于观察台上,将水滴滴在样品表面后记录其接触角随时间的变化。将5 μL的液滴分别连续滴加至双层敷料的正反面,记录水滴在敷料正反面的传输情况。
1.3.3 墨滴扩散测试
将50 μL的蓝色墨滴分别滴在单层纤维膜表面和双层敷料正反面,观察墨滴在200 s内的扩散过程。
1.3.4 吸水性能测试
创伤敷料吸水性能的强弱直接影响伤口的湿润度。为探究制备的材料是否满足敷料的使用要求,根据下式分别计算材料的吸水率和平衡含水量:
式中:WWA为吸水率,%;REWC为平衡含水量,%;m0为干燥的样品质量,g;m1为干燥样品置入10 mL去离子水中平衡2 h后的质量,g。
1.3.5 透气透湿性能测试
按照ASTM D737—2018《纺织织物透气性的标准试验方案》,利用全自动透气量仪测定各样品的透气性。
按照ASTM E96/E96 M—2016《材料水蒸气透过性试验方法》,利用水蒸气透过率测试仪表征各样品的透湿性能。透湿率按照下式进行计算:
式中:RWVT为透湿率,g/(m2·d);t为测试时间,h;m为透湿杯的质量变化,g;A为杯口面积,m2。
1.3.6 力学性能测试
将各样品裁成50 mm × 10 mm,利用电子拉力试验机测试其力学性能,拉伸速率为10 mm/min。每个样品测试5次,结果取平均值。
1.3.7 热稳定性测试
称取5 mg左右的样品,利用热重分析仪在氮气环境下表征各样品的耐热性能,控制温度范围在 35~800 ℃,升温速率为10 ℃/min。
1.3.8 化学结构测试
采用傅里叶红外光谱测试仪表征PHGC、PU以及PU-PHGC的化学结构,测试条件选择吸收模式,波数范围为4 000~400 cm-1。
1.3.9 抗菌性能测试
选择金黄色葡萄球菌和大肠杆菌为实验菌种,未加抗菌剂的双层敷料为空白样。将空白样和含PHGC的双层敷料裁成直径为2 cm的圆片,灭菌后放入25 mL含有2.5 mL菌液的肉汤中,于37 ℃振荡培养2 h,各取0.1 mL的培养液均匀涂于琼脂培养基上,继续培养24 h后观察菌落的生长情况。
1.3.10 细胞毒性及黏附性测试
按照GB/T 16886.5—2017《医疗器械生物评价 第5部分:体外细胞毒性试验》,测定各样品的浸提液对GES-1细胞活力的影响,将无浸提液的培养孔作为对照组[15]。细胞活力按照下式进行计算:
式中:VC为GES-1的细胞活力,%;eOD为490 nm条件下样品100%浸提液光密度平均值;bOD为490 nm条件下空白样光密度平均值。
细胞黏附实验操作步骤[10]:将双层敷料在75%乙醇蒸汽中灭菌后放入培养基中浸渍2 h,随后以 1×104细胞/孔的密度将GES-1细胞分别接种至敷料的内外层表面,然后将其置于37 ℃、95%相对湿度以及5%浓度的CO2条件下进行培养,定时更换培养液,培养48 h后用4%的多聚甲醛固定细胞,烘干后观察样品表面的细胞形貌。
2 结果与讨论
2.1 形貌结构分析
图1(a)和(b)示出双层敷料内外层的扫描电镜照片和直径分布图。可以发现,2种膜的纤维表面光滑均匀,无串珠结构,其中:内层PU-PHGC膜的纤维平均直径为(1.1±0.38) μm,纤维排列疏松,膜孔径较大;而外层PU/PAN-SPA膜的纤维平均直径为(134±35) nm,纤维排列较致密,纤维膜孔径较小。图1(c)示出双层敷料的截面SEM照片。可知,内层PU-PHGC与外层PU/PAN-SPA膜间纤维相互缠绕,结合牢度较好,可构筑出结构稳定的双层敷料。由图1(c)中内外层膜接触角可发现,内层纤维膜呈现明显的疏水性,外层纤维膜为亲水性。说明本文能够将纤维尺寸、孔径以及亲疏水性能差异较大的2种膜复合成双层敷料,利用内外层纤维膜间形成的差动毛细效应驱动液体由疏水内层向亲水外层流动,加速敷料吸收渗液并实现单向导湿效果[2]。
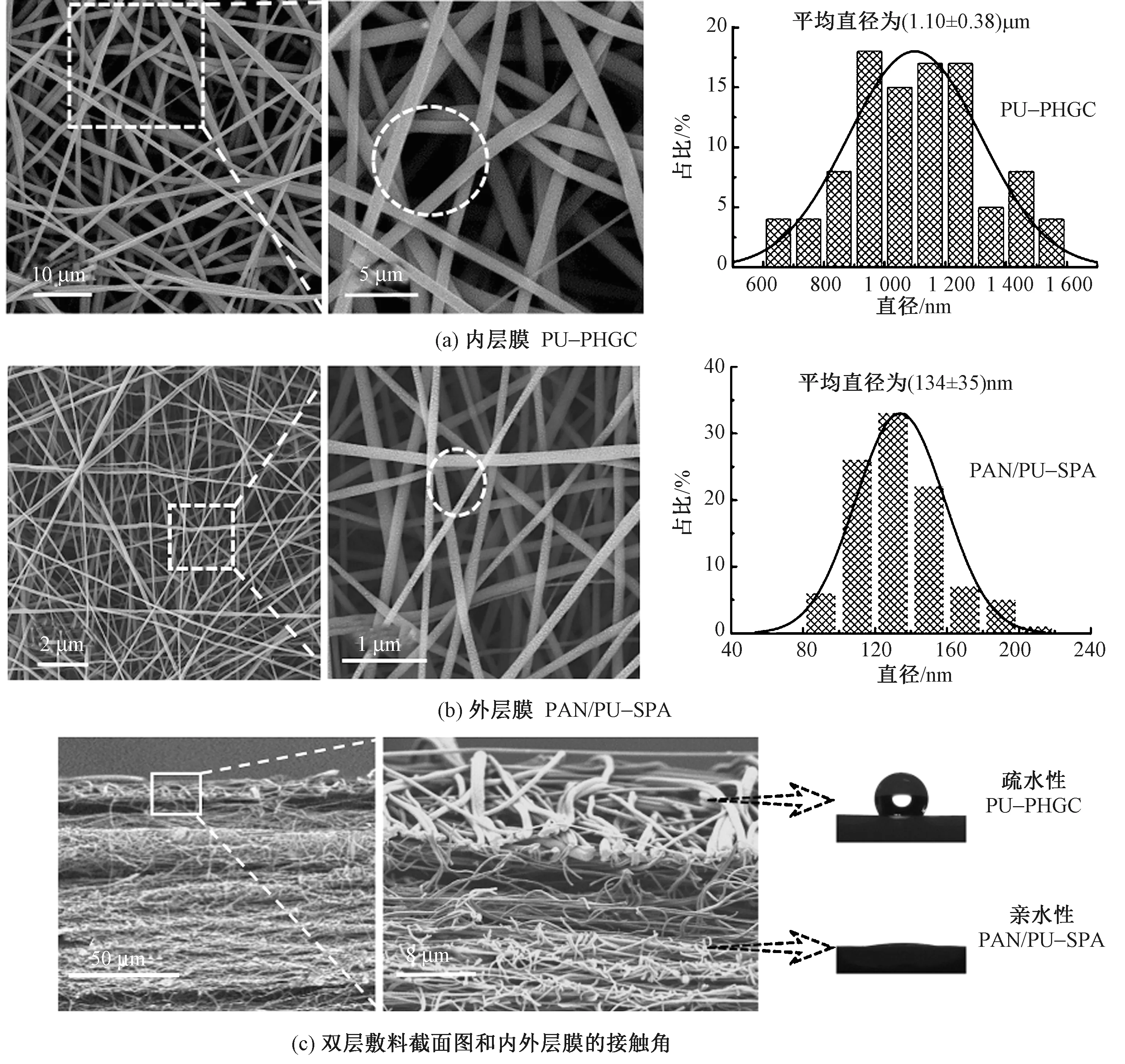
图1 双层纳米纤维敷料的形貌、直径分布图及其水接触角Fig.1 Morphology,diameter distribution and water contact angle of nanofiber dressing.(a) Inner layer PU-PHGC membrane;(b) Outer layer PAN/PU-SPA membrane;(c) Cross-section of bilayer dressing and contact angle of inner and outer layer membrane
2.2 亲水性能分析
图2示出内、外层膜和不同双层敷料正面的动态接触角。可以看出:内层膜的初始接触角约为130°,能够维持60 s无变化,疏水特征显著;而外层膜的初始接触角可在1.2 s内迅速由65°降至0°,呈现出优异的亲水性。对于双层敷料而言,其正面的初始接触角均大于90°,随后降至为0°,但当PU纺丝时间从1 h增至3 h时,其接触角降为0°所需时间由3 s增至8 s。这是因为从双层敷料正面滴水时,水滴先接触到PU层,因其具有疏水性而使双层敷料正面的初始接触角均在90°以上,随后因差动毛细效应的存在使得水滴可经纤维间孔隙向内部渗透,当水滴接触到PAN/PU-SPA亲水层时被快速吸收,导致双层敷料正面的接触角降为0°。不同纺丝时间所得3种双层敷料正面的初始接触角降至0°所用的时间不同,这是因为PU纺丝时间不同使得疏水层的厚度不同。纺丝时间越长,疏水膜越厚,液体穿过PU纤维孔隙所需时间也就越长,导致双层敷料表面液滴被吸收的速度不同。为促进积液排出,选择纺丝1 h的PU纳米纤维膜作为双层敷料的内层进行研究,此时双层敷料正面可在3 s内将积液完全渗出。

图2 内、外层膜和不同双层敷料正面的动态接触角Fig.2 Dynamic water contact angle of inner layer(a),outer layer(b) and inner layer of bilayer dressingPU-1 (c),PU-2(d) and PU-3(e)
图3示出50 μL墨滴在内、外层膜和双层敷料正反面的扩散过程图。可以看出,墨滴在内、外层膜和双层敷料正反面上扩散200 s后的直径依次为0.9、4.2、3.9以及4.2 cm。由于内层PU纤维膜呈疏水性使得其表面的墨滴始终呈球状,而墨滴在单外层膜和双层敷料正反面均能快速扩散,在外层膜和双层敷料反面的扩散直径保持一致,而墨滴在双层敷料正面的扩散面积略小于其反面的扩散面积,表明墨滴在双层敷料内是先沿厚度方向由疏水内层向亲水外层传输,再沿亲水外层膜水平方向扩散。这也证实了亲-疏水双层梯度结构纳米纤维膜能够驱动液体的传输。
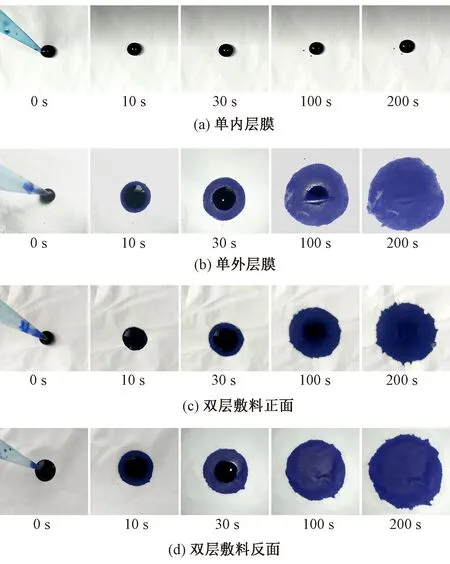
图3 墨滴在样品中的扩散过程Fig.3 Diffusion process of ink drops on samples.(a) Inner layer;(b) Outer layer;(c) Front side of bilayer dressing;(d) Reversal side of bilayer dressing
2.3 单向导湿性能分析
双层敷料正反向的液体传输过程如图4所示。可知,水滴可在3.9 s内由敷料的疏水PU内层向亲水PAN/PU-SPA外层正向穿透,而反向滴入的液滴会在1.5 s内被亲水层迅速吸收,在亲水层表面发生铺展而无法形成反渗。此现象可说明,亲疏水双层梯度结构敷料之间可形成驱动作用力,驱使液体只能由疏水内层膜透过敷料正向传输,而不能反向传输。这是由于双层敷料中疏水PU内层膜可有效阻止亲水层吸收液体后的反向渗透,其较薄的厚度不会影响双层敷料对液体的正向传输,展现出良好的单向导湿功能。

图4 双层敷料正反向液体传输过程Fig.4 Transmission process of water droplets on both sides of dressing.(a) Forward direction;(b) Negative direction
2.4 其他物理力学性能分析
为满足创伤敷料在临床使用中的要求,其应当具备合适的物理力学性能,本文所设计双层敷料的物理力学性能测试结果如表1所示。可知,双层敷料的强度为(6.5±0.5) MPa,断裂伸长率为(45±5)%,其断裂强度和延展性都接近人体皮肤,能够与创面贴合良好并保护创面,满足敷料的力学性能要求。此双层敷料的吸水率和平衡含水量分别为(1 230±50)%和(92±2)%,可保证其对伤口渗出液的高效吸收。伤口愈合过程中细胞活力与氧气浓度有关,敷料应能够为创伤修复提供有利于创面愈合的透气透湿等微环境。研究表明,敷料在中度渗出液伤口处的透湿率在900~1 450 g/(m2·d)范围内较为合理[16],本文制备的双层敷料的透湿率为(1 350±20) g/(m2·d),双层敷料透气率为(6.7±0.5) mm/s,刚好满足此要求。综上可知,所设计双层敷料的其他物理性能均能很好地满足实际需求。
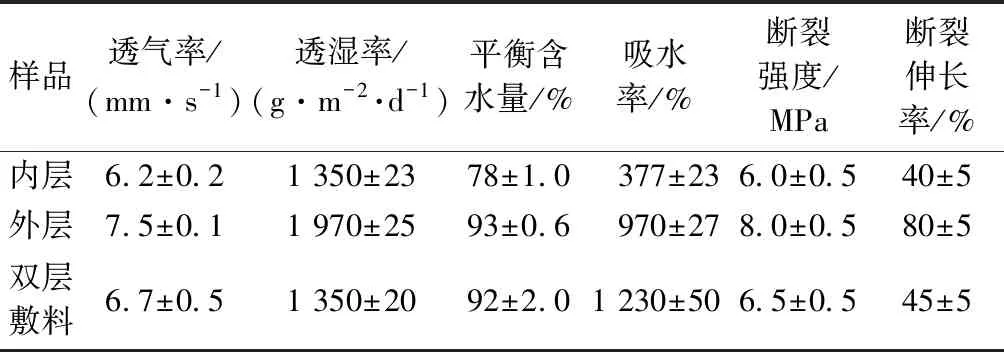
表1 双层敷料的物理性能Tab.1 Physical performance of bilayer dressing
2.5 化学结构及耐热性分析
为探究合成PHGC抗菌剂的稳定性及其与敷料的相容性,测定了PHGC粉末及其复合膜的热重和红外光谱图,结果如图5、6所示。由图5可知,双层敷料和PHGC粉末的热分解温度分别为275和 325 ℃,均具有良好的热稳定性,也表明PHGC抗菌剂在常规使用条件下不会降解成小分子而影响人体安全。
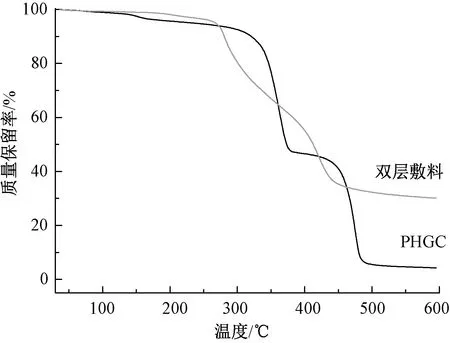
图5 PHGC和双层敷料的热重曲线图Fig.5 TG curves of PHGC and bilayer dressing
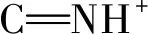
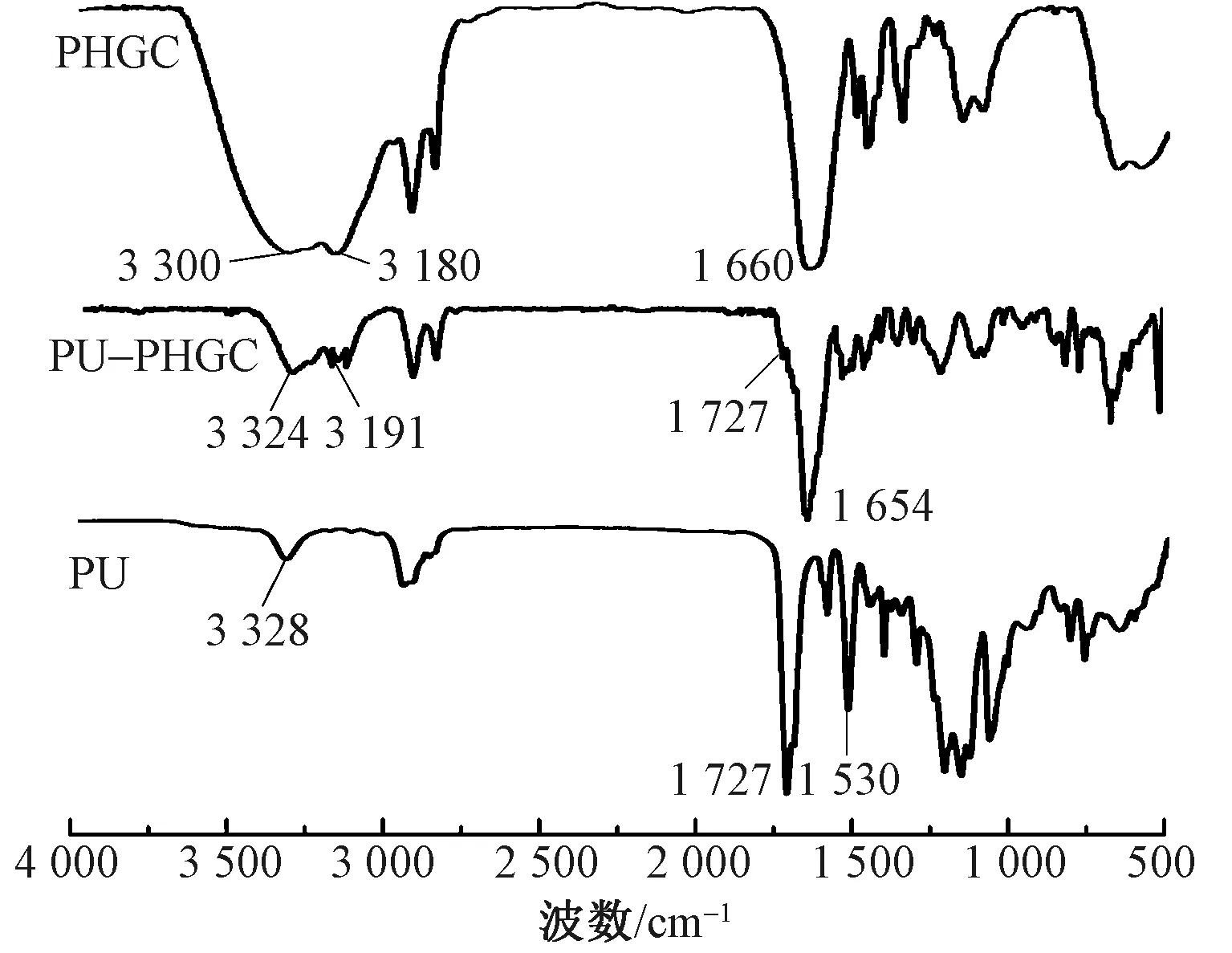
图6 PHGC、PU-PHGC和PU纳米纤维膜的红外图谱Fig.6 FT-IR spectra of PHGC,PU-PHGC and PU nanofibrous membrane
2.6 抗菌性能分析
创伤部位滋生细菌会严重影响创面的愈合,要求敷料具有优良的抗菌性能。本文探究了空白样和含有0.06% PHGC疏水内层组成的双层敷料对金黄色葡萄球菌和大肠杆菌的抗菌效果,结果如图7所示。可以发现,金黄色葡萄球菌和大肠杆菌在空白样的培养基上形成大量菌落,说明空白样抗菌效果较差。而在含有PHGC双层敷料处理的培养基表面,几乎没有观察到金黄色葡萄球菌菌落,仅观察到少量的大肠杆菌,抑菌率均大于95%,证明双层敷料具有较好的抑菌效果。
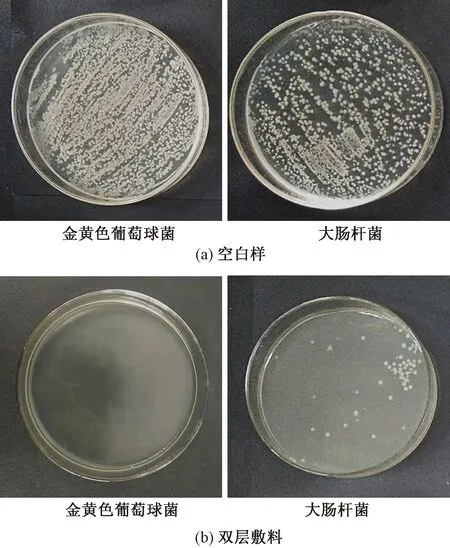
图7 双层敷料的抗菌性能Fig.7 Antibacterial properties of bilayer dressing.(a) Blank sample;(b) Bilayer dressing
2.7 细胞毒性分析
创伤敷料作为医用材料的首要条件是安全无毒。本文以GES-1细胞为实验对象,采用MTT法探究所有样品的细胞活性,结果如图8所示。可知,GES-1细胞在对照组和样品浸提液中培养24 h和48 h后的细胞活力均保持在95%以上。这证明单层膜和双层敷料对GES-1细胞均无毒,也表明所设计的纳米纤维基双层创伤敷料具有优异的生物相容性。
2.8 细胞黏附性分析
理想的创伤敷料应对创面具有较低的黏附性能。本文评价了双层敷料正反面与细胞间的相互作用,结果如图9所示。

图9 双层敷料培养48 h后的细胞黏附性能Fig.9 Bio-adhesion effect of bilayer dressings culturing 48h.(a) Front side;(b) Reverse side
可知,细胞培养48 h后,可清楚地观察到敷料亲水外层膜表面黏附的细胞数量多于疏水内层膜,表明双层敷料中疏水内层膜相较于亲水外层膜呈现出更低的细胞黏附力,这可能是由于细胞更倾向于在亲水性表面生长。实际应用中疏水性PU内层膜接触伤口,其对细胞的黏附力较低,能够避免因细胞粘连伤口而引起的二次创伤,对新生肉芽组织起到保护作用,有利于创面愈合。
3 结 论
本文利用聚合物原料的不同特性,利用静电纺丝技术构建出纤维尺寸、亲疏水性能均不同的聚丙烯腈(PAN)/聚氨酯(PU)-聚丙烯酸钠(SPA)和PU-聚六亚甲基胍盐酸盐(PHGC)纳米纤维膜,分别作为双层敷料的吸液外层和防黏内层,并引入了PHGC抗菌剂,构建出双层敷料并分析其结构和性能,得出以下主要结论。
1)当PU内层膜纺丝时间为1 h时,所得双层敷料能够在3.9 s内将液体由疏水内层向亲水外层单向传输,而不反向渗透,其吸水率高达1 230%,能够迅速导出并吸收创面积液,实现单向导湿。
2)双层敷料的断裂强度为 6.5 MPa,断裂伸长率约为45%,透气率约为6.7 mm/s,透湿率约为 1 350 g/(m2·d),各项物理力学性能基本满足临床对创敷料的要求。
3)合成的PHGC抗菌剂具有较好的稳定性,与纳米纤维相结合所得双层敷料对金黄色葡萄球菌和大肠杆菌具有较好的抗菌性能;体外细胞毒性和生物黏附性实验表明,该双层敷料无细胞毒性,具有良好的生物相容性,且疏水性内层对细胞展示出更低的黏附行为。
FZXB
