异常表达CD13的B细胞恶性肿瘤患者形态学和流式细胞术检测结果分析
2022-07-15刘训涛郭迪媛
刘训涛,王 霞,赵 飞,郭迪媛,张 斌
(河北北方学院附属第一医院检验科,河北 张家口 075000)
CD13(氨肽酶N)作为粒细胞和单核细胞的标记被广泛使用。CD13的表达在淋巴细胞的造血干细胞早期可以被观察到,但随着淋巴细胞的成熟而逐渐消失。有研究结果显示,急性B淋巴(母)细胞白血病(acute B-lymphocytic leukemia,B-ALL)患儿和少数成熟B细胞恶性肿瘤患者CD13异常表达[1]。本研究回顾性分析18例异常表达CD13的B细胞恶性肿瘤患者形态学和流式细胞术检测结果,以提高该类疾病的诊断率。
1 材料和方法
1.1 研究对象
选取2016年9月—2019年11月河北北方学院附属第一医院血液科经MICM分型标准诊断为异常表达CD13的B细胞恶性肿瘤的患者18例,其中男9例、女9例,年龄19~80岁,包括B-ALL 12例、慢性B淋巴细胞白血病(chronic B-lymphocytic leukemia,B-CLL)5例、瓦尔登斯特伦巨球蛋白血症(Waldenström'macroglobulinemia,WM)1例。
1.2 细胞形态学检测
将18例患者骨髓涂片标本经瑞氏染色后,显微镜镜检200个细胞;同时进行组织化学染色,再行显微镜镜检。
1.3 免疫分型检测
取乙二胺四乙酸抗凝骨髓样本1.5~2.0 mL,分离单个核细胞,采用四色免疫荧光标记[异硫氰酸荧光素/藻蓝蛋白/藻红蛋白/CD45多甲藻黄素-叶绿素-蛋白质复合物]。所用抗体包括:B系列CD19、CD9、CD10、 CD20、CD22、CD23、Kappa、Lambda、cyCD79a,T系列CD2、 CD5、CD7、cCD3,髓系CD13、CD117、CD33、cMPO,非系列标志CD34、 CD38、HLA-DR(美国BD公司)。采用FACSCantoⅡ流式细胞仪进行检测(美国BD公司)。
1.4 诊断标准
细胞形态学分析参考2015年国际血液学标准化委员会(the International Council for Standardization in Haematology,ICSH)标准和法国、美国 、英国(French-American-British,FAB) 标准,流式细胞免疫分型分析参考欧洲白血病免疫学分型协作组(European Group for the Immunological Classification of Leukemias,EGIL)标准[2]。
2 结果
2.1 形态学检测结果
12例B-ALL患者胞核不规则,呈扭曲折叠,染色质疏松,核仁1~2个,胞质丰富,部分可见空泡,呈灰蓝色或灰红色,胞质中可见细小的紫红色颗粒,具有较高异质性(图1),形态学误诊率为41.6%,流式细胞术检测结果CD13呈较强表达(32.47%~98.73%,图2),CD34占52.64%~96.85%(表1),侧向散射(side scatter,SSC)呈不均一表现,等高线图显示呈斜形扩散(图3、图4)。5例B-CLL患者CD13占33.35%~70.97% ;1例WM患者CD13占20.11%,其共同特点为胞质中存在细小的紫红色颗粒(图5),SSC呈不均一表现。
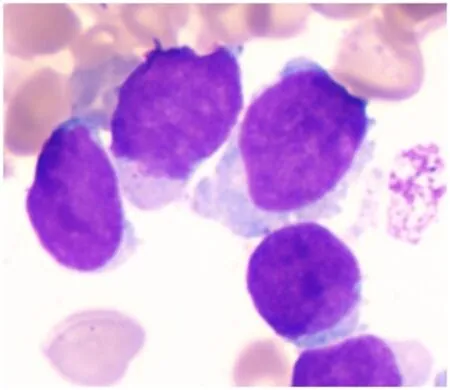
图1 原始细胞形态(×1 000)
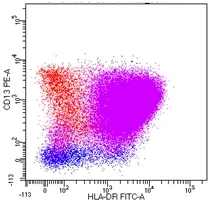
图2 B-ALL异常表达CD13流式散点图
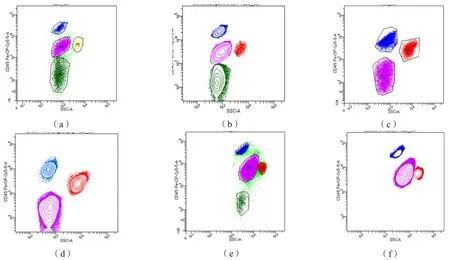
图3 B-ALL患者CD13异常表达散点图和等高线图

图4 B-CLL异常表达CD13的细胞形态(×1 000)
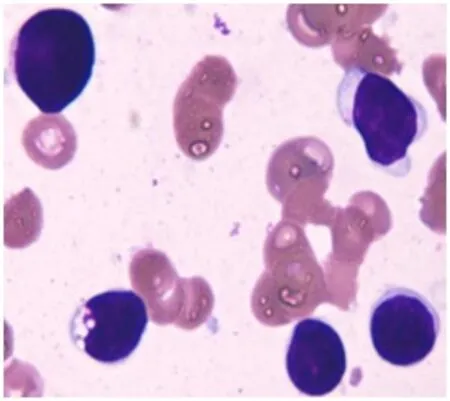
图5 WM异常表达CD13的细胞形态(×1 000)
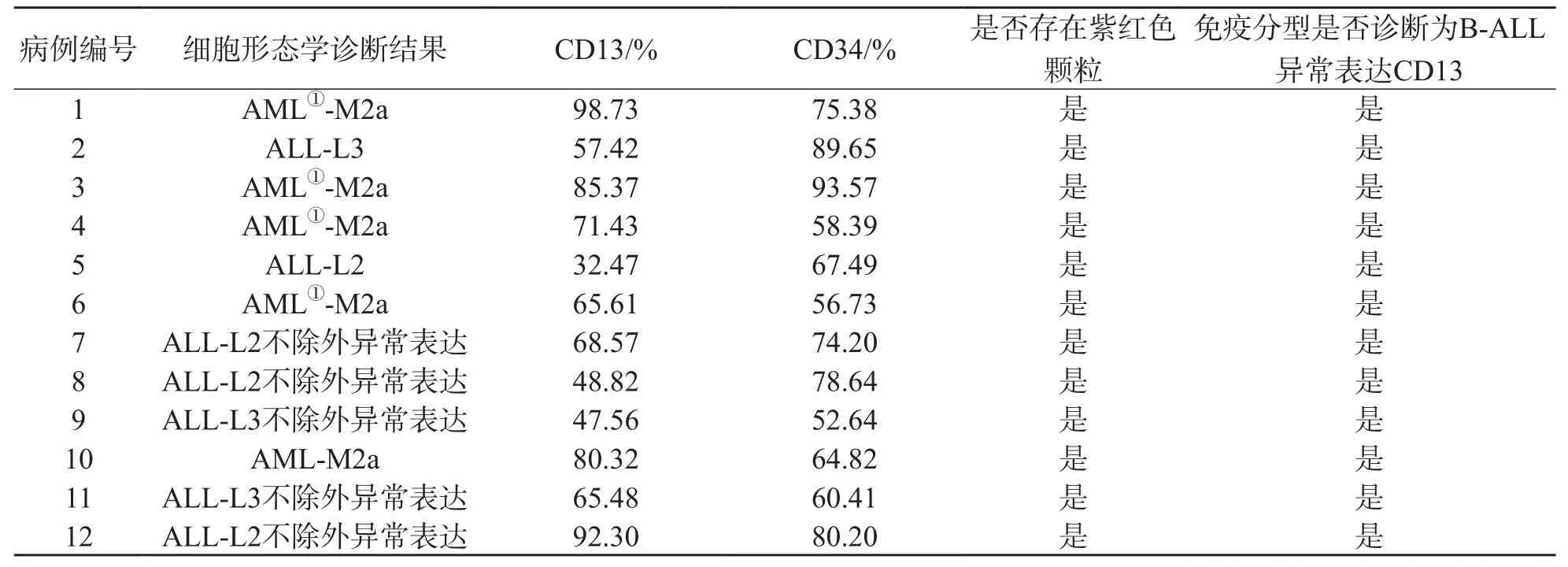
表1 12例B-ALL患者检测与诊断结果
2.2 免疫分型结果
B-ALL患者免疫表型为CD34、CD38、HLADR、CD19、CD22、CD9、cCD79a阳性,异常表达CD13;CLL患者免疫表型为HLA-DR、CD19、CD5、CD20、CD22、CD9、cCD79a阳性,异常表达CD13;WM患者免疫表型为CD38、HLA-DR、CD19、CD5、CD20、CD22、CD9、cCD79a、 CD25阳性,异常表达CD13。
12例B-ALL患者中,1例EVI1阳性,1例MLL/AF4阳性,1例HOX11阳性,有2例患者入院5 d内死亡,未行基因型检测,其他7例患者均为BCR-ABL1(P210)阳性;5例B-CLL患者和1例WM患者未行基因检测。
3 讨论
骨髓细胞形态学分类是诊断B细胞恶性肿瘤的重要方法。本研究异常表达CD13的12例B-ALL患者中,骨髓细胞形态学检查结果均显示骨髓增生极度活跃,细胞胞体体积中等或较大,细胞形态不规则,胞核较疏松,呈粗颗粒感,胞核不规则,呈现出扭曲折叠,染色质疏松,核仁1~2个易见,胞质量丰富,部分可见空泡,因为颗粒的存在,胞质颜色呈灰蓝色或灰红色,颗粒分布不均,颗粒颜色、大小与原始粒细胞非特异性颗粒相似,较难区分,与文献报道[3]一致。细胞胞核颗粒感、染色质疏松程度、胞质颜色和形态、是否有空泡、胞质中出现颗粒是分辨原始淋巴细胞和髓系原始细胞的重要鉴别点,B-ALL患者细胞异质性改变和胞质中出现异常的细小颗粒给形态学检测人员带来了挑战,极易造成误诊,本实验室形态学诊断率为59.4%,低于崔华等[1]对异常表达的B-ALL的诊断率(84.4%),可能与实验室异常表达病例数较少有关,随着经验的积累,诊断率会逐步提高。
本研究结果显示,CD13占32.47%~98.73%,但呈强表达,与髓系CD13表达相似,SSC呈不均一性表现,与部分混合白血病[4]特点类似,但未达到诊断标准;还发现等高线图整体出现斜形趋势,非常接近髓系白血病SSC的特点(呈不均一表现),但B-ALL异常表达CD13图形中,SSC起点较髓系SSC起点小,可能与其胞质中颗粒较小有关。成熟淋巴增殖性疾病流式细胞术检测很少加入髓系抗体,我们在观察患者外周血时发现大量异型淋巴细胞,抽取骨髓染色后发现胞质中存在异常的细小紫红色颗粒,考虑到异常表达CD13的B-ALL胞质中出现同样细小紫红色颗粒情况,加做了髓系相关标记,发现了5例B-CLL和1例WM异常表达CD13的情况。RAIMBAULT等[5]在对3个中心的1 037例B淋巴慢性增殖疾病患者CD13表达的研究中发现,CD13的表达与WM的诊断有显著相关性,CD13可能在IgM副蛋白分泌中起作用。鉴于AGARWAL等[6]提出骨髓微环境在WM发病机制中具有重要意义,CD13可能在淋巴浆细胞与基质的相互作用中发挥重要作用,与浆细胞分化有关。
综上所述,细胞胞核考虑淋系但胞质出现异常颗粒,应考虑淋系异常表达CD13,可降低误诊率;CD13在成熟淋巴细胞增殖性疾病中的表达可能与其功能有关。
