弱磁场-H2O2协同驱动Fe0降解氯霉素废水的研究
2022-07-13王小蝶于媛媛李润瑶张恩山申婷婷
王小蝶,于媛媛,李润瑶,张恩山,杨 娜,申婷婷,2*,孙 静,2*
1.齐鲁工业大学(山东省科学院)环境科学与工程学院,山东 济南 250353;2.齐鲁工业大学(山东省科学院)生物基材料与绿色造纸国家重点实验室,山东 济南 250353
20世纪50年代,氯霉素(CAP)就已经被广泛应用于人类疾病治疗以及水产、家禽养殖产业[1-2]。CAP化学性质稳定,能在环境中富集并长期存在,水环境是CAP的主要汇集地。作为一种广谱类抗生素,水体中残留的CAP导致的耐药性问题,已对人类健康与生态功能了构成了严重威胁[3-4]。随着CAP在污水处理厂的出水、地表水和地下水中频繁被检出[5-8],其研究已在国际、国内引起了广泛关注,也成为了该领域的研究热点与难点之一。目前,水体中CAP污染物的处理方法主要有吸附法[9-10]、光降解[11-12]、生物法[13]、类Fenton法[14-16]等。虽然以上各类处理技术各具特色,但也存在各自的不足之处,比如处理成本高、工艺复杂难以实际应用等。
近年来,零价铁(Fe0)因其比表面积巨大、还原能力强以及反应活性高等特点,逐渐成为处理污染物的一种新方法,已应用于难降解污染物的处理,如染料废水及重金属离子的去除[17-20],然而在抗生素污染物的处理方面相对较少[21-22],有待进一步研究与开发。
因此,尝试利用弱磁场-H2O2与Fe0构建类Fenton体系,对CAP废水进行降解研究,通过优化实验条件与作用机理的分析,评价该体系对CAP的降解效能,为Fe0的应用以及水体中CAP污染物的去除提供新的途径与方法。
1 实 验
1.1 实验材料
主要试剂:氯霉素(CAP,AR)、HCl(37%,AR)、NaOH(AR)、H2O2(30%),铁粉(Fe0)(42%,100目),以上药品均购置于国药集团,并按照实际需要配制成相应浓度;去离子水(Milliopore,USA)。
主要仪器:液相色谱仪(LC-10A,日本岛津)pH计(PHS-3C,上海雷磁);机械搅拌仪(MY300-6,武汉梅宇);扫描电子显微镜(SEM)(S4800,日立);多参数分析仪(上海雷磁,DZS-706);数字高斯计(HT20,上海亨通);滤头(0.45 μm,津腾)。
1.2 实验方法
1.2.1 CAP标准曲线的绘制
CAP溶液的配制:准确称取1.000 0 g (±0.000 5 g)CAP标准品放入盛有超纯水的小烧杯中,在超声清洗机中超声至完全溶解后,转移至1 000 mL棕色容量瓶中定容,获得浓度为1 000 mg/L的CAP标准液。实验时,按照需求移取适量已配置好的CAP标准储备液稀释成实验需要浓度的溶液,贮存方法同上。
CAP浓度检测的高效液相色谱(HPLC)条件:流动相为甲醇∶水(60%∶40%),进样体积1.0 μL,流速为1.0 mL/min,检测波长为278 nm。CAP标准曲线的建立:配置一系列浓度为0.1 mg/L、0.2 mg/L、0.5 mg/L、1.0 mg/L、2.0 mg/L、5.0 mg/L与10.0 mg/L的CAP标准溶液,分别测定其峰面积,利用归一法积分得到标准曲线方程。
1.2.2 CAP降解率的测定
试验过程:配置浓度为10.0 mg/L的CAP废水200 mL,加入一定量的零价铁(Fe0),于机械搅拌仪上进行降解反应,间隔一定时间取样经0.45 μm滤膜过滤后测定。降解过程中CAP浓度采用高效液相色谱法(HPLC)进行测定,并经公式(1)计算CAP去除率。实验中采用NaOH(1.0 mol/L)或HCl(1.0 mol/L)调整体系中的pH。依据CAP标准曲线计算出降解过程中CAP浓度,CAP降解效率由公式(1)进行求算。
其中,R为CAP的去除率(%),C0为初始CAP质量浓度(mg/L),Ct为降解过程中CAP质量浓度(mg/L)。每个样品平行测定三次,最大标准偏差小于等于5.0%,取平均值进行分析。
1.2.3 CAP降解条件的优化
采用单因素实验分别对以下条件进行优化:铁粉用量(0.5 g、1.0 g、1.5 g、2.0 g、2.5 g、3.0 g、3.5 g);溶液pH(3.0、5.0、6.7、7.0、9.0);H2O2用量(0.5 mL、1.0 mL、1.5 mL、2.0 mL、2.5 mL);搅拌速率(100 r/min、200 r/min、250 r/min、300 r/min、400 r/min)以及磁场强度(1.0 mT、5.0 mT、10.0 mT、15.0 mT、20.0 mT)进行优化,通过考察CAP的去除率来获取最佳实验条件。
1.2.4 作用机理分析
1)亚铁离子(Fe2+)的含量的采用邻菲罗啉法进行测定,标准曲线的制作及具体的操作流程参照文献进行[23-24]。
2)单独H2O2体系中氧化还原电位(ORP) 采用多参数分析仪测定。
3)Fe0的表征:采用SEM对原始Fe0和弱磁场作用下的Fe0的表面结构特性进行分析。
2 结果与讨论
2.1 CAP标准曲线的确立
以CAP质量浓度为横坐标,峰面积为纵坐标绘制标准曲线,如图1所示。其线性相关系数R2=0.999 8,该结果表明,CAP质量浓度位于0.0~10.0 mg/L标准曲线具有较好的相关性,可用于试验过程中CAP质量浓度的计算。
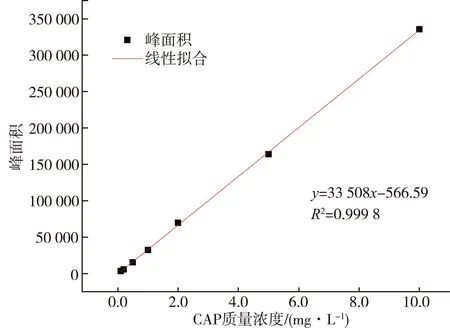
图1 CAP标准曲线
2.2 降解条件的优化
2.2.1 Fe0用量对CAP降解效能的影响
由图2可知,随着Fe0用量的增加,CAP的去除率逐渐上升,但是当Fe0用量为位于2.0~3.5 g时,去除率增长速率增加不明显,从应用和经济角度考虑,本实验中选取Fe0用量为2.0 g。
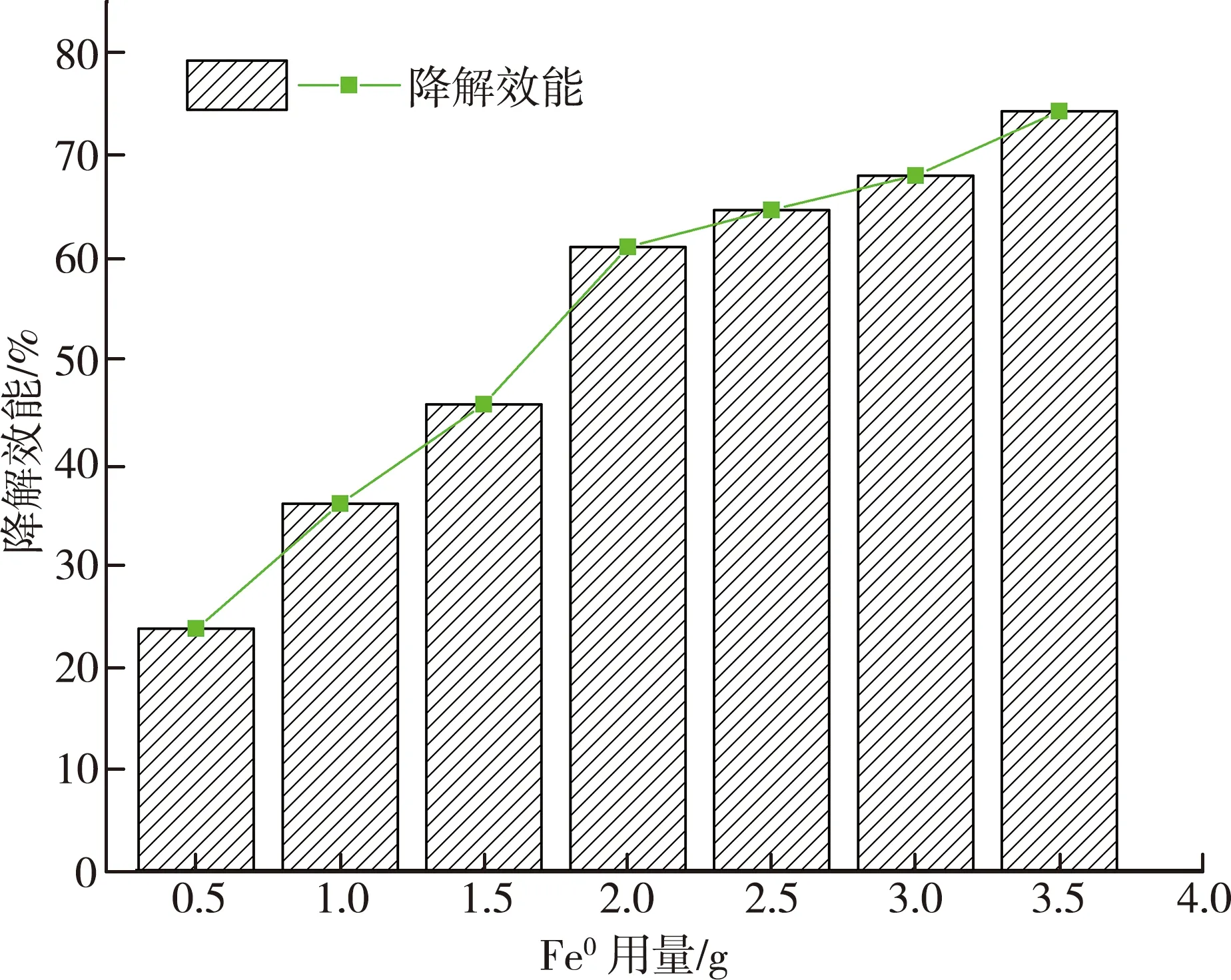
图2 Fe0用量对CAP降解效能的影响
2.2.2 搅拌速度对氯霉素降解效能的影响
从图3中可以看出,当搅拌速度为200 r/min时,CAP降解效率达到最大。这是因为搅拌的目的在于促进Fe0与废水的有效接触,当转速为100 r/min,不利于Fe0与废水的充分接触,抑制了Fe0的降解效能,从而CAP的去除率降低。当转速超过200 r/min时,CAP的去除率变化不显著,考虑到工程运营成本因素,研究中选取200 r/min的转速。

图3 不同的搅拌速度对CAP降解效能的影响
2.2.3 pH对氯霉素降解效能的影响
pH对CAP降解效能的影响如图4所示,结果表明,在上述pH条件下,均能取得较好的降解效果。相对来说,在pH在3.0与5.0之间的降解率优于其他pH。这是因为酸性条件下,Fe0容易失去电子产生更多的Fe2+及还原的[H],促进了CAP的降解。考虑到实际应用中,出水pH均控制在6.0~9.0之间,同时为了节约调整酸用量带来的经济成本,可以选取在CAP原液pH 6.7条件下进行降解研究,本文选取pH 3.0进行研究,目的在于探索其在酸性条件下的作用机理与效能。
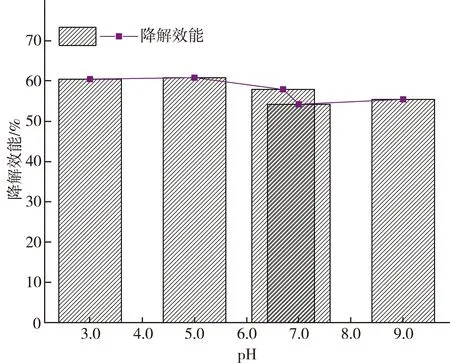
图4 pH对CAP降解效能的影响
2.2.4 H2O2的用量对CAP降解效能的影响
H2O2的用量对CAP降解效能的影响如图5所示。当H2O2的用量为1.0 mL时,CAP去除率提升速率最快。这是因为在体系中,H2O2的加入,与Fe0构成了Fe0+H2O2类Fenton体系,该体系集氧化还原为一体,从而加速了CAP的降解,在Fe0+H2O2体系中,Fe0与H2O2的用量决定体系的氧化还原性能的强弱,过量的H2O2会导致副反应的发生,抑制该体系的氧化还原性能[26],因此,本实验中选用H2O2的用量为1.0 mL。

图5 H2O2的用量对CAP降解效能的影响
2.2.5 磁场强度对CAP降解效能的影响
由图6所示,当外加磁场为10.0 mT的时候,对CAP废水的处理效果最好,这是外加磁场较弱的情况下,促进效果不明显,当磁场强度超过10.0 mT时,在磁场的作用下,铁粉容易被吸附沉降,造成是铁粉颗粒凝聚,与废水接触减弱,从而导致去除效率降低[18]。

图6 磁场强度对CAP降解效能的影响
据以上研究可得到该反应体系的最佳操作条件:CAP初始浓度10.0 mg/L,反应时间为210 min,铁粉粒径100目,铁粉投加量2.0 g,pH为3.0,外加磁场最佳为10.0 mT,H2O2的添加量为1.0 mL (30%),搅拌速度为200 r/min。在最佳反应条件下:单独Fe0体系,Fe0+H2O2体系以及Fe0+H2O2+WM体系对CAP的去除率分别为60.9%、72.9%、86.3%。
2.3 机理研究
2.3.1 Fe0的作用机理
为了研究Fe0的作用机理,对Fe0+H2O2+WM体系中的可能存在的Fe2+与Fe3+的质量浓度进行了测定。为了确定体系中总的Fe2+的量,加入盐酸羟胺溶液,摇匀静置10 min之后,测定吸光度为1.9(稀释原浓度的1/5测定),由Fe2+的标准曲线方程(图7)可计算得到体系中Fe2+的总质量浓度为32.6 mg/L,另外,未加盐酸羟胺时,测定体系的吸光度为1.7,同理可得该体系中净Fe2+质量浓度为29.6 mg/L,由此可得,体系中Fe3+的质量浓度为3.0 mg/L。该结果说明:Fe0+ H2O2+ WM体系是一个集Fe0、Fe2+与Fe3+于一体的共存体系,协同作用于CAP的降解,主要包括以下三个方面的机理:
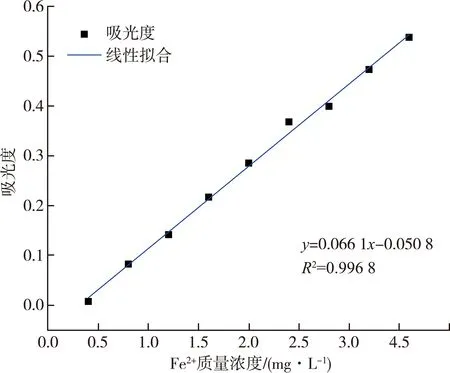
图7 Fe2+标准曲线
1)Fe0作用机理[25]




2)类Fenton反应机理[26]:




3)混凝吸附作用[16]


2.3.2 H2O2作用机理分析
为了考察H2O2对CAP降解中的作用,以单独添加H2O2的CAP体系做了对照实验,结果如图8所示。研究发现,体系中的氧化还原电位(ORP)基本维持不变,而且CAP去除效率也在误差范围之内,由此可以推断:H2O2本身对CAP的氧化降解效率较低,该结果与文献研究相一致[27]。由上述研究结果可知,尽管如此,H2O2可以作为氧化剂,与溶液中Fe0以及产生的Fe2构建类Fenton体系[23],促进CAP废水的降解。

图8 H2O2对CAP降解效能的影响及反应过程中ORP变化
2.3.3 弱磁场作用机理
如图9(a)所示,原始Fe0表面较光滑,孔隙率少,在磁场作用下,Fe0表面变得粗糙且疏松,空隙丰富(图9(b)),该结构有利于比表面积的增大从而提升其表面性能,在一定程度上可有效避免Fe0的凝聚[18-23]。这是因为磁技术在水污染治理中的应用主要是利用磁场的分离能力,具有铁磁性的Fe0颗粒在外部弱磁场(<100 mT)中会被磁化,被磁化的Fe0表面会产生磁感应强度可能比外部磁场更大的非均匀诱导磁场[28-29]。由磁场中的运动带电电荷产生的洛伦兹力会使得电解质溶液中的离子产生对流,Fe2+脱离Fe0,H+向Fe0表面迁移,加强Fe0表面腐蚀;在磁场界面上产生作用于顺磁性离子边界层的磁场梯度力,使得顺磁性Fe2+离子迁移、钝化膜破坏及局部腐蚀[29]。因此,磁技术作为一种物理技术,应用于水处理过程中可减少或避免额外能量和化学品的使用[28]。此外,弱磁场可通过影响电子的自旋作用进而抑制活性自由基的复合而提高反应效率[30]。

(a)—原始Fe0 ;(b)—磁场作用下的Fe0
3 结论
本研究采用弱磁场与H2O2协同驱动Fe0降解氯霉素废水。研究结果表明,该体系对CAP具有较好的降解性能,一方面,外加弱磁场的引入,在提升降解性能的同时可在一定程度上减少化学试剂的使用,从而可有效节约运行成本;另一方面 Fe0+H2O2可在较宽的pH范围应用,是对经典芬顿体系(Fe2++H2O2)的有效拓展,因此,本研究具有一定的理论与应用价值,为Fe0的应用以及抗生素废水的处理提供新的途径与方法。
