贝伐珠单抗联合伊立替康和卡培他滨治疗大肠癌的疗效分析
2022-07-12王婷胡玉海白琳周毅胡红平郑晓丹
王婷,胡玉海,白琳,周毅,胡红平,郑晓丹
大肠癌是一种常见的消化道恶性肿瘤,男性发病率明显高于女性,伴随人们饮食习惯的改变以及饮食结构的调整,我国大肠癌发病率呈不断升高趋势,且1/4左右患者在初次确诊时已处于疾病晚期[1-2]。以手术为主,联合化疗、放疗进行综合治疗是治疗大肠癌的经典方案[3]。以贝伐珠单抗、帕尼单抗以及西妥昔单抗等为代表的靶向药物逐渐被应用于临床。贝伐珠单抗可通过特异性结合血管内皮生长因子(vascular endothelial growth factor,VEGF),对血管内皮细胞生成起负调控作用,继而抑制新生血管形成,最终抑制肿瘤生长[4]。贝伐珠单抗已被批准用于晚期大肠癌的治疗中,贝伐珠单抗联合常规化疗药物治疗晚期大肠癌,可明显改善患者生存情况和肿瘤相关症状,阻滞肿瘤进展[5]。报道[6-7]亦证实,针对采用含贝伐珠单抗化疗的一线治疗方案进行治疗后且未进展的肿瘤患者,维持贝伐珠单抗治疗能够使患者持续受益。但目前针对受益的患者采用含贝伐珠单抗的方案进行维持治疗并未达成一致意见。基于此,本研究通过观察贝伐珠单抗联合伊立替康和卡培他滨方案治疗大肠癌的疗效,并分析其对患者血浆免疫细胞水平、白蛋白/球蛋白比值(albumin/globulin ratio,AGR)和3年生存期的影响,报道如下。
1 资料与方法
1.1 临床资料
选取2016年1月至2018年1月武汉市汉口医院收治的63例大肠癌患者作为研究对象。纳入标准:①符合《中国结直肠癌诊疗规范(2020年版)》[8]有关大肠癌诊断标准;②组织病理学证实为大肠癌,包括初诊不可手术切除的转移性大肠癌和根治手术后复发的大肠癌;③一线或二线治疗后病情得到有效控制;④心肝肾功能基本正常。排除标准:①合并严重内科疾病者;②排除美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分≥3分;③无法耐受一线化疗药物毒性,且未获得生存效益者;④其他恶性肿瘤者;⑤心力衰竭者。按治疗方案不同将患者分为对照组(n=33)和维持组(n=30),两组性别、年龄、体质量指数(body mass index,BMI)、ECOG评分、转移部位等方面存在可比性,差异均无统计学意义(P>0.05),见表1。本次研究取得了医院伦理委员会批准,患者均主动签署书面知情同意书。
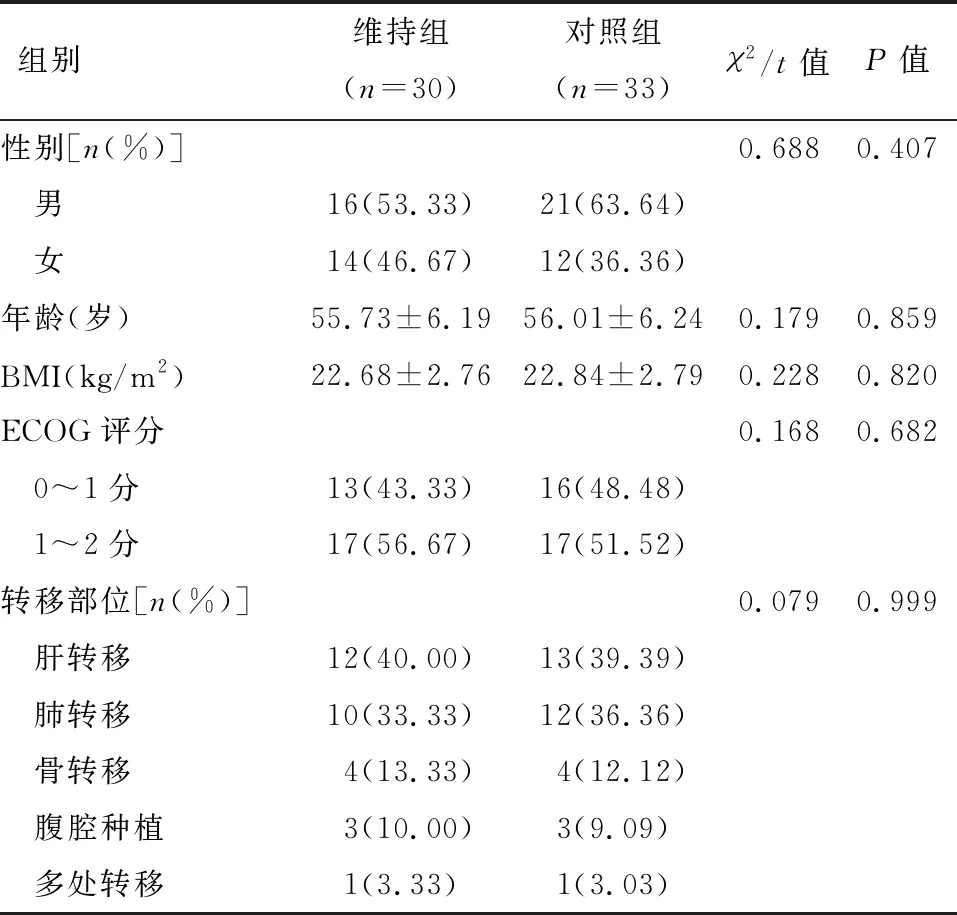
表1 两组一般资料比较
1.2 方法
(1)对照组:应用改良伊立替康和卡培他滨方案,治疗方法如下:伊立替康(国药准字H20068128,规格5 mL:100 mg,齐鲁制药有限公司)200 mg/m2静脉滴注30~90 min,每3周用药1次;卡培他滨(国药准字H20073023,规格:0.5 g,上海罗氏制药有限公司)口服,800 mg/m2bid,2次/d,连续服用2周,休息1周,早晚饭后半小时内温水送服,每3周为1个疗程,患者病情均得到有效控制,对照组停药观察,定时随访。
(2)维持组:继续使用贝伐珠单抗(生产企业:Genentech Inc.,注册证号S20100024)治疗,7.5 mg/kg,第1 d静脉滴注,首次输注时间持续90 min,若患者耐受性良好,则第二次输注时间缩短为60 min,若60 min输注耐受性亦良好,随后输注均按30 min完成,贝伐珠单抗持续治疗直到患者无法耐受患者疾病进展终止,3周为1个周期。连续使用3个周期后对两组患者疗效进行评价。
1.3 观察指标
(1)治疗疗效:治疗疗效参照《实体肿瘤疗效评价标准(response evaluation criteria in solid tumors,RECIST)》[9]判定,内容包括:病灶完全消失且转移性病灶直径小于10mm(complete response,CR);病灶半径总和减少大于及等于30%(partial response,PR);病灶半径改变处于PR和PD之间(stable disease,SD);病灶半径总和增加大于及等于20%(progressive disease,PD),其中客观缓解率=(CR例数+PR例数)/总患者例数×100%。
(2)血浆免疫细胞水平:收集两组患者治疗前后外周血3 mL,采集采用流式细胞仪测定两组患者治疗前后血浆免疫细胞水平(CD3+T细胞、CD4+T细胞、CD8+T细胞、CD4+/CD8+T细胞及NK细胞)。
(3)AGR水平:收集两组患者治疗前后外周血3 mL,检测白蛋白、总蛋白水平,并计算AGR,AGR=白蛋白/(总蛋白-白蛋白)。
(4)不良反应:参照世界卫生组织(world health organization,WHO)抗肿瘤药物不良反应分级标准评价两组患者化疗期间毒副反应发生情况。
(5)生存预后:截止末次随访时间2021年1月,通过电话形式或门诊随访完成随访工作,记录两组患者无进展生存时间(progress free survival,PFS)和总体生存时间(overall survival,OS),随访以患者死亡或末次随访而终止,无进展生存时间为患者疾病开始治疗至第一次疾病进展的时间或发生任何原因的死亡之间的时间,总体生存时间为患者疾病治疗开始时间至死亡或者最后一次随访之间的时间。
1.4 统计学分析
2 结果
2.1 两组治疗疗效比较
维持组客观缓解率为66.67%,显著高于对照组的36.36%(P<0.05),见表2。
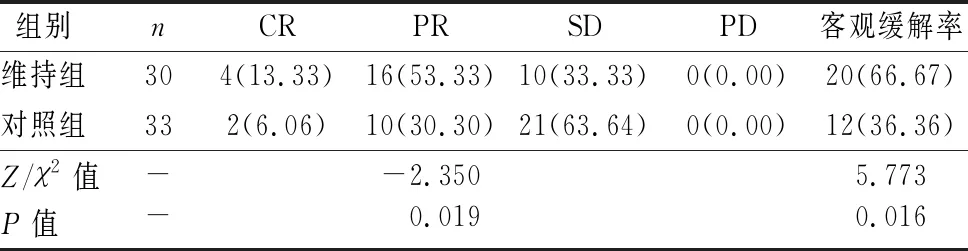
表2 两组治疗疗效比较[n(%)]
2.2 两组血浆免疫细胞水平比较
治疗前,两组CD3+、CD4+、CD8+、CD4+/CD8+及NK水平比较,差异无统计学意义(P>0.05);治疗后,两组CD3+、CD4+、CD4+/CD8+及NK水平较治疗前显著升高(P<0.05),CD8+水平较治疗前显著降低(P<0.05),且维持组CD3+、CD4+、CD4+/CD8+及NK水平显著高于对照组(P<0.05),CD8+水平显著低于对照组(P<0.05),见表3。
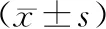
表3 两组治疗前后血浆免疫细胞水平比较
2.3 两组AGR水平比较
治疗前,两组AGR水平比较,差异无统计学意义(P>0.05);治疗后,两组AGR水平较治疗前显著升高(P<0.05),且维持组AGR水平显著高于对照组(P<0.05),见表4。
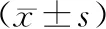
表4 两组AGR水平比较
2.4 两组不良反应发生率比较
维持治疗期间,维持组高血压发生率显著高于对照组(P<0.05),但维持组患者均未出现Ⅳ级严重不良反应。见表5。
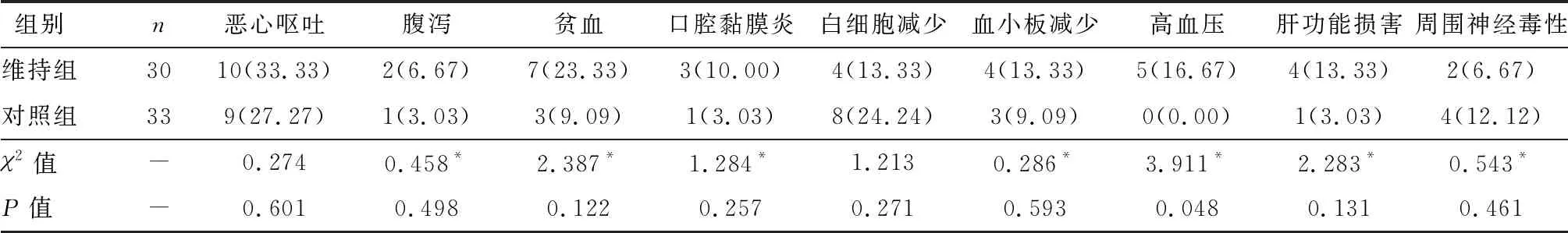
表5 两组不良反应发生率比较[n(%)]
2.5 两组3年生存情况比较
截止末次随访,维持组中位PFS为12.53(95%CI:9.86,15.21)个月,对照组中位PFS为8.16(95%CI:7.04,9.29)个月,差异有统计学意义(P=0.001),见图1;维持组中位OS为19.94(95%CI:17.37,22.52)个月,对照组中位OS为13.62(95%CI:12.13,15.10)个月,差异有统计学意义(P<0.001),见图2。
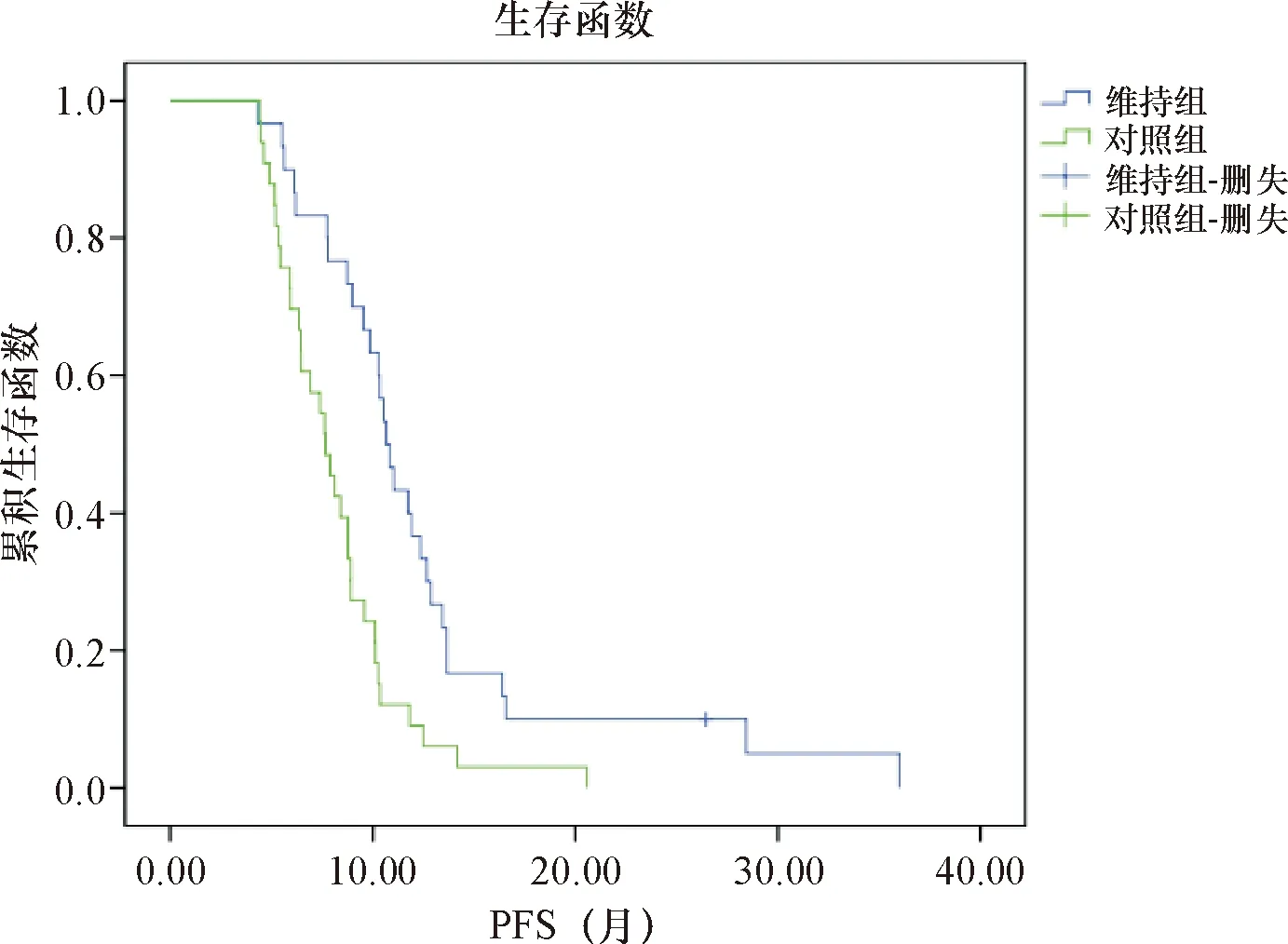
图1 两组无进展生存曲线比较
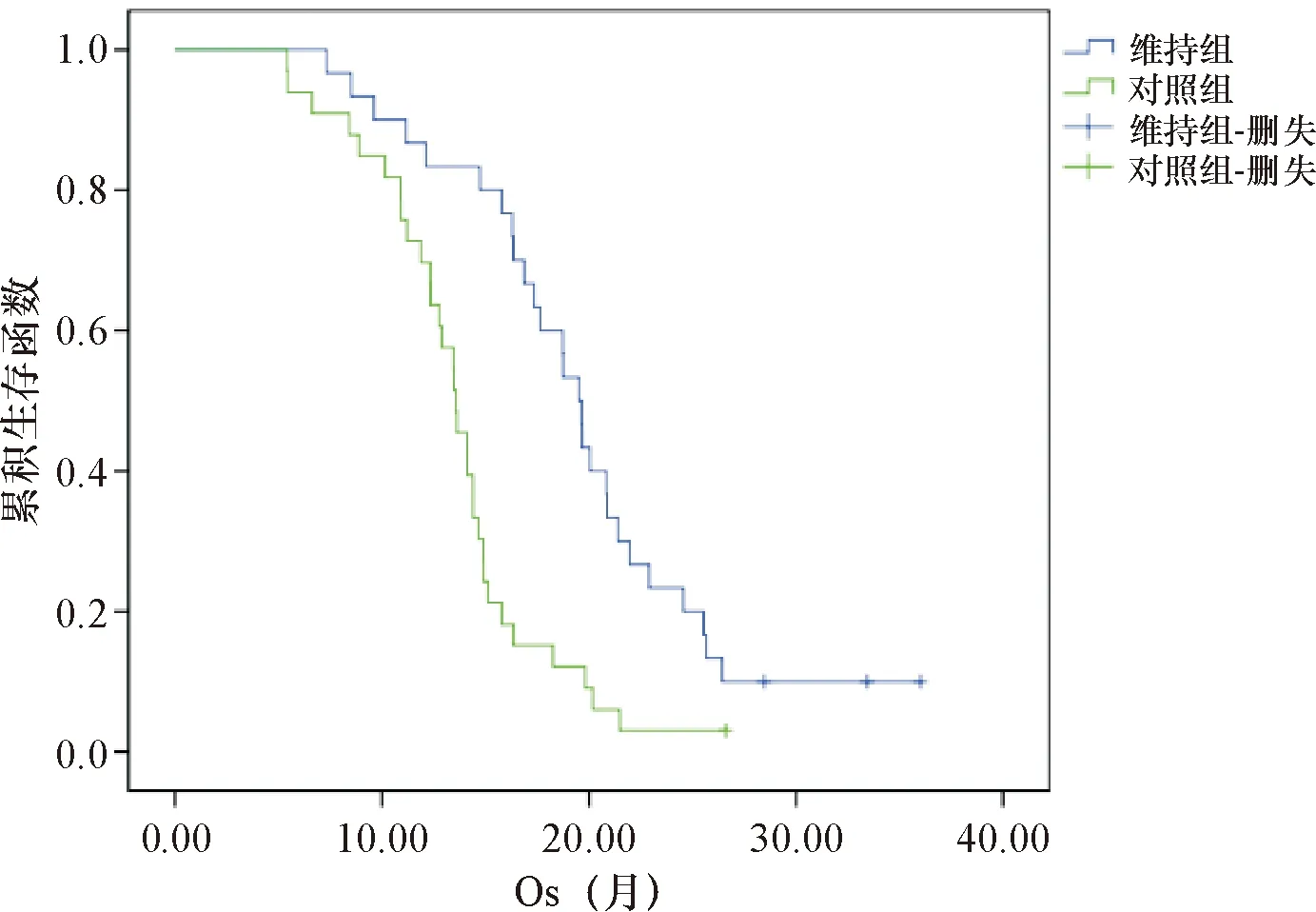
图2 两组总体生存曲线比较
3 讨论
早期大肠癌给予手术治疗后预后较好,患者5年生存率高达90%,而对于无法通过手术治愈的晚期大肠癌,全身化疗则成为其新的选择[10]。但即便通过全身化疗进行控制,晚期大肠癌5年生存率仍低于10%[11-12]。晚期大肠癌目前推荐采用氟尿嘧啶与伊立替康进行联合化疗治疗,但该方案治疗前需进行中心静脉插管,且需每2周进行一次较长时间的输液,患者耐受性较差[13]。卡培他滨为口服用药,且用药周期为每3周一次[14]。与氟尿嘧啶和伊立替康联合化疗方案相比,卡培他滨+伊立替康治疗只需要输液一次,输液时间为2~3 h,每3周治疗一次,且治疗前无需插管[15]。但既往报道[16]表明,卡培他滨联合伊立替康化疗治疗对于欧洲和北美人群具有较大的副作用,患者通常因无法耐受而放弃治疗,进而导致治疗疗效不甚乐观。Xu等[17]报道认为,改良的卡培他滨联合伊立替康具有明显疗效,且患者耐受性良好。Price等[18]亦指明,口服化疗药物(卡培他滨)的化疗方案使得晚期大肠癌的治疗更加简化。目前,《CSCO结直肠癌诊疗指南》已明确将卡培他滨联合伊立替康化疗方案作为晚期大肠癌的二线标准治疗方案。但晚期大肠癌患者在化疗获益后,是继续化疗还是停药观察,亦或选用一种低毒且有效的药物进行维持治疗,一直是临床研究的热点问题。
贝伐珠单抗能够对VEGF与其受体的结合过程发挥抑制作用,进而抑制肿瘤血管生成[19]。既往研究[20-21]证实,贝伐珠单抗联合一线化疗方案可提高晚期大肠癌治疗疗效,还可有效延长患者生存时间。本研究结果显示,维持组治疗总有效率为66.67%,显著高于对照组的36.36%,表明贝伐珠单抗+伊立替康和卡培他滨方案治疗晚期大肠癌效果确切。贝伐珠单抗可特异性结合VEGF并抑制其活性,从而对肿瘤新生血管形成起到抑制作用,进而阻碍肿瘤组织汲取营养,最终延缓肿瘤生长。与洪波等[22]报道相符。晚期大肠癌患者多数存在免疫抑制现象,机体免疫功能低下,以致其抗肿瘤和抗毒副反应能力降低[23],此外还容易增加术后切口感染风险[24]。本研究结果显示,治疗后,维持组CD3+、CD4+、CD4+/CD8+及NK水平显著高于对照组,CD8+水平显著低于对照组,表明联合贝伐珠单抗进行维持治疗可激活机体免疫细胞活性,发挥免疫保护作用。另外,本研究中,维持组AGR水平显著高于对照组,提示贝伐珠单抗维持治疗可抑制机体炎症反应,促进促肿瘤炎症反应和抗肿瘤免疫反应恢复平衡。李生平等[25]报道表明,低AGR水平与结肠癌不良预后有关,积极改善患者AGR状态及增强抗肿瘤免疫功能有着重要的临床意义。进一步分析发现,维持治疗期间,尽管维持组出现4例高血压,但两组恶心呕吐、腹泻、贫血等其余不良反应发生率比较,差异无统计学意义,提示联合贝伐珠单抗并不会显著增加化疗毒副反应。而Kaplan-Meier曲线分析结果显示,相比于对照组,维持组中位PFS和中位OS显著延长,表明贝伐珠单抗联合伊立替康和卡培他滨方案治疗晚期大肠癌可有效控制肿瘤进展,延长患者生存时间。程建平等[26]报道表明,靶向药物西妥昔单抗联合伊立替康和卡培他滨方案治疗转移性大肠癌的客观缓解率和疾病控制率与西妥昔单抗联合伊立替康+醛氢叶酸+氟尿嘧啶方案治疗比较无明显差异,且两种方案的不良反应及患者PFS均无明显差异,提示西妥昔单抗联合伊立替康和卡培他滨方案有可能作为治疗转移性大肠癌的一线方案的备选。本研究与之相符。但本研究收集样本有限,故研究所得结论有待纳入更多样本及开展更多研究以佐证。
综上所述,贝伐珠单抗联合伊立替康和卡培他滨方案治疗大肠癌具有明显疗效,可改善患者免疫功能,延长患者中位生存时间,提高总体生存率,耐受性良好。
