基于网络药理学探讨自拟黄芪首乌酊方对治疗雄激素性脱发的作用机制*
2022-07-11万信良招浩熙蒋洋洋
万信良,招浩熙,贺 颖,蒋洋洋,龙 楠,黄 聪
(贵州中医药大学,贵州 贵阳 550025)
雄激素性脱发(Androgenetic alopecia,AGA)是临床皮肤科最常见的脱发类疾病之一。AGA的发生主要与雄激素代谢紊乱相关,是雄激素依赖性遗传性疾病之一[1]。同时,Öztürk Perihan[2]研究发现雄激素在AGA当中亦占有较重要的地位。据有关调查统计[3],我国约有21.3%的男性和6.0%的女性不同程度地患有雄激素性脱发。AGA症状主要表现为患者发量逐渐减少、毛发逐渐纤细等。AGA在对毛囊破坏的同时,也对患者精神状态方面造成了一定程度的影响,出现焦虑、抑郁等心理疾病[4]。目前,AGA的病因及发病机制尚未明确,但其发病机制与5α-还原酶、双氢睾酮(DHT)和雄激素受体(AR)之间的相互作用密切相关。现代医学主要通过特异性抑制Ⅱ型5α还原酶或增强钾离子通道开放以达到抑制睾酮(T)转化为双氢睾酮(DHT)、促进头皮毛细血管增生及毛囊细胞增殖的作用。临床上主要以非那雄胺、米诺地尔为常见的AGA治疗药物。但口服非那雄胺后可能会出现性功能障碍及焦虑抑郁为主要症状的“非那雄胺综合征”,使用米诺地尔可能导致局部炎症、水肿、心悸等不良反应[5]。
AGA在中医学中属于“发斑脱发”“驻发廯”范畴,以肝肾亏虚、血虚风燥、湿热浸润为主要病机。《素问·上古天真论》曰:“丈夫八岁,肾气实,发长齿更……五八,肾气衰,发堕齿槁”“女子七岁,肾气盛,齿更发长……五七,阳明脉衰,发始堕”,说明毛发的生长与肾气关系密切;《素问·六节藏象篇》曰“肾者,主蛰,封藏之本,精之处也,其华在发”“肺者,气之本,其华在毛”,说明毛发需要肾精滋润,肺气宣发才得以正常生长。自拟黄芪首乌酊方以黄芪、制首乌、熟地黄、墨旱莲、女贞子、侧柏叶、桔梗、生姜等八味药物组成,方中黄芪、何首乌共为君药,补气益血,调补肝肾;臣以墨旱莲、女贞子、熟地黄以补肾填精,乌发生发;佐以侧柏叶、桔梗,清热凉血,宣发肺气;使以生姜,引归肺经;诸药合用,共奏补肝益肾、宣发肺气的功效。
黄芪首乌酊复方成分的复杂性对其具体活性成分、相关靶点及信号通路等方面的研究也产生了制约作用。而网络药理学是一个新兴于大数据时代并利用人工智能系统性地对药物进行研究的学科,其以现代生物信息技术为基础,通过对药物、活性成分、靶点及疾病之间的关联规律分析,对中药及其复方治疗相关疾病的潜在作用进行数据挖掘及网络分析,对我们进行中医药的现代研究有客观促进作用[6]。而目前基于网络药理学探讨中药及复方成分对于治疗AGA的作用机制方面尚属空白,因此本文运用网络药理学方法探讨黄芪首乌酊治疗AGA的作用机制,为治疗AGA提供新的研究思路及相关数据参考。
1 资料与方法
1.1 黄芪首乌酊的有效活性成分及药物靶点的筛选
利用TCMSP(http://tcmspw.com/tcmsp.php)检索黄芪、墨旱莲、女贞子、熟地黄、侧柏叶、桔梗、生姜的主要化学成分,对比药物动力学参数(ADME),将其标准设定为口服利用度(oral bioavailability,OD)≥30%,类药性(drug-likeness,DL)≥0.18,通过以上两项关键指标筛选黄芪、墨旱莲、女贞子、熟地黄、侧柏叶、桔梗、生姜的有效活性化合物;利用BATMAN-TCM数据库(http://bionet.ncpsb.org/batman-tcm/)检索与何首乌相关的有效化学成分,将相关阈值Score cutoff≥20,Pvalue≤0.05作为限定条件初步筛选何首乌活性化合物。选取具有明确作用靶点的活性成分作为黄芪首乌酊候选活性化合物,同时,提取以上药物的靶点蛋白,并通过UniProt数据库(https://www.uniprot.org/)规范靶点蛋白名称。
1.2 AGA靶点收集
在DisGeNET数据库(http://www.disgenet.org/)和OMIM数据库(https://omim.org/)以“Androgenetic alopecia”为检索词,检索AGA的相关靶点,并整合记录,以靶点基因的Score值为参照,AGA的候选靶点以Score值大于中位值的目标靶点为准。
1.3 黄芪首乌酊有效活性成分及药物靶点的网络构建
将黄芪首乌酊的有效活性成分及靶点信息导入cytoscape3.7.2软件,绘制黄芪首乌酊药物-有效活性成分-靶点网络图。
1.4 黄芪首乌酊-AGA蛋白互作(PPI)网络图的构建
将已筛的药物靶点与AGA疾病靶点取核心靶点交集基因后导入String数据库(https://www.string-db.org/),进行蛋白互作网络的拓扑分析,将得到的初步PPI网络图导入cytoscape3.7.2软件,将初步的PPI蛋白拓扑分析网络图进行可视化处理。
1.5 GO和KEGG的富集分析
通过Metascape数据库(http://metascape.org/)、DAVID数据库(https://david.ncifcrf.gov)对黄芪首乌酊治疗AGA的靶点进行GO及KEGG分析,将物种设定为“Homo sapiens”,整合2个数据库结果,选取Pvalue前20的结果(分析结果≤20的以总数计算)进行可视化处理。
2 结果
2.1 黄芪首乌酊有效活性成分及作用靶点蛋白的筛选结果
通过TCMSP数据库和BATMAN-TCM数据库检索获得黄芪活性成分15个,何首乌活性成分16个,女贞子活性成分8个,墨旱莲活性成分8个,熟地黄活性成分2个,侧柏叶活性成分7个,桔梗活性成分3个,生姜活性成分4个。其中共有活性成分5个,合并去重后获得黄芪首乌酊活性成分53个。利用Uniprot对靶点进行规范化命名,最终得到黄芪首乌酊相关靶点基因360个。将有效活性成分及相关靶点基因导入cytoscape3.7.2中,构建“中药-有效活性成分-靶点基因”网络,统一对黄芪首乌酊的药物、有效活性成分、靶点基因进行规范命名:圆形代表各味中药,药物采用药名的大写首字母为编号,如黄芪的编号为“HQ”;正六边形代表有效活性成分,其中各药物唯一成分采用药名的大写首字母加数字的形式,如HQ1、HQ2、HQ3等,多种药物共有成分以A1、A2、B1等作为编码;菱形代表靶点基因。同时,运用软件中的“Analyze Network”,进行度值(degree)计算,度值大小由该节点与其他节点交集度决定,若度值越大,节点面积(Node)越大,连线(Edge)越粗。构建出的“中药-有效活性成分-靶点基因”(图1)。同时,从图1中可观察到槲皮素(quercetin)、木犀草素(luteolin)、β-谷甾醇(beta-sitosterol)、山奈酚(kaempferol)、7-O-甲基异鼠李糖醇(7-O-methylisomucronulatol)、芒柄花素(formononetin)等度值较大,推测这些有效活性成分在黄芪首乌酊治疗AGA当中发挥了重要作用,如表1所示。

图1 中药-有效活性成分-靶点基因网络Fig.1 Network of traditional Chinese medicine-activecomponents-target gene

表1 黄芪首乌酊治疗AGA的主要成分Tab.1 Main effective ingredients of the milkvetchroot-fleeceflower root tincture in the treatment of AGA
2.2 AGA靶点收集结果
通过DisGeNET数据库和OMIM数据库获取“Androgenetic alopecia”的相关靶点基因,并将靶点基因从大到小排列,取Score值中位数1.45,将其大于1.45的靶点基因选取,合并去重后得到相关靶点428个。
2.3 黄芪首乌酊治疗AGA靶点整合
通过将黄芪首乌酊活性成分靶点与AGA疾病靶点进行交集分析,获得35个黄芪首乌酊治疗AGA的共同靶点。并利用Bioinformatics(http://bioinformatics.psb.ugent.be/webtools/Venn/)在线软件绘制黄芪首乌酊成分-AGA靶点Venn图,如图2所示。
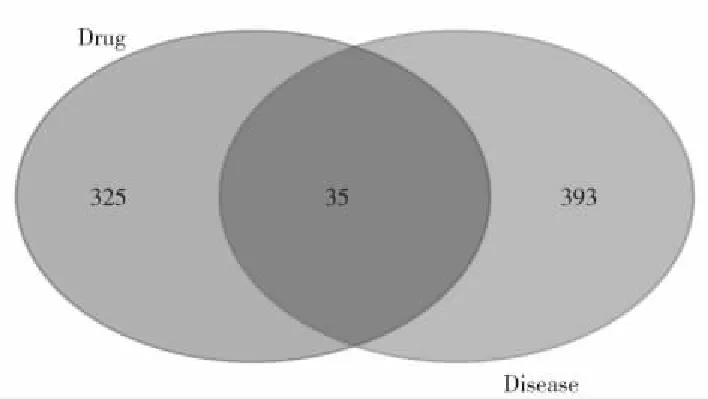
图2 黄芪首乌酊有效活性成分AGA共同靶点Fig.2 Intersection targets of the main effective ingredients ofthe milkvetch root-fleeceflower root tincture and AGA
2.4 蛋白互作网络图(PPI)的构建
将黄芪首乌酊治疗AGA的药物靶点经String数据库得到的初步PPI网络图(图3)导入Cytoscape3.7.2软件,并利用“Analyze Network”绘制PPI网络图,该PPI网络图当中含有35个节点(nodes),306条边(edges),平均节点度值为17.5;节点度值越大,则颜色越红,面积越大,连线越粗。取前20个交集靶点作为核心靶点进行富集分析。绘制出的黄芪首乌酊有效活性成分-AGA靶点PPI图(图4),由图所示,黄芪首乌酊可能通过血管内皮生长因子A(VEGFA)、表皮生长因子受体(EGFR)、白细胞介素6(IL6)、丝氨酸/苏氨酸激酶1(AKT1)、雄激素受体(AR)等关键靶点发挥治疗AGA的作用。
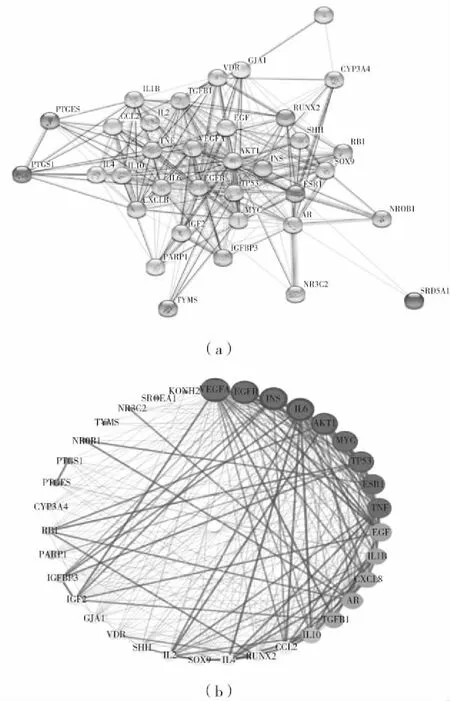
图3 黄芪首乌酊有效活性成分-AGA靶点PPI网络图Fig.3 PPI network map of the targets of the main effectiveingredients of the milkvetch root-fleeceflower roottincture and AGA
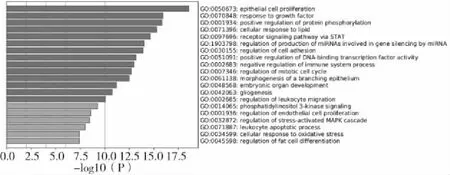
图4 GO富集分析(BP)Fig.4 Analysis of GO enrichment(BP)
2.5 GO功能富集分析
使用Metascape数据库对黄芪首乌酊治疗AGA的核心靶点进行GO功能富集分析,经过校正Pvalue,设定P<0.01后,提取前20个生物学过程(BP)条目,其中主要涉及上皮细胞增殖(epithelial cell proliferation)、对生长因子的反应(response to growth factor)、细胞对脂质的反应(cellular response to lipid)、蛋白质磷酸化的正调控(positive regulation of protein phosphorylation)、通过STAT 的受体信号通路(receptor signaling pathway via STAT)等,见图5所示;总共获取5个分子功能(MF)条目,其中主要涉及受体配体活性(receptor ligand activity)、一氧化氮合酶调节活性(nitric-oxide synthase regulator activity)、DNA结合转录因子结合(DNA-binding transcription factor binding)等,见图6所示;总共获取2个细胞组成(CC)条目,其中主要涉及囊泡腔(vesicle lumen)、血小板α颗粒腔(platelet alpha granule lumen)、分泌颗粒腔(secretory granule lumen)、细胞质囊泡腔(cytoplasmic vesicle lumen)、转录调节复合体(transcription regulator complex)等,见图7。
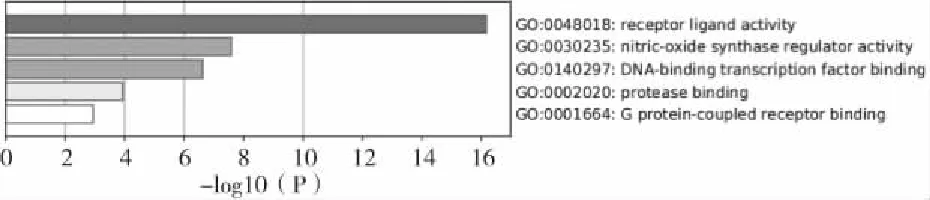
图5 GO富集分析(MF)Fig.5 Analysis of GO enrichment(MF)
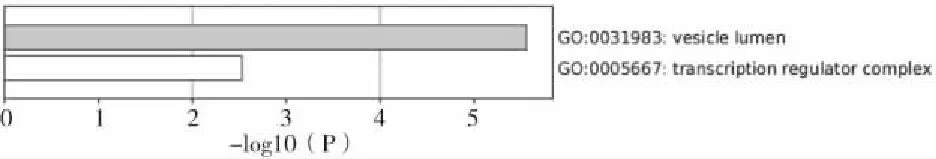
图6 GO富集分析(CC)Fig.6 Analysis of GO enrichment(CC)

图7 KEGG富集分析通路集群Fig.7 Analysis of KEGG enrichment of pathway cluster
2.6 KEGG信号通路富集分析
使用Metascape数据库对KEGG信号通路进行富集分析,并使用Cytoscape3.7.2构建治疗靶点基因-信号通路网络图。通过整合Metascape数据库与DAVID数据库,经KEGG分析得到信号通路76条,设定P<0.01,最小计数为3且富集因子> 1.5,并取排名前20的信号通路建立气泡图,并根据其成员相似性将其分组到相应集群中。总共获取信号通路集群10组,主要涉及PI3K-Akt 信号通路(PI3K-Akt signaling pathway)、癌症中的蛋白多糖(Proteoglycans in cancer)、细胞因子与其受体之间的相互作用(Cytokine-cytokine receptor interaction)、炎症性肠病(Inflammatory bowel disease,IBD)等,见图8所示。通过KEGG通路富集分析获取的气泡图可观察到,排名前20的信号通路主要涉及PI3K-Akt 信号通路(PI3K-Akt signaling pathway)、膀胱癌(Bldder cancer)、炎症性肠病(Inflammatory bowel disease,IBD)、类风湿关节炎(Rheumatoid arthritis)、细胞因子与其受体之间的相互作用(Cytokine-cytokine receptor interaction)等。
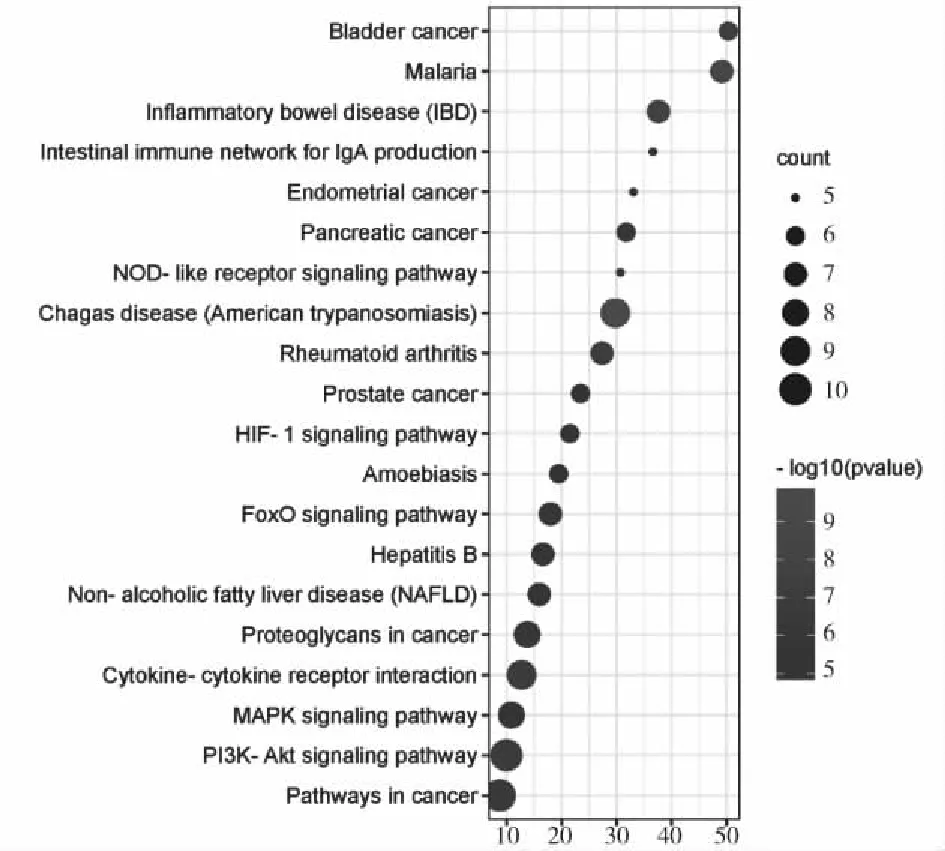
图8 KEGG通路富集分析Fig.8 Analysis of KEGG pathway enrichment
3 讨论
3.1 药物有效活性成分分析
通过本研究发现,黄芪首乌酊发挥补益肝肾、宣发肺气功效的主要活性成分包括槲皮素、山奈酚、木犀草素、β-谷甾醇、豆甾醇、7-O-甲基异鼠李糖醇、芒柄花素等。其中,槲皮素通过抑制CYP17A1 基因表达发挥了对磷脂酰肌醇3-激酶合成雄激素的抑制作用[7];山奈酚可通过调节促炎基因以及阻断NF-kB 和 AP-1来发挥抗炎作用,因炎症因子对雄激素代谢呈正相关影响[8],因此,山奈酚可通过发挥抗炎作用抑制雄激素的分泌增多;谯旭芳[9]研究表明木犀草素可降低大鼠血清中的二氢睾酮(DHT)水平以及对雄激素受体(AR)的表达产生显著抑制作用;吴国欣[10]等研究明确β-谷甾醇可对小鼠血清酸性磷酸酶活力产生抑制作用,进而发挥了抗雄激素及抗炎的活性作用;豆甾醇可通过降低环氧合酶-2( Cox-2 )和NF - kB( p65 )的表达以达到减少氧化刺激和炎症的目的[11],因炎症因子与雄激素的代谢呈正相关关系,故豆甾醇可通过抗炎相关机制达到抑制雄激素分泌增多的目的;芒柄花素可对T47D细胞ERα表达起到增强作用[12],而增强激动ERα表达可使雌激素分泌增多,在雌激素对多种炎症性疾病的调节下[13],可通过抗炎机制对雄激素分泌增多进行抑制。综上所述,黄芪首乌酊当中的关键活性成分通过抑制雄激素合成、发挥抗炎机制作用、增强激动雌激素受体α(ERα)表达能力等方面对AGA的治疗具有潜在作用。
3.2 共同靶点分析
图4显示,VEGFA、EGFR、IL6、AKT1、AR等靶点在黄芪首乌酊治疗AGA当中发挥关键作用。AKT1是一种重要的丝氨酸/苏氨酸蛋白激酶,对细胞的增殖和凋亡具有调控作用。其通过参与PI3K/Akt信号通路正向调控或负向调控AR蛋白的表达,而AR也可通过不同途径抑制或激活Akt[14]。黄芪、制首乌可通过抑制PI3K/AKT信号通路的激活[15-16],负向调控AR蛋白的表达,达到抑制雄激素分泌、治疗AGA的目的。VEGFA是重要的血管内皮生长因子之一,EGFR是一种重要的生长因子受体,两者在对促进血管生成、增强毛囊周围微循环、促进毛囊再生方面发挥着重要作用[17]。黄芪提取物可通过升高VEGF的表达,促进新生血管的形成[18];也可通过调节Wnt/β-catenin信号通路发挥对表皮干细胞增殖分化的促进作用[19]。IL-6是具有免疫调节及促进炎症因子表达功能的一种细胞因子,其在由胰岛素抵抗而引起的代谢综合征(MS)患者血清当中浓度显著升高,而胰岛素抵抗与AGA紧密联系,同时AGA的发生与MS呈正相关关系[20-22]。黄芪、桔梗、墨旱莲、女贞子可抑制血清中IL-6的产生[23-25]。
3.3 生物功能及信号通路分析
通过对核心靶点进行GO和KEGG富集分析,预测黄芪首乌酊治疗AGA参与了多种生物学过程、细胞组成、分子功能及信号通路作用,主要涉及上皮细胞增殖(epithelial cell proliferation)、对生长因子反应(response to growth factor)、蛋白质磷酸化的正调控(positive regulation of protein phosphorylation)、 PI3K-Akt 信号通路(PI3K-Akt signaling pathway)、癌症中的蛋白多糖(Proteoglycans in cancer)、炎症性肠病(Inflammatory bowel disease,IBD)等,这些通路可能在黄芪首乌酊治疗AGA过程中发挥着重要作用。Takahashi T[27]通过观察人头发角化细胞增殖试验说明了成纤维细胞生长因子-7/角质形成细胞生长因子(FGF-7/KGF)等因子可刺激上皮成分的增殖和分化,促进毛干的伸长。Shin HS[28]通过分析人参皂苷治疗AGA小鼠病理模型的作用机制说明可通过干预TGF-β转化通路以降低TGF-β2和SCAP蛋白的表达进而控制细胞凋亡抑制AGA持续发展。而黄芪也可干预TGF-β转化通路降低TGF-β的表达,发挥类似人参皂苷治疗AGA的作用[29]。Kim MH[30]通过探索黄芪甲苷对毛囊凋亡信号传导的潜在机制中发现,黄芪甲苷 IV 可通过抑制由Fas/Fas L 细胞凋亡途径触发的半胱天冬酶依赖性细胞死亡来延缓自发性退行期,同时黄芪甲苷减弱了毛发角质形成细胞的终末分化以及生长因子和细胞因子的水平,促进毛发再生。Zhang L[18]的相关实验研究也证实黄芪提取物可激活AKT/GSK3beta 和 AKT/mTOR 通路和升高VEGF的蛋白质表达,有助于毛囊周围新血管的生成。Zhang X[31]在探究VEGFA是否对AGA患者毛囊干细胞的凋亡产生影响中发现,血管内皮生长因子可通过PI3K/Akt途径保护毛囊干细胞避免受到雄激素诱导的细胞凋亡的影响。
综上所述,通过对黄芪首乌酊治疗AGA的可视化分析得出,其治疗过程呈现出多成分、多靶点、多通路、多环节、非线性的特点,黄芪首乌酊可能通过槲皮素、芒柄花素、7-O-甲基异鼠李糖醇、豆甾醇、山奈酚、木犀草素等有效活性成分作用于VEGFA、EGFR、IL6、AR、AKT1等关键靶点,调控上皮细胞增殖、对生长因子的反应、抑制Fas/Fas L细胞凋亡信号表达、雄激素的分泌代谢、PI3K-Akt 信号通路以及蛋白质磷酸化的正调控等多种生物学过程、信号通路、分子功能来特异性抑制Ⅱ型5α还原酶或增强钾离子通道开放以达到抑制睾酮(T)转化为双氢睾酮(DHT)、促进头皮毛细血管增生及毛囊细胞增殖的作用,但黄芪首乌酊治疗AGA的作用机制是否和癌症中的蛋白多糖、炎症性肠病等通路作用相关有待相关实验的进一步验证。同时,因为药物与疾病数据库的不全可能导致对相关药物活性成分及疾病靶点筛选出现遗漏;在利用网络药理学对黄芪首乌酊的分析中未考虑到中药的炮制、剂量及用法可能影响到药物有效成分及其治疗作用导致其出现偏差,因此后期需要进一步开展相关生物学实验对黄芪首乌酊的治疗靶点、治疗通路进行科学验证,为黄芪首乌酊治疗AGA提供更可靠的科学依据。
