含偶氮苯基团的松香基阴离子表面活性剂的合成及其性能研究
2022-07-06叶圣丰翟兆兰商士斌宋湛谦
叶圣丰, 翟兆兰, 商士斌, 宋湛谦
(1.中国林业科学研究院 林产化学工业研究所;生物质化学利用国家工程实验室;国家林业和草原局林产化学工程重点实验室;江苏省生物质能源与材料重点实验室,江苏 南京 210042;2.南京林业大学 江苏省林业资源高效加工利用协同创新中心,江苏 南京 210037)
表面活性剂,素有“工业味精”之称,被广泛应用于造纸、食品、石油化工、生物医药、化妆品和涂料等领域。随着石油资源的日渐枯竭以及人们环保意识的增强,生物相容性好、生物降解性好的绿色表面活性剂备受青睐。松香作为我国的特色林业资源,具有产量丰富、可生物降解及生物相容性好等优点。同时,松香的主要成分树脂酸中的三环二萜刚性结构赋予其极强的疏水性,碳碳双键和羧基使其易于化学改性[1-2],这些特性使松香成为制备绿色表面活性剂的重要原料[3-4]。目前已有不同类型的松香基表面活性剂被广泛地应用在杀菌、缓释、拒食、农药分散等领域[5-7]。近年来,Zhai等[8]以松香为原料合成了一种pH值响应型松香基阴离子表面活性剂,其对碳纳米管具有较好的分散性,通过调节体系的pH值还可实现碳纳米管的回收利用。同时,由该表面活性剂制备得到的pH值响应型泡沫不仅具有良好的起泡性和稳泡性,还具有突出的响应性能[9]。宋冰蕾等[10]以脱氢枞酸为原料合成了3种松香基双子表面活性剂,表面性能良好,具有较强的稳泡和乳化性能。Yan等[11]以松香为原料合成了一种聚酯型松香基高分子表面活性剂,该表面活性剂不仅具有良好的表面活性和泡沫能力,还具有优良的乳化性能。松香基表面活性剂同样具有良好的发泡性、乳化性和突出的聚集能力。相比于柔性疏水链,松香基刚性结构的存在促使表面活性剂分子在界面的排列更加有序,增加了界面吸附膜的机械强度,从而有利于泡沫、乳液等体系的稳定。因此,以松香为原料制备的刚性表面活性剂在稳定泡沫、乳液方面具有巨大的优势。本研究以改性松香马来海松酸为原料,经D-A加成、酰亚胺化、重氮化、偶合反应在松香刚性骨架上引入了偶氮苯基团,再经乙酯化和酸碱中和反应得到一种全刚性松香基表面活性剂;对合成的化合物的结构进行了表征,探讨了其表面活性和泡沫性能,以期为松香基表面活性剂结构与泡沫性能的关系研究提供基础数据。
1 实 验
1.1 材料与仪器
马来海松酸,实验室自制[12];马来酸酐、对苯二胺、亚硝酸钠、苯酚、溴乙烷、尼罗红(NR)等均为市售分析纯。Sigma 701型表面张力仪,芬兰Biolin;IS10型傅里叶变换红外光谱(FT-IR)仪,美国Nicolet公司;AVANCE Ⅲ HD AN- 400型核磁共振(NMR)仪,瑞士Bruker公司;Zeiss Axiolab 5型偏光显微镜(POM),德国ZEISS公司。
1.2 化合物的合成
1.2.1合成路线 具体合成步骤如图1所示。
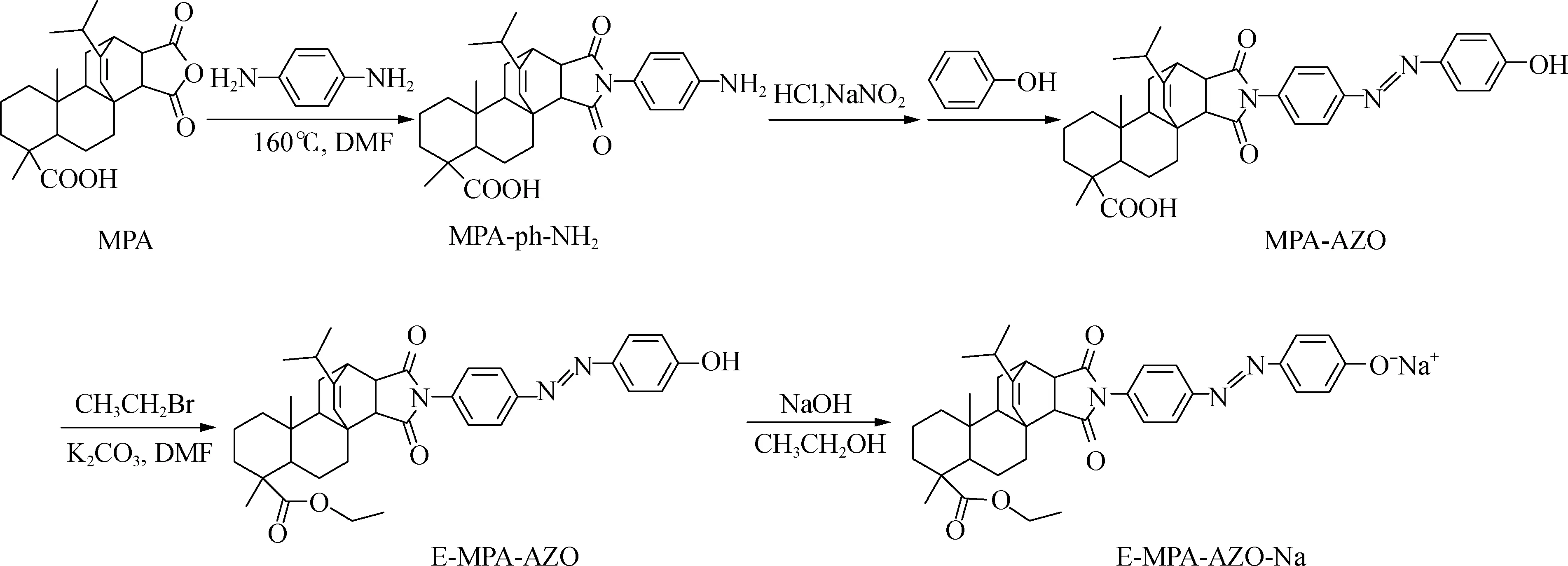
图1 4-马来海松酸乙酯基偶氮苯酚钠(E-MPA-AZO-Na)的合成路线Fig.1 The synthetic routes of compound E-MPA-AZO-Na
1.2.24-马来海松酸基苯胺的合成 准确称取马来海松酸40 g(0.10 mol),对苯二胺12.0 g(0.11 mol)和N, N-二甲基甲酰胺(DMF) 120 g于500 mL三口烧瓶中,加入磁力搅拌子并装好回流装置,升温至80 ℃反应3 h,继续升温至165 ℃反应5 h,反应完毕待反应液冷却至室温,将其倒入400 mL水中,有棕红色固体析出。所得固体经DMF和水重结晶两次得棕色固体,即4-马来海松酸基苯胺(MPA-ph-NH2)。
1.2.34-马来海松酸基偶氮苯酚的合成 将30 g(0.061 mol)MPA-ph-NH2加入烧杯中,冰浴下缓慢滴加水(40 mL)和浓盐酸(45.0 g)的混合液,搅拌至混合均匀后放入冰浴中。将亚硝酸钠5.59 g(0.81 mol)溶于20 mL 水中,冰浴下将其滴入MPA-ph-NH2与浓盐酸体系中,反应过程中保证反应体系为酸性,反应完毕后得到黄色的重氮盐溶液。
将苯酚5.90 g(0.063 mol)和100 mL水加入500 mL三口烧瓶中,搅拌均匀后用NaOH溶液调节pH值至11。冰浴下缓慢滴加重氮盐溶液,并保证反应过程中体系pH值在9~11范围内。滴加过程中有棕黄色固体产生,滴加完毕后继续反应1 h,反应结束后用盐酸调节溶液呈酸性。经抽滤和蒸馏水洗涤2次后得到土黄色粉末,乙醇和水重结晶两次得橙黄色固体,即4-马来海松酸基偶氮苯酚(MPA-AZO)。
1.2.44-马来海松酸乙酯基偶氮苯酚的合成 在N2保护下,将K2CO326.58 g(0.19 mol)和100 mL DMF加入装有磁力搅拌子的500 mL三口烧瓶中,连接好回流装置。搅拌0.5 h后加入MPA-AZO(19.2 g,0.032 mol)的DMF溶液,升温至80 ℃,再一次性加入溴乙烷(3.67 g, 0.034 mol)的DMF溶液,搅拌反应24 h后结束反应。冷却至室温,抽滤,收集滤液,在搅拌下向滤液中加入100 mL冰水,二氯甲烷萃取3次,有机相用去离子水洗涤3次。有机相经无水MgSO4干燥后抽滤,旋蒸除去二氯甲烷,得褐色固体。经石油醚和乙酸乙酯重结晶3次,得橙黄色固体,即4-马来海松酸乙酯基偶氮苯酚(E-MPA-AZO)。
1.2.5目标化合物的合成 将制得的E-MPA-AZO(10.0 g, 0.016 mol)、氢氧化钠(0.67 g,0.017 mol)和80 g的无水乙醇加入装有磁力搅拌子的250 mL单口瓶中,连接好回流装置,将温度升至70 ℃,反应12 h。反应结束后待反应液冷却至室温,旋蒸除去乙醇。用乙醇和丙酮重结晶2次,得橙黄色固体,即为松香基刚性阴离子表面活性剂4-马来海松酸乙酯基偶氮苯酚钠(E-MPA-AZO-Na)。
1.3 结构表征
1.3.1FT-IR分析 采用Nicolet IS10型FT-IR仪对样品进行分析,采用衰减全反射的方法,测试波数范围400~4000 cm-1,每个样品平均扫描16次。
1.3.2NMR分析1H NMR和13C NMR分析均采用Bruker AVANCE 400型NMR仪,溶剂为DMSO-d6和CD3OD,内标物为四甲基硅烷(TMS)。
1.4 表面活性的测定
1.4.1吊片法 采用Sigma 701型表面张力仪Wilhelmy吊片法测定表面活性剂的临界胶束浓度(Ccmc),测定温度为25 ℃。每个点重复测定3次,每个点的测定误差为0.05 mN/m。根据表面张力随浓度的变化曲线可求得E-MPA-AZO-Na的Ccmc和达到临界胶束浓度时的表面张力(γcmc)值。通过Gibbs公式可求得E-MPA-AZO-Na的最大吸附量(Γmax),进一步可得出每个表面活性剂分子在气液界面的最小截面积(amin),计算方法见式(1)和式(2):
(1)
(2)
式中:n—与表面活性剂体系相关的常数,n=2[13];R—气体常数,8.314 J/(mol·K);T—绝对温度,K;γ—表面张力值,mN/m;C—表面活性剂的浓度,mmol/L; dγ/dlgC—表面张力曲线上靠近临界胶束浓度处的最大斜率;NA—阿伏伽德罗常数,6.02×1023。
1.4.2尼罗红荧光探针法 配制0.1 mmol/L 尼罗红(NR)的甲醇溶液10 mL,用取液器量取20 μL配好的NR的甲醇溶液,依次加入到25 mL样品瓶中。用N2将甲醇吹干后,配制10 mL系列浓度的E-MPA-AZO-Na溶液于25 mL样品瓶中。25 ℃下恒温超声波处理2 h后振荡24 h,采用Perkin Elmer LS-55型荧光光谱仪扫描各个溶液中NR的光谱图。激发波长为540 nm,激发狭缝为3 nm,发射狭缝为3 nm,扫描速率为250 nm/min。
1.5 泡沫性能测试
1.5.1泡沫的制备 配制10 mL浓度分别为0.375、 0.75和1.5 mmol/L的E-MPA-AZO-Na水溶液和浓度为1.5 mmol/L的十二烷基硫酸钠(SDS)水溶液,分别置于100 mL的具塞量筒中,用力均匀上下振动20次,室温下静置,记录泡沫体积随时间的变化,绘制表面活性剂的泡沫体积随时间变化的曲线。
1.5.2泡沫粒径的测试 参照1.5.1节中的方法得到相应的泡沫,静置5 min后用吸管吸取一定量的泡沫至载玻片上,用适量的水将泡沫稀释至单层,采用Zeiss Axiolab 5型POM观察泡沫的粒径,将载玻片放置于显微镜的载物台上,调节焦距至图像清晰,并采用ZEISS Axiocam 208拍照系统拍摄泡沫。
2 结果与讨论
2.1 E-MPA-AZO-Na的结构表征

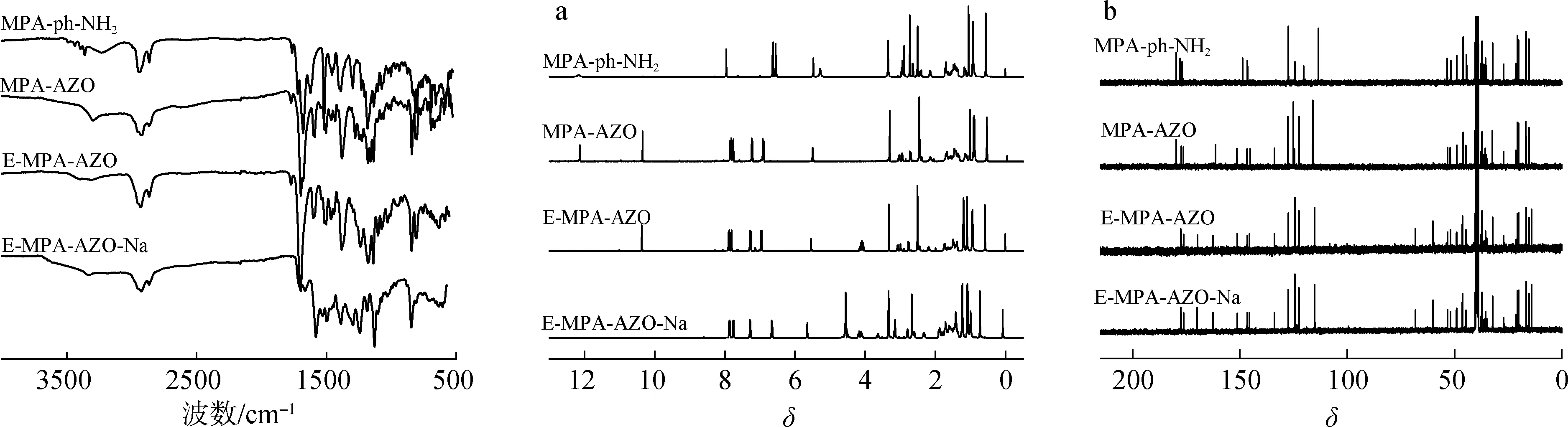
图2 化合物的红外光谱图 图3 化合物的1H NMR(a)和13C NMR(b)Fig.2 FT-IR spectra of compounds Fig.3 1H NMR(a) and 13C NMR(b) spectra of compounds
2.1.2NMR分析 E-MPA-AZO-Na及其中间产物的1H NMR和13C NMR谱图如图3所示。
化合物MPA-ph-NH2,棕色固体,产率76.3%,分子式C30H38N2O4。1H NMR(400 MHz, DMSO-d6)δ: 12.17(s, 1H), 6.64(d,J=8.6 Hz, 2H), 6.55(d,J=8.7 Hz, 2H), 5.50(d,J=13.0 Hz, 1H), 5.28(s, 2H), 3.00~2.91(m, 2H), 2.64(d,J=7.9 Hz, 1H), 2.42(d,J=13.0 Hz, 1H), 2.15(dt,J=13.4, 6.6 Hz, 1H), 1.73~1.34(m, 11H), 1.13(t,J=18.9 Hz, 2H), 1.05(s, 3H), 0.93(dd,J=6.8, 2.2 Hz, 6H), 0.57(s, 3H);13C NMR(101 MHz, DMSO-d6)δ: 179.70, 177.85, 176.87, 148.72, 146.47, 127.40, 124.34, 120.35, 113.48, 53.41, 51.68, 48.98, 45.98, 44.42, 40.44, 37.87, 37.20, 36.41, 35.59, 35.14, 32.32, 27.18, 21.41, 20.70, 20.12, 16.75, 15.40。
化合物MPA-AZO,橙黄色固体,产率62.4%,分子式C36H41N3O5。1H NMR(300 MHz, DMSO-d6)δ: 12.13(s, 1H), 10.35(s, 1H), 7.84(d,J=8.7 Hz, 2H), 7.77(d,J=8.8 Hz, 2H), 7.22(d,J=8.7 Hz, 2H), 6.91(d,J=8.9 Hz, 2H), 5.50(s, 1H), 3.01(dd,J=15.9, 13.2 Hz, 2H), 2.71(d,J=8.2 Hz, 1H), 2.39(s, 1H), 2.22~2.06(m, 1H), 1.51(ddd,J=72.9, 27.8, 11.8 Hz, 11H), 1.13(d,J=12.1 Hz, 2H), 1.02(s, 3H), 0.90(dd,J=6.8, 1.7 Hz, 6H), 0.53(s, 3H);13C NMR(101 MHz, DMSO-d6)δ: 179.71, 177.32, 176.31, 161.32, 151.36, 146.66, 145.27, 133.87, 127.60, 125.09, 124.52, 122.50, 116.05, 53.30, 52.01, 48.94, 45.98, 44.79, 40.55, 37.85, 37.23, 36.42, 35.70, 35.06, 32.37, 27.16, 21.41, 20.74, 20.20, 16.76, 15.39。
化合物E-MPA-AZO,橙黄色固体,产率68.2%,分子式C38H45N3O5。1H NMR(300 MHz, DMSO-d6)δ: 10.35(s, 1H), 7.85(dd,J=20.1, 8.7 Hz, 4H), 7.27(d,J=8.7 Hz, 2H), 6.95(d,J=8.8 Hz, 2H), 5.53(d,J=9.1 Hz, 1H), 4.17~4.01(m, 2H), 3.12~2.95(m, 2H), 2.76(d,J=8.1 Hz, 1H), 2.44(s, 1H), 2.25~2.11(m, 1H), 1.80~1.32(m, 13H), 1.19(t,J=7.0 Hz, 6H), 1.10(s, 4H), 0.95(dd,J=6.8, 1.7 Hz, 9H), 0.58(s, 3H);13C NMR(101 MHz, DMSO-d6)δ: 177.60, 177.23, 176.24, 169.66, 162.53, 151.30, 146.63, 133.85, 127.51, 124.37, 122.49), 115.22, 68.28, 60.03, 53.21, 51.91, 49.08, 46.34, 44.73, 37.69, 37.22, 35.61, 34.98, 32.31, 27.09, 20.67, 20.13, 16.63, 15.36, 14.14。
化合物E-MPA-AZO-Na,橙黄色固体,产率72.5%,分子式C38H44N3O5Na。1H NMR(300 MHz, CD3OD): 7.85(dd,J=20.1, 8.7 Hz, 4H), 7.27(d,J=8.7 Hz, 2H), 6.65(d,J=8.8 Hz, 2H), 5.53(d,J=9.1 Hz, 1H), 4.17~4.01(m, 2H), 3.12~2.95(m, 2H), 2.76(d,J=8.1 Hz, 1H), 2.44(s, 1H), 2.25~2.11(m, 1H), 1.80~1.32(m, 13H), 1.19(t,J=7.0 Hz, 6H), 1.10(s, 4H), 0.95(dd,J=6.8, 1.7 Hz, 9H), 0.58(s, 3H);13C NMR(101 MHz, DMSO-d6)δ: 177.89, 177.27, 176.38, 169.75, 162.43, 151.28, 146.60, 145.56, 133.90, 127.51, 124.43, 122.29, 115.06, 68.29, 60.03, 53.21, 51.97, 49.07, 46.34, 44.76, 40.46, 37.69, 37.26, 36.32, 35.61, 34.97, 32.27, 27.08, 21.30, 20.67, 20.13, 16.63, 15.39, 14.14。
目标化合物的氢谱中,δ7.85处为2个苯环上靠近偶氮基团的4个氢的特征峰,δ7.27为苯环上靠近酰亚胺基团的2个氢的特征峰,δ6.65为苯环上靠近酚钠基团的2个氢的特征峰,δ5.53处为马来海松酸骨架烯烃上氢的特征峰,δ4.17~4.01处为酯基上亚甲基氢的特征峰。目标化合物的碳谱中,δ177.89 处为松香骨架中羧基碳的特征峰,δ177.27, 176.38处为酰亚胺上2个羰基碳的吸收峰,δ169.75 处为与酚钠基团直接相连碳原子的特征峰,δ162.43,151.28处为与偶氮基团相连碳原子的特征峰,δ146.60处则为马来海松酸骨架中与异丙基相连的烯烃碳的特征峰,δ68.29处为酯基上甲基碳的特征峰。结合红外光谱分析可知,目标产物E-MPA-AZO-Na已成功合成。
2.2 表面活性分析
临界胶束浓度(Ccmc)是表面活性剂重要的表面活性参数,Ccmc值越低表明表面活性剂在空气/水界面吸附达到饱和并在溶液中形成胶束的浓度越小,表面活性剂的聚集能力也越强[14]。表面活性剂的溶解性、乳化性、泡沫性与表面活性剂的浓度密切相关,其性质在Ccmc前后通常会发生突变[15]。松香基阴离子表面活性剂E-MPA-AZO-Na的表面张力随浓度的变化曲线如图4(a)所示。由图可知,随着浓度的增加,E-MPA-AZO-Na的表面张力先保持不变后快速下降,继续增加浓度,表面张力随着浓度的增加基本保持不变,此时的浓度即为表面活性剂的Ccmc。E-MPA-AZO-Na的Ccmc值极低,仅为0.035 mmol/L,表明它在水溶液中具有较强的聚集能力。E-MPA-AZO-Na的γcmc值为47.11 mN/m,明显大于普通的表面活性剂。此外,当E-MPA-AZO-Na的pC20值为1.80,表明其能够高效地降低水的表面张力[16]。pC20为表面活性剂溶液的表面张力降低20 mN/m时,所对应表面活性剂浓度的负对数,是表征表面活性剂降低表面张力效率的重要参数。
测定NR的荧光强度(I)对表面活性剂浓度(C)曲线佐证了E-MPA-AZO-Na的Ccmc,结果如图4(b)所示。尼罗红(NR)是一种常见的荧光探针,NR在水中的溶解度极低且对环境的极性非常敏感,其荧光性在极性高的环境中容易被猝灭,几乎不能发射荧光信号;而当体系中形成胶束时,NR便增溶于非极性的表面活性剂胶束内核中,荧光强度会急剧增强。由NR荧光探针法测得该表面活性剂的Ccmc为0.039 mmol/L,与吊片法所得数据基本相同。由此可知,E-MPA-AZO-Na具有极强的聚集能力和较好的表面活性。

图4 E-MPA-AZO-Na的表面张力(a)和NR荧光强度(b)随浓度变化曲线(25 ℃)Fig.4 Variations in the surface tension(a) and intensity of the NR fluorescence(b) with the concn. of E-MPA-AZO-Na(25 ℃)
E-MPA-AZO-Na的Γmax和amin可由Gibbs吸附公式求得,Γmax和amin分别为1.23×10-10mol/cm2和1.35 nm2。表面活性剂分子吸附量越大,分子截面积越小,说明分子在气/液界面上形成了较为紧密的排列。对比普通烷烃链表面活性剂SDS的分子截面积约为0.63 nm2[14],E-MPA-AZO-Na的分子截面积似乎较大,理论上在界面上的排列相对来说不够紧密。但是,E-MPA-AZO-Na分子结构中不仅含有三元菲环刚性骨架,还含有体积较大的刚性偶氮苯基团,这使得E-MPA-AZO-Na的疏水基团具有较大的投影面积[17]。因此,尽管E-MPA-AZO-Na具有较大的分子截面积,但是E-MPA-AZO-Na在气/液界面实际上形成了较为紧密的排列。
2.3 泡沫性能分析
2.3.1起泡和稳泡性能 以1.5 mmol/L的十二烷基硫酸钠(SDS)的泡沫性能作对照,研究了E-MPA-AZO-Na水溶液在不同浓度下的泡沫性能,结果如图5所示。E-MPA-AZO-Na在浓度为0.375、 0.75和1.5 mmol/L时可形成稳定的泡沫,泡沫初始体积分别为8.1、 11.1和16.6 mL,随着浓度的增大,E-MPA-AZO-Na的泡沫初始体积也随之增大。泡沫的半衰期(t1/2),即泡沫的体积降低为初始体积的一半时所需要的时间,是表征泡沫稳定性的重要参数[18]。E-MPA-AZO-Na在浓度0.375、 0.75和1.5 mmol/L时的t1/2分别为1 292、 1 770和2 534 min,均具有较长的泡沫半衰期,表明E-MPA-AZO-Na在3个浓度下均具有较强的泡沫稳定性,且浓度越大稳泡能力也越强。这是因为在低浓度范围内,表面活性剂的浓度越大,吸附到气/液界面的分子越多,对泡沫的稳定作用越强[19-20]。SDS在浓度为1.5 mmol/L时形成的泡沫初始体积为23.4 mL,同等浓度下发泡性能优于E-MPA-AZO-Na。但是,SDS的泡沫半衰期仅为221 min,稳泡性能远远不如E-MPA-AZO-Na。

图5 E-MPA-AZO-Na泡沫体积随时间的变化曲线Fig.5 Variation of foams volume with time of E-MPA-AZO-Na
2.3.2泡沫粒径 气体在不同泡沫之间扩散产生的泡沫粗化过程严重影响着泡沫的稳定性。众所周知,泡沫越小,泡沫抵抗粗化过程的能力越强[21-22]。因此,研究了E-MPA-AZO-Na在不同浓度时泡沫的粒径,结果如图6所示。

a.0.375 mmol/L; b.0.75 mmol/L; c.1.5 mmol/L; d.1.5 mmol/L(SDS)
由图可知,随着E-MPA-AZO-Na浓度的增大,形成的泡沫粒径越小,即泡沫越稳定,与半衰期的实验结果相符。SDS在1.5 mmol/L时形成的泡沫粒径明显大于相同浓度下E-MPA-AZO-Na所形成的泡沫,这也很好地解释了SDS在1.5 mmol/L浓度下泡沫半衰期远小于E-MPA-AZO-Na。相对于含柔性链的表面活性剂,E-MPA-AZO-Na中的松香骨架和偶氮苯基团均为刚性基团,动力学过程缓慢,吸附能垒较大,且吸附过程是不可逆的。因此,表面活性剂分子一旦吸附在气/液界面就难以脱附[23-24]。基于以上原因,该松香基阴离子表面活性剂具有更强的泡沫稳定性。
3 结 论
3.1以改性松香马来海松酸为原料,通过D-A加成、酰亚胺化、重氮化、偶合、乙酯化和酸碱中和反应合成了一种全刚性松香基阴离子表面活性剂E-MPA-AZO-Na,并利用FT-IR、1H NMR、13C NMR确证了结构。
3.2全刚性松香基表面活性剂E-MPA-AZO-Na表现出良好的表面活性,其Ccmc值低至0.035 mmol/L,γcmc为47.11 mN/m,amin为1.35 nm2。
3.3全刚性松香基表面活性剂E-MPA-AZO-Na在浓度为0.375、 0.75、 1.5 mmol/L时的泡沫半衰期分别为1 292、 1 770、 2 534 min,均具有较大的泡沫半衰期,表明E-MPA-AZO-Na在3个浓度下均具有较强的泡沫稳定性,且稳泡能力随浓度的增大而增强。
