肾上皮样血管平滑肌脂肪瘤6例的临床病理分析
2022-06-28封扬夏燕吴玲玲王小双
封扬,夏燕,吴玲玲,王小双
作者单位:宿州市立医院(安徽医科大学附属宿州医院)病理科,安徽 宿州 234000
上皮样血管平滑肌瘤(EAML)由Eble等[1]于1997年首次报道,临床上较少见,约占肾脏肿瘤的0.5‰[2],具有恶性潜能,有复发或转移倾向,其致病机制与结节性硬化症(TSC)基因突变相关[3],目前没有标准的治疗方案,预后无统一认识,术后需严密长期随访。本研究报告6例肾脏上皮样血管平滑肌脂肪瘤,结合临床病史、镜下所见及免疫组化,对其良、恶性诊断及鉴别诊断进行探讨,复习相关文献,以提高对此类肿瘤的认识。
1 资料与方法
1.1 一般资料收集安徽医科大学附属宿州医院2017年3月至2020年8月手术切除且诊断为上皮样血管平滑肌脂肪瘤的病例6例,所有病例均复习临床资料、完善免疫组化标记后经两位副主任及以上医师复片并通过科室内讨论后确诊。本研究符合《世界医学协会赫尔辛基宣言》相关要求。
1.2 方法标本经4%中性甲醛固定,常规脱水、石蜡包埋,HE染色,光镜观察后选取主要病变蜡块行免疫组织化学EnVision法标记。抗体黑色素瘤(HMB-45)、黑色素A(Melan-A),平滑肌肌动蛋白(SMA),内皮细胞标志物(CD34),S-100蛋白(S-100),波形蛋白(Vimentin),转录因子E3(TFE-3),细胞角蛋白(CKpan),共同型急性淋巴细胞白血病抗原(CD10)等试剂均购自福州迈新生物技术开发有限公司,所有标记均设阳性和阴性对照,按试剂说明书操作。
2 结果
2.1 一般资料本研究6 例病人均为女性,年龄最大87岁,最小35岁,平均年龄58.3岁。其中1例为自觉腰部不适伴上腹部胀痛10 d就诊,5例为体检时超声提示肾脏占位,入院CT诊断4例为肾脏占位,肾癌待排,2例为肾错构瘤,本研究6例均无明显结节状硬化特征,3例行根治性单侧肾脏切除术,3例行后腹腔镜下保留肾单位的肿瘤剔除术(NSS)见表1。
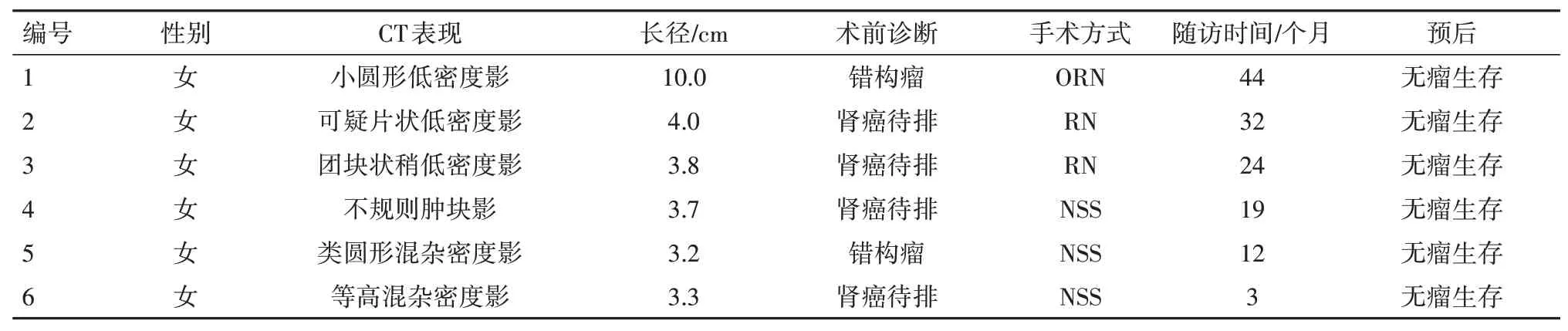
表1 肾脏EAML病人6例临床资料
2.2 巨检6 例EAML 均为手术切除标本,肿块长径3.2~10.0 cm,部分有包膜,与周围组织有较清楚的分界,切面灰红灰白色,部分呈五彩状,质中或质嫩,肿块较大者切面呈囊实性,出血坏死明显,其中一例伴自发性肿瘤破裂。
2.3 镜检6 例EAML 境界均较清楚,肿瘤由上皮样细胞、梭形平滑肌组织、脂肪组织及厚壁血管以不同比例构成,上皮样成分占60%~90%以上。血管大小不一,扭曲变形,管壁增厚,部分伴透明变性。平滑肌组织形态较规则,似成纤维细胞样,部分伴有核的轻度异型性。脂肪组织均发育成熟,呈分叶状分布于肿瘤内。上皮样成分呈巢团状或片状分布,伴不同程度的异型性,细胞圆形,多角形或梭形,胞质丰富,嗜酸,颗粒状,核大小不一,偏位,呈印戒细胞样,核仁较明显,局部可见多核巨细胞及肿瘤性坏死,核分裂像少见(0~1/50HPF)上皮样血管平滑肌脂肪瘤显微镜下特点见图1。

图1 上皮样血管平滑肌脂肪瘤显微镜下特点(HE染色×200):1A为肿瘤细胞呈上皮样,片状或梁索状排列,胞质嗜酸,细胞核中位或偏位;1B为上皮样细胞、厚壁血管及脂肪组织;1C为可见肿瘤性坏死 图2 上皮样血管平滑肌脂肪瘤免疫组化特异性表达(EnVision两步法×200):2A为瘤细胞HMB45弥漫(+);2B为瘤细胞TFE-3弥漫;2C为CD34血管(+)
2.4 免疫组化肿瘤细胞HMB45(5/6),Vimentin(6/6),Melan-A(5/6),SMA(5/6),TFE-3(1/6),S-100,CD34,CD10,CKpan等阴性,Ki-67阳性指数1%~10%上皮样血管平滑肌脂肪瘤免疫组化特异性表达见图2。
3 讨论
血管平滑肌脂肪瘤(AML)是一种良性间叶性肿瘤,好发于肾脏及肝脏,属于具有血管周上皮样细胞分化的肿瘤(PEComa)家族,曾认为是一种错构瘤,近年来通过基因分析,认为是独立的真性肿瘤,也有人认为隶属于多向分化的间胚叶母细胞肿瘤。部分AML病人可伴有TSC,TSC是常染色体显性遗传性神经皮肤病,特点是脑、肾、肺、心、脾、消化道、和骨骼发生错构瘤。临床以智力低下、癫痫和面部皮脂腺瘤为三大特征性表现。肾EAML是AML的特殊亚型,是一种少见的肾脏肿瘤,可以是散发性的,也可以是结节性硬化症的一部分,生物学行为不同于AML,具有一定恶性潜能,有较多复发、转移的报道[4-5]。
3.1 临床特征肾EAML 于2004 年国际癌症组织分为良性、潜在恶性、恶性三种类型[6],有复发或转移倾向,临床较少见,好发于中青年女性,常常无明显症状,其临床表现往往与肿瘤的大小有关,当肿瘤较小时,一般于体检发现,当肿瘤较大时,常伴有严重的腰部酸胀感,病人以下腹部不适伴血尿及腰部酸痛入院检查时发现,病侧肾区可有叩击痛,本组病例中5例均为体检时发现。随着影像学的广泛应用,较小的EAML 发现率明显升高,EAML 因为长径一般比AML 大[7],影像学检查不易与AML 鉴别,确诊主要依据术后病理。发生于肾脏的EAML,因大多为乏脂肪的肿瘤病变,上皮样细胞含量多,CT平扫肿瘤为高密度增强影,T2 加权像呈低信号,增强后为“持续强化”或“快进慢出”,部分表现为“快进快出”,有的病例可见侵及肾周脂肪组织,更易误诊为肾细胞癌[8-9]。有报告显示MRI 检查通过对病灶的T2 加权成像(T2WI)与同相位信号强度指数(SⅠ)比值,与反相位信号强度指数(SⅡ)比值以及动态增强扫描比值(A/D),病变强化均匀可有效对肾癌和EAML 进行诊断[10]。本研究6 例EAML 中4 例影像学考虑为肾癌,仅2例诊断为错构瘤。
3.2 病理学特点肾脏上皮样血管平滑肌脂肪瘤镜下主要由厚薄不等、大小不一的血管,平滑肌、脂肪及上皮样成分组成,各成分以不同比例存在,且可以悬殊差异非常大。若以脂肪组织为主,往往是成熟的脂肪组织或加以少量脂肪母细胞,似脂肪肉瘤。若以血管为主,则为厚壁血管,缺乏血管弹力层,似血管畸形。若以平滑肌为主,可为经典的平滑肌组织,似平滑肌瘤。若平滑肌组织呈上皮样,则称之为上皮样血管平滑肌脂肪瘤(EAML),往往细胞呈巢团状或片状分布,部分绕以血管呈套袖样,易误诊为高级别癌。AML 的肿瘤细胞一般无明显异型性,只是以不同比例存在,EAML 的细胞较大,多角形或四边形,细胞核大,核仁明显,部分似神经节细胞样,可伴有核分裂象,血管浸润,坏死等。Brimo 等[11]认为EAML 具有以下任意三个及以上病理学特征的肿瘤提示有恶性生物学行为:⑴≥70%的上皮样细胞具有非典型性(细胞多形性,细胞核大小是周围细胞核的2倍以上,核仁明显);⑵≥2 个核分裂像/10HPF;⑶病理性核分裂像;⑷坏死。贺慧颖等[12]提出,EAML 不能简单分为良性或恶性,而是要通过结合临床相关指标(肿瘤的生长方式、大小、有无坏死、肾外侵犯及肾静脉浸润),分为低位、中危和高危。本研究6 例EAML 镜下图像与以上描述基本符合,2例可见肿瘤性坏死,伴随70%以上的上皮样细胞显示不典型性,有少量的核分裂像,未见病理性核分裂象,提示具有恶性潜能。有研究表明伴有Xp11.2 染色体异位的TFE-3 基因融合将更具有侵袭性[13]。本研究6 例EAML 中3 例基因检测均未有TFE-3基因融合。
3.3 免疫表型EAML 几乎全部特征性的表达HMB45,Melan-A,Vimtinin 和SMA,S-100,CKpan,EMA 阴性。值得注意的是,S-100 在EAML 中偶见非特异性阳性,若弥漫强阳性需排除恶性黑色素瘤,若散在核阳性则支持本组肿瘤。有报告Ki-67和P53 高表达时可作为EAML 辅助判定良恶性的有效方法之一[14]。
3.4 鉴别诊断肾EAML 的临床表现与影像学均无特异性表现,组织学表现复杂多样,需与以下疾病鉴别:①透明细胞性肾细胞癌:肾EAML与其鉴别有一定困难,当EAML中脂肪组织较少,且上皮样细胞伴透明变,尤其出现肾门静脉瘤栓及被膜侵犯时,影像学上不易与透明细胞性肾细胞癌区分,需要行免疫组化检查。EAML 黑色素标记及肌源性标记阳性,上皮性标记阴性,而肾细胞癌相反,广谱上皮细胞标记CKPan 和EMA 阳性可资鉴别。②上皮样平滑肌肉瘤:EAML 常常因为脂肪组织非常少,以上皮样组织为主伴轻度异型时,易误诊为上皮样平滑肌肉瘤。后者常常细胞单一,异型更明显,间质内无脂肪组织及增生的畸形厚壁血管,免疫组化肌源性标记阳性,但HHMB45 及Melan-A 阴性可与EAML 鉴别。③嗜酸细胞腺瘤:肿瘤由单一形态细胞构成,瘤细胞圆形或卵圆形,染色质细腻,偶见小核仁,瘤细胞多数呈实性巢索状排列,可出现一些怪异细胞核的瘤细胞需与EAML 鉴别。影像学上,嗜酸细胞腺瘤的中心部位可见星芒状瘢痕是其主要诊断依据,同时免疫组化表达上皮性标记,不表达HMB45 及Melan-A 等黑色素标记。④脂肪肉瘤:当肿瘤细胞以脂肪为主,且出现绕以血管的上皮细胞丛时,易当做脂肪母细胞而误诊为高分化脂肪肉瘤。一般经多次取材,往往可以找到三种成分。免疫组化标记HMB45 和SMA 阳性可以进一步明确诊断。⑤肉瘤样癌:对于EAML,当畸形血管和脂肪组织较少时,上皮样细胞和梭形细胞混合成束状或条索状排列,极易与肉瘤样癌混淆,后者免疫组化EMA和CKpan阳性而黑色素标记阴性。
3.5 治疗与预后EAML 是具有潜在恶性的肿瘤,往往作为肾细胞癌处理,首要治疗手段是外科手术局部切除,可术前行RENAL 评分,根据评分选择手术方式,也可肿块剔除做术中冰冻,若结果不能排除恶性或细胞明显异型时[15],建议行肾脏根治术。若术前能确诊为EAML,且肿块长径大于4 cm,应选择根治性肾切除[16]。国外研究发现[17],分子靶向药物索拉非尼对于转移性EAML 的治疗有较好疗效。本组病例中,3例行肿块剔除术,3例行肾脏切除,术后均未继续药物辅助治疗。EAML 以增生的上皮样细胞为主,具有一定的恶性潜能,合并结节性硬化症的几率更高,需长期随访。文献报告约1/3 的EAML 有淋巴结、肝、肺的转移,当肿瘤内出现坏死、核分裂象及肾外转移,免疫组化中Ki-67 增殖指数较高,P53 有突变时,往往提示预后不佳[18-19]。本研究所有病例均有随访,随访时间范围为3~44 月,病人均暂无复发及转移,所有病例作者将长期随访。
