不同胃周动脉类型胃癌患者围手术期结局及中期预后研究
2022-06-27周岳,韩博
周 岳,韩 博
1 西安大兴医院普通外科,陕西西安 710000;2 西安国际医学中心医院消化外科,陕西西安 710100
胃癌是全球发病率最高的癌症之一,近年来,胃癌的发病率和病死率呈上升趋势,在我国胃癌的发病率和病死率分别位居癌症第二和第三,严重威胁着人们的健康[1]。目前,胃癌的治疗策略主要采用综合治疗,其中外科手术是治疗胃癌并提升生存率的主要方法[2]。随着腹腔镜技术的不断成熟与完善,胃癌腹腔镜手术以其创伤小、疼痛轻、恢复快等优势被广泛开展应用[3-4],但其手术的操作仍存在着一定的局限性,如缺乏立体视觉效果和真实触感,难以准确地把握脏器的形态和位置,胃周血管多且易变异等[5]。而且胃癌的诊疗规范和治疗指南明确提出,在根治性胃癌切除术中,需要对胃周淋巴结进行彻底清扫,其主要是将胃周动脉裸化和显露,增加了手术操作难度[2,6]。因此,术者在术前掌握胃周动脉解剖及其变异尤为重要,不仅可以避免对血管的损伤,也有利于胃癌治疗方案的制订。本研究主要对不同胃周动脉类型胃癌患者的围手术期结局及中期预后进行研究,以期为胃癌患者的临床治疗提供参考。
1 资料与方法
1.1一般资料 回顾性分析2016-2018年西安大兴医院收治的108例胃癌患者的临床资料,所有患者术前均采用CT血管造影(CTA)和三维重建对胃周动脉进行分型,且均行腹腔镜胃癌D2根治术。患者的一般资料:年龄38~81岁,平均(58.4±9.8)岁;男63例,女45例;体质量指数(BMI)(23.2±2.6)kg/m2;TNM分期:Ⅰ期 38 例,Ⅱ期 24 例,Ⅲa 期 46 例;肿瘤部位:胃体39例,胃底部22例,胃窦部47例;手术范围:近端胃16例,远端胃43例,全胃49例。本研究经医院医学伦理委员会审核批准,所有患者均自愿参与本研究并签署知情同意书。纳入标准:(1)经胃镜及组织病理学确诊为胃癌;(2)术前评估符合腹腔镜胃癌根治手术适应证;(3)无远处转移;(4)无放化疗史及腹部手术史;(5)临床资料记录完整。排除标准:(1)碘剂过敏者;(2)仅行姑息性手术者;(3)合并其他器官切除,且不耐受手术及麻醉者;(4)术中中转开腹者;(5)伴有严重的心、肝、肾及肺功能障碍者;(6)胃癌急症(如出血、梗阻、穿孔等)手术者。
1.2方法 所有患者术前均行64层螺旋CT平扫及三期增强扫描,扫描结束后将断层图像传输至Start Vitred工作站,采用最大密度投影法(MIP)、容积再现技术(VR)和曲面重建(CPR)对动脉期数据进行重建,取得满意的CTA图像,根据CTA图像确定胃周动脉的走行并对其进行分类。手术医师根据重建结果制订手术治疗方案。所有患者均行腹腔镜胃癌D2根治术,采用气管插管全麻,取仰卧位,采用5孔法行腹腔镜手术,按照TNM分期及病灶部位选择出适合的手术切除范围(即全胃、远端胃或近端胃),采用BillrothⅠ式+Overlap吻合进行消化道重建。
1.3观察指标 (1)胃周动脉按照CTA图像进行分型,并对各类型发生情况进行统计;(2)围手术期结局指标:手术时间、术中出血量、淋巴结清扫个数、术中血管损伤、术后引流量、术后住院时间、术后并发症发生情况;(3)中期预后:鉴于Ⅰ型为胃周动脉的正常型,而Ⅱ~Ⅶ型为胃周动脉不同变异类型,将108例患者分为正常组(82例)和变异组(26例),并进行随访观察,随访截止时间为2020年12月,首次随访于术后3个月进行,随后每6个月进行1次随访,观察患者术后总生存率。
2 结 果
2.1胃周动脉的分型情况及临床病理学资料 根据108例患者所获得的CTA图像进行分型,其结果为Ⅰ型82例(75.9%),Ⅱ型4例(3.7%),Ⅲ型2例(1.9%),Ⅳ型3例(2.8%),Ⅴ型6例(5.6%),其他Ⅵ型9例(8.3%),Ⅶ型2例(1.9%),7种类型TNM分期、肿瘤部位、手术范围等临床病理资料相比,差异均无统计学意义(P>0.05),见表1。
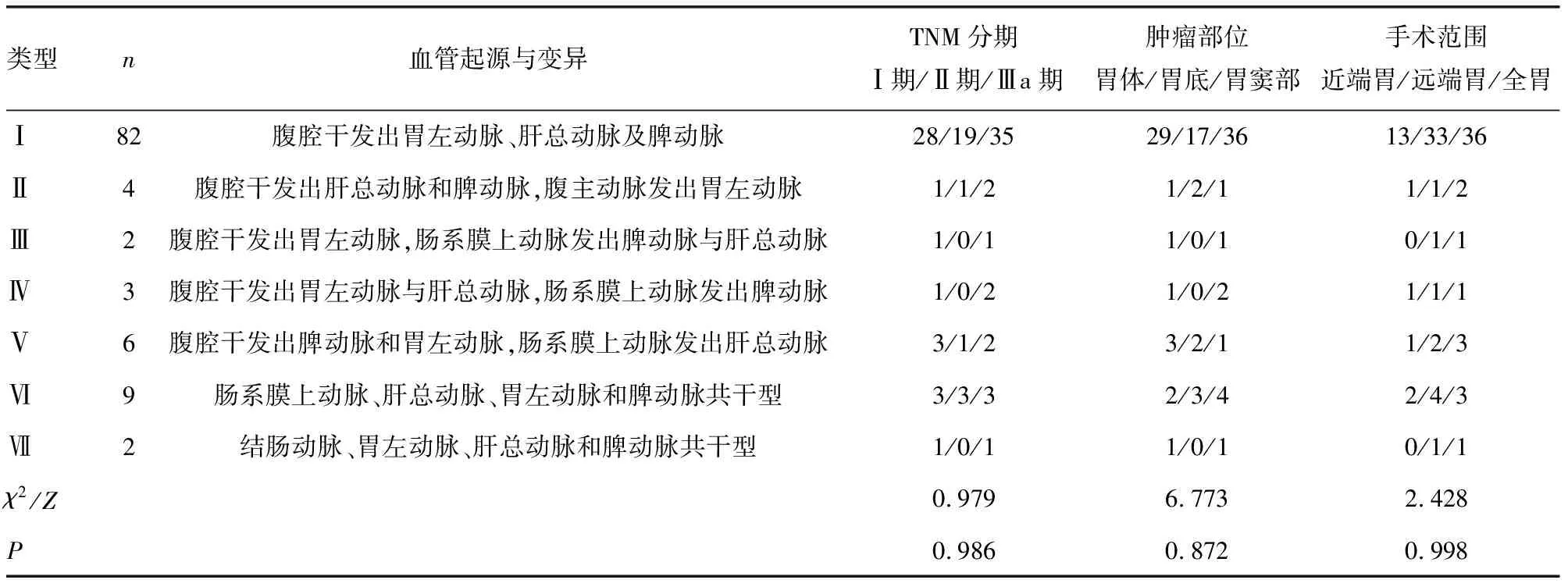
表1 胃周动脉分型及临床病理学资料(n/n/n)
2.2围手术期结局 不同类型胃周动脉的胃癌患者手术时间、术中出血量、淋巴结清扫个数、术后引流量、术后住院时间及术后并发症的发生率比较,差异均无统计学意义(P>0.05),而术中血管损伤情况比较,差异有统计学意义(P<0.05),见表2。术后并发症发生情况:Ⅰ型中切口感染3例,吻合口瘘1例,腹腔感染1例,胃排空障碍1例;Ⅱ型中术后出血1例;Ⅴ型中腹腔感染1例;Ⅵ型中术后出血1例,肝组织坏死1例。

表2 围手术期结局指标比较
2.3中期预后 随访时间为33(24~48)个月。正常组患者失访4例(4.9%),死亡16例(19.5%);变异组患者失访1例(3.8%),死亡7例(26.9%)。通过Kaplan-Meier分析显示,正常组患者总生存率为80.5%,变异组患者总生存率为73.1%,两组患者的总生存率比较,差异无统计学意义(χ2=0.809,P=0.368),见图1。
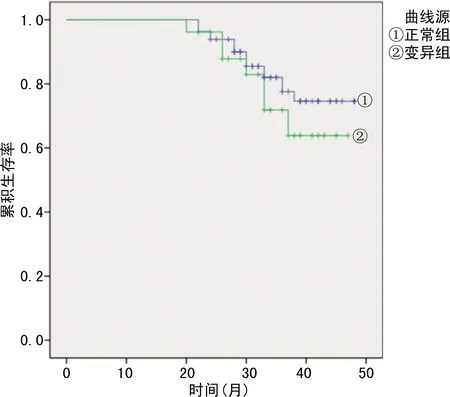
图1 两组患者累积生存率曲线
3 讨 论
胃癌是起源于胃黏膜上皮细胞的恶性肿瘤,是消化内科常见疾病。在胃癌的治疗中,胃癌根治术是较常见的术式,手术过程中需要将胃周血管结扎和离断,尤其是D2根治术,离断通常是在动脉根部,手术时应尽量避免损伤动脉[7-8]。由于肝和胃的血管紧密相连,在手术前充分了解胃周血管的解剖结构,对手术的开展有一定的指导作用[9]。目前,腹腔镜下胃癌根治术在胃癌的治疗中取得了较好的临床效果,虽然此法具有微创外科的传统优势,但是手术操作难度大。其手术操作的难点主要是解剖平面的镜下定位及清扫胃周围血管淋巴结。与传统的开腹手术相比,腹腔镜手术需要保证充分显露术野及直视下锐性分离,但其在操作过程中仍存在一定的局限性[10-11]。近年来,随着CT影像技术和三维重建技术的不断进步与发展,CTA图像得到了更好的展示,进而增强了手术的安全性[12-13]。因此,在腹腔镜胃癌根治术中,应按胃动脉的分布进行适当的操作,不仅可以确保术后残胃血供,而且还可以避免术中出血。
胃周血管丰富且易变异,通常主要由腹腔干供应胃的血供。截至目前,关于胃周动脉的分型有许多报道[14-20]。胃周动脉类型最早是由LIPSHUTZ[14]于1917年提出的,其通过对88例尸体解剖进行研究,根据腹腔干提出了4种分型,其是如今各种分型的核心,但当时发现腹腔动脉分支变异少,满足不了后续研究需求。ADACHI[15]于1930年对LIPSHUTZ分型进行了补充,并提出6种分型。WEIL[16]于1956年通过解剖尸体标本,根据腹腔干提出了7种分型,后来MICHELS[17]又根据肝动脉的分布提出了10种解剖分型,并成为最为经典的分型标准。1958年,张甲年[18]通过对118例解剖尸体进行研究也提出了7种分型,其不仅包含膈下动脉的解剖部位,也提出了国外未发现的变异类型。HIATT[19]于1994 年通过分析肝移植患者的肝动脉,对MICHELS 分型进行了补充与简化,将起源于胃左动脉的副肝左动脉和替肝左动脉划分到Ⅱ型,将起源于肠系膜上动脉的副肝右动脉和替肝右动脉划分到Ⅲ 型。VAROTTI[20]于2004年将MICHELS分型重新进行了分类,划分出了Ⅱa型和Ⅱb 型。虽然有关胃周动脉的分型有许多分类方法,但目前被学术界作为研究标准的仅有MICHELS分型和HITTA分型,其中最为常用的为MICHELS分型。
本研究结果发现,7种类型胃周动脉的胃癌患者围手术期相关指标及术后并发症的发生率比较,差异均无统计学意义(P>0.05),而术中血管损伤情况比较,差异有统计学意义(P<0.05),考虑其原因可能为腹腔干分支变异所致。在随访期间,通过Kaplan-Meier 分析发现,正常组和变异组患者的总生存率比较,差异无统计学意义(P>0.05),考虑可能与本研究随访时间相对较短和研究纳入样本量小有关,所得结论尚需进一步增加样本量和随访时间来证实。目前,本研究尚处于初级研究阶段,研究中所采用的手术技巧尚待进一步提高,笔者认为手术时应注意以下事项:(1)手术时,应按照胃动脉走行进行精细化操作,仔细辨认每一个动脉走行,从而减少术中出血并确保术后残胃血供;(2)动脉内膜脆弱且易断,如出现局部出血或渗血,切勿盲目电凝止血,以防引发更大血管损伤;(3)使用电刀时,应适当将电凝功率调小,并套上硅胶保护套,以降低血管热源性损伤;(4)切勿随意切断任何管道样结构,以防误伤变异动脉,最好将其分离到管道根部再处理。
腹腔镜下胃癌根治术中,需要对胃左动脉、胃右动脉、冠状静脉等胃周血管进行游离和结扎。而腹腔镜下术野狭窄,手术操作难度大,若手术医师对不同胃周动脉类型缺乏正确的把握和认识,极易引发出血和肝、脾等脏器的缺血或坏死。由于胃周动脉类型繁多,因此术前通过全面评估胃周动脉的解剖结构和变异,可以防止胃供血动脉误栓或迷走肝动脉误扎等情况的发生,进而减少胃黏膜糜烂、缺血、肝组织坏死等。同时,胃周血供丰富,通过了解不同胃周动脉类型中血管的起源和变异,也有助于术中指引淋巴结清扫,从而增强肿瘤的根治性。
综上所述,胃周动脉变异的胃癌患者,其术中血管的损伤风险较大,因此,术前熟练掌握胃癌患者不同胃周动脉类型,可以指引淋巴结的清扫,防止血管损伤,以确保手术安全有效地开展。
