液态CO2溶浸作用对煤吸附特征的影响
2022-06-15郝健池任立峰魏高明郑学召
文 虎,郝健池,马 砺,任立峰,魏高明,郑学召
(1.西安科技大学 西部矿井开采及灾害防治教育部重点实验室,陕西 西安710054;2.西安科技大学 安全科学与工程学院,陕西 西安 710054)
0 引 言
二氧化碳的肆意排放是造成温室效应的主要原因,可导致海平面上升,全球气温变暖,大量疾病的传播等恶劣影响,已成为世界各国面临的共同问题[1-3]。为解决上述困境,各国际机构、气候组织和各国政府都在不断探索如何最快、最有效地降低二氧化碳排放量的方法[4],其中发展绿色清洁能源的呼声最为响亮[5-7]。但这些绿色清洁能源技术的起点相对较低,短期内仍无法取代化石能源[8]。因此,CO2捕获及封存技术是目前能实现CO2减排的主要途径[9-10]。
目前,随着该技术的不断发展,已经在煤矿安全生产中得到了广泛应用,但对煤层封存CO2的研究主要集中在煤岩体对超临界及气态CO2的吸附特征[11-13],同时对于CO2的利用及封存一体化技术尚处于探索阶段。因此,有学者提出,将高压液态CO2注入煤层,经液态CO2“溶浸-相变-气态吸附”作用后,既可以达到驱替置换煤层甲烷的目的[14-18],又可以有效地对CO2进行封存。从而将该技术拓展为CO2利用及封存的一体化技术,对煤矿瓦斯灾害防治和实现CO2封存及减排都有着重要意义。
煤矿在进行液态CO2利用及封存时,煤岩体首先会受到液态CO2“溶浸”的作用,从而影响煤体的孔裂隙,进而会影响到煤体对CO2的吸附特性[19-20]。因此文中基于CO2利用及封存一体化技术,通过压汞实验及等温吸附实验对煤体液态CO2溶浸后煤样的孔隙结构及其吸附特征进行了分析,以煤样溶浸前后对CO2气体的吸附解吸量为依据,提出了在液态CO2利用及封存技术过程中预测CO2储量的方法,从而为完善液态CO2利用及封存一体化技术及理论提供依据。
1 液态CO2溶浸前后孔裂隙特征
1.1 煤样溶浸处理
煤样溶浸系统主要包括:液态二氧化碳储罐、高压管路、煤样罐、压力表、泄压阀等,如图1所示。
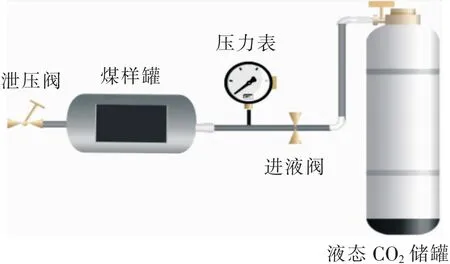
图1 煤样溶浸系统Fig.1 Soaking system of coal sample
实验煤样取自新疆硫磺沟矿(9-15)04工作面长焰煤,工业分析见表1。实验开始时首先将煤样粉碎至80目,在70 ℃条件下进行干燥处理6 h。然后将煤样置于煤样罐内进行溶浸处理,以2 MPa的压力持续注入液态二氧化碳8 h后打开泄压阀,取出煤样后可进行下一步实验。

表1 煤样工业分析
1.2 压汞实验
受液态二氧化碳溶浸作用的影响,煤体内的孔隙结构会发生变化。因此采用压汞法对原煤样及浸溶煤样内部的孔径分布等参数进行测试,对比研究溶浸作用对煤样孔隙结构的影响。
由压汞实验的原理可知,压力P(r)和孔径r存在以下关系[21]
P(r)=2δcosθ/r
(1)
式中P(r)为进汞压力,MPa;r为煤样孔隙半径,nm;δ为金属汞表面张力,0.485 N/m;θ为接触角,实验选取130°。
将煤样放入压汞仪后,通过软件设置初始压力为0.003 MPa,终止压力为242 MPa。设置120个采集压力点,稳定时间5 s,仪器按照设定程序自动记录和保存数据。
1.3 压汞实验(MIP)结果与分析
从表2可以看出,原煤样及溶浸煤样的比表面积分布主要孔径范围均在0~100 nm。其中,原煤样的比表面积为36.647 68 m2/g,浸溶后煤样的比表面积为30.485 49 m2/g,对比溶浸前后煤样的比表面积可知,溶浸后煤样的比表面积相对于原煤样减少了16.82%。溶浸煤样的比表面积峰值趋向大孔径值偏移,说明溶浸作用会影响原煤样的孔隙,造成小孔径逐渐扩张至大孔径。同时会产生新的孔隙,但生成孔隙的量要小于转变量,导致孔径峰值呈上升趋势,比表面积下降。
对煤样孔隙体积的测定发现,与原煤样相比,溶浸后煤样大孔孔隙体积比原煤样增加0.005 mL/g,增长率为8.6%。煤体小孔及中孔的孔隙体积及所占百分比均呈减小趋势,说明煤体孔隙在溶浸作用下会从小孔至中孔再到大孔发展。溶浸煤样的总孔隙体积相比原煤样降低了0.006 mL/g,结合大孔孔隙体积变化可以推断,在液态CO2溶浸作用下孔隙孔径增大,甚至形成宏观的裂隙,有效孔隙体积减小,裂隙发育连通成为裂隙网络。

表2 煤样压汞法比表面积分布
2 溶浸前后煤样的吸附特征
2.1 CO2气体吸附/解吸实验
实验所用仪器为高压气体吸附/解吸仪(PCT),该仪器主要由煤样容器、气动阀、储气池、压力控制单元、温度传感器、真空泵和气瓶组成,如图2所示。
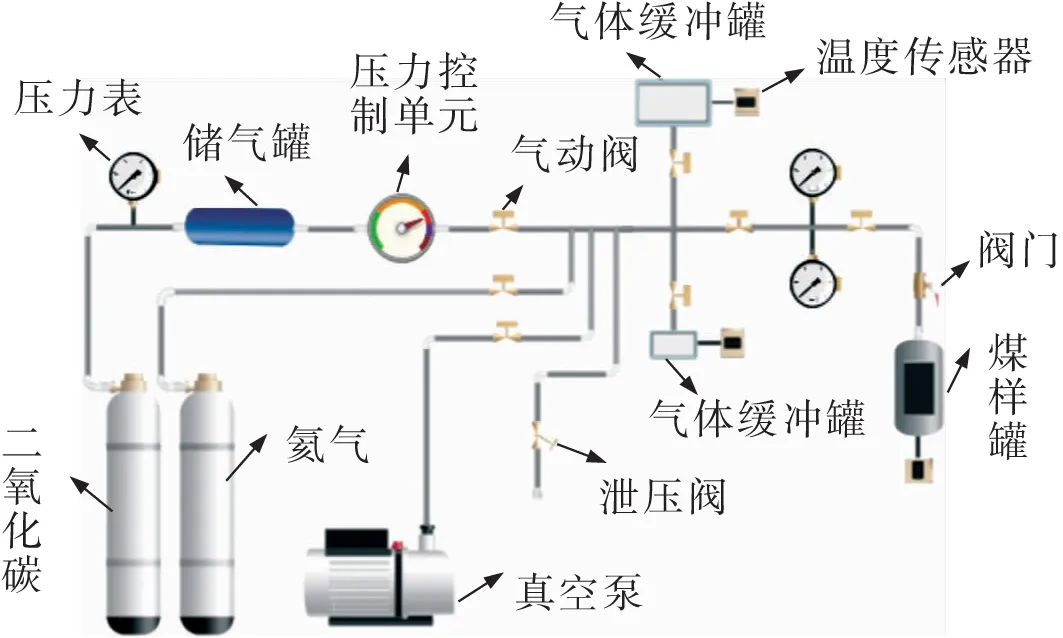
图2 高压气体吸附/解吸仪Fig.2 High pressure gas adsorption/desorption instrument
实验选取粒径80目的原煤样和经液态CO2溶浸处理后的煤样,实验前需对煤样进行干燥处理,然后在压力为0~5 MPa,实验温度为30~70 ℃的条件下进行CO2的吸附、解吸实验。
2.2 液态CO2溶浸前后吸附特征分析
由压汞实验可得经液态CO2溶浸作用后,受煤中孔径变化的影响,煤对CO2气体的吸附量也将发生变化,结果如图3所示。从图3可以看出,不论原煤样还是液态CO2溶浸煤样都对CO2气体的吸附/解吸整个过程都存在“解吸滞后”现象。随着温度的升高,原煤样和溶浸煤样对CO2气体的吸附量均呈减少趋势,“吸附滞后环”也随温度的上升而减小,说明煤体内CO2残余吸附量也随着温度的上升而减小,即随着温度的升高,CO2的解吸量呈上升趋势。这是因为CO2气体吸附及解吸是一个物理过程,CO2解吸属于吸热反应,温度的升高促进了CO2气体的解吸,导致游离态CO2分子增多而造成的。
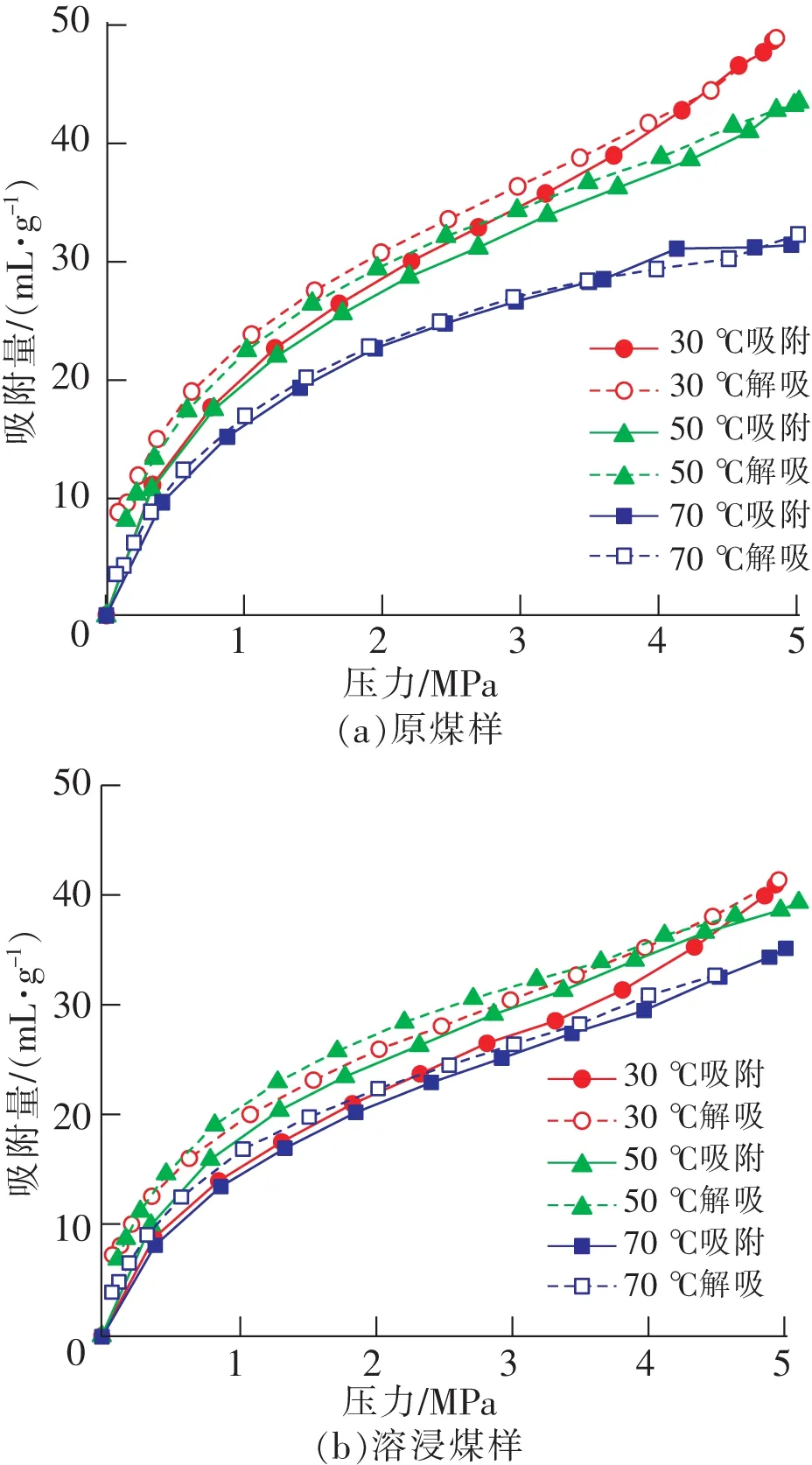
图3 原煤样、液态CO2溶浸煤样吸附、解吸实验曲线Fig.3 Experimental curves of adsorption and desorption of coal samples and liquid CO2 soaked coal samples
同时可以看出,原煤样和溶浸煤样对CO2气体的吸附量均随着注气压力的升高而增大,当温度高于50 ℃时,在3 MPa之前,气体的吸附量迅速增加,超过3 MPa后,CO2气体吸附量的增加趋势逐渐变缓,这是由于煤中存在大量孔隙,随着吸附量的不断积累和压力的不断上升这些孔隙逐渐被CO2分子所占据,最终将达到饱和,因此超过3 MPa压力后煤样对CO2气体的吸附量逐渐趋于稳定;当温度低于50 ℃时,气体的吸附量随压力的增大而增大,且高于3 MPa时依旧有上升趋势,这可能是由于温度越低CO2气体分子的活动自由度也越低,吸附态CO2分子量就越高所造成的。
从表3可以看出,增压吸附过程和降压解吸过程皆可以用Langmuir[21-27]方程进行描述,差值较小,拟合度高,见式(2)。由Langmuir方程可知,a,b为吸附特征常数,其中a代表着煤样的最大吸附量。可以看出,原煤样与溶浸煤样,a的值均随着温度的上升呈下降趋势,这与实验结果完全吻合。同时随着温度的上升,不论原煤样还是溶浸后的煤样,拟合相关性系数均随温度升高而增大,这可能是因为随着温度的升高,CO2气体分子间的活动加剧,分子间距增大,多层吸附的分子逐渐转变为单层吸附,从而造成吸附量的减少且单分子层吸附现象越来越明显。而Langmuir方程所描述是正是单分子层吸附过程,因此拟合相关性系数也越高。

表3 Langmuir方程拟合结果
(2)
式中V为压力p时煤层气吸附量,mL/g;a为煤样最大吸附量,mL/g;b为吸附特征常数。
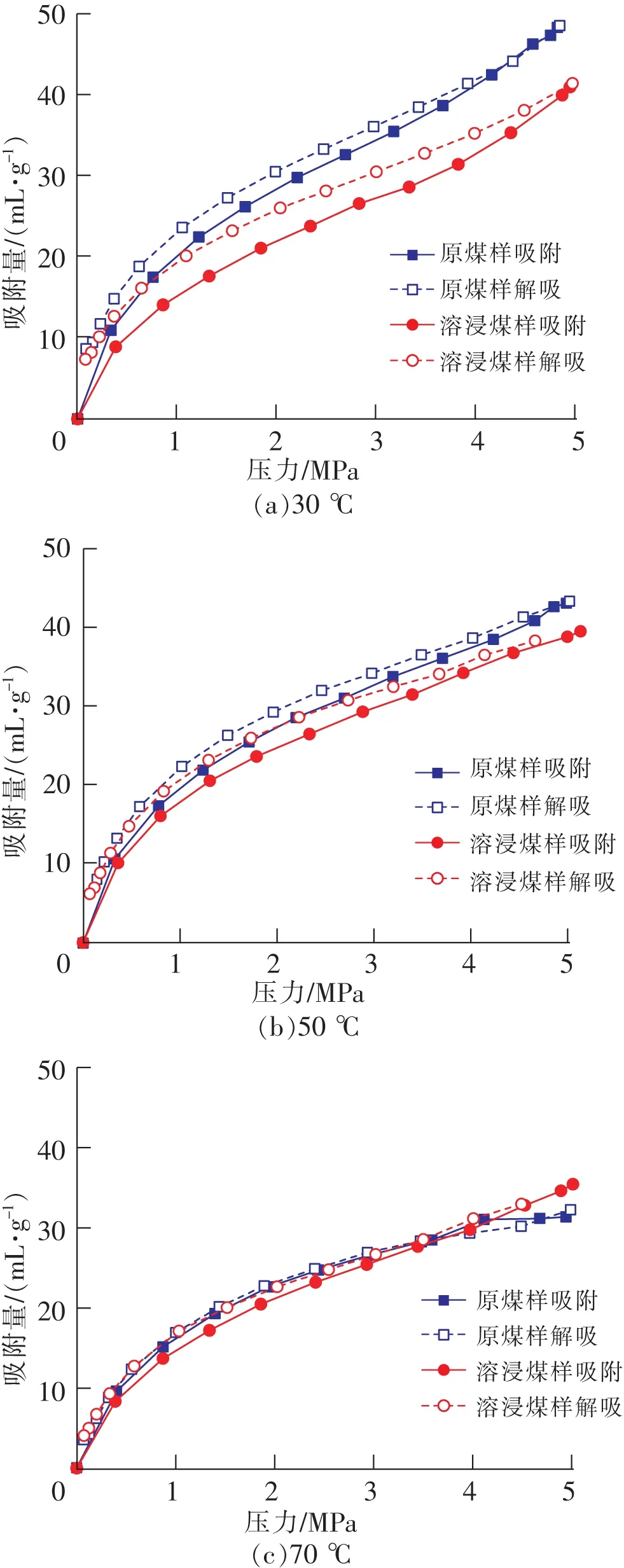
图4 CO2吸附、解吸曲线对比Fig.4 Comparison of CO2 adsorption and desorption curves
从图4可以看出,受温度影响,2种煤样的CO2吸附量均随着温度升高呈减少趋势。随着温度不断上升,溶浸前后煤样对CO2气体吸附量之间的差异将会越来越小,说明溶浸煤样对温度的敏感程度要小于原煤样。结合压汞实验数据来看,煤中孔隙变化是造成溶浸前后煤样对CO2气体吸附量存在差异性的主要原因,其中<100 nm孔隙在这个过程中起到主导作用。
2.3 CO2溶浸前后煤样的等量吸附线
根据煤在不同温度条件下的等温吸附曲线,利用 langmuir方程将等温吸附曲线转换成等量吸附线,分别选择吸附量为0.2,0.4,0.6,0.8,1.0,1.4 mmol/g,等量吸附线如图5所示。
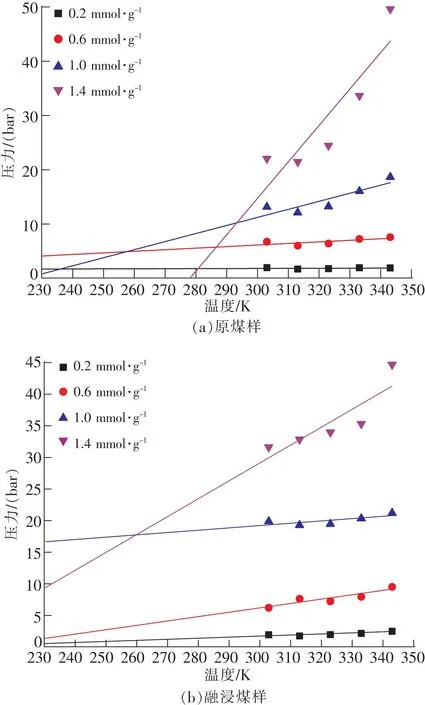
图5 溶浸前后煤样等量吸附线Fig.5 Equivalent adsorption lines of coal samples
从图5可以看出,在吸附量相同的条件下,CO2气体吸附平衡压力与温度之间呈正相关关系,CO2气体的吸附平衡压力随着温度的升高呈上升趋势。这证明溶浸煤样和原煤样对CO2的吸附和解吸作用均属于物理吸附[28]。将 CO2的等量吸附线延长,将会在较小的温度范围内相交,有学者在进行煤对CH4的吸附过程研究中也发现这一现象[29],对于该现象的出现尚未有统一的解释。
3 煤样对CO2吸附的热力学特征
3.1 热力学过程分析
由吸附热力学可知,吸附能力的强弱,可以用吸附热来进行衡量,即吸附能力越强,吸附热就越大。在煤对CO2吸附过程中,CO2分子会在煤基质表面形成单分子吸附层,使得CO2分子活跃程度降低,释放出热量,可以根据Clausius-Clapeyro方程间接计算等量吸附热[30],见式(3)。
(3)
式中Qst为等量吸附热,kJ/mol;P为解吸平衡压力,MPa;R为气体常数,8.314 J/(mol·K);T为实验温度,K;Γ为吸附量恒定。
在等吸附量条件下,lnP与1/T呈线性关系,由其直线斜率可求出Qst。

图6 等量吸附热Fig.6 Equal adsorption heat
由表4和图6可以看出,吸附是放热反应,解吸是吸热反应。在溶浸煤样与原煤样的升压吸附过程与降压解吸过程中,等量吸附热与吸附量呈线性相关。对比溶浸前后煤样的等量吸附热曲线可得,在煤对CO2吸附过程与解吸过程中,原煤样的平均吸附热要比溶浸煤样的吸附热大,吸附量越大这种差异越明显,这也合理的从热力学角度解释了溶浸后煤样对CO2的吸附量要小于原煤样对CO2的吸附量。
同种煤样的等量吸附热在吸附量相同的条件下,CO2解吸过程的吸附热要高于CO2吸附过程。这说明CO2吸附时放出的热量要小于CO2解吸所需要的热量,这是导致CO2解吸曲线滞后于吸附曲线的主要原因。
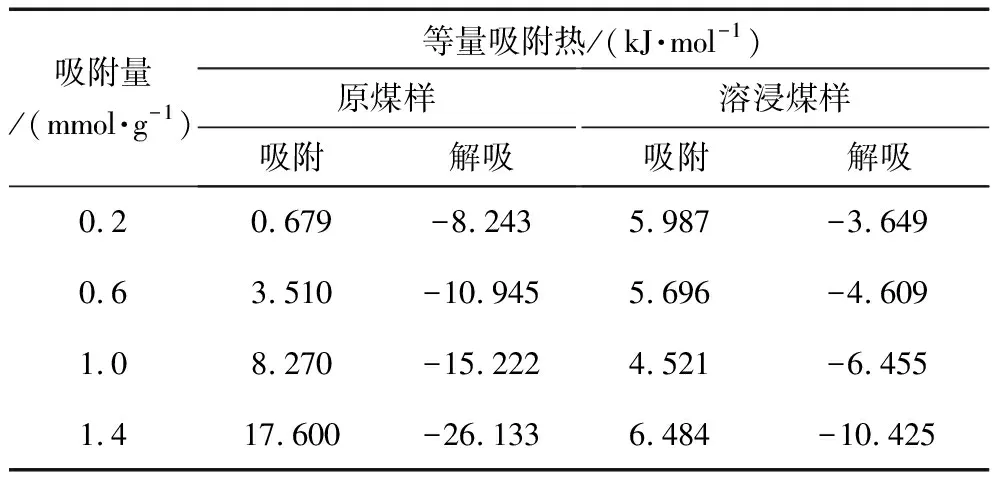
表4 CO2增压(吸附)与降压(解吸)过程吸附热计算结果
3.2 吸附势与吸附空间分析
根据热力学分子吸附理论,单位质量的吸附质从非吸附相的游离状态转移到吸附相的被吸附状态所做的功ε可以表示为
(4)
式中ε为吸附势,J/mol;P0为气体饱和蒸汽压力,MPa;Pi为理想气体在恒温下的平衡压力,MPa;R为普适气体常数,J/(mol·K);T为绝对温度,K。
可采用Dubinin提出的超临界条件下虚拟饱和蒸汽压力经验计算公式计算饱和蒸汽压力P0,见式(5)
(5)
式中P0为临界压力,MPa;Tc为临界温度,K;取CO2临界温度Pc为304.2 K,临界压力Pc为7.39 MPa。
根据吸附空间的定义,采用煤对单一组分气体的等温吸附、解吸数据和式(6)计算[31],即
(6)
式中ω为吸附空间,cm3/g;M为气体的分子量,g/mol;Vad为实测吸附量,mol/g;ρad为气体吸附相密度,g/cm3。根据经验公式计算,即
(7)
3.3 计算结果分析
如图7、表5所示,由吸附势与吸附空间的计算结果可以看出,对于溶浸前后煤样,无论吸附过程还是解吸过程,特征曲线均符合对数函数ε=aln(ω)+b,拟合度较好。在相同压力下,吸附过程中原煤样的吸附势始终大于溶浸煤样的吸附势,且原煤样比溶浸煤样具有更大的吸附空间,说明原煤样对于CO2的吸附能力要强于溶浸煤样,这也是导致原煤样吸附量大于溶浸煤样吸附量的原因之一。但在解吸过程中,溶浸煤样的吸附势要稍大于原煤样,且两者的吸附空间差异不大,这说明解吸过程中溶浸煤样对于CO2的吸附能力要优于原煤样,因此能够解吸出来的CO2量要比原煤样少。
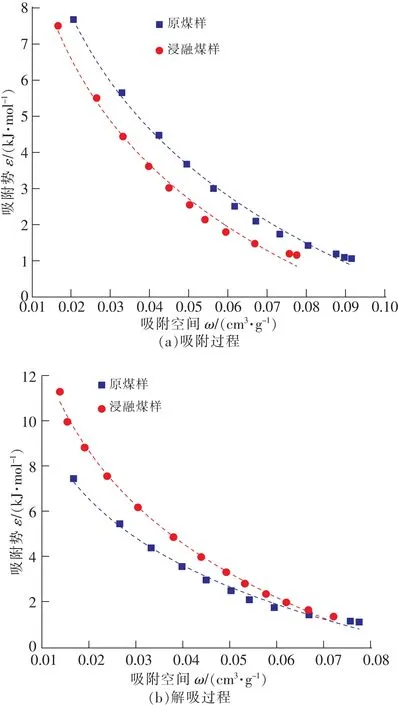
图7 吸附特征Fig.7 Adsorption characteristics
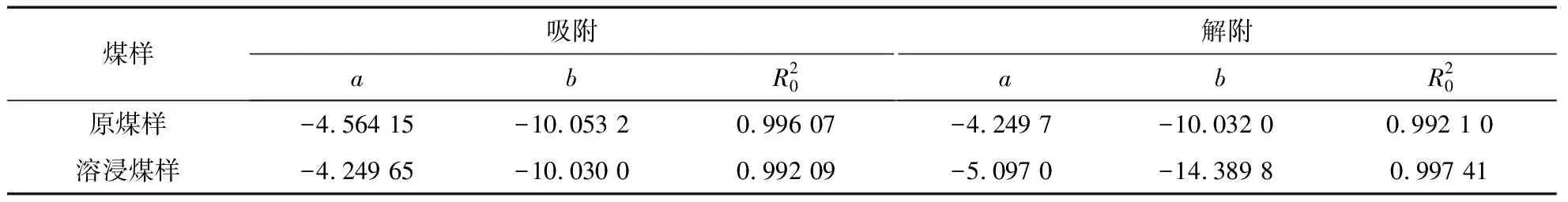
表5 吸附势与吸附空间特征曲线拟合
4 结 论
1)溶浸前后煤样煤中孔隙的变化是造成对CO2气体吸附量存在差异性的主要原因。在溶浸作用下,煤体的孔隙会从小孔至大孔进行转化,其中<100 nm孔径非闭合孔隙在这个过程中起到了主导作用。
2)溶浸前后煤样对CO2的吸附量均随着压力的升高而增大,且随着温度的升高呈减少趋势,但溶浸煤样对温度的敏感度要小于原煤样。
3)从热力学角度解释溶浸前后煤样对CO2的吸附量存在差异的原因,吸附过程中原煤样的吸附热及吸附势始终比溶浸煤样大,且原煤样比溶浸煤样具有更大的吸附空间。解吸过程中,溶浸煤样的吸附热及吸附势稍大于原煤样,但两者的吸附空间差异不大。
