鱼鳔胶原蛋白-壳聚糖-海藻酸钠水凝胶促小鼠皮肤伤口愈合研究
2022-06-14李航婷金明月李诺营莫奕雯杨最素
李航婷,金明月,李诺营,莫奕雯,田 静,杨最素
(浙江海洋大学食品与药学学院,浙江 舟山 316022)
皮肤是人体最大的感觉器官,工作中容易受到意外损伤,在伤口愈合时,需要上皮组织的再生、肉芽组织的形成、瘢痕组织生成等的复杂组合,胶原蛋白的沉积和血管形成是创伤愈合的关键。传统伤口敷料主要是使用脱脂棉纱布等天然纤维材料,使伤口干燥及物理隔离功能等,但换药时容易撕拉伤口,引起再出血等不利于愈合[1]。近年来,海洋胶原蛋白、壳聚糖、海藻酸盐的开发及用于伤口敷料的研究日益增多,而三者复合后制备的水凝胶更是被广大学者所重视。海洋胶原蛋白具有低免疫性、高组织相容性、可降解性及创面止血等多种生物学性质;而壳聚糖是一种天然的正电荷的高分子多糖,具有良好的抗菌、防黏连、促愈合等功效;海藻酸盐具有高吸水性、成胶性、止血性,与Ca2+交联形成海藻酸钠水凝胶,具有良好的生物相容性和较低的细胞毒性,可为伤口提供恒温恒湿的理想环境[2]。
鳗鱼(Anguillidae)肉质鲜美、营养价值高,除日常鲜食外,常被加工成鳗鱼干、烤鳗鱼片等,在加工过程中会产生大量的加工副产物。其中鱼鳔除被少量食用外,大量鱼鳔以废弃物丢弃,浪费了资源,也污染了环境。研究表明,鱼鳔中含有大量的胶原蛋白[3],因此可提取鳗鱼胶原蛋白制备具有高附加值的产品。湿润、透气、抗菌的微环境能促进细胞的增殖与迁移,有利于皮肤伤口的愈合[4]。本试验以鳗鱼鱼鳔胶原蛋白为主药,与Ca2+分别交联的壳聚糖和海藻酸钠为配料制备水凝胶,探讨其对小鼠皮肤伤口的愈合作用,为鳗鱼鱼鳔的高附加值利用和伤口敷料开发提供依据。
1 材料与方法
1.1 材料
1.1.1 仪器 BSA124S 型电子天平(Sartorius AG 公司);RLPHR 1-4LD 型冷冻干燥机(德国Christ 公司);SEM3000S 型扫描电子显微镜(国仪量子技术有限公司);CX31 型光学显微镜(日本Olympus 公司);SpectraMax M2 型多功能酶标仪(美国Molecular Devices 公司)。
1.1.2 药品与试剂 新鲜鳗鱼鱼鳔(舟山市某菜场);鱼鳔胶原蛋白(浙江海洋大学食品与药学学院自制);卡波姆(上海麦克林生化科技有限公司);海藻酸钠(上海生工股份有限公司)、壳聚糖(济南海得贝海洋生物工程有限公司);苏木素-伊红(HE)染液、超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)、丙二醛(MAD)、过氧化氢酶(CAT)、总抗氧化力(T-AOC)试剂盒(南京建成生物工程研究所);白介素-6(IL-6)、白介素-1β(IL-1β)和肿瘤坏死因子-α(TNF-α)试剂盒(武汉伊莱瑞特有限公司)。
1.1.3 动物 ICR 雄性健康小鼠,体重22~24 g,购自浙江省杭州子源实验动物科技有限公司(许可证号SCXK(浙)2019-0004),饲养于浙江海洋大学实验动物房(许可证号:SYXK(浙)2019-0031)。
1.2 方法
1.2.1 鳗鱼鱼鳔胶原蛋白的提取 新鲜鳗鱼鱼鳔预处理后,脱脂,酸法提取条件为乙酸浓度0.5 mol/L、料液比(g/mL)1∶55,酸解处理20 h,透析后冷冻干燥即得酸溶性Ⅰ型胶原蛋白,置于-20 ℃储存备用。
1.2.2 水凝胶的制备
1)凝胶液制备。鱼鳔胶原蛋白0.20 g、卡波姆、海藻酸钠、甘油,蒸馏水30 mL。0.60 g 海藻酸钠加入蒸馏水室温溶胀过夜,0.15 g 卡波姆加入蒸馏水和0.50 g 甘油加热溶胀过夜,将所有物质在常温混匀后置于4 ℃中2 h 脱泡处理,即得凝胶液。
2)交联液制备。制备0.05 mol/L 的CaCl2溶液和0.01 g/mL 的壳聚糖溶液,将两种溶液1∶1 混合均匀,即得交联液,密封保存备用。
3)水凝胶交联。将凝胶液倒入培养皿,均匀平铺薄层即可,放入4 ℃冷存2 h 后取出,将交联剂溶液倒入模具中,使之充分交联后,即得鱼鳔胶原蛋白-壳聚糖-海藻酸钠水凝胶。取出水凝胶片,用蒸馏水冲洗干净后备用。
1.2.3 水凝胶扫描电镜检测 将水凝胶样品冷冻干燥后切割成7 mm 的直径大小,在20 kV 加速电压下,溅射镀金250 s 后,在扫描电镜下观察其超微结构。使用Image J 和Origin Pro 2021 软件(Origin Lab),每张图像分析20 个随机点,统计毛孔的平均直径。
1.2.4 皮肤伤口愈合
1)皮肤伤口制作。24 只雄性ICR 小鼠适应性饲养一周后,随机分为两组即对照组和水凝胶组。各组小鼠应用4%的水合氯醛麻醉,剃去背毛,常规皮肤消毒,用无菌外科剪刀剪出1 cm 直径的伤口区域。对照组伤口区域仅用0.9%生理盐水处理,水凝胶组用水凝胶完全覆盖,水凝胶在使用前用紫外线照射灭菌。试验3、7 和14 d 时观察伤口状态并拍照,使用Image J 软件计算伤口面积,伤口愈合率=(初始伤口面积-特定一天伤口面积)/初始伤口面积×100%。
2)血清抗氧化水平检测。试验3、7 和14 d,处死每组小鼠前进行摘眼球取血,4 ℃下5 000 r/min 离心5 min 收集血清,使用试剂盒说明书检测MAD 含量和CAT、SOD、T-AOC、GSH-Px 活性。
3)血清炎症因子检测。利用试剂盒检测IL-6、IL-1β 及TNF-α 含量。
4)皮肤HE 染色。试验3、7 和14 d 时,处死小鼠后小心取下伤口区域皮肤,4%多聚甲醛固定24 h 后石蜡包埋,切片、脱蜡、水化、HE 染色后在光学显微镜下观察皮肤伤口的组织学结构。
1.2.5 统计学方法 采用SPSS23.0 软件进行统计学分析。计量数据用x±S表示,组间比较采用单因素方差分析t检验,以P<0.05 表示差异具有统计学意义。
2 结果与分析
2.1 水凝胶扫描电镜
水凝胶扫描电镜观察如图1 所示,水凝胶上具有高度互连多孔的结构,水凝胶分子之间相互交联,形成连续密集的小孔,孔径在1~175 μm 间,水凝胶的孔隙率为(84.00±5.46)%。

图1 水凝胶的扫描电镜结构
2.2 小鼠伤口愈合情况
小鼠皮肤伤口愈合如图2A 所示,试验3 d 时对照组皮肤伤口的红肿、炎症情况较为严重,水凝胶组的炎症情况较为轻微并伤口开始缩小。试验7 d 时对照组的伤口炎症有所减轻,伤口开始缩小,而水凝胶组的伤口明显缩小,炎症反应消失。试验14 d 后两组小鼠伤口均显示趋向愈合状态,伤口周围有细小的毛发长出,但对照组尚未完全愈合,且皮肤疤痕比水凝胶组的明显。伤口愈合率结果如图2B 所示,水凝胶组伤口愈合率明显高于对照组。

图2 小鼠伤口及伤口愈合率比较
2.3 血清抗氧化水平检测结果
血清中5 个抗氧化指标的检测结果如图3 所示。试验第3 天两组小鼠的SOD、GSH-Px、CAT 和TAOC 4 个抗氧化指标最低。随着试验时间的延长,抗氧化水平逐渐提高,特别到第14 天时,水凝胶组抗氧化水平上升幅度更大,相比均具有统计学意义;而MDA 含量,对照组第3 天时均较高,第7 天时水凝胶组下降明显。

图3 小鼠血清抗氧化活性检测
2.4 血清炎症因子检测结果
血清中炎症因子的检测结果如图4 所示。对照组IL-1β 在试验第3 天时较高,随后逐渐下降;而水凝胶组的3 个时间段均低于对照组。对照组和水凝胶组IL-6 水平相差较大,后期均有不同程度的下降。TNF-α 水平在试验第3 天时对照组稍高于水凝胶组,在第7 天、第14 天时显著低于对照组。

图4 小鼠血清炎症因子的检测
2.5 皮肤切口HE 染色结果
皮肤切口HE 染色结果如图5 所示。试验第3天时2 组皮肤切口最上方都有染成红色的渗出物,对照组真皮及与皮下组织交界处的炎症细胞浸润更多。第7 天时对照组切口表面形成1~2 层的表皮细胞,真皮内有肉芽组织形成。水凝胶组已形成2~3层的表皮细胞,真皮内有肉芽组织形成;可见新生的皮脂腺、汗腺及导管。第14 天对照组切口表面形成2~3 层的表皮细胞,真皮内有大量的胶原纤维、少量的皮脂腺,汗腺及导管已形成。水凝胶组第14 天切口处已形成复层扁平上皮,可见基底层、棘层、颗粒层、透明层及少量的角质层,真皮与表皮间有明显的乳头层,网状层结构致密,皮脂腺、汗腺及导管明显增多。
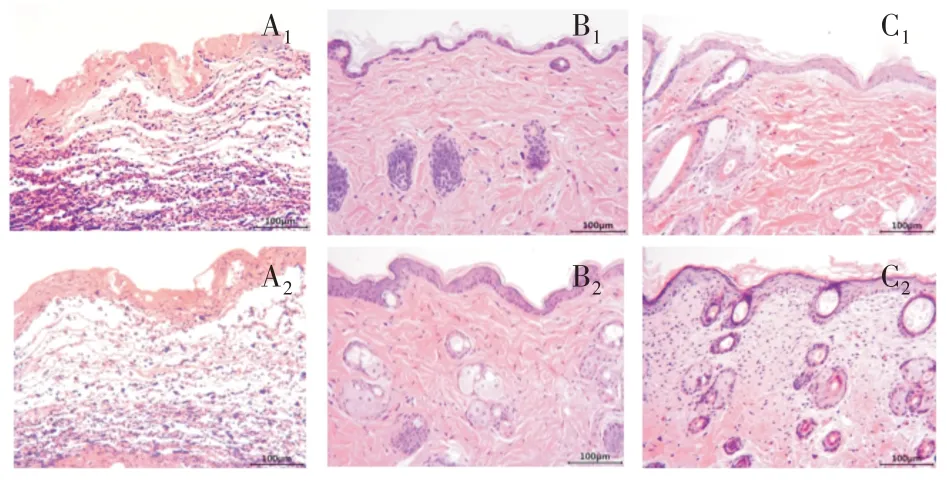
图5 皮肤切口HE 染色结果(×200)
3 小结与讨论
随着海洋生物医药的发展,以海藻酸盐膜为基底膜,配以胶原蛋白和壳聚糖混合后制备的复合敷料已有报导,但所选取的胶原蛋白多来源于鱼皮或鱼鳞,前期处理比较麻烦[5,6]。已有报导从日本黄姑鱼鱼鳔中提取的胶原蛋白具有较好的抗氧化活性,减少出血与渗出,可促进皮肤伤口的愈合[7],但有关以鳗鱼鱼鳔胶原蛋白为主药复合材料制备的伤口敷料目前尚未见报导。
水凝胶敷料是一种新型的创伤敷料,是将水溶性的高分子材料或其单体经加工处理后,形成具有三重网状结构且不溶于水的胶状物质,而孔隙率和孔隙结构是设计水凝胶剂型的关键因素[8]。为检测制备的水凝胶结构,通过扫描电镜技术观察制备的水凝胶是具有多孔隙的三维网络结构,多孔的水凝胶有利于细胞的附着、增殖和迁移,利于新生皮肤组织的生长,因此本试验制备的水凝胶材料是促进伤口愈合使用的理想材料。
在伤口愈合炎症阶段,炎症细胞产生大量ROS[9,10]。过量的ROS 会导致细胞死亡和坏死,不利于伤口愈合,判断氧化应激反应及清除自由基能力可检测血液中的抗氧化指标。随着试验时间的延长,水凝胶组中SOD、GSH-Px、CAT 和T-AOC 的活性比对照组的更高;而MDA 是主要的脂质过氧化终产物,却随着时间的延长而含量逐渐降低,表明水凝胶能较好地清除体内自由基,增加过氧化物酶的活性,提高血清总抗氧化能力,减轻氧化应激反应。
皮肤创面愈合中伴随着炎症反应,是创面修复的起始环节,如何促进创伤愈合、减轻炎症反应是医药界需要解决的难题[11],也是伤口敷料是否合格的标志。研究表明,IL-1β、IL-6 和TNF-α 具有介导炎症反应发生发展的生物学特性[7],检测血清中炎症因子的变化可判断炎症的进展情况。结果表明,水凝胶组3 个炎症因子指标均低于对照组,随着时间的延长均有下降趋势,特别是TNF-α 下降幅度最大,二者的差异更明显,因此认为水凝胶可降低炎症反应,促进皮肤伤口的愈合。伤口敷料是否有利于皮肤损伤后的修复,需要从组织形态学上进行观察。试验发现,水凝胶组的皮肤伤口炎症、渗出明显减轻,肉芽组织的形成、表皮、真皮及附属器官的再生明显早于对照组,表明制备的水凝胶能减轻伤口的炎症反应,促进皮肤再生,有利于伤口的修复。
本试验应用酸法制备的鳗鱼鱼鳔胶原蛋白,复合壳聚糖-海藻酸钠交联后获得的水凝胶是个多孔隙结构,可为伤口修复提供湿润的接触环境,并吸收创口中的渗出液、防止二次损伤等优点,水凝胶能提高抗氧化能力,降低血清中的炎症因子,促进小鼠皮肤伤口愈合,是一种具有开发潜力的伤口敷料。
