高效液相色谱法分析头孢噻肟钠杂质研究
2022-06-08赵丹聂飞贾全任峰孙玉双
赵丹,聂飞,贾全,任峰,孙玉双
(华北制药河北华民药业有限责任公司,河北 石家庄 052165)
头孢噻肟钠作为第3 代头孢菌素,与β-内酰胺酶抑制剂结合可以抵抗耐药菌发挥药效,对多数革兰氏阴性及阳性菌有较好的抗菌作用[1-2],但由于其在临床上常引发过敏性休克反应,严重影响患者生命安全[3]。为了解决药品安全问题,必须对潜在的杂质进行研究。
头孢噻肟钠无菌原料药的杂质主要包括三类:有机杂质、无机杂质和残留溶剂[4]。有机杂质产生于生产和储运过程中,主要包括起始物料、中间产物、副产物、降解产物、试剂、配位体和催化剂等;头孢噻肟钠以7-ACA 和AE 活性酯为主要起始原料,经过合成反应得到头孢噻肟酸,头孢噻肟酸经成盐反应、除菌过滤、雾化干燥[5]等工艺过程后得到头孢噻肟钠原料药。
当产品发生关键变更时,应对产品重新进行杂质研究,考察改变工艺路线或者关键工艺参数;工艺中引入新的溶媒、溶剂、物料或者关键设备的变更等导致杂质的变化,并对杂质档案进行更新。当产品发生重大变更时,根据变更评估的结果,决定是否需要重新进行杂质研究。当产品未发生上述涉及的变更时,每年对杂质档案进行再评估,评估时至少需要连续三批样品的杂质分析数据[6]。结合中国药典[7]、欧洲药典[8]、赵霞等[9]、姚蕾等[10]、王春玲[11]等方法,本文主要对头孢噻肟钠产品的起始原料AE 活性酯可能引入的杂质情况进行分析研究。
1 实验部分
1.1 试剂与仪器
试剂:头孢噻肟钠原料药(自制,批号1907001、1907002、1907003)。AE 活性酯(山东金城医药化工有限公司,批号31031197001)、头孢噻肟对照品(批号BE181005,含量93.3%)、头孢噻肟峰鉴别(批号Y0000506-2)、甲醇为色谱纯、乙腈为色谱纯,水为实验室自制纯化水,试剂均为分析纯。
仪器:Waterse 2695 高效液相色谱仪(配2489型紫外检测器)、Agilent1260 高效液相色谱仪、电子分析天平(梅特勒XS105DU,梅特勒XP)、pH 值计(梅特勒FE20)。
1.2 潜在杂质分析
本文对头孢噻肟钠产品的起始原料AE 活性酯可能引入的杂质情况进行理论分析,根据AE 活性酯生产流程情况(见图1),列出可能存在的潜在杂质(见表1)。

表1 起始物料AE 活性酯中可能存在的潜在杂质Tab.1 Potential impurities that may exist in AE active ester of starting materia

图1 AE 活性酯生产流程图Fig.1 AE active ester production flow chart
1.3 检验方法
1.3.1 AE 活性酯有关物质的检验
(1)色谱条件
色谱柱:岛津VP-ODS 150 mm×4.6×5 um(或其等效的同等类型色谱柱);检测波长:UV,263 nm;进样量:20 μl;流速:1.0 mL/min。
(2)溶液配制
溶液A:称取磷酸二氢钾4.73 g,磷酸氢二钾1.87 g,溶于1 000 mL 纯化水中,调pH 值=5.0(±0.05),过滤,脱气。
溶液B:称取2.0 g 四庚基溴化铵溶于600 mL乙腈中。
流动相:溶液A 至溶液B(V/V=400∶600),混匀,脱气15 min。
(3)系统适用性
氨噻肟酸(杂质AT)相对保留时间为0.60,巯基苯骈噻唑(杂质M)相对保留时间约为0.76,二硫化二苯并噻唑(杂质DM)相对保留时间为5.6,主峰与相邻峰间分离度应大于1.5。
(4)测定过程
对照品溶液:精密称定AE 活性酯对照品(头孢曲松杂质D)约10 mg,置10 mL 量瓶中,加流动相溶解并稀释至刻度,摇匀,马上进样分析。
供试品溶液:精密称定供试品约15 mg,置50 mL 量瓶中,加流动相溶解并稀释至刻度,摇匀,迅速进样分析。
取供试品溶液20 μl 注入液相色谱仪,平行进样两次,记录色谱图;按面积归一化法以峰面积计算供试品中AE 活性酯纯度以及杂质AT、杂质DM、杂质M 的含量。
1.3.2 头孢噻肟钠有关物质的检验
(1)色谱条件
色谱柱:C18 3.9 mm×150 mm,5.0 μm;流速:1.0 mL/min ;检测波长:UV 235 nm;进样体积:10 μl。
(2)溶液配制
稀盐酸溶液:称取盐酸20 g 至100 mL 纯化水中,摇匀。稀氢氧化钠溶液:称取氢氧化钠8.5 g 至100 mL 纯化水中,摇匀。
0.2M 磷酸二氢钾溶液:称取磷酸二氢钾27.22 g至1 000.0 mL 纯化水中,溶解,摇匀。0.2M 氢氧化钠溶液:称取氢氧化钠8.4 g,加入除去二氧化碳的纯化水1 000.0 mL,溶解,摇匀。
pH 值为6.6 缓冲溶液:量取250.0 mL 0.2M 磷酸二氢钾溶液,89.0 mL 0.2M 氢氧化钠溶液,加纯化水稀释至1 000.0 mL,摇匀。
溶液A:流动相B-流动相A(14∶86)。
流动相A:取7.1 g 磷酸氢二钠至1 000 mL 量瓶中,加水溶解并稀释至刻度,用磷酸调节pH 值至6.25。流动相B:甲醇。
(3)梯度洗脱程序
梯度洗脱程序中相关数值如表2所示。

表2 梯度洗脱程序Tab.2 Gradient elution program
(4)系统适用性试验:
取10 μl 对照溶液(c)注入液相色谱仪,记录色谱图,头孢噻肟峰与杂质E 的分离度不得低于3.5,主峰的对称因子不得大于2.0。
(5)测定过程
供试品溶液:取供试品40.0 mg,精密称定,置50.0 mL 容量瓶中,用溶液A 溶解并稀释至刻度,摇匀。对照溶液(a):取8.0 mg 头孢噻肟酸对照品,精密称定,置10 mL 量瓶中,用溶液A 溶解并稀释至刻度,摇匀。
对照溶液(b):量取1.0 mL 供试品溶液,置100.0 mL 的量瓶中,用溶液A 定容至刻度,摇匀。对照溶液(c):量取1.0 mL 稀盐酸溶液,4.0 mL 供试品溶液,在40 ℃水浴中加热2 h。再加入5.0 mL pH 值为6.6 的缓冲溶液,1.0 mL 的稀氢氧化钠溶液,混匀。
对照溶液(d):称取头孢噻肟峰鉴别对照品(含有杂质A、杂质B、杂质C、杂质E 和杂质F)约4 mg,加溶液A 溶解稀释至5 mL,摇匀。
取对照溶液(d)10 μl 注入液相色谱仪,记录色谱图。主峰的保留时间约为13 min,杂质B 的相对保留时间约为0.3,杂质A 的相对保留时间约为0.5,杂质E 的相对保留时间约为0.6,杂质C 的相对保留时间约为1.9,杂质D 的相对保留时间约为2.3,杂质F的相对保留时间约为2.4,杂质G 的相对保留时间约为3.1。取供试品溶液、对照溶液(b)各10 μl 注入液相色谱仪,记录色谱图。按主成分的自身对照法计算供试品中各杂质含量。供试品溶液色谱图中任何小于对照溶液(b)主峰峰面积0.03 倍的峰可忽略不计。
2 结果
2.1 AE 活性酯中杂质追踪
通过1.3.1 节有关物质试验方法,头孢噻肟钠连续三批样品进行检测,分别对特定杂质氨噻肟酸(AT)、二硫化二苯并噻唑(DM)、巯基苯骈噻唑(M)进行定位测定,结合杂质定位情况分析杂质转移情况。系统适用性试验色谱图见图2~4。由表3可知,起始物料AE 活性酯中各项检测指标均符合限度要求。

图2 系统适用性试验分离度溶液Fig.2 System suitability test resolution solution

图3 AE 活性酯杂质定位溶液Fig.3 AE active ester impurity locating solution

图4 AE 活性酯供试品溶液Fig.4 AE active ester test solution

表3 起始物料AE 活性酯杂质检测结果Tab.3 Test results of active ester impurities in starting material AE
2.2 头孢噻肟钠中杂质追踪
通过1.3.2 节有关物质试验方法,取AE 活性酯、头孢噻肟钠连续三批样品进行检测,结合杂质定位情况分析杂质转移情况。系统适用性试验色谱图见图5~6。

图5 头孢噻肟峰鉴别溶液Fig.5 Cefotaxime peak identification solution

图6 头孢噻肟钠供试品溶液Fig.6 Cefotaxime sodium test solution
由表4可知,头孢噻肟钠中检出AE 活性酯所携带的AT 杂质,检测结果为0.23%,小于AE 活性酯中杂质AT 的限度0.3%。检出AE 活性酯残留量是0.02%,残留量很小可忽略。杂质M 虽未检出,但头孢噻肟钠有单独的检测M 的方法,所以杂质M 残留可控。杂质DM 在AE 活性酯原料及成品中均未检出。

表4 起始物料AE 活性酯杂质夹带到成品头孢噻肟钠中的残留检测结果Tab.4 Test results of AE active ester impurity residue of starting materia
由表5可知起始物料AE 活性酯所携带的AT杂质在头孢噻肟钠有关的系统里被检出,残留量为0.02%,AE 活性酯残留量为0.04%,均小于头孢噻肟钠未知单杂限度标准0.05%。
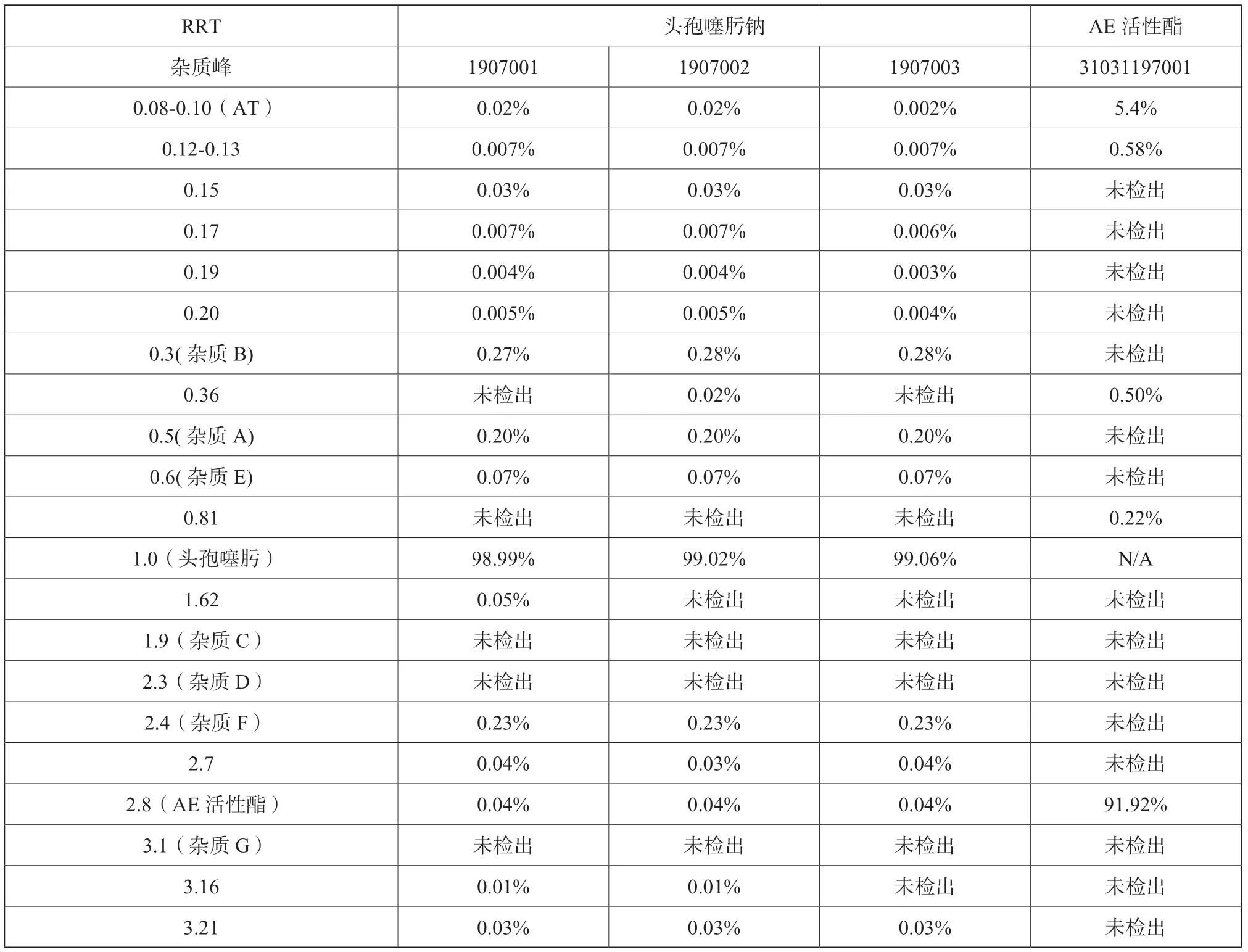
表5 头孢噻肟钠中杂质追踪检测结果Tab.5 Trace detection results of impurities in Cefotaxime Sodium
3 讨论
本实验结果显示,此次杂质分析数据满足杂质考察初期设计标准要求,AE 活性酯中杂质AT 虽被检出0.02%,但是远低于有关物质质量标准。二硫化二苯并噻唑(DM)是AE 活性酯合成起始物料,在AE 活性酯系统中和头孢噻肟钠系统中均未被检出。头孢噻肟钠系统中检出了AE 活性酯0.04%,低于未知单杂限度(0.05%),日常检验用头孢噻肟钠有关物质系统可以控制AE 活性酯残留量。
