一种钴配合物的合成及其结构与DNA性质的研究
2022-05-27王松玲高恩军
王松玲,高恩军
(沈阳化工大学 辽宁省无机分子基化学重点实验室, 辽宁 沈阳 110142)
癌症作为人类生命健康的重大威胁,寻找有效地治愈药物一直是科学家努力研究的方向[1].自从顺铂作为有效的化疗药物投入使用以来,新型金属配合物的研发已成为研究热点[2].顺铂因其毒副作用如肾毒性和脏毒性给患者治疗期间带来更多的痛苦[3],因此研发具有优良的抗肿瘤活性且毒副作用小的新型配合物来弥补顺铂的不足具有现实意义和紧迫性.
配体的选择多以含有N、O元素的有机化合物为主,并且N、O有机物因配位点良好,在配合物的研究中应用较为广泛,过渡区金属因存在适当的氧化还原电位使其成为配合物合成的常用金属,且过渡金属配合物具有良好的生化活性[2].笔者通过溶剂热法,选取4,5-咪唑二羧酸及氯化钴合成新颖的钴配合物,利用X-射线单晶衍射仪确定其结构,通过紫外和荧光技术探索配合物与DNA的作用方式和结合能力强弱,借此判断钴配合物是否能进一步应用于肿瘤细胞的抑制实验.
1 实验部分
1.1 仪器与试剂
BRUKER SMART 1000 CCD X射线衍射仪,美国Bruker公司;Perkin-Elmer LS55荧光分光光度计,美国Perkin-Elmer公司;SHIMADZU UV2700紫外可见分光光度计,日本岛津公司;JY-SPAT水平电泳槽,上海培清科技有限公司.
4,5-咪唑二羧酸(H2L)、N,N-二甲基甲酰胺(DMF)、鲱鱼精DNA(HS-DNA)、亚甲基蓝(MB)、蒸馏水、Tris-HCl、NaCl和二水合氯化钴,均购于国药集团.
1.2 配合物的合成
将4,5-咪唑二羧酸(0.005 g)与氯化钴(0.015 g)常温下溶解于3 mL DMF/H2O(体积比1∶1)溶液中,充分搅拌后置于60 ℃烘箱中加热72 h,缓慢冷却至室温得浅粉色片状晶体.经X-单晶衍射确定其分子式为C16H22CoN6O12,结构式为[Co(HL)2(H2O)2]·2C3H7NO.使用SHELXTL-2013软件程序对合成的配合物进行晶体数据解析,结果如表1所示.
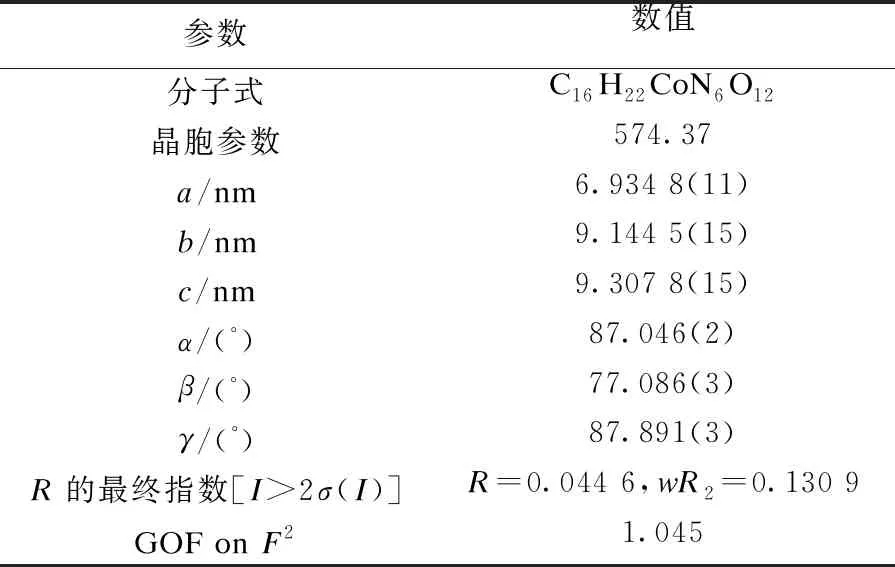
表1 配合物晶体数据
1.3 荧光猝灭实验
在MB-DNA体系[c(MB)=5×10-6mol/L,c(DNA)=1×10-6mol/L]中分别加入0~12 μmol/L的金属配合物,采用荧光光谱法测定金属配合物与DNA的结合能力.反应在Tris-HCl(pH=7.4)缓冲溶液中进行,确定激发波长为680 nm[4],选择扫描范围为600~800 nm.
1.4 紫外光谱滴定
钴配合物的配制浓度为10 μmol/L,配制DNA浓度为10 μmol/L,准确移取3 mL空白溶剂参比液及配合物溶液在220~400 nm范围内扫描,结束后在参比溶液和样品溶液的比色皿中加入10 μL DNA溶液,充分混匀,每隔5 min扫描检测样品吸光度变化[5],多次重复此过程得吸收曲线.
2 结果与讨论
2.1 配合物的结构
图1为钴配合物的结构,展示了其配位环境.钴原子分别与2个N(分别来自两个H4L配体)、4个O(其中2个来自配体H4L,2个来自水分子)以配位键连接[3],形成6配位化合物.Co(1)—N(1)键长为2.105 8 nm,Co(1)—O(1)键长为2.147 1 nm,Co(1)—O(5)键长为2.081 6 nm.

图1 配合物配位环境
配合物一维链状结构如图2所示,配合物单体之间由氢键连接,构成链状结构.配合物的二维平面结构如图3所示,不同链状结构之间由氢键连接形成平面构型.为使配合物结构更清晰,图1、图2、图3中的氢原子已省去[3].

图2 配合物一维链状结构
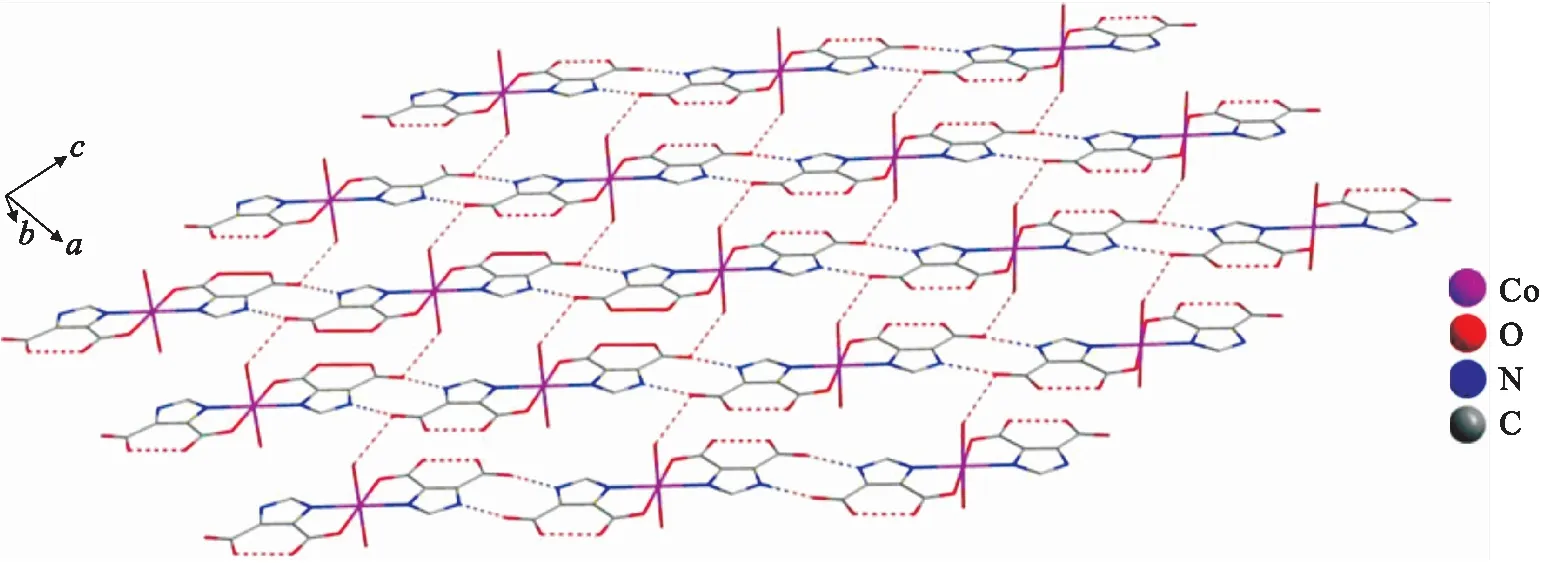
图3 配合物二维平面结构
2.2 配合物与HS-DNA作用的荧光光谱法研究
亚甲基蓝(MB)是用于测定DNA结构常见的荧光探针[6],并且在探索金属配合物与DNA结合的模式和过程等方面具有灵敏性和安全性.亚甲基蓝(MB)长期以来一直作为生物染色剂用于包括癌症在内等疾病的诊断.MB是一种吩噻嗪类染料[5],可作为DNA的敏感荧光探针使用.近年来,亚甲基蓝已逐步取代溴化乙锭成为常用的核酸安全试剂[5].本身荧光性较强的MB与DNA发生静电结合作用后,会出现MB-DNA体系的荧光强度大大降低的现象.当金属配合物与MB-HS-DNA体系混合反应后,会使MB-HS-DNA体系荧光强度上升,说明该金属配合物也能与HS-DNA发生作用,与MB产生竞争吸收,释放MB分子,使荧光强度上升.不同浓度钴配合物与MB-HS-DNA体系作用的荧光光谱如图4所示.1为溶液中只存在MB-DNA体系的荧光强度曲线,2~8为MB-DNA体系中配合物浓度逐渐升高的荧光曲线.由图4可以看出:随着配合物浓度的升高,MB-HS-DNA体系的荧光强度上升,说明钴配合物与HS-DNA具有一定的作用能力.
根据经典Stern-Volmer方程[6]I0/I=1+Ksq·r(I表示体系中存在配合物时的荧光强度;I0代表MB-DNA体系的荧光强度;r值通过配合物与DNA浓度的比值计算得到;Ksq为Stern-Volmer猝灭常数)中Ksq判断配合物与DNA作用能力的强弱.Ksq越小,说明配合物与DNA的作用能力越小,结合能力越弱.根据图5计算得Stern-Volmer猝灭常数Ksq值为0.109 4.
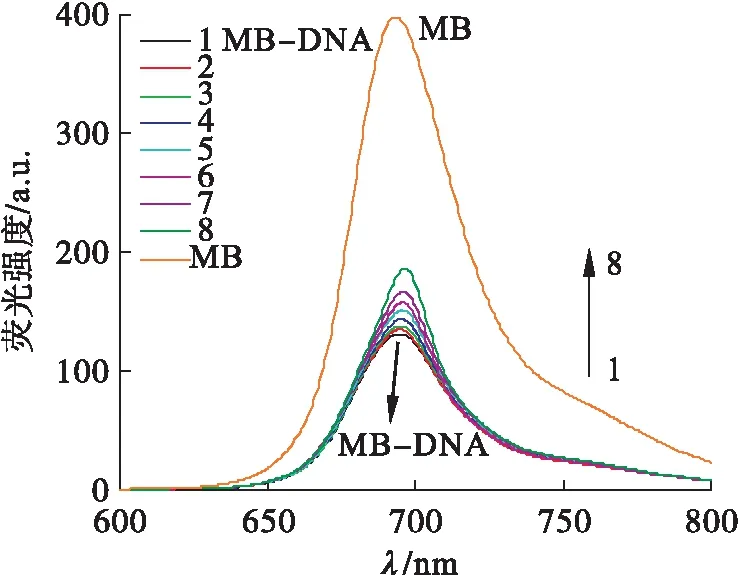
c(MB)=5×10-6 mol/L c(HS-DNA)=1×10-6 mol/L
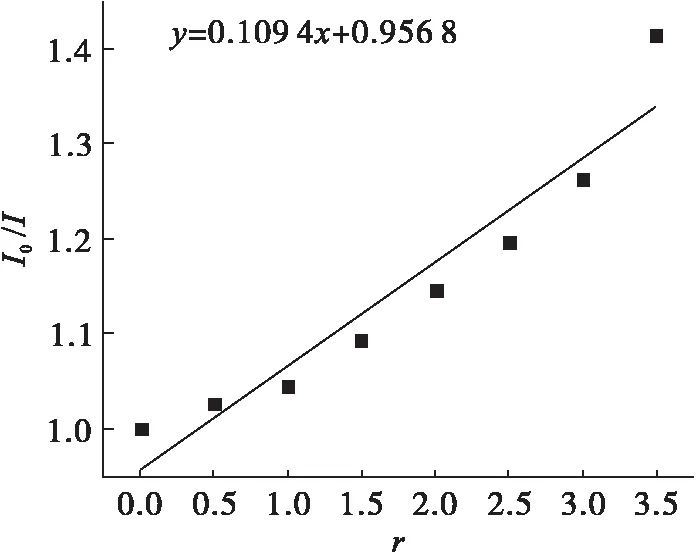
图5 配合物的Stern-Volmer猝灭常数
2.3 配合物与HS-DNA作用的紫外光谱法研究
紫外吸收光谱法是研究金属配合物与DNA作用的常用方法之一[7].配合物与DNA混匀后,若配合物与DNA能够发生相互作用,会产生电子的能级跃迁,此时的吸光度会产生相应地变化,配合物的特征吸收谱带会产生红移或蓝移效果,产生增色效应或减色效应[8].配合物与DNA产生减色效应时,一般认为配合物与DNA发生嵌插作用[9];配合物与DNA发生增色效应时,一般认为是氢键[10]作用或是静电结合作用.不同浓度钴配合物与HS-DNA体系作用的紫外光谱如图6所示.

1 c(HS-DNA)=0 mol/L
1为未加入HS-DNA时配合物的吸光度;2~15为逐滴加入HS-DNA后配合物与HS-DNA体系紫外吸收光谱的变化情况.随着HS-DNA的加入,反应体系呈现出明显的增色效应,基于对配体结构的考量,在配合物结构中的NH与HS-DNA中的腺嘌呤的N或胸腺嘧啶的O之间可以形成有利的氢键[10],判断此钴配合物与HS-DNA的作用方式应为氢键作用[11].
3 结 论
(1) 用配体4,5-咪唑二羧酸与金属盐氯化钴采取溶剂热法合成新型钴配合物[11],通过X-单晶衍射仪确定该配合物为六面体构型,分别与2个N原子、2个配体上的O原子和2个水分子上的O原子形成配位键.
(2) 通过紫外吸收光谱实验确定了该配合物与DNA的作用方式为氢键作用.利用配合物与MB-DNA的竞争实验确定了配合物与DNA有较强的结合能力,计算荧光猝灭常数Ksq值为0.109 4.该配合物与DNA有较好的亲和能力,可作为潜在的抗癌试剂进行进一步研究.
