基于2,5-二羟基对苯二甲酸配体的Cu(Ⅱ)配合物的合成、结构及性质研究
2022-05-26李传碧王家军崔允祚
李传碧,陈 雪,王家军,王 贺,崔允祚,李 琦
(1.吉林师范大学 环境友好材料制备与应用教育部重点实验室,吉林 长春 130103;2.吉林师范大学 化学学院,吉林 四平 136000)
金属有机配位化合物是以金属离子或金属簇为节点,有机配体为连接体,通过自组装的方式形成的一类具有周期性网状结构的晶体材料[1],MOFs 材料拥有多种功能,在磁性[2-3]、气体的分离与储存[4]、催化[5]、电化学[6-7]、荧光传感[8-10]等领域具有广泛的应用前景.芳香酸类配体具有丰富的配位模式,易形成高维、结构特殊的配合物,因而受到人们的青睐[11].本文选择2,5-二羟基对苯二甲酸作为配体[12-13],将之与Cu配位,采用水热法合成了新型金属配合物[Cu(DHBDC)2(H2O)2]n,并对其结构和性质进行了研究.
1 实验
1.1 表征仪器
Bruker Apex Ⅱ CCD单晶衍射仪.Bruker VERTEX 80红外光谱仪,测定范围400~4 000 cm-1,KBr 压片.Perkin-Elmer TGA7热重分析仪.ESCALAB250XI X射线粉末衍射仪.Perkin-Elmer 2400 CHN元素分析仪.
1.2 配合物[Cu(DHBDC)2(H2O)2]n的合成
实验所用原料和试剂均为分析纯,未经任何处理直接使用.称取0.297 g(1.5 mmol)2,5-二羟基对苯二甲酸和0.188 g(1 mmol)Cu(NO3)2溶于15 ml去离子水中,在室温下搅拌均匀,加少许NaOH溶液调节pH至8.0,将混合溶液装入聚四氟乙烯反应釜中,在140 ℃反应3 d.然后以5 ℃/h的速率降至室温,将得到的产物用蒸馏水水洗、干燥,最终得到浅蓝色块状晶体.
采用 Perkin-Elmer 2400 CHN 元素分析仪对配合物中的 C、H、N 元素的含量进行测定分析.分子式为C8H8CuO8,元素分析:理论值(%) C 32.73,H 2.71;实验值(%) C 32.63,H 2.59.由此可以看出实验值与理论值基本一致.IR (KBr,cm-1):3 475(s)、1 750(s)、1 534(m)、1 424(m)、1 332(m)、571(w)、484(w)、435(w).
2 结果与讨论
2.1 晶体结构测试
选取表面干净光滑、尺寸大小为0.28 mm×0.27 mm×0.25 mm的单晶配合物.在Bruker Apex Ⅱ CCD单晶衍射仪上对配合物进行了单晶结构测定,并使用SHELXL程序精修晶体结构.结果表明,配合物属单斜晶系,空间群为C2/c,分子式为C8H8CuO8.表1为配合物[Cu(DHBDC)2(H2O)2]n的晶体结构数据,表2为其主要的键长和键角数据.
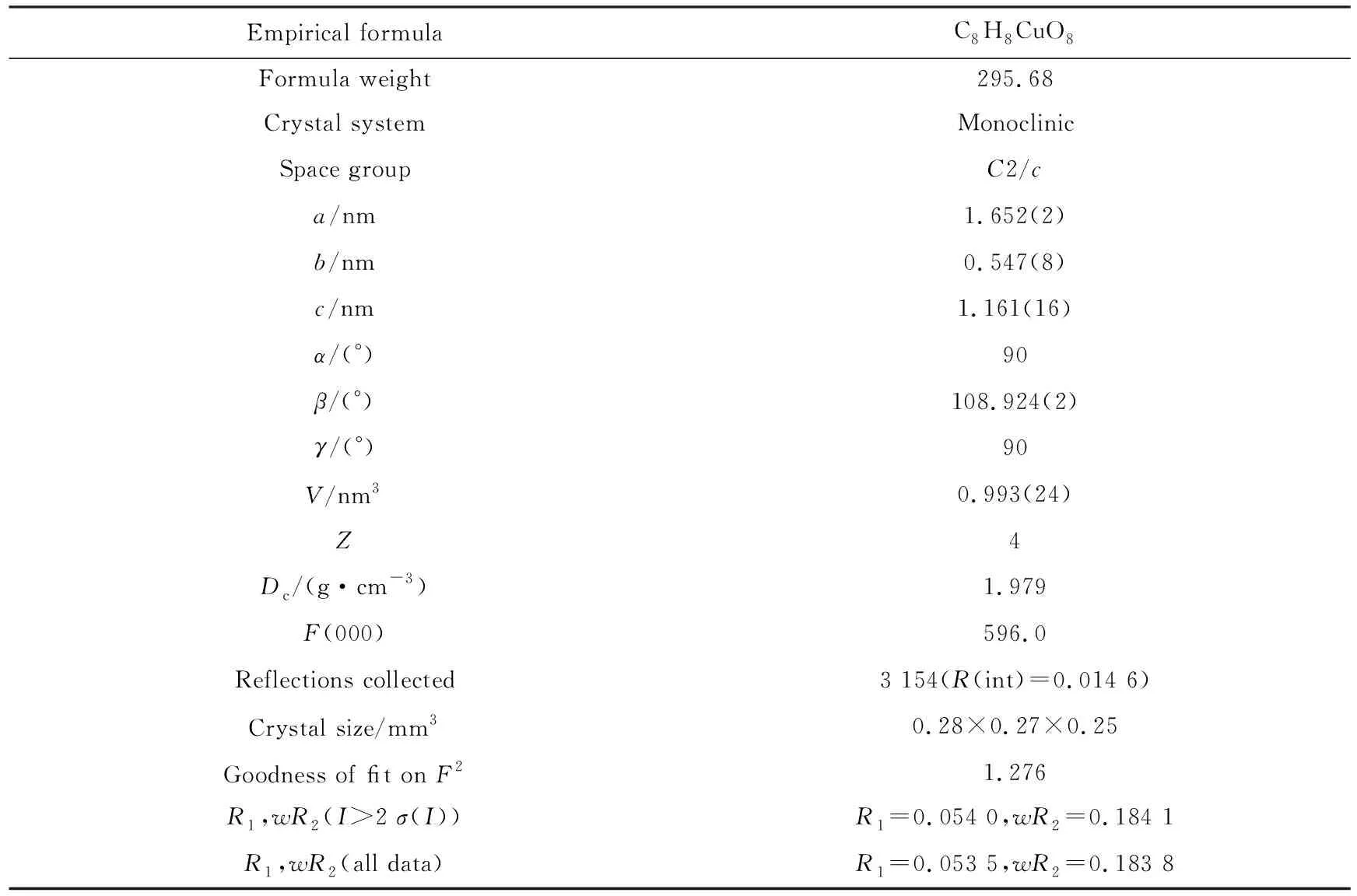
表1 配合物的晶体结构数据
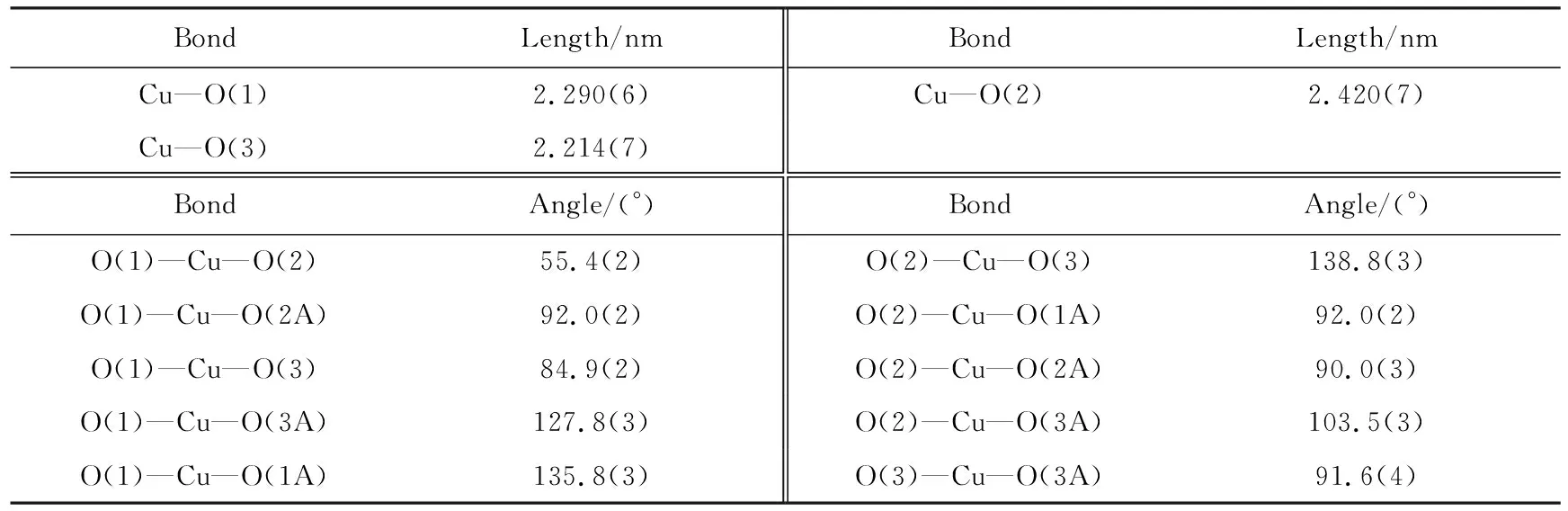
表2 配合物的主要键长和键角数据
2.2 配合物的晶体结构分析
配合物[Cu(DHBDC)2(H2O)2]n的晶体结构表明,在配合物的单元晶胞中含有一个Cu2+离子,两个去质子化的2,5-二羟基对苯二甲酸和两个配位水分子,如图1所示.在这个晶胞中Cu(Ⅱ)与两个水分子(O(3),O(3A))和两个2,5-二羟基对苯二甲酸(O(1),O(2),O(1A),O(2A))进行配位,形成六配位八面体构型.每个2,5-二羟基对苯二甲酸连接两个中心原子Cu并向两个方向延伸,形成一维链状结构,如图2所示.配合物晶体中还存在O(4)—H(4)…O(1)(分子内),O(3)—H(3A)…O(2),O(3)—H(3B)…O(4) (分子间) 氢键(见表3),由于氢键的存在,增加了分子结构的稳定性.
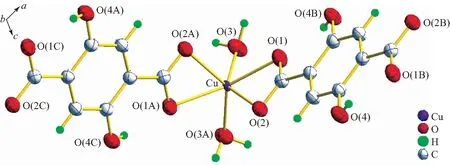
图1 配合物的晶体结构
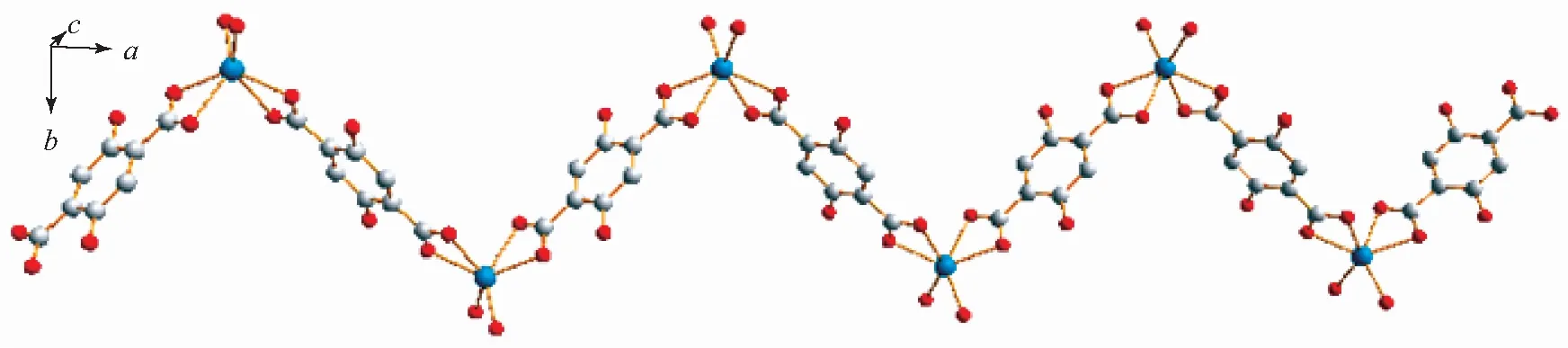
图2 配合物的一维链状结构图
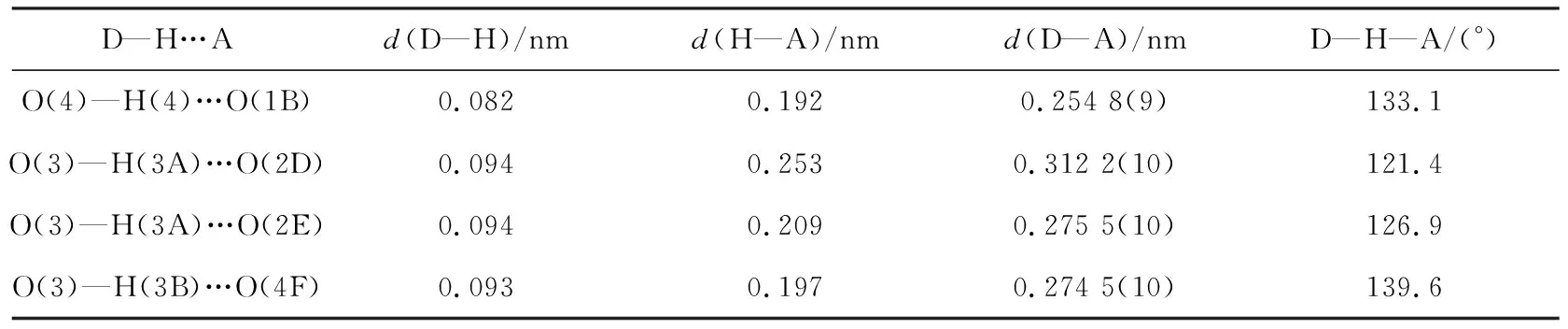
表3 配合物的氢键
2.3 配合物的热稳定性
在0~800 ℃的温度范围内,配合物[Cu(DHBDC)2(H2O)2]n的热重曲线图[14]如图3所示,配合物在110 ℃下保持稳定,并且重量在110~580 ℃的范围内持续降低,在整个失重过程中有两段明显的失重,第一段为110~200 ℃,对应的是晶胞中的配位水的失去,其损失量为13.23%(理论值为12.17%),第二段为200~580 ℃,为配体2,5-二羟基对苯二甲酸经过高温后的结构塌陷,最终剩余物为CuO,总失重为74.86%(理论值为73.10%),与理论值较为接近.结果表明,化合物的热稳定性一般,热重分析数据与晶体结构分析结果基本一致.
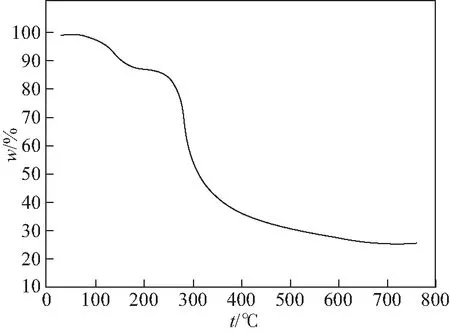
图3 配合物的热重分析曲线
2.4 X射线衍射
采用X射线粉末衍射法对配合物的纯度进行了检测.如图4所示,配合物的 XRD谱图[15]与根据单晶结构模拟的 XRD谱线基本一致,说明所得到的晶态样品较纯.其中粉末X射线衍射强度数据收集时样品晶体取向的不同是造成衍射强度差异的主要原因.
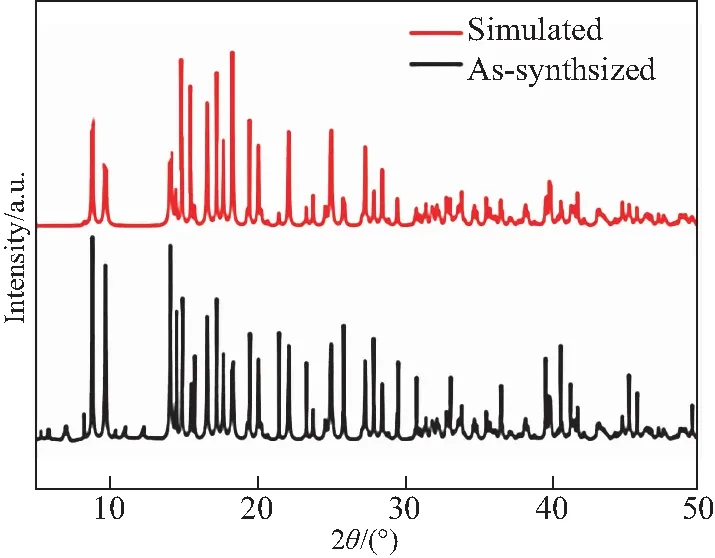
图4 配合物的XRD谱图
2.5 Hirshfeld 表面分析
配合物[Cu(DHBDC)2(H2O)2]n的Hirshfeld 表面分析[16]研究了dnorm、Shape index和Curvedness,如图5(B)所示.dnorm图中红色区域表示配合物有较强的相互作用,通过结构分析,其相互作用为O…H氢键作用,而且颜色很深,表示相互作用较强.Curvedness表面凹凸不平,说明晶体中未形成紧密的分子间排列.如图5(C)所示,经过对配合物[Cu(DHBDC)2(H2O)2]n的二维指纹图进行分析,配合物中存在H…O分子间的相互作用,在指纹图上表现为两个明显地长尖峰.由图5(A)所示,H…H、C…H/H…C、O…H/H…O分别占整个Hirshfeld 表面分析总面积的15.8%、8.3%、38.3%,可以明显地看出配合物中主要的相互作用是O…H/H…O.
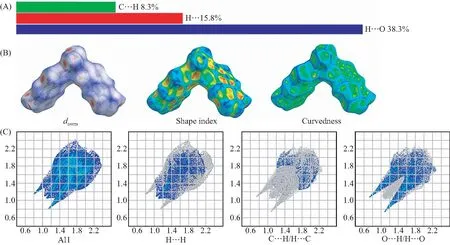
图5 配合物的短程作用占比(A)、dnorm、Shape index和 Curvedness的表面分布情况(B)及2D指纹图(C)
2.6 分子轨道及AIM分析
配合物的量子化学计算采用Gaussian09程序在B3LYP/GenECP水平进行,C、H、O采用6-31+G(d)基组,Cu采用LANL2DZ基组.结构模型是从X射线衍射精修的晶体学信息文件(cif)获得的.为了便于计算,本文在计算中将配合物简化为“单体”,没有进行几何优化.本文计算了配合物的分子轨道、NPA电荷以及电子构型.最后用计算得到的fchk文件,借助于Multiwfn程序[17]来研究配合物的拓扑性质.
计算模型为负二价阴离子,其中包含43个原子、254个电子、586个基函数、1 060个初始高斯函数、121个α电子、120个β电子.由于模型中包含一个成单电子,自旋多重度为2.分子总能量为-4.900×109J,HOMO和LUMO的能量分别为-1.050×104和2.232×105J,ΔE(ELUMO-EHOMO)值为3.282×105J,这表明化合物基态下是稳定的[18].HOMO和LUMO分子轨道如图6所示,从图中可以看出HOMO电子云主要位于包含O(1)、O(1B)的2,5-二羟基对苯二甲酸(DHBDC)配体上,LUMO电子云主要位于两个配位的水分子上.
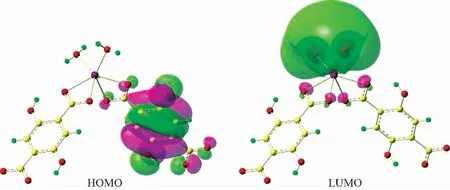
图6 配合物的分子轨道
配合物的部分原子净电荷(NPA电荷)和电子构型列于表4,计算显示中心Cu的电子构型为4s(0.22)3d(9.64)4p(0.27),O的电子构型为2s(1.71,1.73)2p(4.97~5.20)3p(0.00,0.01)3d(0.01).Cu为+2价,它从配位的DHBDC和水分子得到部分电子,这表明配合物中心Cu原子带有正电荷,电荷为0.862 95.表3中,所有配位氧原子电荷都为负值,模型中配位氧原子的NPA电荷:O(1)为-0.778 86,O(2)为-0.706 13,O(3)为-0.949 45,O(1A)为-0.773 32,O(2A)为-0.715 52,O(3A)为-0.949 59.

表4 配合物的部分原子净电荷与电子构型
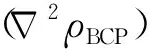
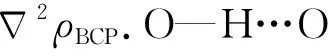
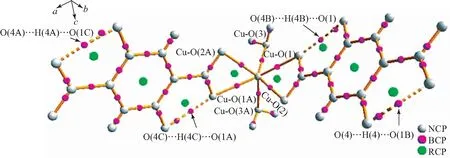
图7 NCP、BCP、RCP、配位键和分子内氢键
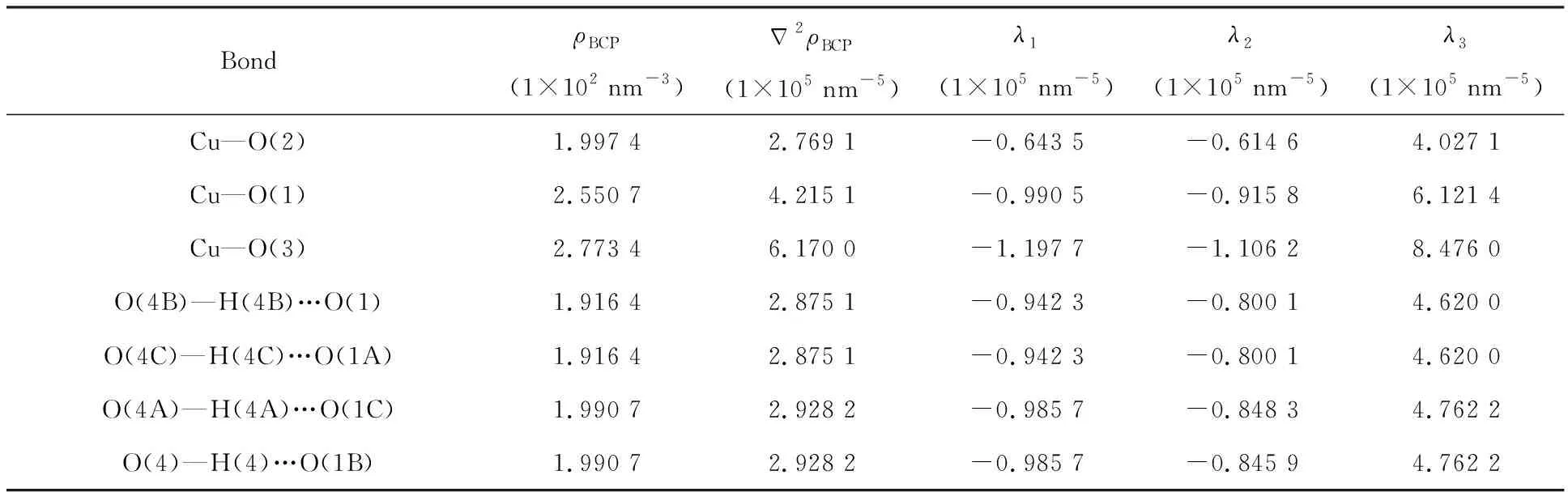
表5 配合物的ρBCP电子密度,拉格朗日电子密度以及在BCP处的Hessian特征值
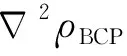
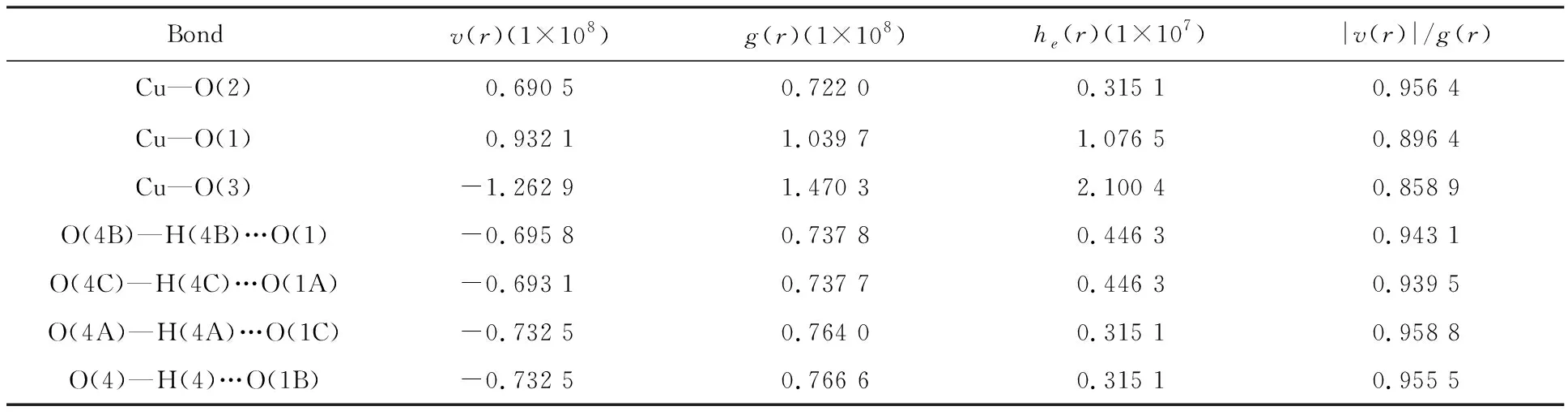
表6 配合物在BCP处的局部特征
3 结论
采用水热合成法构筑了一种具有新颖结构的Cu基配合物[Cu(DHBDC)2(H2O)2]n,X射线单晶衍射结构表明该配合物属于单斜晶系.配合物的结构单元包括一个Cu(Ⅱ),两个2,5-二羟基对苯二甲酸,两个配位水分子,形成六配位模式.结果表明:配合物具有中等的热稳定性.Hirshfeld 表面分析表明配合物有较强的氢键作用.配合物O—H…O相互作用是闭壳层相互作用.
