介孔氧化镍材料的制备和性能研究
2022-05-26吕世权齐春玉
吕世权,齐春玉
(吉林师范大学 物理学院,吉林 四平 136000)
0 引言
近年来,随着全球的经济快速发展,增长的能源需求加剧化石能源的消耗,随之而来的能源危机和环境污染问题迫切需要对可再生能源和新型能源技术进行开发,保证能源和环境的可持续发展.氢由于其环境友好被认为是满足全球能源需求的有利解决方案[1-6].电催化水解作为将电能转化为化学能的电化学装置,是最有前景的开发可再生能源的制备技术之一,已成为各国能源领域研究的热点.然而,由于动力学缓慢的析氧反应(OER),其使用受到限制,并且由于其在热力学和动力学上不利于去除四个电子以形成氧-氧双键而导致该过程中的能量损失[7-8].

1 实验
1.1 材料制备
介孔金属氧化物NiO是通过配位协同自组装法合成的.1.36×10-4mol P123作为模板、5 mmol柠檬酸作为螯合剂、16 mmol浓HNO3调节pH,在磁力搅拌下溶解在70 mmol 1-丁醇溶液中,然后加入2.5 mmol Ni(NO3)2·6H2O作为镍源,在室温下剧烈搅拌数小时直至形成透明溶胶.将溶胶转移到培养皿(直径90 mm)中并于烘箱内挥发溶剂,为了使挥发溶剂的过程中金属氧化物不分相,采用分段式挥发:80 ℃蒸发1.5 h、100 ℃蒸发3 h、120 ℃蒸发1 h.然后将得到的中间产物在空气中梯度煅烧:150 ℃下煅烧4 h(升温速率为2 ℃/min)、250 ℃下煅烧2 h(升温速率为2 ℃/min)、350 ℃下煅烧2 h(升温速率为2 ℃/min),最终产生高度结晶的介孔NiO产物.
SDC催化剂的制备采用柠檬酸燃烧法.按照化学计量比准确称取Ce(NO3)2·6H2O和Sm(NO3)2·6H2O加入去离子水中,持续搅拌直至完全溶解,按照n(金属阳离子)∶n(柠檬酸)=1∶2加入一水合柠檬酸(C6H8O7·H2O)并用氨水调节pH至8~10,在200 ℃下持续加热搅拌,直到溶液成凝胶状.然后将凝胶转移至1 000 mL蒸发皿中,置于电炉上持续加热至自燃生成淡黄色粉末,最后将粉末在800 ℃下煅烧6 h以除去残留有机物.
1.2 催化剂薄膜的制备
进行电化学表征之前,需要对催化剂材料进行处理.首先按照质量比1∶1称取0.05 g的催化剂样品(NiO或者NiO/SDC复合材料)和0.05 g的导电炭黑置于小号离心管中.使用移液枪取450 μL的乙醇作为溶剂加入离心管中,另外加入100 μL Nafion溶液充当粘结剂.为了使得催化剂样品与导电炭黑能够在溶剂中分散均匀,将离心管进行超声处理1 h,得到混合均匀的催化剂浆料悬浮液.吸取5 μL上述催化剂浆料滴在事先打磨抛光的玻碳电极(直径3 mm)的表面,等待乙醇和Nafion挥发殆尽,获得均匀的催化剂薄膜.
1.3 性能表征
使用Perkin-Elmer 580B光谱仪记录了400~4 000 cm-1波长范围内的红外(IR)光谱.用JEOL JSM-6700F场发射扫描电子显微镜(SEM)表征产物的微观形貌.场发射透射电子显微镜(TEM)、高分辨率TEM (HRTEM)图像是使用在200 kV下运行的FEI Tecnai G2 F20 s-twin D573 场发射TEM获得.在Bruker D8 Advance X射线衍射仪上收集粉末X射线衍射(XRD)谱图,在40 kV和40 mA下使用CuKα辐射.N2吸附-解吸等温线在-196 ℃下在Quantachrome NOVA 4200e上测量,样品在分析前在100 ℃下脱气至少4 h.使用Brunauer-Emmett-Teller(BET)方程和密度泛函理论模型(NLDFT)计算比表面积和孔径分布.
1.4 电化学性能测试方法
采用AMETEK VersaSTAT 3电化学工作站对催化剂材料的电化学性能进行测试,实验采用三电极体系进行测试,其中玻碳电极作为工作电极,Hg/HgO电极作为参比电极,碳棒作为对电极.实验采用1 mol/L的KOH溶液作为测试所使用的电解液.OER极化曲线扫描范围为0.306~1.306 V,扫描速率为5 mV/s.
2 结果与讨论
本实验通过配位协同自组装法将羧基配位的无机前体与两亲性表面活性剂组装在一起,制备出均匀的介孔结构.傅里叶变换红外光谱(FT-IR)验证了柠檬酸中的羧基与金属前驱体进行配位,如图1所示,未配位的羧基振动峰出现在1 711 cm-1和1 756 cm-1,而配位后的样品的羧基振动峰几乎消失,证明羧基与Ni原子进行了配位作用.在空气中350 ℃煅烧后,在504 cm-1处的吸收峰是Ni—O键的振动峰,证明最终形成了NiO材料.对煅烧后的样品进行结构表征,其XRD谱图如图2所示.在350 ℃下煅烧的样品显示出良好的特征衍射峰,为立方结构,所有衍射峰均与其标准数据(JCPDS No.47-1049)完全匹配,表明介孔NiO的结晶度良好.用Scherrer方程计算得知,介孔NiO纳米晶尺寸为9.55 nm.
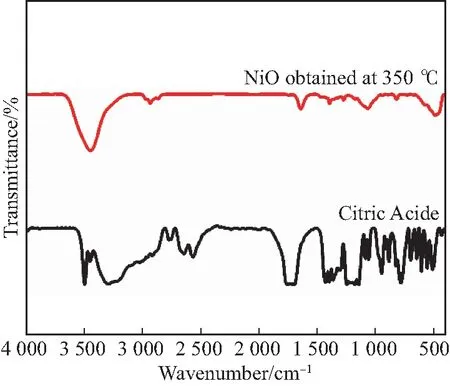
图1 柠檬酸和介孔氧化物NiO的傅里叶变换红外光谱图
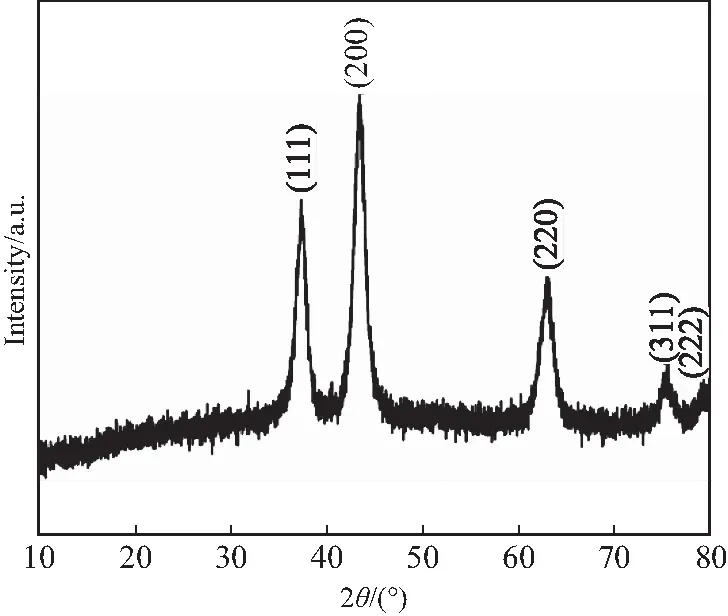
图2 介孔金属氧化物 NiO 煅烧后的XRD谱图
采用扫描电镜(SEM)研究了介孔NiO的孔结构和形貌.SEM图像表明,NiO的形貌为表面粗糙的不规则块体(图3(A)).利用透射电镜(TEM)表征了样品的形貌和微观结构.根据TEM图像可知形成的材料保持其无序的蠕虫状介孔结构,并且介孔孔壁由高度结晶的约为9.6 nm的NiO纳米晶体构成(这与Scherrer方程计算的结果相吻合),孔径约为3.5 nm(图3(B—C)).HRTEM图像可以清楚地观测到间距为0.209 nm宽的晶格条纹,对应于(200)晶面,进一步表明合成的样品结晶良好(图3(D)).

图3 介孔NiO的SEM图像(A)、TEM图像(B—C)和HRTEM图像(D)
采用氮气吸附-脱附分析研究了样品的孔结构.图4(A)表明样品的氮气吸附等温线具有典型的IV型曲线,说明样品具有丰富的介孔结构.在相对压力范围为0.3~0.7内有一个典型的H2型回滞环和明显的毛细管凝结现象,证明样品中存在均匀的介孔.通过密度泛函理论模型(NLDFT)计算得出孔径主要集中在3.5 nm(图4(B)).该样品的Brunauer-Emmett-Teller(BET)比表面积和孔体积分别为69 m2/g和0.055 cm3/g.
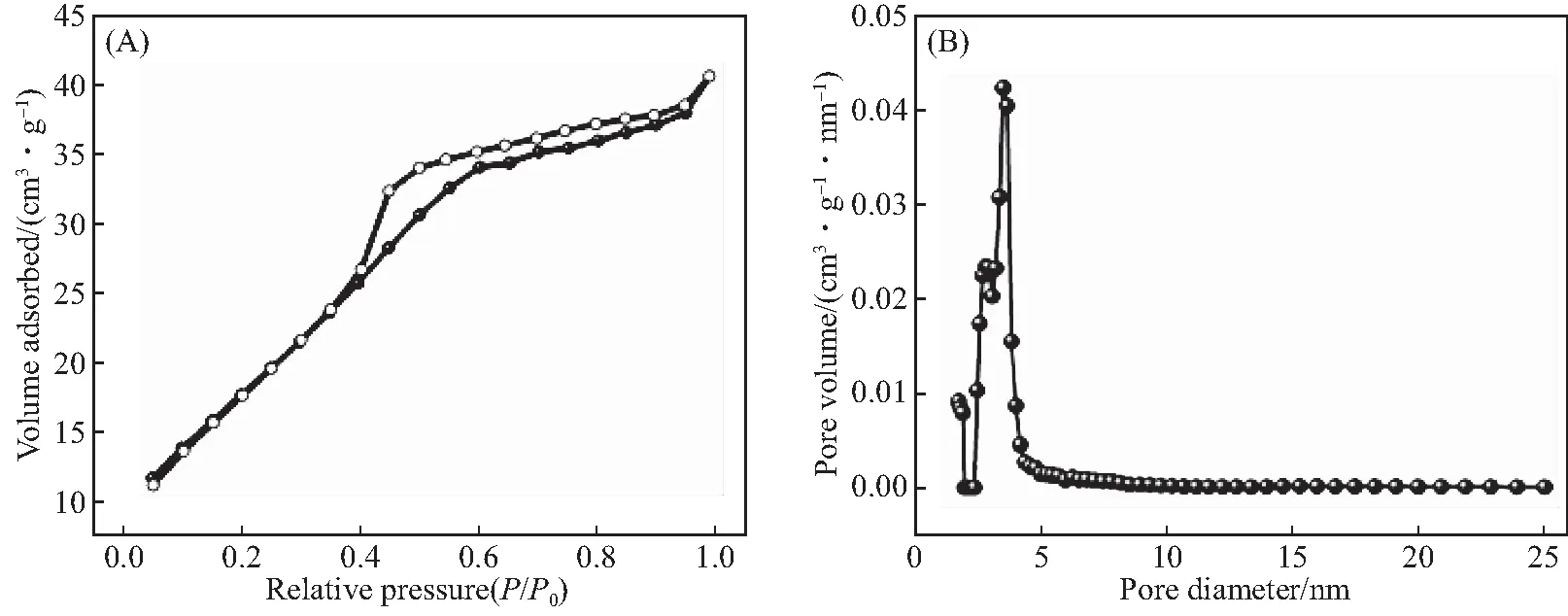
图4 介孔NiO 粉末的氮气吸附-脱附等温线(A)和孔尺寸分布曲线(B)
图5为介孔NiO及NiO+SDC复合材料在室温下氧气饱和的1 mol/L KOH电解液中的LSV曲线.从图5可以看出,介孔NiO和NiO+SDC复合材料的起始电位出现在~1.35 V左右.比较在10 mA/cm2的电流密度时的过电位是评价催化剂质量的一个重要指标,介孔NiO作为催化剂在10 mA/cm2的电流密度时的过电位为2.056 V,在复合了SDC材料以后,过电位降低到1.520 V.因此可以看出,在添加了SDC制成复合材料之后,具有最好的OER催化性能.

图5 介孔NiO及NiO+SDC复合材料的LSV极化曲线
为了进一步研究介孔NiO及其复合材料的OER性能,按照塔菲尔(Tafel)方程(1)得到塔菲尔曲线.
η=b·log(j/j0).
(1)
其中:η为过电位,j是电流密度,b是塔菲尔斜率,j0是交换电流密度.
图6为介孔NiO和NiO+SDC复合材料的Tafel曲线,从图中可以看出,介孔NiO和NiO+SDC复合材料的Tafel斜率分别为345.4 mV/dec和258.3 mV/dec.小的塔菲尔斜率表明NiO+SDC复合材料具有比介孔NiO更好的动力学性能.这可能是由于引入多孔的SDC材料增加了催化活性位点,使得OER催化活性得到了增强.
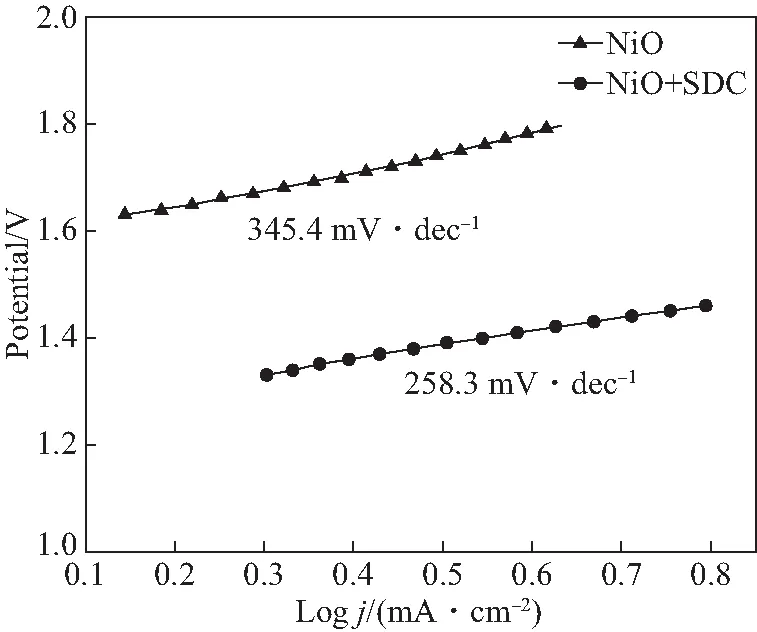
图6 介孔NiO和NiO+SDC复合材料的Tafel曲线Fig.6 Tafel curves of mesoporous NiO and NiO+SDC composites
为了探究介孔NiO和NiO+SDC复合材料在碱性环境中的析氢性能,在1 mol/L KOH电解液中进行电化学性能测试.扫描范围为-0.924~-1.924 V,扫描速度为5 mV/s.其LSV曲线如图7所示,在析氢反应中,电流密度为-10 mA/cm2时的过电位是评价一种材料催化性能的重要标准.从图中可以看出,介孔NiO的过电位为858.4 mV,NiO+SDC复合材料的过电位为871.0 mV.可见两者的析氢性能相差不大,同时,介孔NiO和NiO+SDC复合材料的Tafel曲线如图8所示,介孔NiO的Tafel斜率为319.9 mV/dec,NiO+SDC复合材料的Tafel斜率为495.7 mV/dec.因此,介孔NiO和NiO+SDC复合材料的析氢反应性能较差.
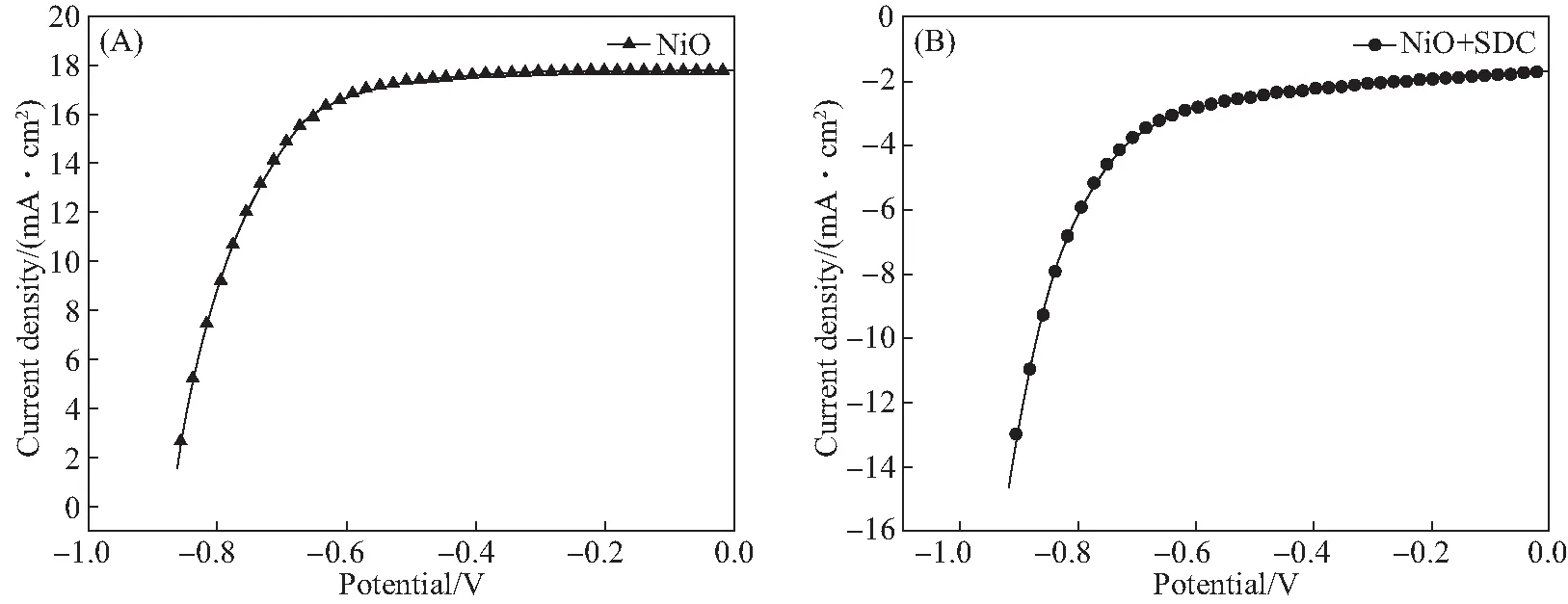
图7 介孔NiO及NiO+SDC复合材料的LSV极化曲线

图8 介孔NiO和NiO+SDC复合材料的Tafel曲线
3 结论
通过配位协同自组装法,采用柠檬酸作为螯合剂、正丁醇作为溶剂、金属硝酸盐和三嵌段共聚物 Pluronic P123分别用作前体和模板、浓HNO3调节pH合成了介孔金属氧化物材料,所得的介孔NiO为结晶度良好的立方结构,具有高的比表面积和大的孔体积,因此为反应提供了更多的活性位点,使其成为优秀的电化学材料.合成的NiO+SDC复合材料在10 mA/cm2的电流密度时过电位为1.520 V,是良好的OER催化性能材料.
