银/金纳米线阵列表面增强拉曼基底的制备及对孔雀石绿的高灵敏度检测
2022-05-25夏大成蔡志伟姬晓旭任小明何云斌
夏大成,周 瑞,涂 博,蔡志伟,高 难,姬晓旭,常 钢,任小明,何云斌
(1.功能材料绿色制备与应用教育部重点实验室,高分子材料湖北省重点实验室,湖北大学材料科学与工程学院,武汉430062;2.南阳师范学院物理与电子工程学院,南阳473000)
孔雀石绿(MG)是一种三苯基甲烷类染料,通常被用于丝绸和造纸工业,也可作为抗寄生虫剂和生物杀菌剂用于水产养殖业[1].MG被人或动物吸收后,易被代谢成为具有致癌性、致畸性和诱变性的无色孔雀石绿(LMG)[2,3],因此许多国家禁止在水产养殖业中使用MG.尽管如此,由于其低廉的价格及对真菌和寄生虫的良好抗性[4],至今仍然存在非法使用MG的现象.因此,MG的检测对环境监测和人类健康具有重要意义.
近年来,高效液相色谱[5]、液相色谱-质谱[6]、荧光传感器[7]和毛细管电泳[8]等技术被应用于MG的检测,但这些技术通常需要较长的样品制备时间、液体检测环境和昂贵的设备.SERS作为一种快速、高灵敏度、无损且低成本的技术,近年来受到了广泛的关注[9,10],众多的SERS基底被应用于MG检测,如银纳米枝晶[11]、氧化石墨烯/金纳米颗粒复合材料[12]、金纳米棒[13]和银纳米颗粒/MoS2复合材料[14]等.已报道的关于SERS检测多采用合成SERS基底,以获得对MG表面拉曼信号增强的效果,但如何制备具有良好重现性、稳定性和可回收性的新型SERS基底仍然是一个挑战.
拉曼“热点”是拉曼信号能够得到大幅度增强的区域,通常出现在纳米尺度的尖锐边缘或紧密堆积的等离子体纳米结构之间的小间隙处.规则排列的阵列状金或银纳米材料产生的电磁场耦合作用可以带来大量的拉曼“热点”,从而大幅度提高拉曼信号强度,因而成为当前SERS研究的热点之一[15~20].有序的二维结构比无序结构具有更优越的光、电、磁性能.大面积均匀排列的纳米结构可以带来更好的信号稳定性,而纳米线阵列具有较高的比表面积,在SERS应用中,纳米线阵列可以为待测物提供更多的吸附位点,提高SERS基底的灵敏度[21].目前,已经有较多技术被用于制备具有规则阵列结构的贵金属纳米材料,如多孔阳极氧化铝(AAO)模板法[22]、物理气相沉积法[23]和自组装法[24],但这些方法成本高且操作难度大,难以投入大规模实际应用.因此,迫切需要开发一种简单有效的方法制备规则排列的金或银纳米阵列SERS基底.
在银/金纳米材料中,金具有较好的化学稳定性,而银具有更高的电磁场增强性能.但银的活泼性较强,在银纳米材料制备的过程中很难保证其形貌的均一性,小尺寸银纳米颗粒也非常容易在合成过程中发生团聚,从而影响后期应用效果[25].虽然金的电磁场增强性能不及银,但金纳米材料的形貌可控性较强,性质更加稳定.因此,在提高金基纳米材料的SERS性能的过程中通常需要在金的支撑材料上引入银元素.在对MG的SERS检测中,受测试环境的影响可能导致银纳米材料的结构发生变化,使得SERS性能下降,而金基纳米材料可以很好地保持形貌稳定性,从而保证检测效果[26].
本文使用两步湿化学方法,在玻璃基底上制备了垂直Ag/Au NWs阵列作为SERS基底.首先以种子介导的软模板法制备Au NWs阵列,并通过改变反应温度来调控Au NWs阵列的形貌和结构;然后使用抗坏血酸还原硝酸银的方法在Au NWs阵列上沉积Ag NPs以制备Ag/Au NWs阵列.以R6G作为拉曼探针分子进行了SERS性能检测,探究了Ag NPs沉积状态以及Ag/Au NWs阵列的形貌与SERS性能的关系.分别对单个基底上的15个随机点的SERS信号进行了比较,使用同一个基底进行了18 d的信号重复稳定性测试,以确定SERS基底的信号均匀性和时间稳定性.对实际样品的测试结果表明,Ag/Au NWs阵列基底可应用于高灵敏环境水体中MG的检测.
1 实验部分
1.1 试剂与仪器
HAuCl4·3H2O、3-氨基丙基三乙氧基硅烷(APTES)和4-巯基苯甲酸(4-MBA)(上海阿拉丁生化科技股份有限公司);L-抗坏血酸(L-AA)、硼氢化钠(NaBH4)、硝酸银(AgNO3)和孔雀石绿(国药集团化学试剂有限公司);所用试剂均为分析纯;实验用水为超纯水(电阻率>18.2 MΩ·cm).
SIGMA 500型场发射扫描电子显微镜(SEM,德国蔡司公司);LabRAM HR Evolution拉曼光谱仪(日本堀场公司);P60-CY超纯水净化系统(湖南科尔顿水务有限公司);TECNAI G2 20 S-TWIN型透射电子显微镜(TEM,美国FEI公司);Thermo scientific ESCAlab 250xi型X射线光电子能谱(XPS,美国Thermo公司).
1.2 金纳米颗粒的制备
在用王水清洗过的250 mL锥形瓶中注入99.8 mL水,在剧烈搅拌下将HAuCl4(294μL,0.1 mol/L)注入到锥形瓶中加热至沸腾.将2.7 mL质量分数为1%的柠檬酸三钠水溶液快速注入沸腾的HAuCl4溶液中,煮沸10 min后,溶液颜色由无色变为深蓝色,再变为酒红色[27,28],说明金纳米颗粒制备成功.在搅拌下冷却至室温后,将含有金纳米颗粒(Au NPs)的溶液在4℃下储存在棕色试剂瓶中.
1.3 Ag/Au NWs阵列的制备与清洗
图1示出了Ag/Au NWs阵列的制备过程.为了在玻璃片上制备Au NWs阵列,将1 cm×1 cm玻璃片分别用去离子水和乙醇超声清洗15 min后,用N2气干燥.将玻璃片用O2等离子体预处理5 min以提高其表面亲水性,然后与APTES溶液(5 mmol/L)反应4 h,将玻璃片氨基官能化.将氨基官能化的玻璃片浸入Au NPs溶液中浸泡5 h,使金纳米颗粒充分吸附在玻璃片上,用水和乙醇冲洗吸附了Au NPs的玻璃片以去除未吸附牢固的Au NPs.将吸附Au NPs的玻璃片浸入含有HAuCl4(1.7 mmol/L)、4-MBA(550 μmol/L)和L-抗坏血酸(4.1 mmol/L)的恒温生长溶液中15 min,以制备Au NWs阵列,接着用乙醇冲洗带有Au NWs阵列的玻璃片并在空气中干燥,备用.冰水浴下将制备好的Au NWs阵列浸入25 mmol/L NaBH4溶液中10 min,以去除吸附在Au NWs阵列表面的4-MBA.最后,将清洗过的Au NWs阵列浸入含有AgNO3(0.05 mmol/L)和L-AA(10 mmol/L)的反应溶液中,室温下反应15 min.反应结束后,用去离子水清洗样品,室温干燥待用,产物记为Ag/Au NWs阵列.将吸附Au NPs的玻璃片浸入上述相同的反应溶液中制备Ag/Au NPs作为对照实验.
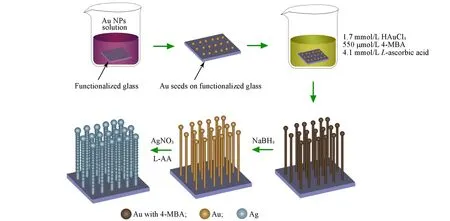
Fig.1 Schematic illustration of the preparation of the Ag/Au NWs array
1.4 SERS性能测试
在SERS测试实验中,将制备好的SERS基底浸入5 mL R6G或MG溶液中30 min,用乙醇冲洗3次以去除游离分子,然后在室温下干燥.在增强因子(EF)的计算中,选用R6G作为探针分子,将10μL 1×10−4mol/L的R6G溶液均匀滴涂在基板上并在室温下干燥.以633 nm激光为激发源,激光在基底上的光斑直径为1.4μm.用数值孔径(NA)为0.55的50×倍物镜测量拉曼光谱,激光功率为4.25 mW,积分次数、采集时间和曝光时间分别为5 s,5 s和1 s.
2 结果与讨论
2.1 Ag/Au NWs阵列的表征
Au NPs最初作为“种子”被锚定在玻璃片上,强配体4-MBA可以结合在这些金种子表面以抑制金原子的沉积,使得金原子只能沉积在Au NPs和玻璃片之间的位点,4-MBA不能与这些位点有效结合;新沉积的金原子立即被配体覆盖,而金种子面向玻璃片的底部会保持无配体结合并为下一轮沉积保持活性,当金的还原速率与4-MBA的吸附速率达到动态平衡时,金纳米晶体就可以生长成为线状[29~32].
Au NWs阵列制备完成后,阵列表面会留下一层4-MBA,其具有较强的拉曼响应,且4-MBA层也会影响其它分子的吸附[33],因此必须去除Au NWs阵列表面的4-MBA层.然而,4-MBA是通过Au—S键化学吸附在Au NWs阵列的表面[34],除非使用特殊的物理或化学方法,否则无法断裂Au—S键.实验中使用NaBH4断开Au—S键以去除Au NWs阵列表面的4-MBA层.由图2(A)和(B)可见,在NaBH4洗涤前后,Au NWs阵列的微观形貌没有发生明显变化.对洗涤前后的Au NWs阵列进行拉曼光谱测试,由图2(C)可见,在经过NaBH4洗涤后,1075和1583cm−1处的拉曼峰消失,表明4-MBA分子已从Au NWs阵列的表面去除.
2.1.1 Au NWs阵列与Ag/Au NW阵列的微观形貌 银在激光照射下可增强表面电磁场,从而表现出优越的拉曼增强效果.银修饰的有序纳米结构常被用作SERS基底,且表现出了优异的SERS性能[35,36].本文将Au NWs阵列用作Ag NPs化学沉积的支撑基底,通过在Au NWs阵列上修饰一层Ag NPs以提高SERS基底的信号增强能力.图3(A)和(B)及其中插图分别为Au NWs阵列和Ag/Au NWs阵列的SEM照片,通过对比可见Au NWs阵列表面沉积一层Ag NPs后,纳米线的直径略有增加且表面粗糙度提高,Ag/Au NWs阵列很好地保留了纳米线阵列的原始微观形貌与结构[图3(E)].从图3(C)中Ag/Au NWs阵列的TEM照片可以看出,Ag NPs均匀地地分布在丛状的Au NWs上.这种具有大比表面积的森林状结构可以带来更多的吸附位点,密集的纳米线阵列结构也可产生更多的拉曼“热点”.图3(D)插图中的EDS分析结果表明,银元素均匀分布在Au NWs阵列上.分别使用Au NWs阵列和Ag/Au NWs阵列对探针分子R6G进行检测,结果如图3(E)所示.可以发现,由于Ag NPs的修饰,Ag/Au NWs阵列上的R6G的SERS信号远高于Au NWs阵列上的SERS信号,说明Ag/Au NWs阵列的拉曼信号增强的能力优于Au NWs阵列.
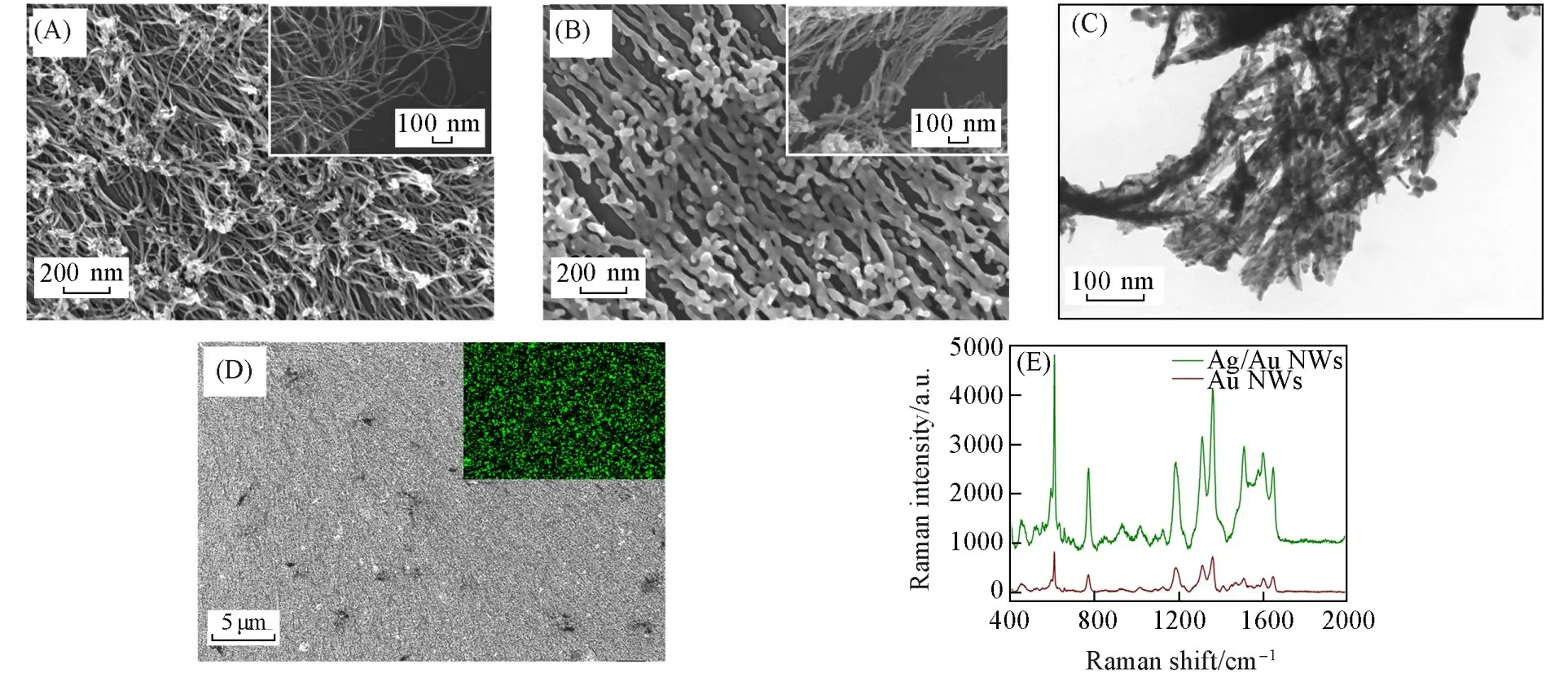
Fig.3 SEM images of Au NWs array(A)and Ag/Au NWs array(B),TEM image of Ag/Au NWs array(C),SEM image of Ag/Au NWs array and EDS mapping(inset)of silver on Ag/Au NWs array(D)and SERS spectra of 1×10−4 mol/L R6G on Au NWs array and Ag/Au NWs array(E)
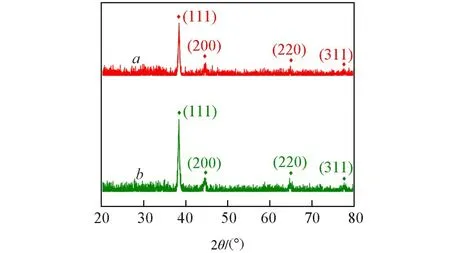
Fig.4 XRD patterns of Au NWs array(a)and Ag/Au NWs array(b)
2.1.2 Au NWs阵列与Ag/Au NWs阵列的晶体结构 制备的Au NWs阵列与Ag/Au NW阵列的XRD谱图如图4所示,在2θ=38.4°,44.5°,64.9°和77.8°处可观察到特征衍射峰,分别与Au(JCPDS#04-0784)或Ag(JCPDS#04-0783)的(111),(200),(220)和(311)晶面衍射峰对应.Au与Ag都是面心立方结构且晶格参数相近,因此Au NWs阵列与Ag/Au NWs阵列的晶面衍射峰峰位也非常相近[37].
2.1.3 Au NWs阵列与Ag/Au NWs阵列的XPS表征
分别测定了Au NWs阵列与Ag/Au NWs阵列的XPS谱.如图5(A)所示,Au NWs阵列与Ag/Au NWs阵列都存在Au与O两种元素,在Ag/Au NWs阵列中检测到Ag元素,来源于化学沉积的Ag NPs.图5(B)~(D)所示高分辨率XPS窄谱中的峰位归属均与拟合曲线一致.Au NWs阵列与Ag/Au NWs阵列中Au元素的核心电子能级为83.9和87.8 eV,分别归属于Au4f7/2和Au4f5/2[图5(B)和(C)].Ag/Au NWs阵列中Ag元素的核心电子能级为374.5和367.2 eV,分别归属于Ag3d3/2和Ag3d5/2[图5(D)][38].结果表明,Au NWs阵列中的Au元素以及Ag/Au NWs阵列中的Ag元素和Au元素均为单质;证实在Au NWs阵列上化学沉积了单质Ag NPs,制备出了Ag/Au NWs阵列.
基底的纳米结构是影响SERS增强性能的另一个关键因素.实验中研究了Ag/Au NWs阵列的形貌演变,这些样品是分别用在不同温度(25,45和65℃)下生长的Au NWs阵列作为支撑模板而制备的.在不同温度下生长的Au NWs阵列的形貌如图6所示.结果表明,温度对Au NWs阵列的形貌有一定影响,相同的反应时间下,Au NWs的长度和直径随着反应温度的升高而增加,说明可以通过改变生长温度来调控Au NWs阵列的形貌.使用不同温度下生长的Au NWs阵列作为支撑基底用于Ag NPs沉积的同时,作为对照实验,Au NPs也被用作Ag NPs沉积的支撑基底.如图7(A)所示,平均直径为15 nm的Ag/Au NPs均匀地固定在玻璃基板的表面上.图7(B)~(D)展示了使用在不同生长温度下(25,45和65℃)制备的Au NWs阵列为支撑模板制备的Ag/Au NWs阵列.当生长温度为25℃时,Ag/Au NWs的长度较短且稀疏地分布在玻璃基板上;当生长温度升至45℃时,由于Au NWs的生长速度相对较快,Ag/Au NWs的长度明显得到增加,且在较大面积上表现出规则的阵列结构;当温度升高至65℃,Au NWs的过快生长速度使阵列结构变得更加密集,同时纳米线也出现了部分倒塌,失去了规则排列的阵列结构.
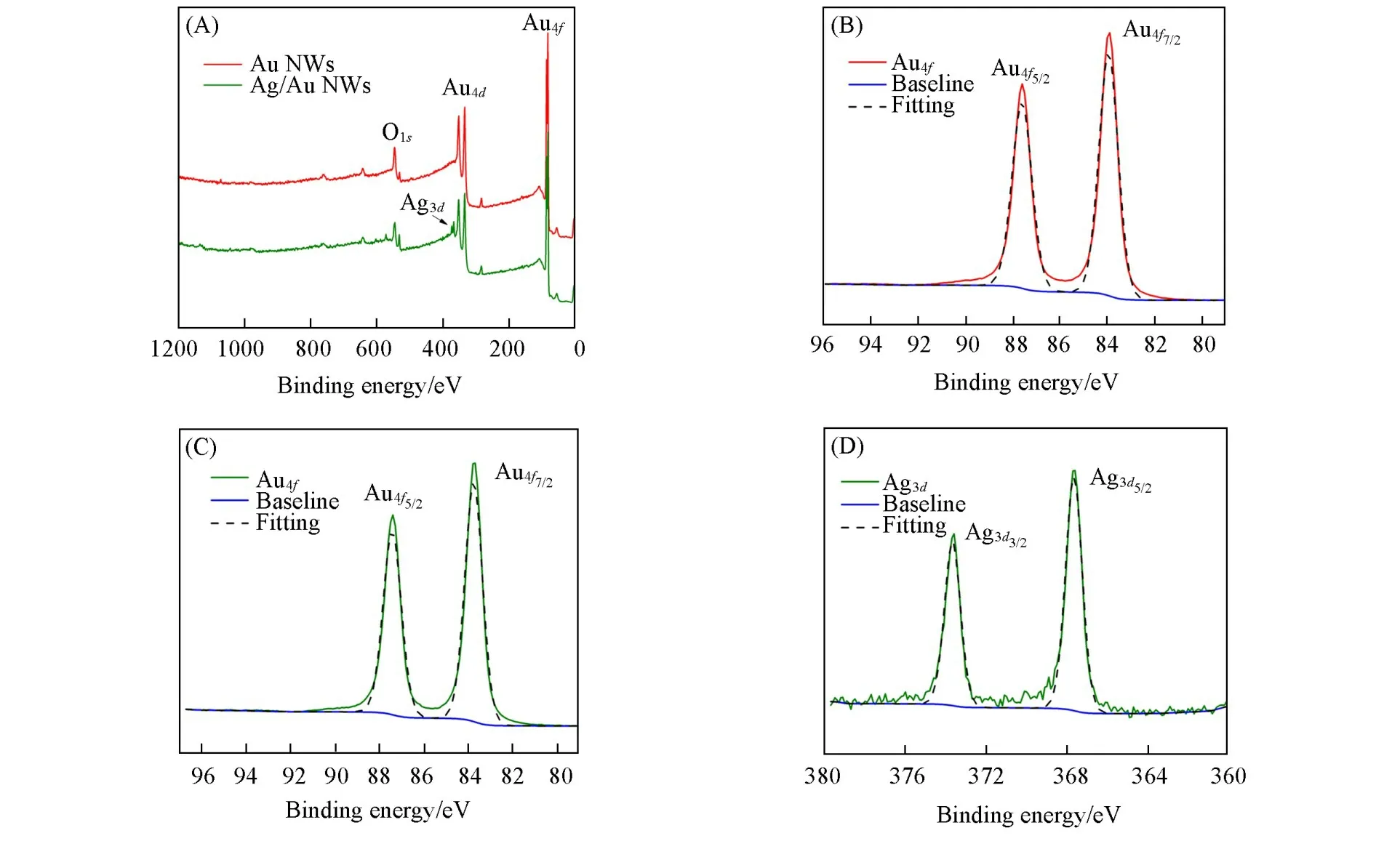
Fig.5 Survey⁃scan XPS spectra of Au NWs array and Ag/Au NWs array(A),high⁃resolution spectra for Au4f of Au NWs array(B),Au4f of Ag/Au NWs array(C)and Ag3d of Ag/Au NWs array(D)

Fig.6 SEM images of Au NWs array prepared at 25°C(A),45°C(B)and 65°C(C)
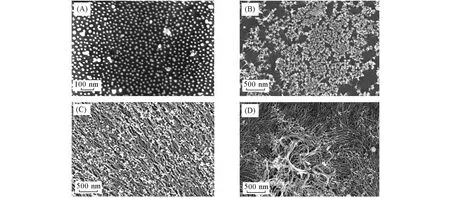
Fig.7 SEM images of Ag/Au NPs(A)and Ag/Au NWs array prepared with Au NWs array as templates at 25°C(B),45°C(C)and 65°C(D)
2.2 Ag/Au NWs阵列的SERS性能
为了探究Ag NPs的沉积状态对SERS基底性能的影响,对化学沉积时使用的AgNO3浓度进行了优化.在进行化学沉积Ag NPs时,AgNO3浓度分别设定为0.025,0.05,0.15和0.3 mmol/L.结果如图8所示,当AgNO3浓度为0.15和0.3 mmol/L时,Ag/Au NWs阵列表面有较大的Ag NPs生成[图8(C)和(D)];当AgNO3浓度低至0.05 mmol/L时,Ag/Au NWs阵列表面无较大的Ag NPs生成[图8(B)].为避免大的Ag NPs对SERS基底的信号均匀性产生影响,在测试前将制备的SERS基底用去离子水反复冲洗以去除附着在Ag/Au NWs阵列表面的大Ag NPs,使用清洗后的SERS基底对探针分子R6G(1×10−4mol/L)进行SERS检测,结果见图8(E);从不同SERS基底上选取5个随机点收集的610.3 cm−1峰的平均SERS强度见图8(F).当AgNO3浓度为0.05,0.15和0.3 mmol/L时,SERS基底的性能并无明显变化,当浓度低至0.025 mmol/L时,银的沉积量不足导致SERS信号强度显著下降,因此沉积Ag NPs时设定AgNO3浓度为0.05 mmol/L.
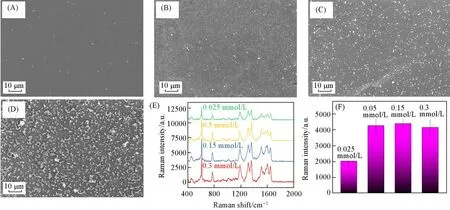
Fig.8 SEM images of Ag/Au NWs array prepared with AgNO 3 concentration of 0.025 mmol/L(A),0.05 mmol/L(B),0.15 mmol/L(C)and 0.3 mmol/L(D),SERS spectra of 1×10-4 mol/L R6G on Ag/Au NWs array prepared with different concentrations of AgNO3(E)and comparison of average Raman intensi⁃ty of the peak at 610.3 cm−1 on Ag/Au NWs array prepared with different concentrations of AgNO 3(F)
使用Au NPs、不同温度下生长的Au NWs阵列、Ag/Au NPs以及不同温度下生长的Au NWs阵列为支撑基底制备的Ag/Au NWs阵列作为SERS基底,以R6G作为探针分子进行SERS检测,收集了SERS基底上1×10−4mol/L R6G的SERS光谱[图9(A)和(C)],从不同SERS基底上选取5个随机点收集的610.3 cm−1峰的平均SERS强度[图9(B)和(D)].将在25℃下生长的Au NWs阵列表示为Au NWs/25℃,使用Au NWs/25℃为支撑基底制备的Ag/Au NWs阵列表示为Ag/Au NWs/25℃,在其它温度下制备的样品也用相同方式表示.对比9(A)和(C)及图9(B)和(D),经过Ag NPs修饰的Au纳米结构的SERS性能比未修饰前有较大提升.如图9(C)所示,Ag/Au NWs的信号增强性能比Ag/Au NPs更加优秀,这是由于相比于Ag/Au NWs,Ag/Au NPs的分布更加稀疏,相对比表面积更小,无法提供较多的拉曼“热点”及更大的有效吸附面积;在纳米线结构的性能比较中,由于Ag/Au NWs/25℃的纳米结构分布稀疏,不利于拉曼“热点”的形成,导致SERS活性较低;Ag/Au NWs/65℃紧密堆积的纳米线结构会造成电磁场耦合作用减弱,导致基底的SERS活性下降,过于密集密且倒塌的纳米线阵列结构会导致拉曼探针分子的有效吸附面积不足.相比之下,Ag/Au NWs/45℃拥有最佳的SERS性能,其规则排列的结构具有较大比表面积可供待测分子吸附,纳米线之间的适当间距也可提供更多的拉曼“热点”,为SERS基底提供了更高的灵敏度.因此,在后续实验中采用Ag/Au NWs/45℃作为SERS基底材料.
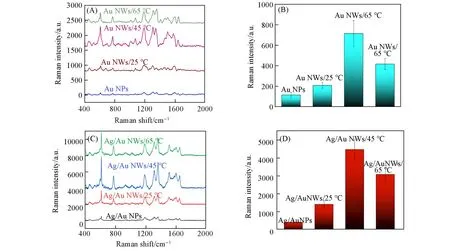
Fig.9 SERS spectra of 1×10-4 mol/L R6G on Au NPs and Au NWs array grown at different temperatures(A),comparison of average Raman intensity of the peak at 610.3 cm−1 on Au NPs and Au NWs array(B),SERS spectra of 1×10-4 mol/L R6G on Ag/Au NPs and Ag/Au NWs array prepared with Au NWs array grown at different temperatures(C)and comparison of average Raman intensity of the peak at 610.3 cm−1 on Ag/Au NPs and Ag/Au NWs array(D)
为了定量表征这种SERS基底的信号增强能力,可根据下述公式计算EF值[39]:

式中:ISERS和IBULK分别代表SERS基底上R6G分子在610.3 cm−1处的SERS峰强度和R6G晶体在610.3 cm−1拉曼峰强度;NBULK和NSERS分别是激光光斑内晶体中和SERS基底上R6G的分子数量.NBULK通过结合入射到晶体上的激光光斑的聚焦体积和R6G晶体的密度来计算,NSERS通过假设一定量溶液中的分子均匀分布在基底上,然后计算激光光斑面积下的分子获得,NBULK/NSERS可通过下面公式计算:
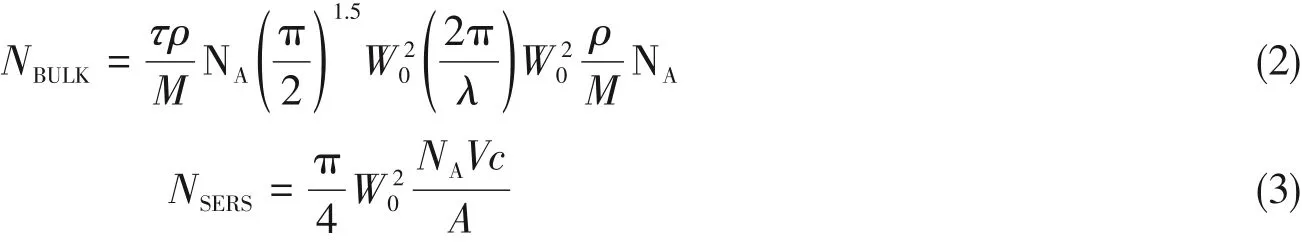
式中:激光光斑直径W0=1.22λ/NA,聚焦深度Z0=(2π/λ)W02,聚焦体积τ=(π/2)1.5W02Z0,基底面积A=1 cm2,R6G密度ρ=1.28 g/cm3,溶液体积V=10μL,溶液浓度c=1×10−4mol/L,经过换算可得到下式:
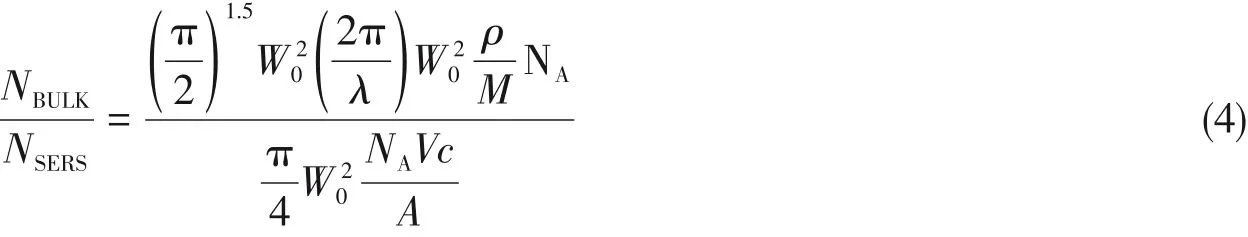
通过式(4)计算得到NBULK/NSERS=1.59×104.经过测试,ISERS和IBULK分别为4415.26和86.22.最终计算得到的EF值为8.1×105.由上述步骤计算所得Ag/Au NPs,Ag/Au NWs/25℃和Ag/Au NWs/65℃的EF值分别为9.6×104,2.7×105和5.6×105.由此得知,Ag/Au NWs/45℃拥有最好的SERS活性.
2.3 Ag/Au NWs阵列的信号均匀性和时间稳定性
为了探索Ag/Au NWs/45℃阵列的信号均匀性,从Ag/Au NWs/45℃阵列上随机选择15个点收集了1×10−4mol/L R6G的SERS光谱,结果如图10(A)所示.这15个SERS信号的强度表现出良好的重现性,610.3 cm−1峰强度的相对标准偏差(RSD)为9.24%,说明Ag/Au NWs阵列的信号均均匀性良好.除了信号均匀性之外,SERS传感器的时间稳定性对其能否投入实际应用也很重要.将SERS基底储存在4℃的乙醇中,每隔3 d对1×10−4mol/L R6G进行检测,在SERS基底上选取5个随机点收集SERS信号.由图10(B)可看出,1×10−4mol/L R6G的610.3 cm−1峰的SERS信号在18 d后仍保持在初始强度的80%,证实了Ag/Au NWs/45℃具有优异的稳定性.
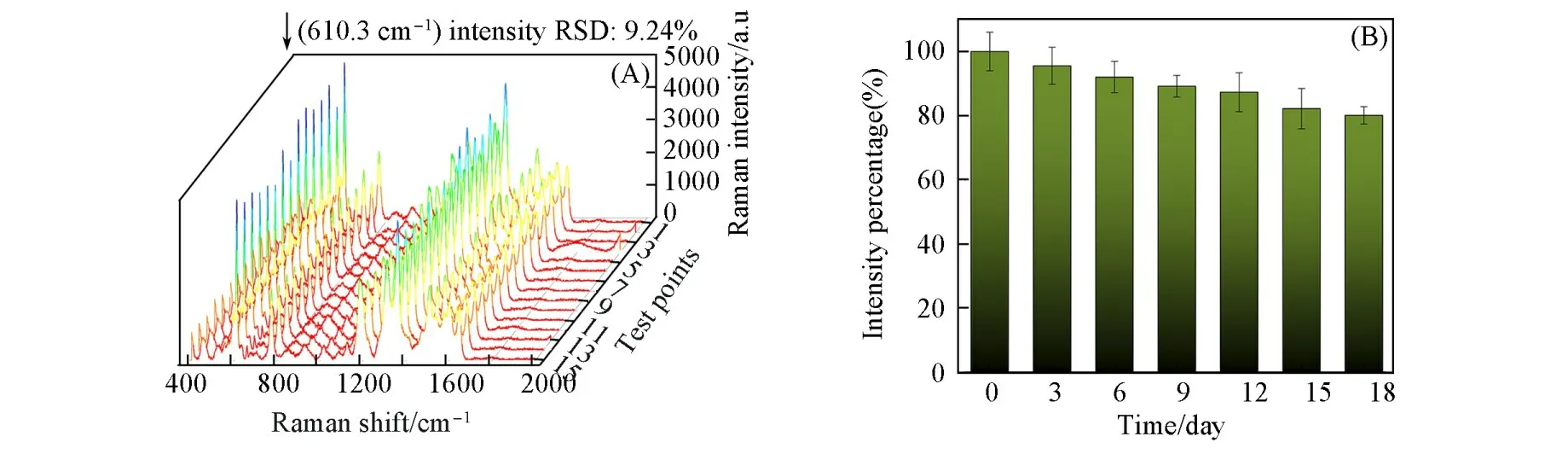
Fig.10 SERS spectra of 1×10-4 mol/L R6G from 15 random points(A)and Raman intensity change of R6G(1×10-4 mol/L)at 610.3 cm-1 on Ag/Au NWs array in 18 d(B)
2.4 对水溶液中MG的SERS检测
为了考察Ag/Au NWs/45℃用于检测水溶液中MG的可行性,使用新制的SERS基底对不同浓度的MG溶液(1×10−8~1×10−4mol/L)进行了测试,得到的SERS光谱如图11(A)所示.在MG的SERS光谱中,各主要峰位归属如下:436 cm−1处的峰由平面外苯基-C-苯基振动引起;526和916 cm−1处的峰归因于芳环的振动;794 cm−1处的峰归因于平面外环上C—H振动;1174 cm−1处的峰由面内环上C—H弯曲振动引起;1367和1616 cm−1处的峰则分别对应N—苯基伸缩振动和环上C—C伸缩振动.为了识别SERS光谱上1×10−8mol/L的特征峰,将图中信号放大了5倍,可见,在信噪比为3的情况下,对MG的检出限可低至1×10−8mol/L.SERS信号的强度随着MG浓度的增加而逐渐增大,为了探究SERS峰强度与浓度之间的关系,在图11(B)中建立了1174 cm−1处SERS峰强度与浓度对数的线性校准曲线,可见1×10−8~1×10−4mol/L的浓度对数与SERS信号强度呈现良好的线性相关性,且具有较高的线性相关度(R2=0.989),线性回归方程为I1174cm−1=31402.3+3900.9lgc.

Fig.11 SERS spectra of MG solution with different concentrations of 10-8—10-4 mol/L detected on Ag/Au NWs array(A)and linear correlation of Raman intensity at 1174 cm−1 vs.the logarithm of MG con⁃centration(B)
为探索Ag/Au NWs/45℃在实际样品测试中的性能,以当地湖水为溶剂制备MG溶液并进行检测,由每个SERS基底上选取25个随机点的1174 cm−1峰强度计算RSD值,结果见表1.检测湖水中的MG得到的回收率分别为114%和97.7%,信号的RSD<10%.所得结果表明,Ag/Au NWs/45℃在环境安全检测方面具有巨大应用潜力.

Table 1 Results for detection of MG in real samples(n=3)
NaBH4是一种有效且低成本的清洁剂,可以有效去除贵金属纳米材料上的吸附分子[40],从而回收SERS基底.因此,实验中研究了这种SERS基材的可回收性.如图12所示,首先使用新制的Ag/Au NWs/45℃基底用于检测1×10−4mol/L MG,然后用NaBH4溶液处理该使用过的SERS基底,并再次将其用于检测1×10−4mol/L MG.可见,经NaBH4处理后仅保留有基础噪音,表明Ag/Au NWs/45℃阵列上MG分子被洗去.在光谱图中可以发现,第一次和第二次对1×10−4mol/L MG进行SERS测试得到信号的强度并未发生变化,且在Ag/Au NWs阵列收集的MG的SERS信号强度几乎相同,表明Ag/Au NWs/45℃具有较好的可回收重复使用性.
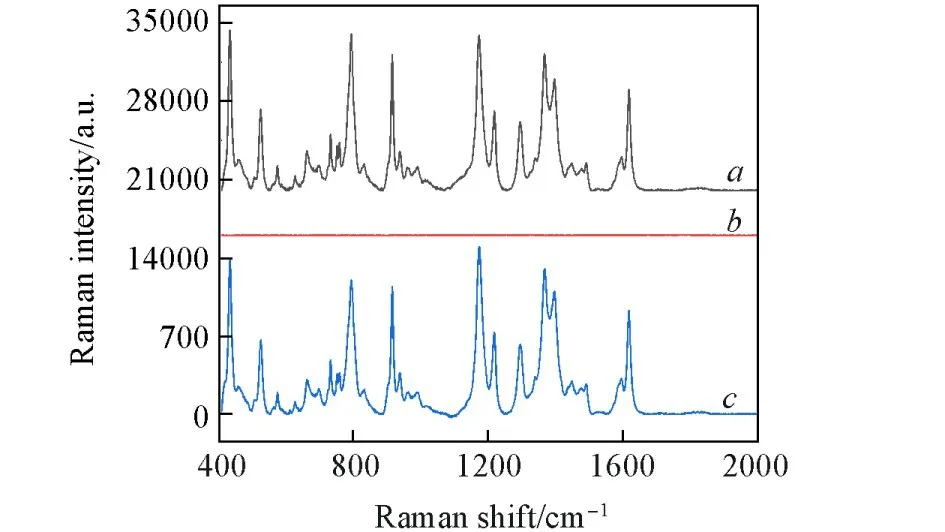
Fig.12 SERS spectra of 1×10-4 mol/L MG on new⁃ly prepared Ag/Au NWs array(a),used Ag/Au NWs array treated with NaBH 4(b)and second test for 1×10-4 mol/L MG on Ag/Au NWs array treated with NaBH 4(c)
3 结 论
发展了一种在玻璃片表面制备具有规则阵列结构的Ag/Au NWs的简便方法,并将其用于对水中MG的高灵敏度SERS检测.通过种子介导的软模板法在玻璃基底上制备了垂直生长的Au NWs阵列,在Au NWs阵列上化学沉积Ag NPs制备Ag/Au NWs阵列作为SERS基底.通过调节生长温度可改变Au NWs阵列的形貌,以调控Ag/Au NWs阵列的形貌,进而调控基底的SERS性能;发现在以45℃下生长的Au NWs阵列为支撑基底制备的Ag/Au NWs/45℃具有最优的SERS性能,该SERS基底具有高EF值(8.1×105)的同时也表现出优异的信号均匀性和时间稳定性,对MG具有优异的检测性能,检出限低至1×10−8mol/L,检测的线性范围为1×10−8~1×10−4mol/L.Ag/Au NWs/45℃经过NaBH4处理后表现出良好的可重复利用性.在实际应用中,用Ag/Au NWs/45℃检测环境水质中的MG分子,获得了良好的回收率.基于上述优点,Ag/Au NWs有序阵列基底在SERS传感领域将拥有广阔的应用前景.
