地枇杷的化学成分及抗氧化活性研究
2022-05-25何芷芸石松云魏雪娇刘呈雄陈剑锋
何芷芸,石松云,魏雪娇,刘呈雄,陈剑锋,邹 坤,程 凡
三峡大学生物与制药学院 天然产物研究与利用湖北省重点实验室,宜昌 443002
地枇杷药材系桑科榕属植物地果FicustikouaBur.的干燥地上部分[4],其植物名又称地瓜藤、地石榴等,且因其匍匐木质藤本,茎贴地生长又称之为地板藤,全株有白色乳液。在我国广泛分布于湖北、云南、贵州、广西、四川、西藏等地[1],地枇杷是彝族、壮族、苗族、哈尼族等少数民族广泛使用的民族药,在贵州作为苗族习用药材,在云南则为彝族、哈尼族等少数民族的常用药,有着悠久的药用历史,是独具特色的地方中草药。该药材最初记录于明初兰茂所著的《滇南本草》(1977年)[2],《全国中草药汇编》记载其功能主治为清热、利湿、活血、解毒[3]。在本课题组参与编撰的2018版《湖北省中药材质量标准》[4]中,详细记载了地枇杷性状及鉴别方法,同时也记载了其清热解毒、清肺止咳、润燥止泻的功能。
根据国内外文献记载,地枇杷化学成分主要有黄酮、甾体、香豆素、三萜类等成分[5],对于该药材的现代药理学研究较少,主要集中在抑菌、对酪氨酸酶活性的影响,此外,Yang等[6]采用DPPH法对地枇杷提取物及不同溶剂萃取部位进行了抗氧化活性测定,发现其乙酸乙酯萃取部位及正丁醇萃取部位均具有良好的DPPH自由基清除能力,本课题在此基础上,综合DPPH自由基清除能力、总抗氧化能力测定,超氧阴离子清除能力这三种抗氧化活性评价方法,对从该药材中分离得到的化合物进行抗氧化活性评价,期望为天然抗氧化剂的开发提供一定参考价值。
1 材料与方法
1.1 仪器与试剂
BrukerAV400型核磁共振波谱仪(瑞士布鲁克公司);Dionex Ultimate 3000型高效液相色谱仪(美国戴安公司);Waters UPLC-MS(QDa)超高效液相串联质谱仪(美国Waters公司);Venusil XBP C18色谱柱(半制备型:250 mm×10 mm,10 μm;分析型:250 mm×4.6 mm,5 μm,天津博纳艾杰尔科技有限公司);Waters 1525 EF高效液相色谱仪(美国Waters公司);低温冷冻干燥机(美国Labconco公司);TECAN infinite F200PRO酶标仪(瑞士帝肯公司);Smart-S15UVF超纯水仪(上海和泰仪器有限公司);UV-1000型紫外可见分光光度计(上海翱艺仪器有限公司);电子天平(上海民桥精密仪器有限公司);AB-8大孔吸附树脂(东鸿化工有限公司);正相色谱硅胶(烟台化学工业研究所);反相色谱硅胶(日本YMC公司);DPPH(上海源叶生物科技有限公司);T-AOC试剂盒(南京建成生物工程研究所);抗坏血酸(上海阿拉丁生化科技股份有限公司);邻苯三酚(上海麦克林生化科技有限公司);PBS(上海麦克林生化科技有限公司);高效液相用乙腈、甲醇均为色谱纯(美国Tedia公司);水为超纯水;其他试剂均为分析纯(国药集团化学试剂有限公司)。
1.2 植物材料
植物材料于2020年8月采自湖北省宜昌市长阳土家族自治县,经三峡大学生物与制药学院王玉兵教授鉴定为桑科榕属植物地果FicustikouaBur.。植物标本现保存于天然产物研究与利用湖北省重点实验室(三峡大学)。
1.3 实验方法
1.3.1 提取分离
将地果地上部分经干燥处理后进行粉碎(7.46 kg),95%乙醇回流提取3次(3×70 L),提取时间分别为4、3、2 h。将得到的乙醇提取液减压浓缩并干燥至无醇味,得到地枇杷醇提总浸膏812 g。向总浸膏中加入适量的纯水均匀混悬后,依次使用石油醚、乙酸乙酯、正丁醇溶剂进行萃取,萃取三次合并萃取液,将萃取液减压浓缩,分别得到石油醚萃取部位(127.5 g),乙酸乙酯萃取部位(31.9 g),正丁醇萃取部位(102 g)。
取正丁醇部位80 g,用纯水溶解,少量不溶于水的样品干燥研磨后混悬于水中,使用AB-8型大孔树脂进行分离,依次用纯水、30%乙醇水(体积百分数,下同),60%乙醇水,90%乙醇水,100%乙醇洗脱,将洗脱液减压浓缩并干燥得到30%洗脱部位(17.1 g),60%洗脱部位(14.6 g),90%洗脱部位(10.3 g)。使用反向硅胶柱色谱分离30%乙醇水部位,乙腈-水梯度洗脱,经分析型高效液相色谱分析,得到27个组分Fr.1~27(12.5 g)。Fr.11经半制备型HPLC纯化(乙腈-水30%~50%)得到化合物6(5.5 mg,tR= 33.7 min)、7(4.9 mg,tR= 36.1 min)、8(12.9 mg,tR= 40.0 min)、9(2.3 mg,tR= 46.8 min);Fr.14经半制备型HPLC纯化(乙腈-水23∶77)(体积比,下同)得到化合物3(10.4 mg,tR= 23.3 min)。
取乙酸乙酯部位29 g,1∶1正相硅胶拌样,使用正相硅胶填料Flash柱干法上样对乙酸乙酯部位样品进行快速分离洗脱,对洗脱液进行浓缩并使用高效液相色谱分析合并得到Fr.A1~Fr.A3。Fr.A1经200~300目正相硅胶柱层析分离得到Fr.A1a~Fr.A1c。Fr.A1a经半制备型HPLC分离(乙腈-水55∶45)得到化合物4(2.7 mg,tR= 10.6 min)、5(3.5 mg,tR= 13.1 min)、1(2.5 mg,tR= 22.2 min);Fr.A1b经半制备型HPLC分离(乙腈-水30∶70)得到化合物13(25.7 mg,tR= 12.3 min)、14(7.9 mg,tR= 14.6 min)。Fr.A2经200~300目正相硅胶柱层析分离Fr.A2a~Fr.A2d,Fr.A2a经半制备型HPLC分离(乙腈-水44∶56)得到化合物15(12.4 mg,tR= 17.3 min)、10(2.8 mg,tR= 17.0 min);Fr.A2b经半制备型HPLC分离(乙腈-水44∶56)得到化合物11(8.5 mg,tR= 25.9 min)、12(7.1 mg,tR= 30.9 min);Fr.A2c经半制备型HPLC分离(乙腈-水43∶57)得到化合物16(5.8mg,tR= 17.8 min)、17(3.4 mg,tR= 24.5 min);Fr.A2d经半制备型HPLC分离(乙腈-水41∶59)得到化合物2(2.8 mg,tR= 7.5 min)。
1.3.2 抗氧化活性测定
1.3.2.1 DPPH清除能力测定
实验方法在参考Ji等[7]方法的基础上稍作修改:称取一定质量DPPH粉末,加无水乙醇配置得到400 μmol/L DPPH工作液待用。取100 μL浓度为60 μmol/L的供试液分别与100 μL的DPPH溶液充分混匀,室温下避光反应30 min,使用酶标仪在517 nm波长下测量其吸光度A1,与此同时,测定100 μL浓度为60 μmol/L的供试液和100 μL无水乙醇混合溶液吸光度A2,100 μL无水乙醇和100 μL DPPH工作液吸光度A0,根据以下公式计算DPPH自由基清除率,每个样品重复测定三次。
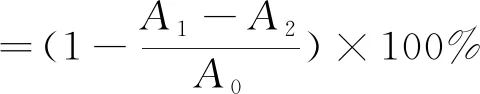
1.3.2.2 总抗氧化能力测定
按照总抗氧化能力测定试剂盒说明书分别配置不同测定管溶液和对照管溶液:1、测定管:3.5 mL工作液和0.2 mL待测液混合,使用旋涡混匀器充分混匀,37 ℃水浴30 min,然后加入0.1 mL显色剂混匀,室温下放置10 min,波长520 nm,超纯水调零,测定吸光度值;2、对照管:将3.5 mL工作液使用旋涡混匀器充分混匀,37 ℃水浴30 min,然后加入0.2 mL待测液和0.1 mL显色剂混匀,室温下放置10 min,波长520 nm,超纯水调零,测定吸光度值,每个样品重复测定三次。
单位定义:在37 ℃时,每分钟每毫摩尔化合物,使反应体系的吸光度值,每增加0.01时,为一个总抗氧化能力单位(U)。

式中,总抗氧化能力单位为U/mmol;V反总:反应液总体积,mL;V样:取样量,mL;C样:样品初始浓度,mmol/L;30:反应时间为30 min。
1.3.2.3 超氧阴离子自由基清除能力
将0.1 mL初始浓度为500 μmol/L的待测溶液与2.8 mL PBS缓冲液(pH = 7.8)加入比色皿中,随后加入0.1 mL邻苯三酚(10 mmol/L),快速混匀,在319 nm下测定其吸光度值,每隔30 s测定一次,一共测定300 s。30 s的吸光度值为A30,300 s的吸光度值为A300,ΔA样=A300-A30。对照组以0.1 mL PBS缓冲液代替待测溶液,ΔA0=A300-A30,每个样品重复测定三次。

1.3.3 数据处理
采用Graphpad Prism数据分析软件进行one-way ANOVA显著性分析,实验数据表示为平均数±标准差,当P<0.05时,表示组间差异显著,有统计学意义。
2 实验结果
2.1 结构鉴定
化合物1淡黄色针状结晶;ESI-MS:m/z337 [M+H]+,分子式为C20H16O5。1H NMR(400 MHz,CDCl3)δ:13.15(1H,s,5-OH),7.82(1H,s,H-3),7.40(2H,d,J=8.6 Hz,H-2′,H-6′),6.90(2H,d,J=8.7 Hz,H-3′,H-5′),6.72(1H,d,J=10.1 Hz,H-4′′),6.33(1H,s,H-8),5.62(1H,d,J=10.0 Hz,H-3"),1.47(6H,s,2"-CH3×2);13C NMR(100 MHz,CDCl3)δ:152.7(C-2),123.6(C-3),181.0(C-4),157.0(C-5),105.4(C-6),159.7(C-7),95.0(C-8),157.4(C-9),106.2(C-10),156.1(C-4′),123.3(C-1′),130.1(C-2′,C-6′),115.7(C-3′,C-5′),78.2(C-2"),128.4(C-3"),115.6(C-4"),28.4(2"-CH3×2)。以上数据与文献[8]报道一致,故鉴定该化合物为高山金莲花素。
化合物2褐色粉末;ESI-MS:m/z291 [M+H]+,分子式为C15H14O6。1H NMR(400 MHz,DMSO-d6)δ:6.71(1H,d,J=2.1 Hz,H-6′),6.67(1H,d,J=8.1 Hz,H-3′),6.58(1H,dd,J=8.2,2.1 Hz,H-2′),5.87(1H,d,J=2.3 Hz,H-8),5.69(1H,d,J=2.3 Hz,H-6),4.47(1H,d,J=7.4 Hz,H-2),3.82(2H,m,H-3),2.63(1H,dd,J=16.1,5.4 Hz,H-4b),2.33(1H,dd,J=16.0,8.0 Hz,H-4a);13C NMR(100 MHz,DMSO-d6)δ:81.2(C-2),66.5(C-3),28.0(C-4),156.4(C-5),95.4(C-6),156.6(C-7),94.4(C-8),155.6(C-9),99.3(C-10),130.8(C-1′),118.7(C-2′),115.3(C-3′),145.1(C-4′,C-5′),114.7(C-6′)。以上数据与文献报道一致[9],故鉴定该化合物为(+)-儿茶素。
化合物3无色片状结晶;ESI-MS:m/z409 [M+H]+,分子式为C20H24O9。1H NMR(400 MHz,CD3OD)δ:7.86(1H,d,J=9.5 Hz,H-4),7.40(1H,s,H-5),6.71(1H,s,H-8),6.20(1H,d,J=9.5 Hz,H-3),4.88(1H,overlap,H-2′),4.59(1H,overlap,H-1′′),3.50(1H,dd,J=16.0,6.8 Hz,H-3′),3.42(1H,d,J=2.3 Hz,H-6b′′),3.35(1H,d,J=2.3 Hz,H-6a′′),3.26(1H,dd,J=18.3,9.1 Hz,H-3′′),3.23(1H,m,H-4′′),3.04(1H,m,H-5′′),3.00(1H,dd,J=9.2,2.3 Hz,H-2′′),1.36(6H,s,H-4′,H-5′);13C NMR(100 MHz,CD3OD)δ:165.2(C-2),112.2(C-3),144.5(C-4),125.1(C-5),127.7(C-6),163.8(C-7),98.1(C-8),146.3(C-9),114.1(C-10),30.5(C-1′),91.9(C-2′),79.2(C-3′),22.4(C-4′),23.8(C-5′),98.9(C-1′′),77.5(C-2′′),78.1(C-3′′),71.4(C-4′′),75.2(C-5′′),62.2(C-6′′)。以上数据与文献[10]报道一致,故鉴定该化合物为异紫花前胡苷。
化合物4白色针状结晶;ESI-MS:m/z187 [M+H]+,分子式为C11H6O3。1H NMR(400 MHz,CDCl3)δ:7.81(1H,d,J=9.5 Hz,H-4),7.70(1H,d,J=2.3 Hz,H-2′),7.69(1H,s,H-8),7.48(1H,d,J=0.9 Hz,H-5),6.83(1H,dd,J=2.3,1.0 Hz,H-3′),6.38(1H,d,J=9.5 Hz,H-3);13C NMR(100 MHz,CDCl3)δ:161.2(C-2),114.8(C-3),144.2(C-4),120.0(C-5),125.0(C-6),156.6(C-7),100.1(C-8),152.2(C-9),115.6(C-10),147.1(C-2′),106.5(C-3′)。以上数据与文献[11]报道一致,故鉴定该化合物为补骨脂素。
化合物5白色晶体;ESI-MS:m/z217 [M+H]+,分子式为C12H8O4。1H NMR(400 MHz,CDCl3)δ:8.16(1H,dd,J=9.8,0.9 Hz,H-4),7.59(1H,d,J=2.4 Hz,H-2′),7.13(1H,s,H-8),7.02(1H,dd,J=2.4,1.0 Hz,H-3′),6.27(1H,d,J=9.8 Hz,H-3),4.26(3H,s,5-OCH3);13C NMR(100 MHz,CDCl3)δ:161.4(C-2),112.7(C-3),139.4(C-4),149.7(C-5),60.2(5-OCH3)112.8(C-6),158.5(C-7),94.0(C-8),152.8(C-9),106.5(C-10),144.9(C-2′),105.2(C-3′),。以上数据与文献[12]报道一致,故鉴定该化合物为佛手柑内酯。
化合物6白色粉末;ESI-MS:m/z583 [M+H]+,分子式为C28H38O13。1H NMR(400 MHz,DMSO-d6)δ:6.55(1H,s,H-8),6.29(2H,s,H-2′,H-6′),4.19(1H,d,J=5.8 Hz,H-4),4.08(1H,d,J=7.7 Hz,H-1′′),3.76(3H,s,7-OCH3),3.63(6H,s,3′-OCH3,5′-OCH3),3.28(3H,s,5-OCH3),2.99~3.69(6H,m,H-2′′,3′′,4′′,5′′,6′′),3.12(1H,t,J=8.4 Hz,H-1a),2.60(1H,dd,J=15.2,4.4 Hz,H-1b),2.01(1H,m,H-3),1.50(1H,m,H-2);13C NMR(100 MHz,DMSO-d6)δ:32.30(C-1),37.7(C-2),64.3(C-2a),70.1(C-3a),44.4(C-3),40.7(C-4),148.0(C-5),59.0(5-OCH3),137.3(C-6),146.4(C-7),55.7(7-OCH3),107.2(C-8),128.6(C-9),124.8(C-10),137.6(C-1′),106.0(C-2′,C-6′),147.6(C-3′,C-5′),56.1(3′-OCH3,5′-OCH3),133.6(C-4′),103.1(C-1′′),73.5(C-2′′),76.8(C-3′′,C-5′′),70.6(C-4′′),61.3(C-6′′)。以上数据与文献[13]报道一致,故鉴定该化合物为(+)-南烛木树脂酚-3α-O-β-D-葡萄糖苷。
化合物7白色无定形粉末;ESI-MS:m/z553 [M+H]+,分子式为C27H36O12。1H NMR (400 MHz,DMSO-d6)δ:6.54(1H,s,H-8),6.33(2H,s,H-2′,H-6′),4.29(1H,d,J=5.8 Hz,H-4),4.16(1H,d,J=7.7 Hz,H-1′′),3.76(3H,s,7-OCH3),3.63(6H,s,3′-OCH3,5′-OCH3),3.27(3H,s,5-OCH3),2.99~3.69(4H,m,H-2′′,3′′,4′′,5′′),3.03(1H,t,J=8.4 Hz,H-1a),2.63(1H,dd,J=15.2,4.4Hz,H-1b),1.96(1H,m,H-3),1.51(1H,m,H-2);13C NMR(100 MHz,DMSO-d6)δ:32.4(C-1),38.1(C-2),61.2(C-2a),44.4(C-3),64.0(C-3a),40.7(C-4),146.9(C-5),58.0(5-OCH3),137.3(C-6),146.5(C-7),55.7(7-OCH3),106.8(C-8),128.5(C-9),124.9(C-10),137.5(C-1′),106.0(C-2′,C-6′),147.5(C-3′,C-5′),56.1(3′-OCH3,5′-OCH3),133.3(C-4′),103.4(C-1′′),73.6(C-2′′),77.0(C-3′′,C-5′′),70.1(C-4′′)。以上数据与文献[14]报道一致,故鉴定该化合物为(+)-南烛木树脂酚-3α-O-β-D-吡喃木糖苷。
化合物8白色粉末;ESI-MS:m/z523 [M+H]+,分子式为C26H34O11。1H NMR(400 MHz,DMSO-d6)δ:6.80(1H,d,J=1.9 Hz,H-2),6.68(1H,d,J=8.0 Hz,H-5),6.60(1H,s,H-2′),6.48(1H,dd,J=8.0,1.9 Hz,H-6),6.07(1H,s,H-5′),4.03(1H,d,J=10.7 Hz,H-7),3.94(1H,d,J=7.6 Hz,H-1′′),3.91(1H,dd,J=10.0,2.6 Hz,H-9′a),3.72(3H,s,3-OCH3),3.70(3H,s,3′-OCH3),3.64(1H,d,J=2.0 Hz,H-9a),3.60(1H,dd,J=10.6,3.4 Hz,H-9′b),3.41~3.49(2H,m,H-6′′),3.11~3.18(1H,m,H-9b),2.95~3.05(4H,m,H-2′′~5′′),2.71(2H,d,J=7.9 Hz,H-7′),1.90(1H,m,H-8′),1.71(1H,m,H-8);13C NMR(100 MHz,DMSO-d6)δ:137.0(C-1),113.9(C-2),147.2(C-3),55.6(3-OCH3),144.1(C-4),115.5(C-5),121.2(C-6),45.6(C-7),44.2(C-8),67.7(C-9),127.1(C-1′),111.8(C-2′),145.5(C-3′),55.5(3′-OCH3),144.5(C-4′),116.3(C-5′),132.8(C-6′),32.6(C-7′),37.53(C-8′),62.8(C-9′),104.2(C-1′′),73.6(C-2′′),76.7(C-3′′),70.1(C-4′′),76.9(C-5′′),61.1(C-6′′)。以上数据与文献[15]报道一致,故鉴定该化合物为异落叶松脂素-9-O-β-D-吡喃葡萄糖苷。
化合物9白色粉末;ESI-MS:m/z555 [M+H]+,分子式为C27H38O12。1H NMR(400 MHz,DMSO-d6)δ:6.33(2H,s,H-2′,H-6′),6.32(2H,s,H-2,H-6),4.10(4H,d,J=7.8 Hz,H-9′,H-9),3.67(6H,s,OCH3×2),3.66(6H,s,-OCH3×2),3.95~2.93(overlap,xylosylprotons),2.60~2.42(4H,overlap,H-9,H-9′),1.05(2H,br s,H-8,H-8′);13C NMR(100 MHz,DMSO-d6)δ:131.5(C-1),106.3(C-2,C-6),147.7(C-3,C-5),55.9(3-OCH3,5-OCH3),133.3(C-4),34.5(C-7,C-7′),40.5(C-8),70.2(C-9),131.0(C-1′),106.3(C-2′,C-6′),147.7(C-3′,C-5′),55.8(3′-OCH3,5′-OCH3),133.4(C-4′),42.2(C-8′),56.1(C-9′),103.3(xyl-1),76.8(xyl-2),76.9(xyl-3),73.7(xyl-4),69.1(xyl-5)。以上数据与文献[13]报道一致,故鉴定该化合物为ssioriside。
化合物10淡黄色结晶;ESI-MS:m/z437 [M+H]+,分子式为C22H28O9。1H NMR(400 MHz,DMSO-d6)δ:6.64(4H,s,H-2,H-2′,H-6,H-6′),4.83(2H,d,J=7.2 Hz,H-7),3.75 ( 12H,s,3,3′,5,5′-OCH3,),3.50(4H,m,H-9,H-9′),2.12(2H,m,H-8′);13C NMR(100 MHz,DMSO-d6)δ:133.3(C-1,1′),103.7(C-2,C-2′),147.9(C-3,C-3′,C-5,C-5′),134.7(C-4,C-4′),82.1(C-7,C-7′),53.51(C-8,C-8′),60.40(C-9,C-9′),56.0(3-OCH3,3′-OCH3,5-OCH3,5′-OCH3)。以上数据与文献[16]报道一致,故鉴定该化合物为华中冬青素。
化合物11淡红色粉末;ESI-MS:m/z361 [M+H]+,分子式为C20H24O6。1H NMR(400 MHz,DMSO-d6)δ:6.68(1H,d,J=8 Hz,H-5),6.63(1H,d,J=1.9 Hz,H-2),6.60(1H,s,H-2′),6.48(dd,J=8.1,1.9 Hz,1H,H-6),6.08(1H,s,H-5′),3.72(1H,d,J=9.5 Hz,H-7),3.70(3H,s,3′-OCH3),3.69(3H,s,3-OCH3),2.67(2H,m,H-7′),1.84(1H,m,H-8),1.62(1H,m,H-8′);13C NMR(100 MHz,DMSO-d6)δ:132.0(C-1),113.3(C-2),145.5(C-3),55.7(3-OCH3),144.1(C-4),115.3(C-5),121.5(C-6),45.9(C-7,C-8),59.9(C-9),127.2(C-1′),111.9(C-2′),147.3(C-3′),55.6(3′-OCH3),144.6(C-4′),116.3(C-5′),137.2(C-6′),32.3(C-7′),38.1(C-8′),63.6(C-9′)。以上数据与文献[17]报道一致,故鉴定该化合物为异落叶松脂素。
化合物12黄色无定型固体;ESI-MS:m/z361 [M+H]+,分子式为C20H24O6。1H NMR(400 MHz,DMSO-d6)δ:6.90(1H,s,H-2),6.75(1H,s,H-6),6.74(1H,s,H-4),6.69(1H,s,H-2′),6.68(1H,s,H-6′),5.40(1H,d,J=6.8 Hz,H-7),3.76(3H,s,5′-OCH3),3.74(3H,s,3-OCH3),3.68~3.60(2H,m,H-9),3.42(2H,m,H-9′),3.41(1H,m,H-8),2.53(2H,t,J=6.8 Hz,H-7′),1.69(2H,m,H-8′);13C NMR(100 MHz,DMSO-d6)δ:132.0(C-1),110.4(C-2),147.6(C-3),55.7(3-OCH3),115.3(C-4),146.3(C-5),118.5(C-6),86.9(C-7),53.3(C-8),63.1(C-9),135.0(C-1′),116.5(C-2′),129.1(C-3′),145.6(C-4′),143.3(C-5′),55.7(5′-OCH3),112.5(C-6′),31.6(C-7′),34.7(C-8′),60.2(C-9′)。以上数据与文献[18]报道一致,故鉴定该化合物为(7R,8S)-3,5′-二甲氧基-4′,7-环氧-8,3′-新木脂烷-5,9,9′-三醇。
化合物13白色针晶;ESI-MS:m/z249 [M+H]+,分子式为C13H12O5。1H NMR(400 MHz,DMSO-d6)δ:7.46(1H,d,J=8.5 Hz,H-2),7.45(1H,s,H-5),7.20(1H,s,H-8),6.84(1H,d,J=8.5 Hz,H-3),3.80(6H,s,6-OCH3,7-OCH3);13C NMR(100 MHz,DMSO-d6)δ:140.2(C-1),167.4(1-COOH),123.5(C-2),115.1(C-3),151.1(C-4),107.0(C-5),147.3(C-6),56.0(6-OCH3),147.2(C-7),55.6(7-OCH3),112.8(C-8),121.8(C-9),121.8(C-10)。以上数据与文献[19]报道一致,故鉴定该化合物为6,7-二甲氧基-4-羟基-1-萘甲酸。
化合物14白色晶体;ESI-MS:m/z183 [M+H]+,分子式为C9H10O4。1H NMR(400 MHz,DMSO-d6)δ:7.34(1H,d,J=2 Hz,H-2),7.29(1H,dd,J=8.2,2.0 Hz,H-6),6.78(1H,d,J=8.2 Hz,H-5),4.22(2H,q,J=7.1 Hz,H-8),1.28(3H,t,J=7.1 Hz,H-9);13C NMR(100 MHz,DMSO-d6)δ:121.8(C-1),116.2(C-2),145.2(C-3),150.7(C-4),115.3(C-5),120.6(C-6),165.8(C-7),60.1(C-8),14.3(C-9)。以上数据与文献[20]报道一致,故鉴定该化合物为3,4-二羟基苯甲酸乙酯。
化合物15无色油状物无色油状物;ESI-MS:m/z225 [M+H]+,分子式为C13H20O3。1H NMR(400 MHz,DMSO-d6)δ:5.78(1H,s,H-4),5.68(1H,dd,J=15.6,5.4Hz,H-8),5.67(1H,d,J=15.6 Hz,H-7),4.18(1H,m,H-9),2.36(1H,d,J=17.0 Hz,H-2a),2.05(1H,d,J=17.0 Hz,H-2b),1.80(3H,s,H-13),1.11(3H,d,J=6.4 Hz,H-10),0.93(3H,s,H-11),0.91(3H,s,H-12);13C NMR(100 MHz,DMSO-d6)δ:40.9(C-1),49.4(C-2),197.4(C-3),125.5(C-4),164.4(C-5),77.9(C-6),127.9(C-7),135.9(C-8),66.1(C-9),24.1(C-10),24.0(C-11),23.1(C-12),19.0(C-13)。以上数据与文献[21]报道基本一致,故鉴定该化合物为bluemenol A。
化合物16褐色粉末;ESI-MS:m/z219 [M+H]+,分子式为C12H10O4。1H NMR(400 MHz,DMSO-d6)δ:9.02(2H,s,2×Ar-OH),8.91 (2H,s,2×Ar-OH),6.88(2H,d,J=2.1 Hz,H-2,H-2′),6.76(2H,dd,J=8.1,2.1 Hz,H-6,H-6′),6.74(2H,s,H-5,H-5′);13C NMR(100 MHz,DMSO-d6)δ:132.1(C-1,C-1′),113.5(C-2,C-2′),144.2(C-3,C-3′),145.4(C-4,C-4′),116.0(C-5,C-5′),116.9(C-6,C-6′)。以上数据与文献[22]报道一致,故鉴定该化合物为3,3′,4,4′-四羟基联苯。
化合物17白色晶体;ESI-MS:m/z383 [M+H]+,分子式为C18H22O9。1H NMR(400 MHz,DMSO-d6)δ:7.39(1H,d,J=15.8 Hz,H-7′),7.01(1H,d,J=2.3Hz,H-2′),6.95(1H,dd,J=8.2,2.3 Hz,H-6′),6.75(1H,d,J=8.2 Hz,H-5′),6.11(1H,d,J=15.9 Hz,H-8′),5.01(1H,m,H-3),3.99(2H,q,J=7.1 Hz,H-8),3.88(1H,m,H-5),3.58(1H,dd,J=4.9,3.2 Hz,H-4),2.12(1H,m,H-2a),2.07(1H,m,H-6a),1.92(1H,dd,J=13.7,3.6 Hz,H-2b),1.77(1H,dd,J=12.7,9.3 Hz,H-6b),1.11(3H,t,J=7.1 Hz,H-9);13C NMR(100 MHz,DMSO-d6)δ:73.1(C-1),35.3(C-2),71.1(C-3),69.6(C-4),67.2(C-5),37.2(C-6),173.1(C-7),60.3(C-8),13.8(C-9),125.3(C-1′),114.5(C-2′),145.2(C-3′),148.8(C-4′),115.9(C-5′),121.6(C-6′),146.6(C-7′),113.9(C-8′),165.5(C-9′)。以上数据与文献[23]报道一致,故鉴定该化合物为绿原酸乙酯。
2.2 抗氧化活性结果
2.2.1 DPPH清除率结果
单体化合物的DPPH清除能力实验结果显示,黄酮(1~2)及香豆素类(3~5)化合物有一定的DPPH清除作用,木脂素类(6~12)化合物普遍具有较强的DPPH清除作用,其中化合物10的DPPH清除率为(52.44±1.87)%,与同浓度阳性对照效果相当(56.3±2.54)%。此外,多酚化合物14、16具有较高的DPPH清除率,分别为(60.37±2.83)%、(60.50±2.97)%,均高于同浓度下阳性对照药物的DPPH清除率值,结果见图1。

图1 化合物1~17的DPPH清除率
2.2.2 总抗氧化能力测定结果
单体化合物的总抗氧化能力结果显示,黄酮及香豆素类化合物仅有较弱的总抗氧化能力,木脂素类化合物抗氧化活性较为明显。其中木脂素类化合物9的总抗氧化能力为(65.44±3.11) U/mmol、酚酸化合物13总抗氧化能力为(79.58±3.31) U/mmol、多酚类化合物16总抗氧化能力为(85.39±6.31) U/mmol,均显著大于同浓度下阳性药物Vc的总抗氧化能力(59.74±4.67) U/mmol,实验结果见图2。

图2 化合物1~17的总抗氧化能力
2.2.3 超氧阴离子清除能力
结果显示木脂素类化合物及多酚类化合物具有一定的超氧阴离子清除能力,其中化合物9的清除率为(35.50±4.1)%,化合物13的清除率为(40.66±2.5)%,化合物16的清除率为(46.31±5.5)%,实验结果见图3。

图3 化合物1~17的超氧阴离子清除率
3 讨论与结论
人体内产生的过量自由基会攻击体内脂质、蛋白质、DNA等生物大分子,破坏细胞正常结构,干扰人体的正常代谢活动,从而引起疾病并加速人体衰老。因此寻找外源性抗氧化剂对于维持人体正常代谢是非常有必要的,天然抗氧化剂由于其低毒、高效的特点,已经逐渐进入了研究者的视野[24]。
本研究从土家族民间药物地枇杷中分离并鉴定得到17个化合物,包括黄酮、香豆素、木脂素、多酚等化合物结构类型。由于抗氧化实验的多样性及复杂性,通常要求抗氧化活性采用2种以上的抗氧化活性方法进行测定。本实验通过测定化合物的DPPH清除率、总抗氧化能力、超氧阴离子清除能力,来对地枇杷中分离得到的化合物进行一个简单的活性测定。发现木脂素类化合物及多酚、酚酸类化合物具有较强的抗氧化活性,甚至超过同浓度阳性对照的抗氧化能力。表明地枇杷中木脂素及多酚类化合物可能为其抗氧化活性药效物质基础。本研究进一步丰富了地枇杷的化学成分及药理活性,提示地枇杷可能具有较大的被开发为天然抗氧化剂的潜能,为土家族民间用药地枇杷的开发与利用奠定基础。
