微电解无菌水系统在实验动物屏障设施中应用的跟踪监测
2022-05-24张志妮邓新燕
张 薇, 唐 彬, 赵 勇, 张志妮, 邓新燕
(中山大学实验动物中心,广州 510006)
目前,国内实验动物屏障设施中无菌水的相关报告很少。实验动物屏障设施的无菌水系统犹如人体的血液循环系统,不仅供给动物不可或缺的饮用水,也为屏障内的日常清洁等工作提供用水,是影响动物质量和干扰实验研究的潜在因素。根据国家标准《实验动物环境与设施》GB 14925—2010 要求,清洁级以上的实验动物饮用水应达到无菌要求;而对于清洁级以上屏障设施中日常工作用水则没有明确规定,但要求屏障环境中的沉降菌最大平均浓度[每0.5 h内φ90 mm 平皿中菌落形成单位(colony-forming unit,CFU)]≤3。屏障环境用水一旦污染也将导致动物生存环境污染,因此,屏障设施内的日常工作用水也应达到无菌要求。有些屏障设施中无菌水系统制水不能持续保持无菌,遂采用高压灭菌器灭菌制备动物饮用水,而屏障设施内日常工作用水则采用添加化学消毒剂的方法制备。但是能达到灭菌效果的化学消毒剂较少,且化学消毒或灭菌剂效果受影响的因素较多,如物体表面有机物、尘埃、水的酸碱性及水中有机物等均会降低灭菌效果。因此,屏障环境工作用水同样需要控制微生物而达到无菌,才能消除屏障环境与动物污染隐患。
中山大学实验动物中心于2008年开始将微电解无菌水系统应用到屏障设施中供应SPF 级动物饮用水和日常工作用水,并于2018 年11 月新增微电解仪备用机。前期研究表明,微电解无菌水可以持续保持无菌,并对SD大鼠的血液生化等临床指标没有影响[1]。2018年4月~2022年3月本中心对微电解无菌水系统的使用情况进行了跟踪观察,然后对微电解无菌水系统配置、运行管理中的细节加以总结和分析,以供同行借鉴。
1 材料与方法
1.1 微电解无菌水系统
微电解无菌水系统由超滤、微电解仪、循环输水管路和屏障实设施内终端供水口组成。微电解仪1 号和2 号互为备用,当其中一台发生故障时,启用另外一台。微电解用220 V 电源,实际工作电压≤80 V,功率为280 W;微电解仪产生的电流为2 A~10 A。超滤材料主要有5 μm保安过滤膜、1 μm精密过滤膜、0.1 μm超滤膜。微电解无菌水系统由广州惜水科技有限公司提供。系统工艺流程见图1 所示,虚线左侧为屏障环境设施内管网布局,右侧为屏障环境设施外管网及机房布局。
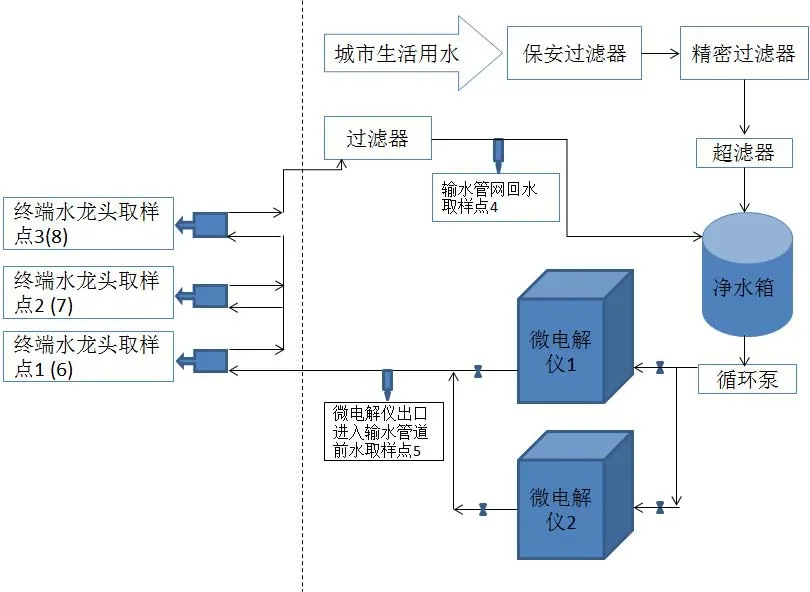
图1 微电解无菌水系统的工艺流程简图Figure 1 Process flow diagram of micro-electrolyzed sterile water system
1.2 主要试剂与仪器
SPX-600 智能生化培养箱购自上海鸿都电子科技有限公司;DHP-9162电热恒温培养箱购自上海一恒科学仪器有限公司;脑心浸液肉汤、硫乙醇酸钠肉汤无菌采样瓶、大豆蛋白冻肉汤培养基均购自于广东环凯微生物科技有限公司;化学纯36%~38%盐酸购自广州化学试剂厂(批号:2021030216)。
1.3 水采样点的设置及编号
设8个取水样点。1、2号微电解仪的3个水龙头是共同的终端出水实体。屏障设施内3 个终端水龙头对应1号微电解仪的水样标记为1号、2号、3号取样点,对应2 号微电解仪的水样标记为6 号、7 号、8 号;屏障设施外微电解机房的2 个取水点,即输水管网回水取样点(标记为4 号)和微电解出水进入输水管网前取样点(标记为5号)各1个。
1.4 水样采集
超滤水采样:确认微电解仪均处于关闭状态,开启,1、2、3 号终端出水口放水5 min,然后用酒精灯烧灼出水口,用采样瓶以无菌操作的方法对上述取水点进行水样采集,500 mL/瓶,每份水样各2瓶。
微电解水采样:开启微电解仪1 h后采样。采样点包括3 个终端出水口(1 号微电解仪启用时命名为1、2、3 号水样;2 号微电解仪启用时命名为6、7、8 水样)、1 个输水管网回水取样点4 号、1 个微电解出水口至输水管网前的取样点5 号。对采样出水口放水5 min,用酒精灯烧灼出水口,以无菌操作的方法采集水样500 mL/瓶,每份水样各2瓶。
酸化水采样:对终端出水口的水人工添加36%~38%化学纯盐酸,达到pH测试纸值2.5~3,以无菌操作的方法采集水样500 mL/瓶,每份水样各2瓶。
1.5 样品接种培养
过滤法检测:依据《中华人民共和国药典》2020版中纯化水、注射用水的检测方法。于水平流洁净工作台上进行操作。每份样品随机取其中1 瓶500 mL 水样,经0.22 μm无菌薄膜过滤器滤过后,取出滤膜,菌面向上贴于R2A 琼脂培养基,30~35 ℃培养至少5 d,观察菌落数。
国标法检测:依据国家标准GB 14925—2010《实验动物环境及设施》、GB 14926.41—2001《实验动物无菌动物生活环境及粪便标准的检测方法》检测。另1瓶500 mL水样按无菌操作分别吸取0.5 mL样品,分别接种到脑心浸液肉汤、硫乙醇酸钠肉汤、大豆蛋白冻肉汤、血琼脂平皿培养基中。其中,接种脑心浸液肉汤、硫乙醇酸钠肉汤培养基后,置于(36±1)℃培养至少14 d,并在第7和第14天时采用革兰染色法镜检;接种血琼脂平皿后,放置35~37 ℃培育箱中48~72 h,观察血琼脂平皿中有无细菌生长,以及其菌落数;接种大豆蛋白冻肉汤培养基后,置于25~28 ℃培养至少14 d,观察有无真菌生长。
1.6 结果判断
光学显微镜下未观察到细菌,同时R2A 琼脂培养基和血琼脂皿上无细菌生长,大豆蛋白冻肉汤培养基中无真菌生长,即判断水质合格,无菌水符合无菌要求,结果表示为阴性“-”。任何一个培养基中出现阳性结果,即判断为不符合无菌要求,结果表示为阳性“+”。
2 结果
2.1 超滤水与微电解水的检测结果对比
关闭微电解仪时,经过超滤处理的1、2、3 号水样进行微生物检测,结果均为阳性。开启2 号微电解仪1 h 后,4、5、6、7、8 号水样进行微生物检测的结果均为阴性。两种水样采用过滤法的检测结果与依据GB 14925—2010、GB 14926.41—2001国标检测的结果一致,具体见表1。

表1 超滤水与微电解水的检测结果比较Table 1 Comparison between ultrafiltration water and micro electrolysis water
2.2 微电解仪故障与正常运行期间的检测结果
2018 年4 月~2022 年3 月跟踪检测期间,在编号为20180921 和20181011 的二次连续检测时发现1、2、3 号终端出水口水样有细菌,对应1 号微电解仪故障,此后增加备用微电解仪(命名为2 号微电解仪);另外,在编号20210923 和20211215 的检测时发现6、7、8 终端水样有细菌,对应2 号微电解仪故障。结果提示,微电解仪正常运行时,终端水样检测结果为阴性;若微电解仪出现故障,终端水样检测结果为阳性(表2)。
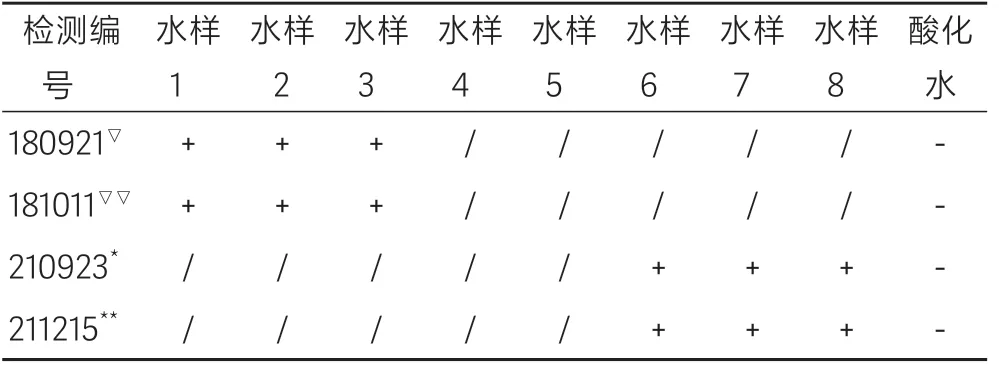
表2 微电解仪故障时的水样检测结果Table 2 Detection result of water samples in case of failure of micro-electrolyzed sterile water system
2.3 微电解无菌水跟踪监测微生物结果
2018 年4 月~2022 年3 月共进行17 次采样检测,除编号为20180921、20181011、20210923、20211215的终端水样检测有细菌(分别对应1号和2号微电解仪故障)外,其他时间的跟踪检测结果显示微电解无菌水系统的终端出水口1、2、3、6、7、8水样、回水口4水样、微电解出水口5水样、酸化水样经培养14 d后均无细菌和真菌生长(表3),符合GB 14925—2010、GB/T 14926.41—2001国家标准。

表3 2018年4月—2022年3月微电解无菌水微生物检测情况Table 3 Microbial detection of micro-electrolyzed sterile water from April 2018 to March 2021
3 讨论
本中心所用的微电解无菌水系统在跟踪前期的检测结果显示,仅经过超滤的水不能达到无菌,且在微电解仪故障时,所制终端水不能达到无菌;开启微电解仪并正常工作1 h后所制水能达到无菌。国内有学者比较了反渗透实验动物饮用水与高压灭菌水,发现前者不能达到无菌[2-3]。不能保持所制水无菌的原因可能与反渗透膜、前置超滤膜自身微生物滋生以及输水管道内、终端开放口微生物滋生有关。同时,前期的检测水样采用过滤法与国标法(水样未经过滤)的检测结果一致,因此在后期的跟踪监测中采用了GB 14925—2010、GB/T 14926.41—2001 国家标准推荐的方法。
屏障设施无菌水系统均由灭菌环节、输水管路、供水终端组成。目前,国内应用到屏障设施的无菌水系统主要有反渗透或+浸没式紫外线、超滤(超滤+臭氧发生器+浸没式紫外线)、在线灭菌。反渗透和超滤均是利用膜过滤法进行净化水。反渗透可以截留9×101道尔顿的小分子,能有效清除溶解于水中的无机物、有机物、细菌、热源等。超滤可以截留相对分子质量在1×103~1.5×105,不能过滤水溶性无机离子,也通常作为反渗透的前置过滤。但反渗透和超滤均需要防止过滤膜被细菌污染或堵塞,需定期监控并更换过滤膜,否则导致过滤失败,系统滋生细菌[4-5]。也有学者认为,反渗透只可以去除大部分细菌,而不是全部[6]。同时这2 种系统的输水管道以配置成循环管路为佳,而维持输水管路内的无菌则是防止污染的关键点和难点。在线高温灭菌是将水高温灭菌结合降温输送,有文献[2]报道其可以保持终端出水的无菌,但随着在饮水瓶储存时间延长,滋生细菌逐渐增多,同时能耗较高。微电解是通过改变电场强度,影响细菌的生理代谢而导致其死亡,同时水分子通过微电解发生强的氧化还原反应,并释放活性物质[O]、HO2-、H2O2等自由基到循环水中发挥杀菌作用[1]。微电解的优势是保持循环输水系统持续存在强氧化活性物质而达到灭菌作用,尤其是可以持续保持输水管路的无菌[1];但将其灌装饮水瓶后能维持多长时间的无菌,尚未做监测。本研究通过对微电解无菌水系统多年的跟踪观察发现,微电解无菌水系统的终端出水口水样检测无菌表明整个无菌水系统无菌;回水口水样无菌表明输水管路无污染;微电解出水口进入供水网管前水样无菌表明微电解仪器工作正常;而酸化水监测结果保持阴性,是无菌水系统的第二屏障,可弥补无菌水不能实时监测带来的污染风险。
屏障设施无菌水系统的污染环节主要发生在灭菌主机功能减弱或故障、膜过滤或输水循环管路污染、单行无循环管路或供水末端的逆行污染、动物自动饮水嘴的逆行污染。本中心在对微电解无菌水系统的跟踪监测过程中发现,取样点的科学设置非常重要。因此在观察中不仅设置了终端取水点,还设置了循环管路的回水取样点和微电解仪出水口进入管网前的取样点,以此达到对无菌水系统的各关键环节点起到准确监控作用。一旦发现污染,可以通过污染取样点位置判断无菌水系统污染发生的具体环节,即准确判断是微电解仪器问题、输水管路问题、终端水逆行污染还是取样操作污染问题。通过几年跟踪观察发现:微电解无菌水系统多以微电解仪发生故障导致杀菌失败,在1号微电解仪工作时2次检测阳性,维修发现电解极片结垢板结,在两极片中形成隔离层,使微电解减弱或不能正常工作。因此,微电解仪的维护非常重要。微电解无菌水系统维护的关键点是:定期清洗除垢,每月一次,每500 L 加柠檬酸500 g,开启微电解无菌水系统,使柠檬酸水在系统中循环保持1~2 h,减少矿物质等杂质在电极片上的结垢,保持阴极片、阳极片正常发挥电解作用;过滤膜定期更换,保安过滤每3个月、精过滤膜6 个月、超滤膜12 个月更换一次。过滤膜的配置起到拦截微量悬浮物和微小杂质颗粒以及部分微生物的作用,可实现水的预处理,减少电极片的结垢,但其不具备自净功能,不能持续保持无菌。经2015—2017年[1]及近4年来的跟踪监测发现,在微电解系统正常工作时,微电解仪出水口、输水管路、终端出水均没有污染,后期还设置了备用微电解仪器,交替使用,以确保生产屏障设施中动物饮用水和日常工作清洁用水的无菌。如没有备用微电解仪且仅有的一台微电解仪故障时,应用高压灭菌水替代,以保障屏障设施内动物饮用水和日常工作用水符合无菌要求。
屏障设施中动物饮用水和日常用水一旦污染将直接导致动物和环境的污染,因此,维持并保持屏障设施无菌水系统的无菌显得极其重要。经过多年跟踪监测的结果表明,微电解无菌水在屏障设施中应用是可行的,但也存在一些关键的细节问题。一方面,无菌水仅仅靠微电解仪尚不能达到持续无菌,输水管路的科学配置是极其关键的因素,必须设置循环回路,使微电解的杀菌物质在循环管路中持续保持。笔者了解到国内目前约25家实验动物设施使用了微电解无菌水系统,另有2 家单位在尝试应用微电解系统时发现所制水不能达到无菌而放弃使用,究其原因是配置的输水管路没有设置循环回路、输水管网有过长过多盲端、输水管网中形成旁通独立闭环等,导致输水管路死角和部分不能循环的水存在,管网中的水不能全部回流而重新进入微电解杀菌循环系统中,从而导致水中细菌的滋生。因此,在实验动物屏障设施的设计规划中,对无菌水系统中输水管路的布局需要考虑循环输水管路的设计,尽可能减少输水死角。另一方面,目前的微电解无菌水系统没有即时报警系统。本中心自2018年11 月起在系统中配置了在线微电解仪电流检测表,以监控微电解仪产生的电流,小于或等于2 A时应立即停用,启用备用机。此外,准确判断仍然需要取水样进行微生物检测,历时2~14 d才能报告结果,因此水质微生物检测结果的判断迟于污染发生的实际时间。未来工作中,将考虑利用微电解水中的主要灭菌成分设置在线检测报警系统以达到实时监控的作用。
