超声内镜对胃肠道间质瘤诊断价值的荟萃分析
2022-05-13刘东鑫余荣国
刘东鑫, 余荣国, 徐 超
(1. 河北北方学院研究生院,河北 张家口 075000;2. 厦门大学附属福州第二医院骨科,福建 福州 350007;3. 邯郸市中心医院消化内科,河北 邯郸 056001)
胃肠道间质瘤(gastrointestinal stromal tomosis,GIST)是一种威胁生命的恶性肿瘤,是消化道中最常见的间质肿瘤,占所有胃肠道癌症的0.1%~3%[1-2]。Ducimètiere 等[3]报道,每年 GIST 发病率为每 10 万人中有1.1 例, 但对GIST 的发病估计存在巨大差异[4]。 例如,自 2001 年以来,美国每百万居民中有6.8 例新发病例[5],而在中国和挪威的发病率是每百万人中 19~22 例新病例[4]。由于 GIST 的病变在黏膜下层,普通内窥镜检查无法准确区分;而超声内镜(endoscopic ultrasonography, EUS) 可以评估起源、回声和淋巴结,是一种针对GIST 的准确诊断技术。EUS 有助于区分GIST 与其他黏膜下肿瘤, 对制定准确的治疗策略以使患者获得最佳疗效至关重要。近来, 关于EUS 对黏膜下肿瘤诊断价值的报道越来越多,但在评估GIST 方面的诊断价值很少。GIST容易与其他低回声黏膜下病变相混淆,但恶性度更高。 因此,本研究通过EUS 评估GIST 的诊断价值。
材料和方法
一、检索策略
于2020 年10 月搜索 Cochrane 对照试验中央注册系统 (Cochrane Central Register of Controlled Trials, CENTRAL)、EMBASE (Excerpt Medica Database)、PubMed、Web of Science、Clinical Trials、VIP date、中国知网和万方数据库自建库以来的数据,主要检索词是“胃肠道间质瘤”“gastrointestinal stromal tumor”和“超声内镜”“endoscopy ultrasound”,采用MeSH 主题词、自由词、布尔逻辑检索等方式逐一检索, 并尽可能检索查阅了会议摘要、protocol、图书馆等其他数据。
二、选择标准
主要纳入标准: ①研究样本数量至少应为10 个或更多, 以免因样本数量太小而造成二类误差;②研究数据涉及EUS(指标测试)和病理评估(参考标准)的比较结果;③足够的数据来构建2×2 列联表,以便可以将表中的单元格标记为真阳性(true positives, TP)、真阴性(true negative,TN)、假阳性(false positive, FP)和假阴性(false negative,FN);④这些研究通常包括回顾性和前瞻性系列患者。 如果确定以下任何因素,则排除试验:①综述、讲座、动物实验和病例报告;②无法获取全文或完整数据;③所有重复的研究(指相同的研究组、机构和时期)。
三、统计分析与数据综合
所有数据都由3 位作者单独提取和汇总,如有不一致之处,则请资深作者共同作出决定。 从选定的文献中提取相关数据,并且记录所包括研究的第一作者、出版年份、研究类型和国家等信息。诊断试验文献质量评价标准-2(quality assessment diagnostic accuracy studies-2,QUADAS-2)用于评估所包括的文献,该工具包括选择索引测试参考标准以及流量和时间4 个关键区域。每个小组都评估偏见的风险,前3 个小组还评估了关注点的适用性。 根据以下风险之一,对包括在研究中的每个关键项目进行了评估,并对其完全符合、部分符合、完全符合或未报告项目所表达的特征进行评分, 分为低风险、高风险和不清楚[6]。通过使用STATA 16.0 软件的Metan和Midas 程序,参考I2和Q 测试分析所包含对象的异质性,如果I2>50%或Q<0.05,则认为研究结果存在异质性。根据双变量方法[7],使用耦合森林图来显示TP、TN、FP 和FN 的数量,以及敏感性和特异性,对于所有纳入的研究,其置信区间(confidence interval,CI)为95%。 使用综合受试者工作特征曲线(summary receiver operating characteristic curve,SROC 曲线) 图来显示ROC 空间中单个研究的结果。 为了找出可能导致异质性的潜在因素,对受试者进行荟萃回归分析和亚组分析。通过线性回归方法检测漏斗图的不对称性,以评价出版偏倚并绘制Deeks 漏斗图,以 P>0.05 为 Deeks 漏斗图无明显不对称。
结 果
一、检索结果
通过数据库检索到文献217 篇,并通过其他来源(如会议摘要、已完成实验数据未发表以及图书馆等)获得文献7 篇,共发现224 项潜在相关的研究。 阅读摘要剔除 76 篇,阅读全文剔除 130 篇。 最终有12 篇文章符合条件, 其中前瞻性研究5 篇,回顾性研究5 篇,前瞻性研究与回顾2 篇,筛选流程见图1。
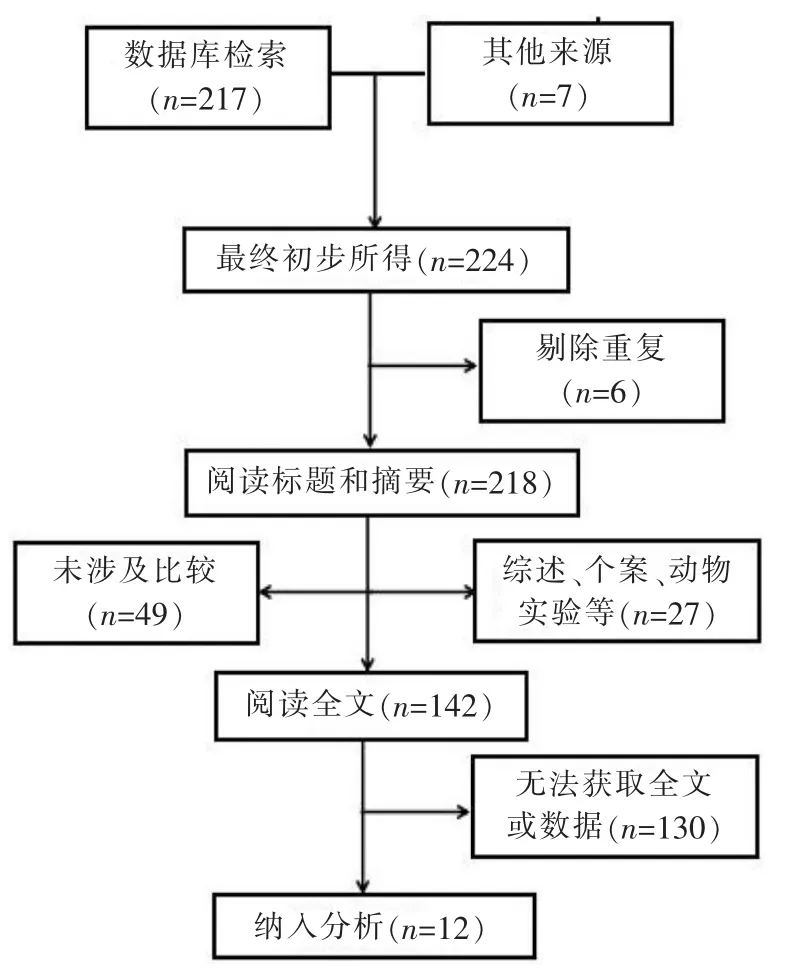
图1 文献检索及筛选图
二、包含研究的功能和质量评估
总共12 项研究[8-19]包括529 个病变。 研究类型包括多种形式,如表1 所示,“金标准”为术后病理结果。分别使用诊断准确性研究QUADAS-2 进行了偏倚风险的评估,显示所选研究的质量良好。 但由于缺乏对病理诊断是否会在不了解内窥镜诊断结果的情况下进行解释的描述,因此所有研究均存在参考标准不清楚的风险。并非所有患者都包括在分析中,因此只有一项研究[9]具有较高的流量和时间风险(见图 2、3)。
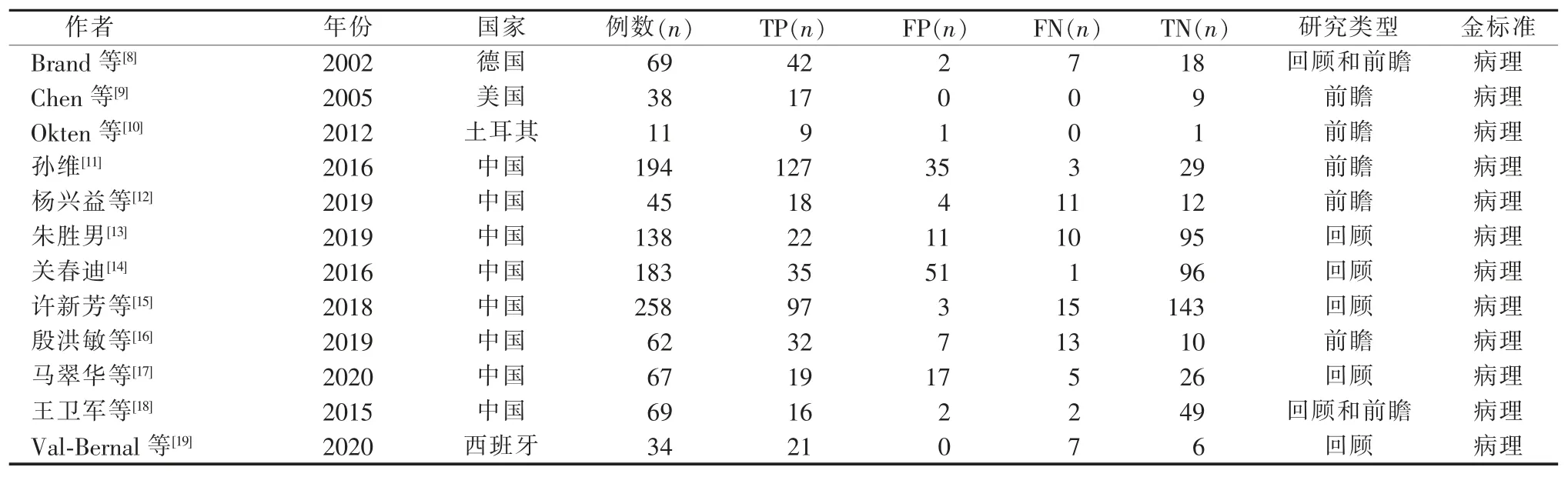
表1 所纳入文献特征及相关结果

图2 偏倚风险和适用性问题
三、荟萃分析
EUS 诊断GIST 的合并灵敏度、特异度、阳性似然比(positive likelihood ratio, PLR)和阴性似然比(negative likelihood ratio, NLR) 为 0.88 (95%CI:0.78~0.93)、0.84 (95%CI:0.70~0.93)、5.6 (95%CI:2.7~11.4)、0.15(95%CI:0.08~0.27)(见图 4)。 LR 散点图显示,PLR 与NLR 的合计点位于右下象限(见图 5);SROC 显示了汇总点、95%CI 和预测区域(见图 6)。 AUC 为 0.93。 Fagan 图示: 以前被归类为GIST 的 EUS 概率从正值时GIST 的平均患病率20%增加到58%,而当负值时,其减少的概率为4%(见图 7)。
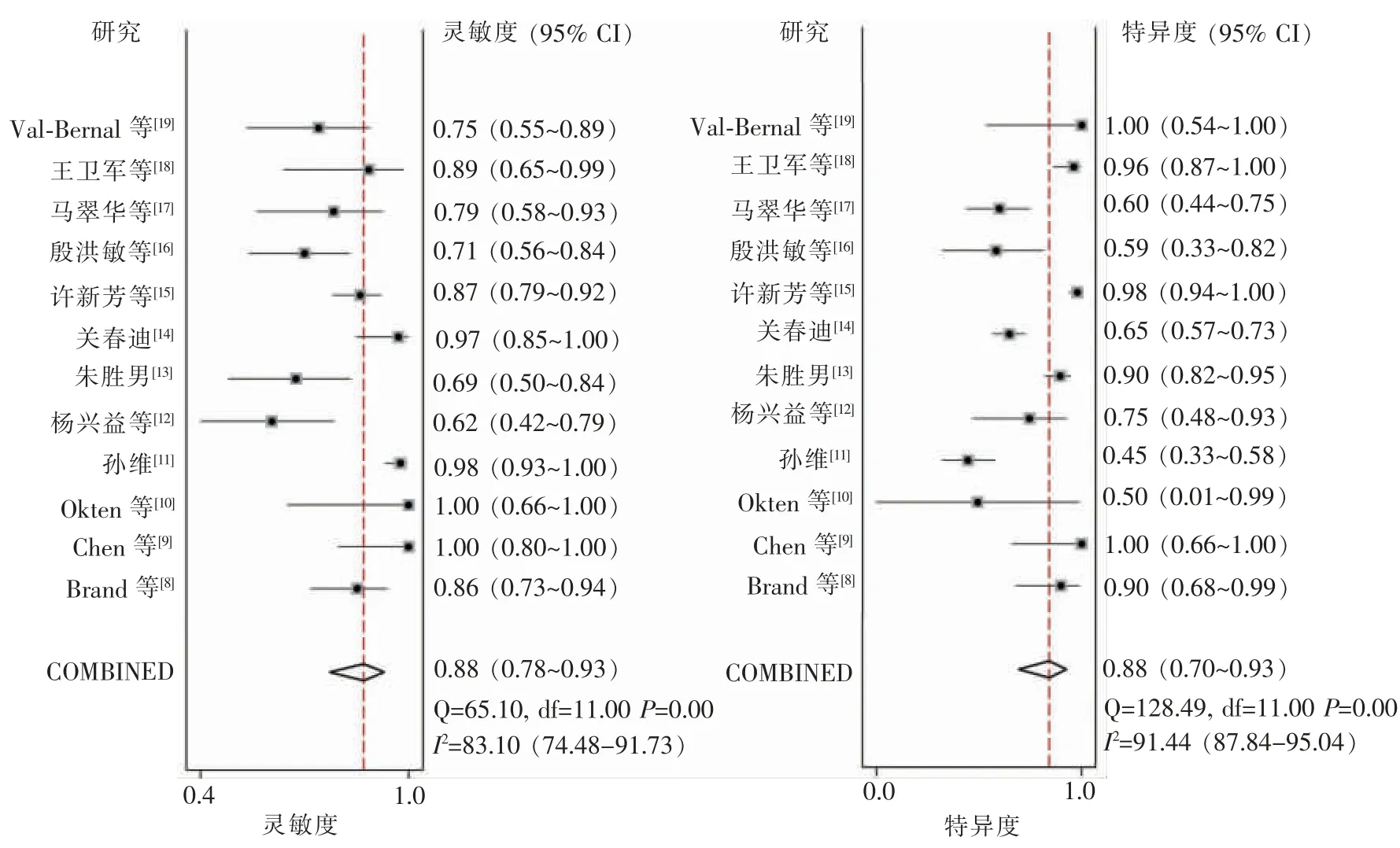
图4 森林图
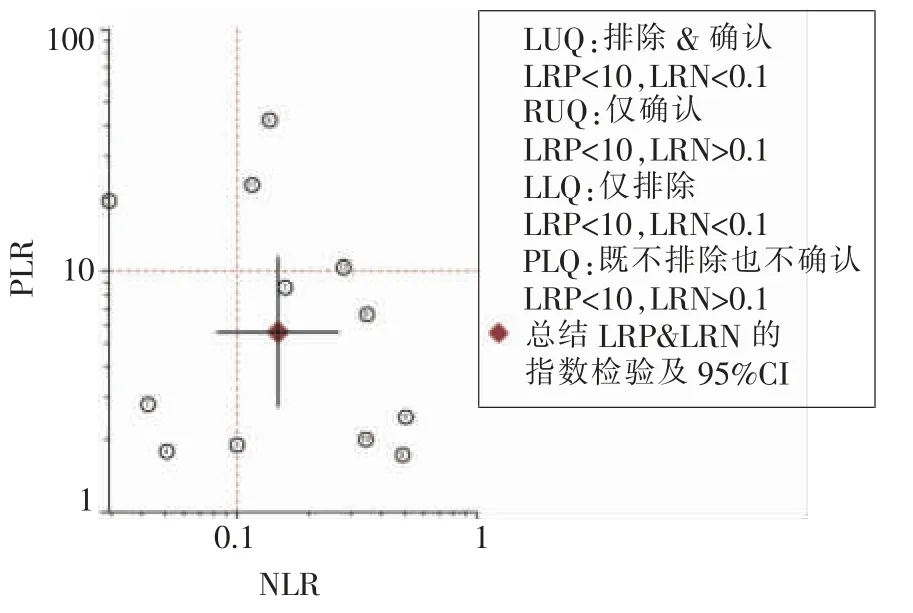
图5 似然比(LR)散点图
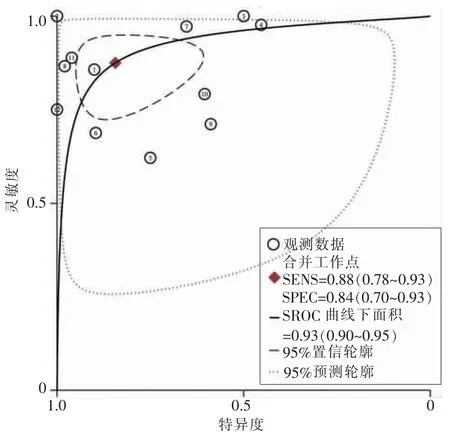
图6 具有预测区间和置信区间的SROC
1. 元回归和亚组分析: 异质性分析的结果显示,Q 检验 P<0.05, I2≥50%, 这意味着研究之间可能存在异质性。SROC 曲线不是“肩臂式”分布,表明异质性不是由阈值效应引起的。 根据研究的特点,分别对研究年份和研究国家进行了元回归分析。为了不遗漏异质性的原因,将P 限制设置为0.1。结果表明,各国之间存在异质性(见表2)。 按子组对其进行分析,EUS 在西方国家诊断GIST 的诊断效力较高(见表 2、表 3)。

表2 荟萃回归
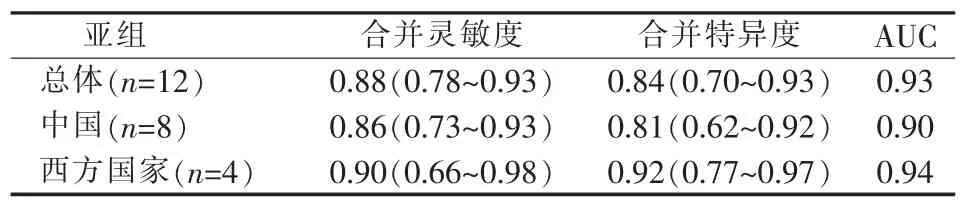
表3 亚组分析
2. 出版偏倚的检测结果: 线性回归为P=0.21。漏斗图上没有明显的不对称性(见图8)。
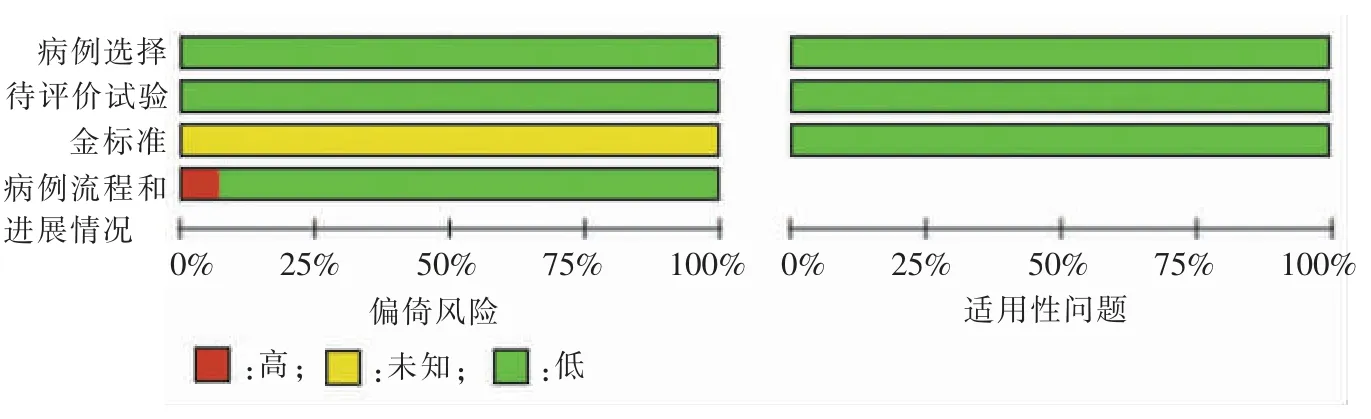
图3 偏倚风险和适用性问题图
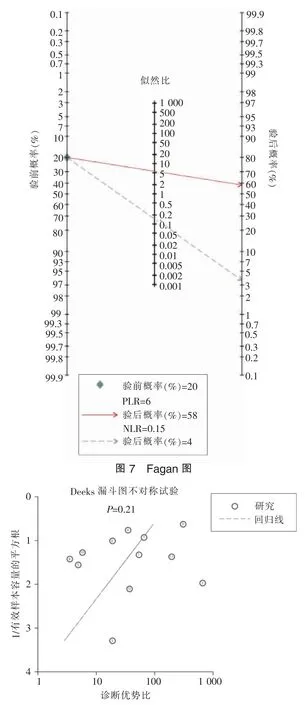
图8 纳入文献的漏斗图
讨 论
在EUS 对GIST 的诊断价值的系统评价中,本研究使用了专门用于诊断荟萃分析的统计方法,并对现有证据进行了定量总结。 总体来说,EUS 为GIST 的诊断提供了临床有用的信息, 有助于临床医师作出有关患者治疗管理的决策。对纳入研究进行质量评估发现,大多数研究没有报告指标测试和参考测试之间的间隔, 几乎不会影响最终结果,因为临床病理诊断通常在很短的时间内(天或周)。反过来,这不足以改变疾病的阶段。因此,可以认为所纳入研究质量良好。EUS 的合并灵敏度和特异度分别为 0.78~0.93 和 0.70~0.93,均显著高于 0.50。 这意味着EUS 的性能优于通过投掷硬币分配给每一患者的概率(即50%)。贝叶斯分析的结果验证了这一发现。 表明EUS 的诊断效果也要优于根据随机概率估计患者的患病情况。 EUS 诊断GIST 的PLR和 NLR 为 5.6 (95%CI 2.7~11.4) 和 0.15 (95%CI 0.08~0.27)。一般认为 PLR>10 或 NLR<0.1 时,诊断或排除疾病的机会大大增加。 但NLR、PLR 的合计点位于右下象限, 表明EUS 可能不是对GIST 的最佳确诊或排除手段。 SROC 曲线的AUC 为0.93,通常认为AUC 高于0.9 便具有更高的诊断价值。Fagan 图提示EUS 可以更好地诊断GIST,当测试为阳性时,其将概率从20%增至58%,而当测试为阴性时,其将相同的概率降低为4%。以上所有结果表明,EUS 对GIST 的诊断价值很高,但是诊断准确性需要提高。
值得一提的是, 本荟萃分析存在一些局限性。首先,只能在已出版的研究文章中,确定国家(在西方研究中结果更好且均一)是异质性的根源。 由于缺乏数据,无法排除其他潜在的异质性来源,例如EUS 检查的频率和内镜检查的经验。 因此,需要更多研究来阐明EUS 在各种情况下对GIST 的诊断效果。其次,该分析中的研究并不完善,很少有前瞻性的随机盲法试验专门探讨EUS 在GIST 诊断中的诊断效果。 为提高研究质量,建议在临床试验设计上应更严格。第三,可能存在潜在的语言偏见,因为该语言仅限于中文和英文。 最后,荟萃分析不能替代大量的临床研究样本,仍然需要更多的临床研究验证。
比较现有文献, 发现有必要探索EUS 对GIST的诊断价值[20]。 一方面,关于EUS 对黏膜下肿物的诊断价值有许多研究。与其他低回声的黏膜下肿瘤相比,GIST 的恶性率更高[21],因此有必要单独进行探讨。同时,我们与目前诊断GIST 相关技术进行了比较, 普通内镜诊断仅观察病变的大小和表面状况, 而不能像EUS 那样显示黏膜下肿物的性质。EUS-FNA(fine-needle aspiration)是一种侵入性技术,用于评估胃肠道和邻近器官的良性和恶性黏膜下病变[22],尽管与EUS[23-25]相比,其诊断准确性已得到显著提高。 然而,EUS-FNA 不仅存在技术实施困难,例如器械定位和介入性血管结构,还存在假阴性结果、出血和感染性风险[26-27]。 因此,考虑着重与其他非侵入性诊断技术进行比较。①传统的非侵入性诊断技术:包括腹部超声、CT、增强 CT 和 MRI。在GIST 的评估中, 由于皮下或内脏脂肪和胃肠道气体的原因,经腹超声检查存在明显局限性,增强CT 诊断 GIST 诊断率不超过 50%[28]。而 MRI 检查时间较长,且成本更高[29]。 ②传统的非侵入性诊断技术:内镜超声弹性成像(EUS elastography, E-EUS)对表现为硬性弹性图案的平滑肌瘤与GIST 存在一定的鉴别困难; 定量弹性成像EUS 诊断依赖于正确选择病变代表性区域。
据报道[28,30-33],谐波造影增强超声内镜(contrastenhanced harmonic endoscopic ultrasonography,CE-EUS)虽可区分GIST 和良性SET。 但其评估更多地取决于操作员的技能和主观分析。
总之, 使用当前的成像技术将GIST 与其他黏膜下包块, 特别是平滑肌瘤区分开来仍然是挑战。EUS 是一种非侵入性技术,价格适中,耐受性好且传播迅速。 我们认为EUS 在GIST 的诊断中具有一定的价值,但不能被准确地诊断或排除。 相信随着内镜设备的更新和临床医师经验的积累,其准确性将进一步提高,从而避免良性病变误诊为GIST。
