臭氧过氧化氢(O3/H2O2)降解2,4,6-三氯酚的多因素影响
2022-05-12王希诚高乃云
王希诚,高乃云
(同济大学污染控制与资源化研究国家重点实验室,上海 200092)
2,4,6-三氯酚(2,4,6-TCP)作为一种典型的氯酚类物质,大量应用于工厂生产,包括用作防腐剂、杀菌剂、防霉剂等。因此,在水体表面、水体底泥和土壤中都可以检测到它的存在[1-3],且2,4,6-TCP除毒性较大外,还具有遗传毒性,可引发癌症等众多病症。按照世卫组织规定,其在饮用水中的极限质量浓度为200 μg/L,我国城市供水标准限定其在水中的质量浓度≤0.01 mg/L[1-2,4]。此外,由于2,4,6-TCP含有抗降解的芳环结构和毒性较强的氯代原子,使其成为一种持久性难降解的有机污染物[5]。在德国,它已经被列入25种有毒物质之一,我国和美国等也将其列入优先控制污染物[1,4,6-7]。此外,根据周昕彦[8]的研究,2,4,6-TCP还是嗅味物质的前驱体,在水处理或废水处理中引起嗅味问题。
高级氧化工艺(AOPs)具有氧化能力强、处理效果好等特点,可以有效去除多种有机污染物。目前,比较常见的AOPs有O3/H2O2、UV/H2O2、UV/TiO2、UV/O3/H2O2、芬顿等,其中O3/H2O2组合工艺开始应用于实际生产。本文基于O3/H2O2高级氧化技术对水溶液中的2,4,6-TCP进行降解,研究不同H2O2浓度、2,4,6-TCP初始浓度、pH等因素以及不同阴离子对其降解情况的影响,初步探讨2,4,6-TCP的水处理动力学模型,旨在从中获得对含有2,4,6-TCP的废水降解的启发。
1 材料与方法
1.1 试验流程
如图1所示,试验采用均质反应器,其O3发生器产自哈尔滨久久电化学科技有限公司,型号为DHX-IX。反应器采用玻璃制造,容积约为1 500 mL,试验期间向反应器内投加的反应液体积为1 000 mL,水温为(19±2) ℃。
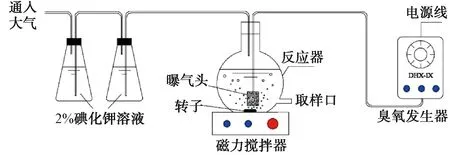
图1 试验流程图Fig.1 Flow Chart of Experiment System
①反应瓶中装入适量浓度的2,4,6-TCP溶液和转子,通过磁力搅拌器的快速搅拌,使反应溶液快速混合均匀,然后通入O3并同时投加定量的H2O2。
②试验期间,在反应瓶中每隔一段时间t,通过反应瓶上的取样口取样分析,取出的水样通过滴加过量的亚硫酸钠(Na2SO3,质量分数为10%)终止反应。
③O3尾气由2%的碘化钾溶液吸收。
采用碘量法测定溶液中的O3浓度,具体方法为:首先在两个吸收瓶中均放入20% KI,O3直接通入吸收瓶40 min,测出总O3量与时间的比值即为O3产生量。
1.2 试验药剂
2,4,6-TCP(Sigma公司,纯度≥98%)储备液质量浓度为100 mg/L,用超纯水配制,使用时根据需要进行稀释;流动相甲醇、冰醋酸为HPLC级(Sigma公司);H2O2(国药集团,30%)用超纯水配制成10 g/L的溶液;所需溶液的pH用分析纯药剂配制的H2SO4和NaOH溶液进行调节;调节阴离子浓度所需加入的Na2SO4、NaCl、NaHCO3、Na2CO3、NaNO3皆为分析纯,溶液摩尔浓度为10 mmol/L。
1.3 分析方法
2,4,6-TCP的浓度变化采用岛津LC-2010 AHT的高效液相色谱仪测定;检测波长λ=289 nm;使用Shim-pack VODS色谱柱(C18,250.0 mm×4.6 mm);流动相采用V(甲醇)∶V[水(含质量分数为1%的乙酸)]=80∶20;流动相流速v=1.0 mL/min;柱温T=40 ℃;分析时间为10 min。pH采用雷磁 PHS-3C精密pH计测定。DOC采用CPH CN200型TOC-L检测仪(配ASI-L型进样器)测定。
2 反应动力学分析
仅使用O3氧化时,有机污染物的降解过程包括两个方面:①分子态O3对污染物的直接氧化;②O3转化产生的羟基自由基(·OH)对有机污染物产生的间接氧化[4,9]。
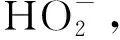
因此,O3/H2O2高级氧化工艺比仅O3氧化时大大提高了产生·OH的能力,反应如式(1)~式(5)[10-11]。
(1)
(2)
(3)
(4)
(5)
2,4,6-TCP的降解反应主要为O3的直接氧化和·OH的间接氧化,反应如式(6)~式(7)。
2,4,6-TCP+O3→降解产物
(6)
2,4,6-TCP+·OH→降解产物+H2O
(7)
反应过程中生成的·OH在水中寿命极短(小于1 μs),无法进行直接定量计算。因此,本试验对2,4,6-TCP的降解采用拟一级动力学方程进行表征,其动力学方程如式(8)~式(10)。

(8)
(9)

(10)
其中:kO3——O3直接氧化的反应速率常数,L/(mol·min);
k·OH——·OH氧化的反应速率常数,L/(mol·min);
t——反应时间,min;
[O3]——O3的摩尔浓度,mol/L;
[·OH]——·OH的摩尔浓度,mol/L;
[2,4,6-TCP]——2,4,6-TCP的摩尔浓度,mol/L。
本试验装置为连续式反应器,O3流量和H2O2投加量为固定值,且有磁力搅拌器快速将其混合均匀,可认为反应液中O3浓度及·OH产生量稳定。因此,O3/H2O2与2,4,6-TCP的反应可认为符合一级动力学。可将式(10)简化为式(11),通过积分再进一步转化为式(12)。
(11)
(12)
其中:k——准一级动力学反应常数,min-1;
[2,4,6-TCP]0——2,3,4-TCP的初始摩尔浓度,mol/L。
3 结果与讨论
3.1 不同H2O2投加量对2,4,6-TCP降解速率的影响
在固定臭氧发生器的O3产生量为0.68 mg/min、2,4,6-TCP的初始质量浓度为5 mg/L、初始pH值=5.05的情况下,研究了不同H2O2投加量对2,4,6-TCP的降解效果的影响。利用式(12)拟合ln([2,4,6-TCP]/[2,4,6-TCP]0)与反应时间t的关系如图2所示,拟合参数k(速率参数)、t1/2(半衰期)、R2(相关系数)如表1所示。对待测2,4,6-TCP样品进行DOC检测,其矿化情况如图3所示。

图2 不同H2O2浓度对2,4,6-TCP降解的影响Fig.2 Effect of Different Concentrations of H2O2 on Degradation of 2,4,6-TCP

表1 不同H2O2浓度情况下,对2,4,6-TCP降解的拟合参数 (准一级动力学模型)Tab.1 Fitting Parameters for Degradation of 2,4,6-TCP under Different Concentrations of H2O2 (Quasi-First-Order Kinetic Model)

图3 不同H2O2浓度对反应液中DOC去除率的影响Fig.3 Effect of Removal Efficiency of DOC with Different Dosages of H2O2
由图2~图3可知,H2O2投加量为0~10 mg/L的条件下,随着H2O2投加量的增加,2,4,6-TCP的去除率也同时增加,降解速率有所提高,其样品矿化率也逐渐增加,但样品降解速率和矿化率提高的程度却越来越小。其中,当H2O2的投加量为10 mg/L时,反应的降解速率比仅O3处理时提高近30%,矿化率提高近17%,这说明O3/H2O2组合工艺具有比单独O3工艺更好的处理效果,且效果十分明显。
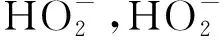
3.2 不同反应液初始浓度对对2,4,6-TCP降解速率的影响
在O3产生量为0.68 mg/min、H2O2投加量为5 mg/L的条件下,对不同初始质量浓度的2,4,6-TCP(10、5、3 mg/L)进行降解,利用式(12)拟合ln([2,4,6-TCP]/[2,4,6-TCP]0)与反应时间t的关系,如图4所示,拟合参数如表2所示。
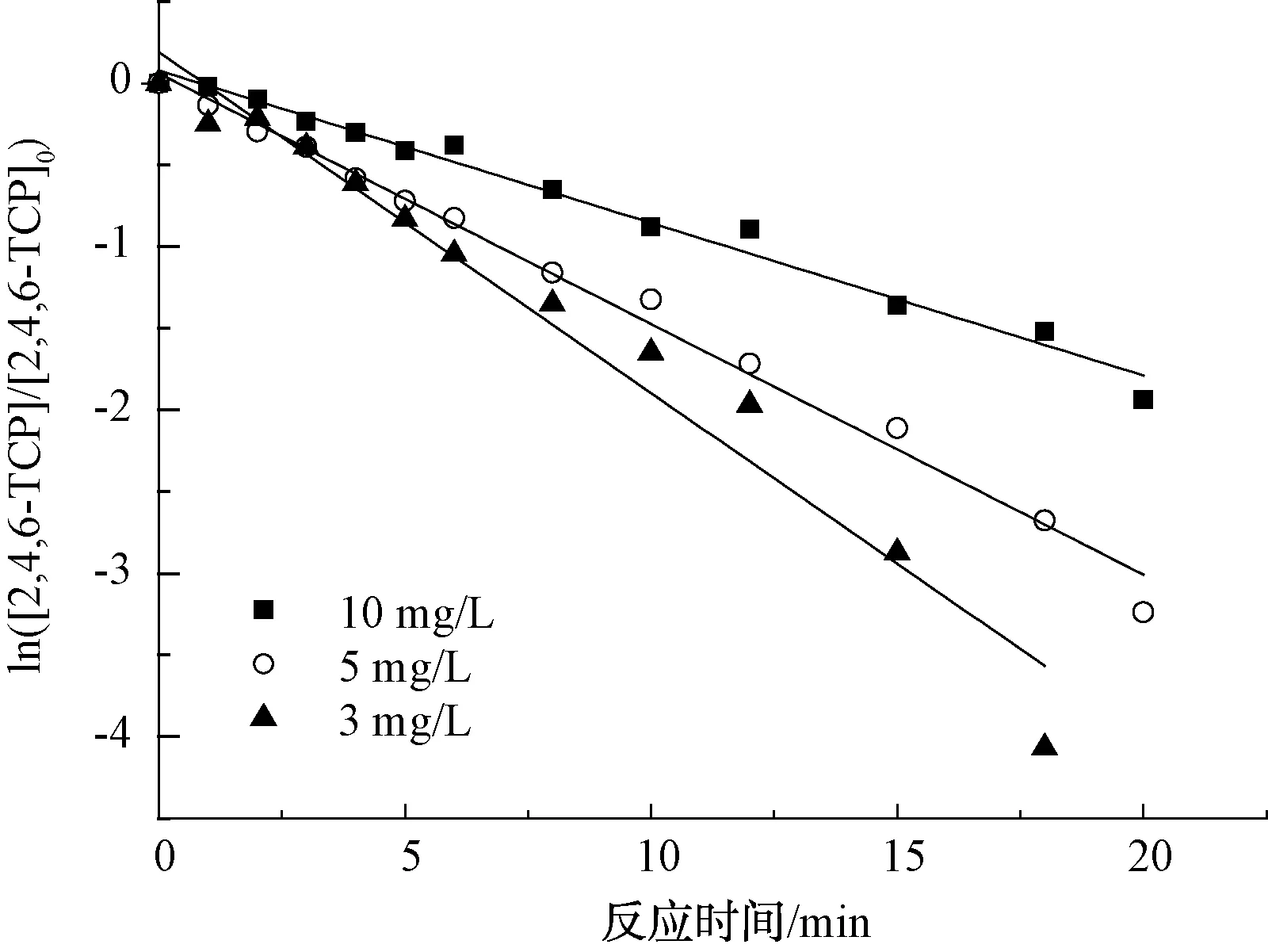
图4 不同初始质量浓度对2,4,6-TCP降解的影响Fig.4 Effect of Initial Concentrations of 2,4,6-TCP on Degradation Efficiency

表2 不同2,4,6-TCP初始质量浓度情况下,对2,4,6-TCP降解的拟合参数 (准一级动力学模型)Tab.2 Fitting Parameters of Degradation of 2,4,6-TCP under Different Initial Mass Concentrations (Quasi-First-Order Kinetic Model)
由图4与表2可知,随着2,4,6-TCP初始浓度的减少,反应物的降解速率增高十分明显。当2,4,6-TCP的初始质量浓度由10 mg/L降低到3 mg/L时,O3对2,4,6-TCP的降解速率也由原来的0.093 3 min-1增加到0.182 5 min-1,速度增快近2倍。这是因为O3和H2O2投加量为固定值的情况下,2,4,6-TCP的初始浓度增加,单位质量的反应物在一定时间内所获得的O3直接氧化和·OH氧化的概率降低,反应物的降解速率也将明显降低。
3.3 不同pH对2,4,6-TCP降解速率的影响
在2,4,6-TCP的初始质量浓度为5 mg/L、O3投加量为0.68 mg/L、H2O2投加量为5 mg/L的条件下,调节反应液的pH进行试验。各个试验工况的pH实测值分别为2.94、5.03、7.02、9.02、10.96。利用式(12)拟合ln([2,4,6-TCP]/[2,4,6-TCP]0)与反应时间t的关系,如图5所示,拟合参数如表3所示。

图5 不同pH值对2,4,6-TCP降解的影响Fig.5 Effect of Different pH Values on Degradation Efficiency

表3 不同pH条件下,对2,4,6-TCP降解的拟合参数 (准一级动力学模型)Tab.3 Fitting Parameters of Degradation of 2,4,6-TCP under Different pH Value Conditions (Quasi-First-Order Kinetic Model)
由图5和表3可知,O3/H2O2对2,4,6-TCP降解速率随着pH的增加,降解速率也逐渐增加。相同pH的增加量,在酸性条件下对降解速率的影响明显比碱性条件影响大,如pH值由2.94升至7.02时,其降解速率k由0.073 0 min-1升至0.185 3 min-1,pH值=7.02的降解速率是pH值=2.96的2倍多。可能的主要原因如下。

②由式(2)、式(3)可知,O3氧化在碱性条件下间接反应的活性更强,已被冯冬梅等[4]证实。
3.4 不同的阴离子对2,4,6-TCP降解速率的影响


图6 不同阴离子(离子摩尔浓度均为10 mmol/L)对2,4,6-TCP降解的影响Fig.6 Effect of Different Anions (10 mmol/L) on Degradation of 2,4,6-TCP by O3/H2O2

表4 不同阴离子条件下,对2,4,6-TCP降解的拟合参数 (准一级动力学模型)Tab.4 Fitting Parameters of Degradation of 2,4,6-TCP under Different Anions (Quasi-First-Order Kinetic Model)


(13)
(14)


4 结论
(1)采用先向反应器中投加一定浓度的H2O2,而后连续投加O3的AOPs,对2,4,6-TCP进行降解试验。结果表明,O3/H2O2对溶液中的2,4,6-TCP有较高的降解效果,降解模型模拟符合一级动力学,相关系数R2>0.970 0。

